成熟期增生性瘢痕與正常皮膚來源表皮干細胞生物學特性的對比研究
徐永飛 張建文 劉林嶓 周樹萍

[摘要]目的:探討成熟期增生性瘢痕與正常皮膚來源表皮干細胞的生物學特性。方法:選擇本院成熟期增生性瘢痕患者病理組織,正常皮膚為本院行游離皮片移植術患者的全厚皮片,分別進行分離培養,獲取種子細胞,利用免疫細胞化學技術檢測角蛋白19、整合素β1在兩組中的表達情況,應用CCK-8檢測兩組表皮干細胞生長曲線,酶標儀檢測兩組表皮干細胞450~630nm的吸光度值。結果:角蛋白19及整合素β1在兩組中均呈陽性表達,差異無統計學意義(P>0.05);且兩組表皮干細胞具有相似的生長曲線,其不同時間的450~630nm吸光度值比較,差異均無統計學意義(P>0.05)。結論:成熟期增生性瘢痕組織中也存在表皮干細胞,且與正常皮膚來源表皮干細胞具有相近的生物學特性,為整形外科中成熟期增生性瘢痕組織表皮的再利用提供理論基礎。
[關鍵詞]增生性瘢痕;表皮干細胞;生物學特性;整形外科;缺損;修復
[中圖分類號]R619+.6 [文獻標志碼]A [文章編號]1008-6455(2018)04-0102-03
Comparative Study of Biological Characteristics of Epidermal Stem Cells from Human Hypertrophic Scar in Mature and Normal Skin
XU Yong-fei1,ZHANG Jian-wen2,LIU Lin-bo2,ZHOU Shu-ping3
(1.Department of Plastic Surgery,Luoyang Central Hospital Affiliated to Zhengzhou University,Luoyang 471000,Henan,China;
2.Department of Plastic Surgeny, the First Affiliated Hospital of Zhengzhou University,Zhengzhou 450000,Henan,China;
3.Department of Microsurgery,NO.153 Central Hospital of the PLA,Zhengzhou 450000,Henan,China)
Abstract: Objective To investigate the biological characteristics of mature epidermal stem cells derived from hypertrophic scars and normal skin. Methods The pathological tissues of patients with mature hypertrophic scar were selected. The normal skin came from the full-thickness skin slices of free skin graft in our hospital. They were isolated and cultured respectively to obtain seed cells. Immunocytochemistry was used to detect the expression of keratin 19 and integrin β1 in both groups. The growth curve of epidermal stem cells and the absorbance of 450~630nm were detected by CCK-8 and microplate reader. Results Keratin 19 and integrin β1 in both groups were positive expression, and the difference was not statistically significant (P>0.05). Two groups of epidermal stem cells had similar growth curves, and there were no significant difference in absorbance value between 450 and 630nm at different time(P>0.05). Conclusion Epidermal stem cells also exist in mature hypertrophic scars, and have similar biological characteristics with normal skin derived epidermal stem cells, which provides a theoretical basis for the reutilization of hypertrophic scar tissue in the orthopedic period.
Key words: hypertrophic scars; epidermal stem cells; biological characteristics; plastic surgery; defect; repair
瘢痕是是創面愈合的最終結果,不僅影響美觀,而且常伴畸形及功能障礙,嚴重影響身心健康,臨床上常主張手術治療[1],手術原則為徹底切除瘢痕組織,以游離皮片或皮瓣覆蓋創面,最大限度的恢復患者外觀及功能[2],但從正常皮膚中獲取游離皮片或皮瓣必然會帶來新的創傷。瘢痕組織的表皮能否再利用已成為目前討論的熱點[3]。本研究旨在探討人成熟期增生性瘢痕與人正常皮膚來源表皮干細胞的生物學特性,現報道如下。
1 材料和方法
1.1 實驗試劑及儀器:PBS液、4%多聚甲醛(UBIO,中國)、無水乙醇、酒精、正丁醇、二甲苯、石蠟、中性樹膠;激光掃描共聚焦顯微鏡、Megafuge離心機、組織包埋機、全自動輪轉切片機、全自動輪轉切片機、電熱鼓風干燥箱、倒置相差顯微鏡。
1.2 成熟期增生性瘢痕組織:成熟期增生性瘢痕組織來源于2012年7月-2015年7月于本院整形外科行瘢痕切除的20例患者,均經病理證實。其中男12例,女8例;年齡20~75歲,平均46歲;致病原因:燒傷、外傷、手術及皮膚感染等。正常皮膚來源于同期本院行游離皮片移植術的20例患者的全厚皮片,其中男11例,女9例;年齡18~74歲,平均46歲。兩組患者性別、年齡比較,差異無統計學意義(P>0.05)。納入標準:①患者6個月內病變組織無破潰、感染及癌變等;②6個月內未口服抗瘢痕藥物或激素類藥物者;③6個月內未接受放射治療者;④無精神性疾病及相關器質性疾病。所有患者對本研究知情同意并簽署相關知情同意書。
1.3 表皮干細胞的培養及鑒定:將手術獲取的瘢痕組織和正常皮膚于無菌環境下帶入實驗室,均修剪為1.0cm×0.3cm中厚皮片,用PBS液沖洗獲取組織,加入DiapaseⅡ,再次用PBS液進行沖洗,過濾上清液并分離獲得表皮組織,加入胰蛋白酶進行消化,分散細胞,除去上清液,獲取細胞懸液,放置于無菌培養皿中進行培養,并更換KM培養基,并分別加入胰蛋白酶和膠原,再次更換KM培養基,此時分離培養的細胞即為種子細胞。利用免疫細胞化學技術檢測表皮干細胞的陽性標記物角蛋白19、整合素β1對兩組中是否存在表皮干細胞進行鑒定。角蛋白19陽性表達表現為細胞漿呈紅色熒光,整合素β1陽性表現為細胞膜呈紅色熒光[4]。
1.4 檢測指標:使用酶標儀檢測兩組表皮干細胞450~630nm的吸光度值,吸光度值越高,表明表皮干細胞增殖能力越強[5],并連續檢測其7d生長曲線。參照Constantine的標準,高倍鏡(200×)綜合染色強度和陽性細胞所占比例進行半定量測定:按照染色強度(無染色為0分,淡染色為1分,黃色2分,棕褐色3分)和陽性細胞數(在400倍光鏡下至少5個視野,細胞陽性數≤1%為0分,1%~10%為1分,10%~20%為2分,≥20%為3分)統計記分,以上兩項相加為總分,0分為陰性(-),1~2分為(+),3~4分(++),5~6分為(+++)。
1.5 統計學分析:數據采用SPSS l8.0統計軟件進行分析。計量資料采用樣本均數t檢驗進行組間比較,計數資料行χ2檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 表皮干細胞鑒定結果:角蛋白19、整合素β1在兩組組織中均呈陽性表達,且差異無統計學意義(P>0.05),證明成熟期增生性瘢痕組織中同樣存在表皮干細胞。見表1,圖1~4。
表1 角蛋白19和整合素β1在兩組組織中的表達情況 (n=20,例)
分組 角蛋白19總分分級 整合素β1總分分級
- + ++ +++ - + ++ +++
增生性瘢痕組 0 3 15 2 0 4 15 1
正常皮膚組 0 4 16 0 0 5 15 0
χ2值 0.934 0.963
P值 0.334 0.328
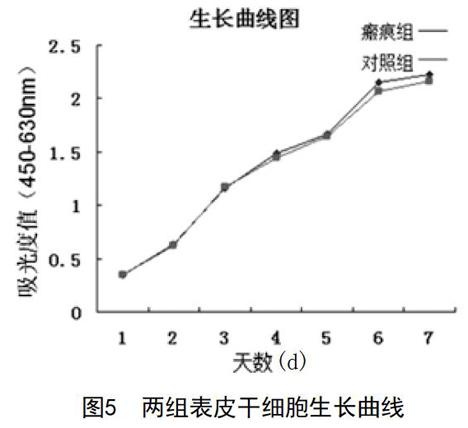
2.2 生長曲線:兩組總體生長趨勢大致相同,第1~2天生長緩慢,第3~4天生長迅速,第5天達到高峰,第6~7天相對平穩,形成一個平臺期。兩組表皮干細胞生長曲線大致相同,見圖5。
圖5 兩組表皮干細胞生長曲線
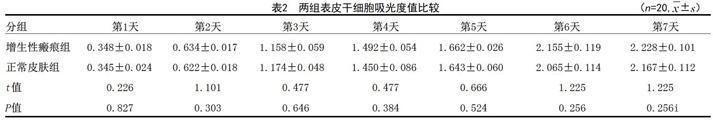
2.3 吸光度值:瘢痕組表皮干細胞與正常皮膚組表皮干細胞吸光度值比較,差異無統計學意義(P>0.05)。見表2。
3 討論
增生性瘢痕是創傷愈合留下的痕跡,也是組織修復愈合的最終結果,輕者影響美觀,重者影響功能,給患者身心可帶來巨大影響,臨床上對于嚴重影響患者功能的增生性瘢痕,常采用手術治療,完全切除瘢痕組織,徹底松解皮膚,缺損創面以游離皮片或皮瓣覆蓋,最大限度的恢復患者的功能及外觀[6-8]。然而,切除的瘢痕組織常被廢棄,以機體其它部位的游離皮片或皮瓣去修復創面必然會帶來新的創傷[9]。表皮干細胞存在于皮膚中,通過其不斷的增殖及分化,維持皮膚結構及功能的完整性[10]。近年來,隨著表皮干細胞研究的不斷深入,從生物細胞學角度講表皮干細胞應用于臨床已成為研究熱點[11-12]。周樹萍等[13]的研究發現,當增生性瘢痕成熟,即穩定后,其能夠進行穩定的新陳代謝,從而維持瘢痕組織皮膚組織結構完整性及細胞內環境穩定性。基于此,本研究推測成熟期增生性瘢痕組織具有表皮干細胞,并針對其生物學特性與正常皮膚表皮干細胞進行了對比研究。
謝一帆等[14]研究發現,表皮干細胞能夠特異性表達角蛋白19、整合素β1。Yoshikawa K等[15]的研究發現瘢痕組織中細胞的生長曲線及第1~7天吸光度值可反應細胞生長能力。本研究分兩部分進行,第一部分利用免疫組織化學方法證明兩組表皮組織中表皮干細胞的存在;第二部分從增殖能力方面對比性研究兩組表皮干細胞的生物學特性。本實驗標本來源于本院成熟期增生性瘢痕患者,發病均在2年以上,且臨床表現趨于穩定,顏色變淡,質地變軟,并經病理證實,采用中性蛋白酶消化分離瘢痕真皮細胞,避免真皮細胞對實驗帶來干擾,將表皮組織進行分離培養,獲得種子細胞,應用免疫組織化學方法對其特異性標志物角蛋白19、整合素β1進行鑒定,結果表明角蛋白19、整合素β1在兩組均呈陽性表達,且差異無統計學意義,說明所獲得的種子細胞均為表皮干細胞,從而證明成熟期增生性瘢痕組織表皮與正常皮膚表皮均存在表皮干細胞,這與相關研究相符。通過繪制兩組表皮干細胞的生長曲線及第1~7天吸光度值檢測結果發現,兩組表皮干細胞均呈S形生長,生長曲線相似,且吸光度值無明顯差異。
本實驗從兩方面證明,成熟期增生性瘢痕組織中存在表皮干細胞,且其生物學特性與正常皮膚來源表皮干細胞相似,提示臨床上切除的瘢痕組織可以再利用,提取瘢痕組織的表皮組織可作為創面修復的皮片來源。但本研究不足之處在于僅僅通過組織化學及增殖能力方面對表皮干細胞進行研究,要全面應用于臨床,有待于之后從基因學及蛋白學角度進一步進行臨床實驗研究。
[參考文獻]
[1]徐靜靜,蔡景龍,王黔,等.人瘢痕組織脫細胞真皮基質的組織結構和生物力學性能[J].中華醫學雜志,2015,95(10):770-772.
[2]李艷.點陣CO2激光聯合積雪苷霜軟膏治療痤瘡凹陷性瘢痕療效觀察[J].中國醫療美容,2014,4(2):57-58.
[3]楊玲,劉善榮,仵敏娟,等.成人體皮表皮干細胞的定位及分離培養[J].第二軍醫大學學報,2004,25(8):815-816.
[4]Butzelaar L,Ulrich MM,Mink van der Molen AB,et al.Currently known risk factors for hypertrophic skin scarring:A review[J].J Plast Reconstr Aesthet Surg,2016,69(2):163-169.
[5]劉玲,陳敏亮,雷永紅,等.表皮干細胞表型的成纖維樣細胞在瘢痕中的表達[J].中國美容醫學,2009,18(5):645-647.
[6]周樹萍,蔡景龍,牛扶幼,等.人增生性瘢痕與正常皮膚中表皮干細胞的生物學特性及含量比較[J].中華醫學雜志,2014,94(14):1097-1099.
[7]陳甫寰,宋慧鋒,王統民,等.汗腺細胞在人體皮膚創傷及修復中的研究進展[J].中國美容醫學,2015,24(19):73-75.
[8]Sharquie KE,Noaimi AA,Al-Karhi MR.Debulking of Keloid Combined with Intralesional Injection of 5-Flurouracil and Triamcinolone versus Intralesional Injection of 5-Flurouracil and Triamcinolone[J].J Cosmet Dermatolog Sci Appl,2014,4(2):85.
[9]陳鑫,張一嗚,樊東力,等.干細胞療法在創面愈合中的研究進展[J].中華醫學美容美學雜志,2014,20(4):315-317.
[10]丁毓威,辛國華,曾元臨,等.干細胞誘導分化為毛囊及再生的研究進展[J].中國組織工程研究,2016,20(50):7570-7580.
[11]錢李科,錢明元.豬脫細胞真皮與人表皮干細胞構建組織工程皮膚修復全層皮膚缺損[J].中國組織工程研究,2017,21(2):227-228.
[12]Zhang C,Chen P,Fei Y,et al.Wnt/β-catenin signaling is critical for dedifferentiation of aged epidermal cells in vivo and in vitro[J].Aging Cell,2012, 11(1):14-23.
[13]周樹萍,黃繼龍,馬繼光,等.人增生性瘢痕表皮干細胞修復裸鼠皮膚創面的實驗研究[J].中華整形外科雜志,2014,30(4):289-231.
[14]謝一帆,吳巖.表皮干細胞的研究進展[J].中國組織工程研究與臨床康復,2010,14(19): 3578-3580.
[15]Yoshikawa K,Naiton M,Kubota H,et al.Muitipotent stem cells are effectively collected from adult human cheek skin[J].Biochem Biophys Res Commun,2013,431(1):104-110.

