中學化學課堂自主學習教學模式實踐探究
胡云賀+羅桂山
以“一杯廢液處理的背后——電解質在水溶液中的反應”教學為例,在課堂教學中,通過創設情境、小組互助合作以及自主探究學習的方式實踐化學課堂(新授課)自主學習教學模式。
一、問題的提出
“課堂自主學習”是指學生在教師的科學指導下,在課堂上一定的時間內,對指定的學習內容,通過能動的創造性的學習活動,實現自主性發展的教學實踐活動。通過自主學習模式的構建,能有效激發學生內在的學習興趣,培養學生學習的自主性、主動性和創造性,使之不僅會學習,而且愛學習,進而養成良好的學習習慣,并為其終身學習奠定堅實的基礎。
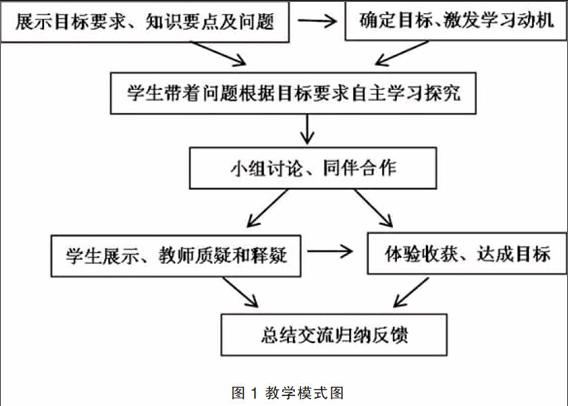
筆者有幸參加羅桂山老師主持的“化學課堂自主學習教學模式的建構研究”課題組,通過不斷地實踐探究,課題組提出新授課的教學模式。
該流程圖包含三個環節,首先教師展示目標要求、知識要點及問題,采用任務驅動,確定目標、激發學生的學習動機;此環節中,教師要盡可能創設問題情景,把學生的思維引入與問題有關的情境中,調動學生的主動性,使學生萌生解決問題的愿望。環節二是學生的自主探究學習過程,采用小組討論、同伴合作的學習方式;此環節中教師要盡可能地參與各小組的討論,引導學生有效的沿著問題的思路去探究。環節三是學生代表展示、教師質疑和釋疑,在教師的評價中學生體驗收獲的喜悅,教學也達成目標。在實踐此教學模式時,如何采用任務驅動,激發學生的學習動機;在學生自主學習過程中,教師如何引導學生進行有效討論;如何使課堂教學過程流暢,達成教學目標。結合“一杯廢液處理的背后——電解質在水溶液中的反應”教學的過程進行詮釋。
二、設計思路
電解質在水溶液中的反應屬于理論教學,理論教學一直是化學教學中的一個難題,如何將枯燥的化學理論轉化為學生的知識并指導其學習呢?古希臘生物學家普羅塔弋說過這樣一句話:“頭腦不是一個要被填滿的容器,而是一把需被點燃的火把。”根據這種情況,首先我創設一個情景:“一杯實驗室收集的廢液在倒入下水道之前如何處理呢?”采用的是任務驅動教學法,激發學生的學習動機。接著我采用了分組實驗探究、小組討論和閱讀探究相結合的方式,給學生創設自主學習的空間和時間。在此過程中,我再采用歸納分析法、多媒體輔助教學法,讓學生能自主、積極地參與知識的形成過程,實現“三維”教學目標。對于難點處理則采用了思維建模的方法,將難點分散到各個環節中。學生主要采用實驗探究、觀察思考、交流研討的方法進行自主學習,邊實驗,邊觀察、邊記錄、邊思考,在教師的引導下,按科學的方法處理所得的材料,得出結論,達成學習目標。
三、教學實錄
教學環節一:情景引入,生成要探究的問題
PPT展示:水污染圖片。
師:桌面上有一杯在實驗室收集的廢液,能不能直接倒入下水道?
生1:不能,會污染我們的水資源。
生2:污水在排放之前要凈化處理。
師:這種廢液中的Ag+、Ba2+、Cu2+屬于重金屬離子,若直接排放會污染水源,如何處理才能排放?
板書:電解質在水溶液中的反應
生1:加入NaCl溶液、Na2SO4溶液、NaOH溶液,產生AgCl、BaSO4、Cu(OH)2沉淀。
生2:加入鹽酸、稀硫酸、KOH溶液,產生AgCl、BaSO4、Cu(OH)2沉淀。
生3:加入含Cl-、SO42-和OH-的溶液,產生AgCl、BaSO4、Cu(OH)2沉淀。
師:三種電解質溶液加入廢液中反生了化學反應,產生沉淀,從而除去這些重金屬離子。電解質溶液之間是如何反應的?反應和離子有什么關系?如何選擇電解質以及選擇哪些電解質?
教學環節二:實驗探究,小組合作進行自主學習
實驗探究1:稀硫酸和氫氧化鋇在溶液中反應的導電性實驗,教師播放錄制的“微課視頻”。
師:觀看視頻,在學案上記錄實驗現象,并小組交流討論“電流表指針的變化說明了什么問題”“溶液顏色的變化是什么原因引起的”“白色沉淀的成分是什么,如何形成”“稀硫酸與Ba(OH)2溶液混合后反應的實質是什么”四個問題。
學生觀看微課視頻,小組交流討論,展示匯報討論的結論。
師: 稀硫酸與Ba(OH)2溶液反應的實質是電離出的離子發生了反應;反應向著離子濃度減小的方向進行。
師:電解質溶液間反應的實質:電解質電離得到的離子發生了反應。離子反應若要發生需要具備哪些條件?電解質溶液中的離子是否全部都參加了反應?
實驗探究2:取2ml0.01mol/LCuSO4溶液于試管中,滴加少量NaOH溶液;取2ml0.01mol/LNa2CO3溶液于試管中,滴加過量鹽酸;取2ml0.01mol/L的NaOH溶液于試管中,滴加一滴酚酞試液,再逐滴加入鹽酸至過量;取2ml0.01mol/LCuSO4溶液于試管中,滴加少量NaCl溶液。
學生思考,小組實驗探究;并小組交流討論,展示匯報討論的結論。
生:第1個實驗產生藍色沉淀,因為Cu2+和OH-反應,產生了Cu(OH)2沉淀;第2個實驗有氣體產生,因為CO32-和H+反應產生CO2氣體;第3個實驗溶液紅色逐漸褪去,是因為OH-和H+反應生成水;第4個實驗無現象,不符合復分解反應的條件,沒有反應。我們組得出的結論是離子反應若要發生需要能產生沉淀、氣體和水,和復分解反應反生的條件是一樣的。
師:沉淀的物質屬于難溶電解質,水屬于難電離的物質,CO2是氣體,屬于揮發性物質。
師:電解質溶液間的反應實質是離子間的反應,在以上的分析過程中我們也看到,并非所有的離子都參加了反應,因此我們就用實際參加反應的離子符號來表達離子反應,稱之為離子反應方程式。請同學們自主學習離子方程式的書寫。
板書:離子方程式(用實際參加反應離子的符號來表示化學反應的式子)。
學生閱讀教材第32頁,完成學案上離子方程式的書寫,小組交流討論,展示匯報。
責任編輯黃博彥endprint

