脫鋁超穩(wěn)Y沸石負載磷鎢酸銫鹽催化合成乙二醇二甲醚
于清躍,張云良,孫 飛,朱新寶
脫鋁超穩(wěn)Y沸石負載磷鎢酸銫鹽催化合成乙二醇二甲醚
于清躍1,張云良1,孫 飛2,朱新寶3
(1.南京科技職業(yè)學院 化工與材料學院,江蘇 南京 210048;2.南京安鼎化工科技有限公司,江蘇 南京 210048;3.南京林業(yè)大學 化學工程學院,江蘇 南京 210037)
采用水蒸氣脫鋁法制備脫鋁超穩(wěn)Y沸石(DUSY)載體,負載磷鎢酸銫鹽(Cs2.5PW)制備了系列催化劑,并在固定床反應器上考察了系列催化劑催化二甲醚(DME)與環(huán)氧乙烷(EO)合成乙二醇二甲醚(DMEG)反應的性能,優(yōu)化了Cs2.5PW負載量、GHSV、反應溫度、反應壓力、催化劑的使用時間等條件。采用XRD、31P NMR、29Si NMR、N2吸附-脫附、FTIR等方法對催化劑進行表征。表征結(jié)果顯示,系列催化劑試樣與DUSY載體發(fā)生了強相互作用,在DUSY表面高度分散且保持完整Y沸石的孔道結(jié)構。實驗結(jié)果表明,在Cs2.5PW負載量為30 %(w)時,催化劑試樣的NH3吸附量可達618 μmol/g,B酸與L酸吸附量分別為350,268 μmol/g;在n(DME):n(EO)= 3,80 ℃,GHSV = 1 800 h-1,0.70 MPa,反應30 h的最優(yōu)條件下,EO完全轉(zhuǎn)化,DMEG選擇性達62.6%;連續(xù)反應240 h后,EO轉(zhuǎn)化率達98.1%,DMEG選擇性未見下降,催化劑保持著較好活性。
環(huán)氧乙烷;二甲醚;乙二醇二甲醚;磷鎢酸銫鹽
乙二醇二甲醚(DMEG)是性能優(yōu)越的極性溶劑,廣泛用于醫(yī)藥抽提、有機中間體合成及化學工業(yè)。以醇鈉為催化劑的Williamson傳統(tǒng)合成法工藝路線長、副產(chǎn)物多、分離難度大。為獲得純凈產(chǎn)品需要中和堿液產(chǎn)生大量工業(yè)鹽和廢水,環(huán)境污染嚴重,采用環(huán)境友好非均相催化工藝是理想的選擇[1-3]。
固體催化劑中改性超穩(wěn)Y沸石(USY)具有較好的催化活性。Qiao等[4]用檸檬酸與乙二胺四乙酸對USY進行改性獲得不同層次的高結(jié)晶度分子篩;王希龍等[5]發(fā)現(xiàn)超細NaY分子篩深度脫鋁后,脫除的鋁在分子篩中以無定形的非骨架鋁形式存在;黃朝暉等[6]對USY分子篩表面酸性進行調(diào)變并研究它在催化脫除芳烴中烯烴的應用;Cromwell等[7]將 Ir,Pt,Pd,Ni等負載到 USY 上用于催化甲基環(huán)己烷脫氫制甲苯;Aelst等[8]應用堿處理負載釕USY催化劑用于植物油中亞油酸及共軛亞油酸的結(jié)合。H3PW12O40(PW)作為強而均一的固體超強酸具有很高的酸催化性能,然而DMEG作為極性溶劑對PW具有溶解性,使得負載PW催化劑由于PW的流失而失去活性。將PW制備成負載磷鎢酸銫鹽催化劑,既能充分利用PW的超強酸性,又能克服PW穩(wěn)定性差的缺陷,具有工業(yè)應用價值。
本工作采用水蒸氣脫鋁法制備脫鋁超穩(wěn)Y沸石載體,負載磷鎢酸銫鹽制備了系列催化劑,并在固定床反應器上考察了系列催化劑催化二甲醚(DME)與環(huán)氧乙烷(EO)合成DMEG反應的性能,優(yōu)化了Cs2.5PW負載量、GHSV、反應溫度、反應壓力、催化劑的使用時間等條件。采用XRD、31P NMR、29Si NMR、N2吸附-脫附、FTIR等方法對催化劑進行表征。
1 實驗部分
1.1 主要試劑
USY:工業(yè)純,周村催化劑廠;PW:分析純,上海化學試劑有限公司;NH4NO3:分析純,上海國藥集團化學試劑有限公司;Cs2CO3:分析純,上海凌峰化學試劑有限公司;EO:工業(yè)純,江蘇怡達化工有限公司;DME:工業(yè)純,久泰能源(張家港)有限公司。
1.2 催化劑的制備
將裝有USY的石英舟放在石英管內(nèi),置于550 ℃的管式電阻爐中。石英管一端連接水蒸氣發(fā)生裝置,稍低的另一端敞口連接大氣,水蒸氣處理時間3 h。將處理后USY試樣用0.05 mol/L的NH4NO3水溶液洗滌3次,再用去離子水洗滌3次后,置于110 ℃下干燥6 h,再于550 ℃下焙燒3 h,得到脫鋁USY,記為DUSY。
配制0.1 mol/L的Cs2CO3水溶液和0.08 mol/L的PW水溶液。以1 mL/min的速率將Cs2CO3溶液滴加到攪拌狀態(tài)的計量PW水溶液中,滴加完成后繼續(xù)攪拌30 min以上,室溫靜置12 h后,60 ℃蒸干水分,所得白色固體于110 ℃干燥,再于300 ℃下焙燒3 h,即得Cs2.5H0.5PW12O40鹽,記為Cs2.5PW。
將上述制備DUSY加入設定量Cs2CO3水溶液中至吸附平衡,加熱攪拌并蒸干水分,550 ℃下焙燒4 h;將焙燒后試樣與PW水溶液按照設定質(zhì)量比混合,室溫攪拌12 h,磁力加熱攪拌至試樣蒸干水分,室溫下陳晾24 h,再于120 ℃下干燥12 h,得系列wCs2.5H0.5PW12O40/DUSY催化劑(w為Cs2.5H0.5PW12O40在催化劑中的質(zhì)量分數(shù)),記為wCs2.5PW/DUSY。
將一定量的DUSY和PW乙醇水溶液(V(乙醇)∶V(水)=1∶1)在室溫下按0.1 g/mL的比例混合,攪拌12 h;然后將醇水緩慢蒸發(fā)至半干,室溫陳晾,再于110 ℃下干燥得催化劑試樣,記為xPW/DUSY(x為PW在催化劑中的質(zhì)量分數(shù))。
1.3 催化劑的表征
采用德國Bruker公司D8 ADVANCE型X射線衍射儀對催化劑試樣進行XRD表征,Cu Ka射線,管電流30 mA,管電壓40 kV;采用美國Coulter公司Omnisorp-100CX型物理吸附儀對催化劑試樣的比表面積和孔徑分布進行N2吸附-脫附表征,液氮溫度-196 ℃。采用法國Setarm公司Tian-Calvet型熱流式量熱儀測定試樣氨吸附量;采用德國Bruker公司ADVANCE 400D 型交叉極化核磁共振譜儀進行31P NMR和29Si NMR表征;采用美國Thermo Nicolet公司NEXUS470型傅里葉紅外光譜儀原位進行NH3FTIR表征;采用美國ThermoFinnigan公司Tempus型氣質(zhì)聯(lián)用儀對產(chǎn)物進行定性表征,彈性石英毛細管柱(30 m×0.32 mm×0.5 μm),柱溫40 ℃,汽化溫度260 ℃,檢測器溫度260 ℃;采用山東魯南公司的SP-6800A型氣相色譜儀對DMEG及副產(chǎn)物進行分析,15 m長FFAP毛細管色譜柱,F(xiàn)ID檢測,汽化溫度260 ℃,檢測溫度260 ℃,柱溫在65 ℃恒溫2 min后,以25 ℃/min的速率升至230 ℃保持2 min,面積歸一化法計算。
1.4 催化劑的性能評價
量取5 mL石英砂,裝入管式反應器;再量取5 mL催化劑試樣(催化劑粉末經(jīng)壓片、研磨和過篩,30~40目)與石英砂混合成10 mL混合物,裝入反應管;最后量取5 mL石英砂裝入反應管上部。各催化劑試樣使用前均于設定溫度、氮氣保護下焙燒活化3 h。
EO和DME從鋼瓶底部通過導管分別壓入裝有高氯酸鎂干燥劑的汽化器,關閉入口閥門,恒溫90 ℃,計量EO和DME流量后,進入預熱器恒溫氣化,進入反應器,在催化劑作用下,EO與DME開環(huán)醚化反應生成DMEG。冷凝收集產(chǎn)物與尾氣,檢測產(chǎn)物與尾氣組分與含量。
2 結(jié)果與討論
2.1 XRD表征結(jié)果
圖1為系列催化劑的XRD譜圖。

圖1 系列催化劑試樣的XRD譜圖Fig.1 XRD spectra of serials catalysts.PW:H3PW12O40;USY:ultra stable Y zeolite;DUSY:dealumination USY.
由圖1a可知,DUSY譜圖呈現(xiàn)出USY沸石特征衍射峰,試樣保持較高相對結(jié)晶度,說明水蒸氣脫鋁DUSY試樣孔道保持完整,結(jié)構沒有坍塌。xPW/DUSY試樣均呈現(xiàn)出與DUSY一致的特征峰,催化劑保持完好Y沸石的孔道結(jié)構。未檢測出與PW晶體相一致的特征峰,說明PW在DUSY表面高度分散。由圖1b可知,Cs2.5PW衍射峰的峰位與PW接近,說明制備的Cs2.5PW晶體結(jié)構與純PW相似。隨著負載量增加,Cs2.5PW與DUSY載體發(fā)生強相互作用,表現(xiàn)為載體DUSY的特征衍射峰強度降低,但依然存在特征衍射峰,說明催化劑孔道結(jié)構保持完整。
2.2 核磁表征結(jié)果
圖2為系列催化劑試樣的29Si NMR和31P NMR譜圖。

圖2 系列催化劑試樣的29Si NMR和31P NMR譜圖Fig.2 29Si NMR and 31P NMR spectra for various catalysts.
由圖2a可知,DUSY,30%PW/DUSY,30%Cs2.5PW/DUSY沒有顯著的化學位移變化,說明DUSY負載PW與Cs2.5PW后,沸石的孔道結(jié)構保持完整,這與XRD表征結(jié)果一致。USY試樣譜圖中δ =-39 200,-42 000 兩處分別歸屬于 Si(OSi)2(OH)2和Si(OSi)3(OH)兩個單元。DUSY試樣位于δ= -39 600處的峰強度低于USY試樣,說明經(jīng)水蒸氣脫鋁后,試樣表面Si—OH含量明顯減少[13-15]。由圖2b可知,δ= -4 400處歸屬于PW峰位;δ= -4 400,-3 640兩處歸屬于30%PW/DUSY峰位,其中,δ= -3 640處的峰位說明PW雜多陰離子與載體DUSY表面羥基發(fā)生強相互作用,而δ= -4 400處峰位說明PW雜多陰離子與載體之間存在弱相互作用[12]。由圖2b可知,試樣30%Cs2.5PW/DUSY呈現(xiàn)出的肩峰歸屬于載體DUSY與Cs2.5PW陰離子之間存在的強弱兩種相互作用峰的疊加。這種存在于載體和Cs2.5PW間的強相互作用,使得負載后的30%Cs2.5PW/DUSY在用作催化劑時,Cs2.5PW不易脫落,同時Cs2.5PW相對PW在產(chǎn)品DMEG中的難溶性,在催化反應過程中也一起表現(xiàn)為催化劑的穩(wěn)定性。
2.3 孔結(jié)構
表 1為試樣的物性參數(shù)。由表1可知,DUSY經(jīng)高溫水蒸氣作用,二次孔壁打開,微孔疏通,比表面積、孔體積與平均孔徑均增大。負載Cs2.5PW后催化劑比表面積減小,這是由于Cs2.5PW占據(jù)了DUSY孔道后,導致試樣孔體積下降、孔徑收縮。
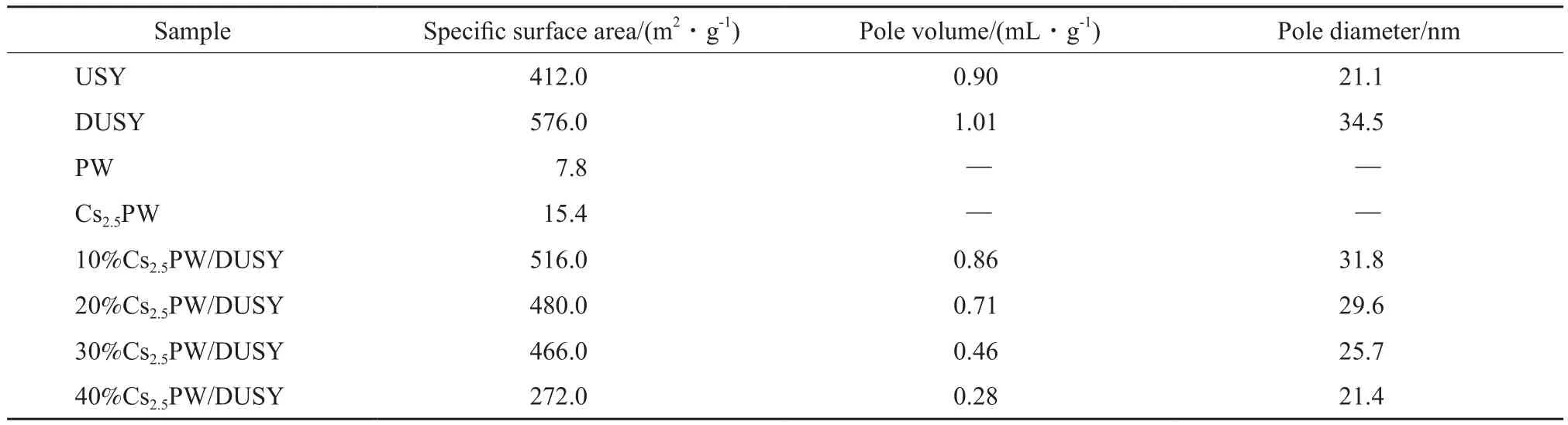
表1 試樣的物性參數(shù)Table 1 Properties of different samples
2.4 FTIR表征結(jié)果
表2為試樣NH3-FTIR表征結(jié)果。由表2可知,PW和Cs2.5PW呈現(xiàn)B酸性,USY兼具B酸與L酸性,DUSY由于沸石骨架硅鋁比的增大而B酸含量增加。由于DUSY具有較大的比表面積,使得負載后試樣中Cs2.5PW在載體孔道中均勻分散,活性酸位得到充分利用。在Cs2.5PW負載量為30 %(w)時,Cs2.5PW在DUSY表面呈現(xiàn)最大分布,催化劑試樣的NH3吸附量可達618 μmol/g,B酸與L酸吸附量分別為 350,268 μmol/g。

表2 試樣的酸性質(zhì)Table 2 Acidic properties of different samples
2.5 反應影響因素
2.5.1 Cs2.5PW負載量的影響
當DMEG選擇性為45.3%時,產(chǎn)物中二甲醚二乙二醇(DMDG)及多乙二醇二甲醚(DMTrG)生成量最少,這是因為Cs2.5PW比表面積小,導致產(chǎn)物DMEG在催化劑顆粒表面形成后,快速擴散離開催化劑表面。EO在催化劑B酸中心同時進行二聚、多聚及異構反應,生成較多1,4-二氧六環(huán)(Diox)、多聚物及異構產(chǎn)物。DUSY表面具有較大的酸量及B酸與L酸分布(見表2),合成DMEG的EO轉(zhuǎn)化率達到96.6%,DMEG選擇性(表中為含量)為42.6%。在Cs2.5PW負載量為30%(w)時,催化劑上EO完全轉(zhuǎn)化,DMEG選擇性達到62.6%,二聚產(chǎn)物Diox、異構產(chǎn)物乙醛及多聚產(chǎn)物含量少。這是由于Cs2.5PW在DUSY表面極大分散,提高了利用效率,因而酸量較大,同時適宜的B酸與L酸分布協(xié)同催化效果明顯;較大的催化劑孔徑使得生成的DMEG快速離開催化劑表面,因而EO自聚、異構及多聚產(chǎn)物少,DMEG選擇性高。對其他wCs2.5PW/DUSY催化劑試樣來說,無論Cs2.5PW負載量升高或降低,催化劑酸量均降低,EO轉(zhuǎn)化率均下降,說明EO開環(huán)活性與催化劑酸量有關,酸量小,EO開環(huán)活性低。
2.5.2 氣態(tài)空速的影響
圖3為GHSV對合成DMEG反應的影響。

圖3 GHSV對合成DMEG反應的影響Fig.3 Effect of GHSV on DMEG synthesis.Reaction conditions:30%Cs2.5PW/DUSY,80 ℃,n(DME) :n(EO) = 3,0.70 MPa,30 h.■ Conversion of EO;● Selectivity to DMEG;▲ Selectivity to DMDG;▼ Selectivity to DMTrG;? Selectivity to Diox EO:ethylene oxide;DMEG:dimethylether ethylene glycol;DMDG:dimethyl etherdiethyleneglycol;DMTrG:dimethyl ethertriethyleneglycol;Diox:1,4-dioxane.
GHSV低,EO在催化劑表面停留時間長,EO轉(zhuǎn)化率高,生成的DMEG不能快速擴散離開催化劑表面,而進行連串反應生成DMDG及DMTrG。GHSV高,EO在催化劑表面停留時間短,導致EO異構與聚合產(chǎn)物多、聚產(chǎn)物Diox含量高、EO異構產(chǎn)物與EO繼續(xù)反應等,使產(chǎn)物含量增高,表現(xiàn)為DMEG選擇性降低;EO與催化劑接觸時間短、轉(zhuǎn)化率低,未反應的EO由于安全性低難于循環(huán)使用,進入尾氣后對環(huán)境危害很大。因此,取GHSV =1 800 h-1最適宜,環(huán)氧乙烷完全轉(zhuǎn)化,DMEG選擇性達到62.6 %,同時連串反應及自聚/異構副產(chǎn)物較少。
2.5.3 反應溫度的影響
圖4為溫度對合成DMEG反應的影響。由圖4可知,反應溫度為70 ℃時,EO轉(zhuǎn)化率為89.6%,DMEG選擇性為51.5%,Diox選擇性12.4%。反應溫度為90 ℃時,EO完全轉(zhuǎn)化,反應生成的DMEG在催化劑表面繼續(xù)進行連串反應,生產(chǎn)較多的DMDG及DMTrG,Diox選擇性為5.8%。低溫對EO聚合與異構有利,而反應溫度較高則對EO開環(huán)與DME生產(chǎn)DMEG有利。高溫時生成的DMEG繼續(xù)和EO反應生成DMDG與DMTrG。因次,適宜的反應溫度為80 ℃,該溫度下,EO完全轉(zhuǎn)化,產(chǎn)物DMEG選擇性達到62.6%,副產(chǎn)物少。
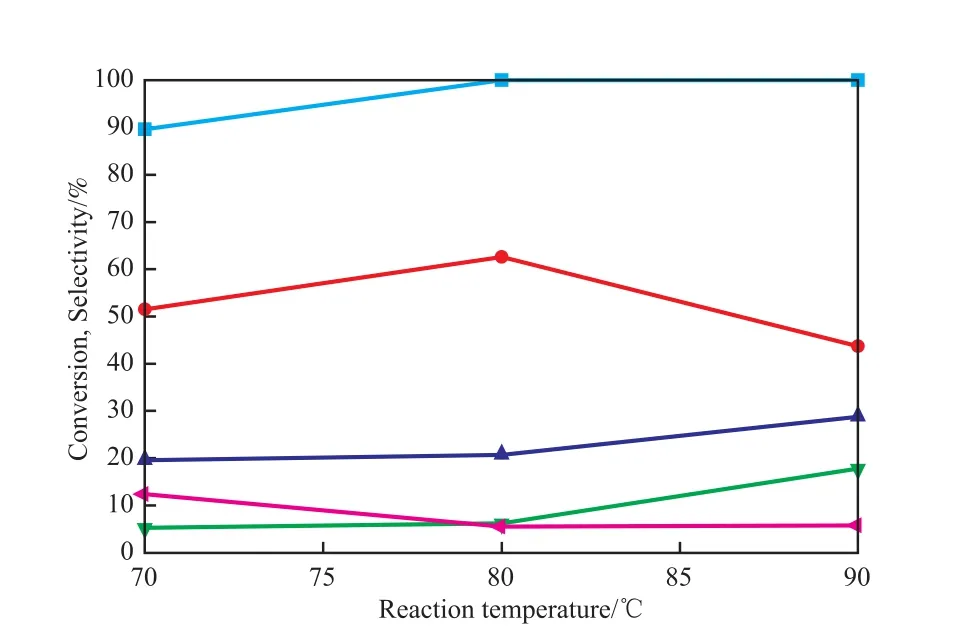
圖4 溫度對合成DMEG反應的影響Fig.4 Effect of reaction temperature on the synthetic activities.Reaction conditions:30%Cs2.5PW/DUSY,n(DME) :n(EO) =3,0.70 MPa,GHSV = 1 800 h-1,30 h.■ Conversion of EO;● Selectivity to DMEG;▲ Selectivity to DMDG;▼ Selectivity to DMTrG;? Selectivity to Diox
2.5.4 反應壓力的影響
圖5為反應壓力對合成DMEG反應的影響。由圖5可知,反應壓力0.50 MPa時,EO轉(zhuǎn)化率為99.2%,DMEG選擇性為40.1%,Diox選擇性達到24.3%。反應壓力為0.70 MPa時,EO完全轉(zhuǎn)化,DMEG選擇性達到62.6%,EO異構及二聚產(chǎn)物含量低。繼續(xù)升高反應壓力,DMEG的選擇性開始下降,DMDG和DMTrG含量則明顯增加。EO與DME生成DMEG過程,以及EO二聚過程均為體積縮小反應,升高壓力有利于反應平衡向生成產(chǎn)物方向移動,然而由于原料中DME過量,因而不同壓力對EO反應方向的影響程度不同[13]。反應壓力低,有利于EO異構反應與自聚反應,產(chǎn)物中Diox及異構產(chǎn)物乙醛等含量多。反應壓力高,對EO開環(huán)插入DME反應生成DMEG有利,表現(xiàn)為DMEG選擇性高。繼續(xù)升高反應壓力,EO及DME液化現(xiàn)象嚴重,產(chǎn)物DMEG在催化劑表面油膜增厚,不利于產(chǎn)物向催化劑外擴散,使得體系中DMDG和DMTrG含量增多;高壓對設備耐壓及體系的安全性要求也隨之提高。因此,優(yōu)選反應壓力為0.70 MPa。

圖5 反應壓力對合成DMEG反應的影響Fig.5 Effect of pressure on the synthetic activities for dimethoxyethaneonreaction.Reaction conditions:30%Cs2.5PW/DUSY,n(DME) :n(EO) = 3,80 ℃,GHSV = 1 800 h-1,30 h.■ Conversion of EO;● Selectivity to DMEG;▲ Selectivity to DMDG;▼ Selectivity to DMTrG;? Selectivity to Diox
2.5.5 催化劑的穩(wěn)定性
圖6為催化劑使用時間對合成DMEG反應的影響。

圖6 催化劑使用時間對合成DMEG反應的影響Fig.6 Effect of catalyst life on synthetic activities for DMEG.Reaction conditions:30%Cs2.5PW/DUSY,n(DME) :n(EO) = 3,80 ℃,0.70 MPa,GHSV = 1 800 h-1.■ Conversion of EO;● Selectivity to DMEG;▲ Selectivity to DMDG;▼ Selectivity to DMTrG;? Selectivity to Diox
由圖6可知,催化劑使用30 h時,EO完全反應,DMEG選擇性為62.6%,DMDG選擇性為20.7%,Diox及異構產(chǎn)物含量低;催化劑使用180 h時,催化劑保持EO完全轉(zhuǎn)化的高活性,產(chǎn)品DMEG選擇性維持在60%,副產(chǎn)物含量沒有明顯變化;催化劑使用240 h時,EO轉(zhuǎn)化率為98.1%,DMEG選擇性為54.3%,Diox及乙醛等異構產(chǎn)物含量顯著增大。Cs2.5PW在DMEG中的不溶性[13]、Cs2.5PW與DUSY的強相互作用及DUSY載體自身可轉(zhuǎn)換的B酸與L酸協(xié)同催化,使得催化劑在使用較長時間后仍然表現(xiàn)出較高的DMEG選擇性,可見,催化劑性能穩(wěn)定。
3 結(jié)論
1)系列催化劑試樣與DUSY載體發(fā)生了強相互作用,在DUSY表面高度分散,且保持較高相對結(jié)晶度,并保持完整Y沸石的孔道結(jié)構,結(jié)構沒有坍塌。
2)在Cs2.5PW負載量為30%(w)時,Cs2.5PW在DUSY表面呈現(xiàn)最大分布,催化劑試樣的NH3吸附量可達618 μmol/g,B酸與L酸吸附量分別為350,268 μmol/g。
3)30%Cs2.5PW/DUSY催化劑用于EO與DME合成DMEG反應,在n(DME) :n(EO)= 3,80 ℃,GHSV = 1 800 h-1,0.70 MPa,反應30 h的最優(yōu)條件下,EO完全轉(zhuǎn)化,DMEG選擇性達62.6%;連續(xù)反應240 h后,EO轉(zhuǎn)化率達98.1%,DMEG選擇性未見下降,催化劑保持著較好活性。
[1] Lee B. Solubility of carbon dioxide in poly(ethylene glycol)dimethyl ether[J].Korean Chem Eng Res,2017,55(2):230-236.
[2] 劉云霞. 聚合物電解液添加劑對鋰硫電池性能的影響[J].電源技術,2016,40(6):1194-1195.
[3] Sun S,Xu Q,Lan G,et al. Solubility of dilute sulfur dioxide in binary mixtures of ethylene glycol and tetraethylene glycol dimethyl ether[J].Fluid Phase Equilib,2015,394(1):12-18.
[4] Qiao Ke,Wei Linjiao,F(xiàn)eng Rui,et al. Preparation and characterization of hierarchical USY by post-treatment[J].Appl Petrochem Res,2015,5(4):313-319.
[5] 王希龍,宋金娜,葉修群,等. 超細NaY分子篩的深度脫鋁[J].催化學報,2012,33(7):1217-1223.
[6] 黃朝暉,劉乃旺,姚佳佳,等. USY分子篩表面酸性的調(diào)變及其在催化脫除芳烴中烯烴的應用[J].化工進展,2016,35(1):138-144.
[7] Cromwell D,Vasudevan P,Pawelec B,et al. Enhanced methylcyclohexanedehydrogenation to toluene over Ir/USY catalyst[J].Catal Today,2016,259(1):119-129.
[8] Aelst V,Philippaerts A,Turner S,et al. Heterogeneous conjugation of vegetable oil with alkaline treated highly dispersed Ru/USY catalysts[J].Appl Catal,A,2016,526(1):172-182.
[9] 張富民. 雜多化合物催化劑的制備及其催化性能[D].南京:南京工業(yè)大學,2006.
[10] Joost V,Mohamed H,Elena G,et al. Hierarchization of USY zeolite by NH4OH:A postsyntheticprocess investigated by NMR and XRD[J].J Phys Chem C,2014,118(46):27182-27182.
[11] Qi Long,Alamillo R,Elliott W,et al. Operando solid-state NMR observation of solvent-mediated adsorption-reaction of carbohydrates in zeolites[J].ACS Catal,2017,7(5):3489-3500.
[12] Sosa A,Gorsd M,Blanco M,et al. Synthesis and characterization of tungstophosphoric acid-modified mesoporous silica nanoparticles with tuneable diameter and pore size distribution[J].J Sol-Gel Sci Technol,2017,83(2):355-364.
[13] 于清躍. 環(huán)氧乙烷醚化反應及CNT增強環(huán)氧樹脂性能研究[D].南京:南京林業(yè)大學,2017.
(編輯 楊天予)
Synthesis of dimethoxyethaneover cesium phosphotungstate supported on dealuminated ultra stable Y zeolite catalyst
Yu Qingyue1,Zhang Yunliang1,Sun Fei2,Zhu Xinbao3
(1. College of Chemical amp; Material Science,Nanjing Polytechnic Institute,Nanjing Jiangsu 210048,China;2. Nanjing Anding Chemical Science amp; Technology Ltd.,Nanjing Jiangsu 210048,China;
3. College of Chemical Engineering,Nanjing Forestry University,Nanjing Jiangsu 210037,China)
The catalyst for synthesis of dimethoxyethane(DMEG) with ethylene oxide(EO) and dimethyl ether(DME) on one-step way in fixed-bed is prepared by cesium phosphotungstate(Cs2.5PW)supported on ultra-stable Y zeolite water vapor dealumination. The catalyst is characterized by XRD,31P NMR,29Si NMR,N2adsorption-desorption and FTIR. The result shows that cesium phosphotungstate takes a great interaction with dealuminium ultra stable Y zeolite(DUSY). Cs2.5PW presents highly distribution on the supporter when the loading amount reaches 30%(w). The N2adsorption of catalyst reaches 618 μmol/g. When optimal conditions are mole ratio DME to EO of 3,reaction temperature 80 ℃,reaction pressure 0.70 MPa,and mixed gaseous hourly space velocity of 1 800 h-1,the reaction shows that conversion of EO is 100.0%,and yield of dimethoxyethane 62.6%.When the catalyst continuous works 240 h,conversion of EO is 98.1% and selectivity of main product keeps no decreasing significantly.
ethylene oxide;dimethyl ether;dimethoxyethane;cesium phosphotungstate
1000-8144(2017)11-1366-07
TQ 426.6
A
10.3969/j.issn.1000-8144.2017.11.004
2017-07-10;[修改稿日期]2017-08-01。
于清躍(1970—),男,江蘇省海安縣人,博士,副教授,電話 13182920069,電郵 qingyueyunj@126.com。
江蘇高校科研產(chǎn)業(yè)化項目(JHZD2012-15);江蘇“青藍工程”基金項目;江蘇高校校長基金資助項目;骨干教師境外研修(2013)基金資助項目。

