成人型成骨不全并發心臟瓣膜病1例
趙琳琳 欒毅 何紅
成人型成骨不全并發心臟瓣膜病1例
趙琳琳 欒毅 何紅
患者男,37歲。因“反復心悸伴胸口隱痛3年”于2016年12月28日至我科門診就診。既往曾有多次不明原因骨折:足月順產,出生時未見異常,發育與正常兒童無異,30年前第一次骨折,左側前臂骨折,外固定處理,恢復良好;此后(7~16歲)無暴力下出現骨折共累計6次,部位限于雙側脛腓骨和骨盆,最嚴重的2次分別發生于右側脛腓骨和右側尺骨鷹嘴部,均采取手術治療;1年前因交通意外造成肋骨骨折。否認高血壓糖尿病史,否認風濕熱及藥物濫用史,否認吸煙史。父親骨折3次(具體不詳),主動脈瓣重度反流;母親體健;弟弟無類似骨折病史;配偶體健;育有1子(目前8歲),自幼受外力后易骨折。體格檢查:神志清,血壓132/72mmHg,心率 85次 /min,呼吸 18次/min,體溫 37℃,身高 163cm,體重 65kg,鞏膜淺藍,瞳孔等大等圓,聽力正常,牙本質較好,口唇無紫紺,全身淺表淋巴結無腫大。頸靜脈無充盈怒張,胸廓無畸形,脊柱無側彎,兩肺呼吸音清晰,心界無明顯擴大,心尖部觸及震顫,可聞及4/6級收縮期雜音,呈吹風樣,心律齊,腹部軟,肝脾未及腫大,四肢無畸形,無水腫。輔助檢查:血常規,肝腎功能,堿性磷酸酶,血中微量元素,凝血功能,血沉等未見明顯異常。血脂:TC 6.32mmol/L,TG 5.51mmol/L,HDL-C 1.06mmol/L,LDL-C 4.11mmol/L。常規十二導聯心電圖:竇性心律,左心室高電壓。胸部X線平片:兩肺紋理大致正常,未見實變;經胸超聲心動圖:二尖瓣后葉脫垂,考慮小腱索斷裂,致對合不攏;二尖瓣中量反流(圖1);基因檢測結果(圖2):成骨不全(osteogenesis imperfecta,OI),外周血基因組SNA測序發現致病基因為COL1A1,致病突變位于基因COL1A1外顯子45,突變為c.3269delC,該突變可能導致COL1A1基因第1090以后發生移碼和蛋白質截短(p.Gln1090Lysfs*18)。先證者本人為該突變的雜合子,其父親也攜帶相同突變。
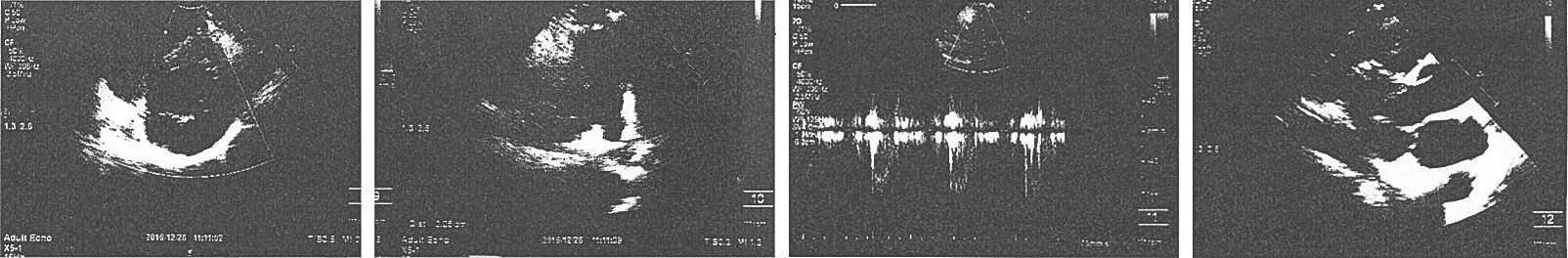
圖1 患者超聲心動圖表現

圖2 患者及其父親基因診斷結果
根據以上檢查結果,診斷為“OI伴心臟瓣膜病、高脂血癥”,予以琥珀酸美托洛爾緩釋片(47.5mg/片,阿斯利康制藥有限公司)口服控制心室率,阿司匹林腸溶片(100mg/片,拜耳醫藥保健有限公司)口服抗血小板聚集,輔以輔酶Q10營養心肌等對癥支持治療。因該患者無明顯心功能不全癥狀,且心超提示二尖瓣中量反流,左心室舒張末期內徑(LVEDd)為53mmm,左心室射血分數(LVEF)65%;未見有癥狀的重度二尖瓣反流和(或)左心室收縮功能障礙,且心超結果不符合LVEDd>70mm,左心室舒張末期容量指數(LVDEVI)>200ml/m2,LVEF <50% 等 條件,目前暫無外科手術指征。建議離院后定期復查心超,長期隨訪。
討論OI又稱脆骨病,是一組以骨骼脆性增加及膠原代謝紊亂為特征的全身性結締組織疾病。其臨床表現為骨脆性增加、骨關節進行性畸形等癥狀,還常常累及其他結締組織,臨床十分罕見。OI是一種常染色體遺傳的先天性疾病,系由于多基因異常突變導致中胚層發育異常而使間充質組織發育不全、膠原形成障礙而造成的罕見遺傳性疾病。90%的OI是編碼I型膠原的基因COL1A1或COL1A2發生突變而引起的常染色體顯性遺傳疾病,其余OI則主要是由于調節I型膠原基因轉錄或翻譯的基因(CRTAP、LEPRE1、PPIB、SERPINH1、FKBPIO 等) 發生突變所致。傳統將OI分為Ⅰ~Ⅳ型,Glorieux、Ward、Cabral[1]等結合遺傳缺陷特點又將5種罕見的亞型歸入其中,將其改良為9種亞型,使得OI的分型逐漸趨于完善(表1)。
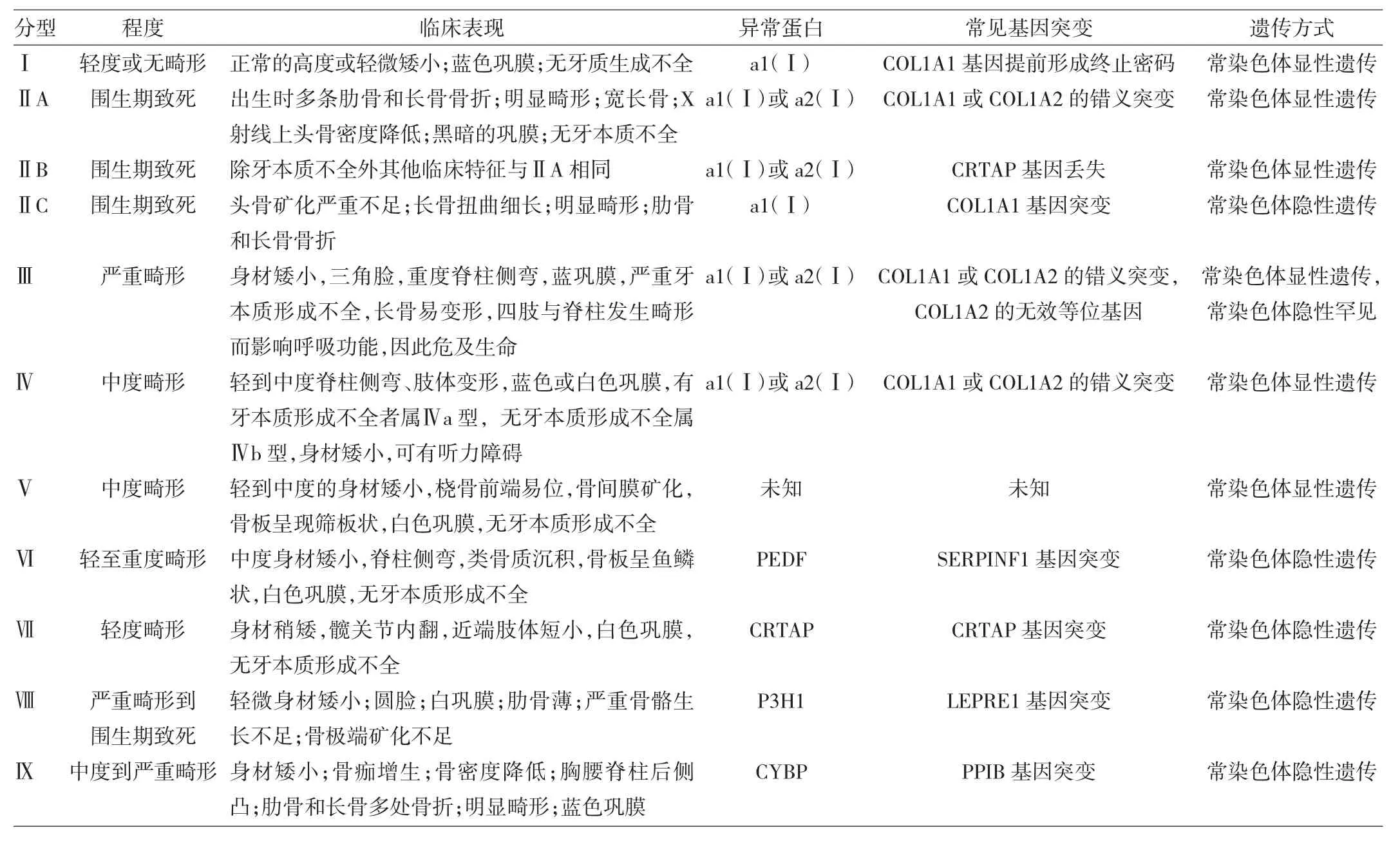
表1 OI的新分類
目前治療OI主要是通過藥物或進行外科手術,但隨著遺傳學的發展,基因治療及干細胞移植將成為治療該病的根本途徑和主要研究熱點。最新的研究發現將基因靶向定位(genetargeting)和誘導多能干細胞(iPSC)分化相結合可產生能生成正常膠原蛋白的特異性骨形成細胞,有望用于治療OI[2]。
然而OI病變不僅限于骨骼,還常常累及其他結締組織如眼、耳、牙齒、皮膚等,其特點是藍鞏膜、聽力下降、牙本質發育不全及皮膚異常。同時,該病也是心臟瓣膜病的罕見病因之一,臨床主要表現為主動脈瓣、二尖瓣反流,主動脈根部增寬以及因此而繼發的血流動力學改變。本例患者為中青年男性,既往7~8次不明原因骨折,查體:藍鞏膜,體型矮小。輔助檢查基因檢測提示COL1A1突變,導致蛋白質截短,提示終止密碼子形成,可診斷為OI(Ⅰ型),另患者因合并心臟瓣膜病,排除其他病因如高血壓病,風濕性心瓣膜病,考慮OI并發心臟瓣膜病。本例OI合并二尖瓣脫垂,是OI伴發心臟瓣膜病臨床中頗為罕見的類型之一。國內有關案例經驗相對缺乏,國外也僅有個例伴發二尖瓣脫垂的報道,這些個體患有感染性心內膜炎(IE)的風險增加10~100倍。眾所周知,IE患者的病死率較高(10%~30%)[3-4],故二尖瓣脫垂患者積極預防IE尤為重要,美國心臟協會強調需保持良好的口腔衛生,積極根除牙病,同時保留對預后不良或高危患者抗生素的預防治療[4]。另外,據挪威OI注冊表中99例患者瓣膜病的報告顯示:有10.1%輕度和10.1%中度主動脈瓣關閉不全,57.5%輕度和7.1%中度二尖瓣反流[5]。此外,OI不僅僅累及心臟瓣膜,近年有新研究表明,其對心室結構和功能也具一定影響:成人OI患者左心室及右心室的舒縮功能較對照組均降低,根據回歸分析顯示,OI是一個重要獨立的危險因素作用于右室心肌功能[6]。
雖然心臟瓣膜異常在OI中較為少見,但若合并嚴重的瓣膜性心臟病者,則需行人工瓣膜置換術或瓣膜成形術。此時,心臟手術病死率和并發癥發病率的增加又與OI相關。OI患者行心臟外科手術的風險增加15%~25%,其原因是由于潛在的結締組織疾病,引起組織和毛細血管脆性增加、血小板功能障礙、凝血機制異常等,從而導致大量出血或傷口愈合欠佳、遲緩[7-8]。上世紀90年代,OI患者行心外科手術的存活率不容樂觀,據Thibault[9]報道的20例OI合并心臟瓣膜病患者,13例行心外科手術治療,其中6例死于術后早期,4例行心臟瓣膜置換術者只有l例存活。隨著醫學研究的發展、前沿技術的不斷涌現,術者們不斷學習提高累積經驗且樂于互相交流,現如今,局勢較前有一定改善,然術后并發癥的現象仍層出不窮。據2013年Najib等[8]報道的5例OI合并心臟瓣膜病的男性患者中,平均年齡為48.6歲,其中3例行主動脈瓣置換術(AVR),1例行AVR和二尖瓣修復成形術,另1例行二尖瓣修復成形術。手術過程中大多數患被注意到存有松散組織和出血的情況,術后5例患者LVEF均較前下降,其中1例需要植入雙腔埋藏式除顫儀。由此可知,組織脆性和手術過程止血困難依然是外科治療所面臨的挑戰。雖有文獻報道OI患者行二尖瓣膜置換術生物瓣安全性優于機械瓣,但由于個體差異不同,外科術前仍需仔細評估與思考[10]。同時,OI患者術后心功能的改善、并發癥的減少、存活率的上升及生活質量的提高也是臨床治療中可掌握和發展的新機遇。
[1]周琦,白露.成骨不全的相關研究進展[J].現代預防醫學,2014,41(3):572-575.
[2]Deyle D R,Khan I F,Ren G,et al.Normal collagen and bone production by genetargeted human osteogenesis im-perfecta iPSCs[J].Mol Ther,2012,20(1):204-213.doi:10.1038/mt.2011.209.
[3]Que Y-A,Moreillon P.Infectious endocarditis[J].Nat Rev Cardiol2011,8:322-336 doi:10.1038/nrcardio.2011.43
[4]Vandersteen A M,Lund A M,Ferguson D J,et al.Four patients with Sillence type I osteogenesis imperfecta and mild bone fragility,complicated by left ventricular cardiac valvular disease and cardiac tissue fragility caused by type I collagen mutations[J].Am J Med Genet A,2014,164A(2):386-391.doi:10.1002/ajmg.a.36285.
[5]Radunovic Z,Wekre L L,Diep L M,et al.Cardiovascular abnormalities in adults withosteogenesis imperfecta[J].Am Heart J,2011,161(3):523-529.doi:10.1016/j.ahj.2010.11.006.
[6]Radunovic Z,Steine K.Prevalence ofCardiovascular Disease and Cardiac Symptoms:Left and Right Ventricular Function in Adults With Osteogenesis Imperfecta[J].Canadian Journal of Cardiology,2015,31(11):1386-1392.doi:10.1016/j.cjca.2015.04.016.
[7]Dimitrakakis G,Pericleous A,Dimitrakaki I A.Osteogenesis imperfecta in cardiac surgery[J].Asian Cardiovascular and Thoracic Annals,2013,21(1):116-117.doi:10.1177/0218492312463149.
[8]Najib MQ,Schaff H V,GanjiJ,et al.Valvular Heart Disease in Patients with Osteogenesis Imperfecta[J].2013,28(2):139-143.doi:10.1111/jocs.12064.
[9]Thibault G E.Clinical problem-solving.The heart of the matter[J].N Engl J Med,1993,329(19):1406-1410.doi:10.1056/NEJM199311043291909.
[10]Dimitrakakis G,Challoumas D,von Oppell U O.What type of valve is most appropriate for osteogenesis imperfecta patients?[J].Interactive Cardio-Vascular and Thoracic Surgery,2014,19(3):499-504.doi:10.1093/icvts/ivu152.
10.12056/j.issn.1006-2785.2017.39.22.2016-1007
310016 杭州,浙江大學醫學院附屬邵逸夫醫院心內科
何紅,E-mail::hehong179@163.com
2017-05-03)
沈昱平)

