不同劑量人臍帶間充質干細胞移植治療MS效果觀察
楊幸文,路青山,楊霄鵬,陳夢茹,豐雪
(1鄭州大學第二附屬醫院,鄭州450000;2鄭州市第一人民醫院)
不同劑量人臍帶間充質干細胞移植治療MS效果觀察
楊幸文1,路青山2,楊霄鵬1,陳夢茹1,豐雪1
(1鄭州大學第二附屬醫院,鄭州450000;2鄭州市第一人民醫院)
目的對比觀察不同劑量人臍帶間充質干細胞(hUC-MSC)移植治療多發性硬化(MS)的臨床效果。方法將60例MS患者隨機均分為A、B、C、D組。從足月健康新生兒臍帶中提取hUC-MSC;各組均采用BEAM方案(卡莫司汀、替尼泊苷、阿糖胞苷、美法侖)進行預處理。A、B、C組采用腰椎穿刺術經蛛網膜下腔分別注射hUC-MSC 1.5×106/kg、7.5×106/kg、15×106/kg,D組給予相同體積生理鹽水。每2周移植1次,共移植3次。治療前后采用擴展致殘狀況評分量表(EDSS)對患者神經功能缺損程度進行評分,采用MR檢查頭顱、脊髓病灶數量及病灶體積變化,統計患者治療期間發生的不良反應。結果與治療前比較,治療后A、B、C組EDSS較D組低(P均<0.05),且C組 多發性硬化;人臍帶血間充質干細胞;干細胞移植 多發性硬化(MS)是一種自身免疫性疾病,其主要病理特點是中樞神經系統白質炎性脫髓鞘病變,致殘率較高。大多數MS患者表現為反復發作的神經功能障礙。目前MS的治療效果仍不樂觀。人臍帶間充質干細胞(hUC-MSC)是一種具有自我更新、多向分化潛能的成體干細胞。研究表明,hUC-MSC移植能有效緩解MS的癥狀[1~3]。同時,由于hUC-MSC具有來源豐富、取材簡單、培養條件方便、能夠通過血-腦脊液屏障、避免出現倫理問題等優點,引起了臨床的關注。但hUC-MSC最佳移植劑量仍未見報道。目前認為間充質干細胞(MSC)發揮有效免疫調節作用的輸注劑量為(1.0~2.0)×106/kg[4]。本研究對不同劑量hUC-MSC移植治療MS的效果進行對比。 1.1 臨床資料 選取2015年6月~2017年3月于鄭州大學第二附屬醫院及鄭州市第一人民醫院就診的MS患者60例,均符合MS的診斷標準[5]。其中,男27例、女33例,年齡18~60歲、中位年齡36歲,病程12~130個月、中位病程37個月。納入標準:近2年行常規抗炎治療無效,病情最嚴重時EDSS 3.0~7.0分;無感染病灶;入院肺、肝、脾、心、腎功能檢查無明顯異常;女性患者均為非妊娠期。患者均簽署知情同意書,經醫院倫理委員會批準。將患者隨機均分為A、B、C、D組。四組臨床資料具有可比性。 1.2 hUC-MSC提取方法 在無菌條件下,取足月正常分娩、排除傳染性疾病及家族遺傳性疾病的新生兒臍帶。剝離臍帶動脈和靜脈后,將剩余的臍帶組織用去血清的F12培養基清洗殘留血液,用無菌剪刀剪成肉糜樣大小的組織塊。用PBS充分沖洗至組織塊發白后放入50 mL離心管中,離心去除組織塊表面的黏液,將其轉移至培養皿中,加入雙抗的F12培養基和10%胎牛血清后置于37 ℃、5% CO2培養箱中培養,期間重復上述清洗過程3遍以上,直至完全清除臍帶組織表面的黏液。待細胞從組織塊周圍游出進行傳代培養,培養至第5代。用生理鹽水洗滌細胞3次,調至1.0×106/μL備用。 1.3 hUC-MSC移植方法 各組采用BEAM方案(卡莫司汀300 mg/m2、1 d,替尼泊苷150 mg/m2、1~4 d,阿糖胞苷200 mg/m2、1~4 d,美法侖140 mg/m2、1 d)進行預處理。用腰椎穿刺術行蛛網膜下腔注射,穿刺成功后緩慢注入hUC-MSC懸液。A、B、C組每次注射劑量分別為1.5×106/kg、7.5×106/kg、15×106/kg[4],D組每次給予相同體積的生理鹽水。術后去枕平臥6 h。每2周移植1次,共移植3次[1]。移植治療期間各組給予常規抗炎治療。 1.4 指標觀察方法 ①治療前后采用擴展致殘狀況評分量表(EDSS)[6]對患者各個系統(感覺、直腸和膀胱、小腦、腦干、大腦神經功能及總體功能等)神經功能缺損程度進行評價[7],得分越高說明神經功能缺損越嚴重。②治療前后采用MR檢查頭顱、脊髓病灶數量及病灶體積變化。③統計患者治療期間發生的不良反應。 2.1 各組治療前后EDSS比較 治療前各組EDSS比較差異無統計學意義(P>0.05);治療后D組EDSS較治療前無明顯變化(P>0.05),A、B、C組EDSS較D組低(P均<0.05),且C組 表1 各組治療前后EDSS比較(分 2.2 各組頭顱和脊髓病灶數目、體積比較 治療前各組病灶數目及體積比較差異無統計學意義(P均>0.05);治療后D組病灶數目及體積均較治療前增多,但比較差異無統計學意義(P均>0.05);治療后A、B、C組病灶數目及體積均較D組小(P均<0.05),且C組 表2 各組治療前后MR檢查結果比較 2.3 不良反應 治療過程中B、D組各出現1例低等發熱,經對癥處理后均于3 d內恢復正常。 MS主要特征是大腦與脊髓內播散的脫髓鞘病變,并伴有軸索的損害。目前,公認MS發病的重要因素是遺傳因素、自身免疫及感染等。其中,在免疫因素中T細胞、B細胞等免疫細胞通過釋放多種細胞因子參與炎癥反應,從而實現免疫調節。細胞因子既可以參與髓鞘的損壞又可以參與調節異常的自身免疫反應,從而在MS的發病機制中起重要作用。近年來,多項研究證明,MSC移植促進髓鞘再生,能有效治療MS[8~14]。其可能的作用機制:MSC的免疫調控功能可抑制與IL-15及IL-2相關的NK細胞增殖,從而抑制炎性因子前列腺素E2、TNF-γ等的分泌[15];調節B淋巴細胞的增殖、趨化及抗體分泌;抑制DC的分化,削弱其對B淋巴細胞的刺激及DC的抗原遞呈作用;抑制T細胞增殖,但并不引起T淋巴細胞凋亡和耐受;同時在活化的T淋巴細胞或炎性因子TNF-γ存在下可增加吲哚胺-2,3雙加氧酶的催化反應能力,進而減弱T細胞的分裂增殖能力。另外研究表明,MSC還可通過分泌具有調節免疫及營養神經的因子減輕中樞神經系統的炎癥反應,從而達到促進內源性髓鞘再生及保護神經的作用[16~18]。 hUC-MSC與其他MSC相比,免疫細胞幼稚、不易觸發免疫反應及引起移植物的抗宿主病,易采集、易保存和運輸,且采集時不會對產婦及新生兒產生危害及損傷,倫理學爭議少。目前hUC-MSC治療MS的小樣本臨床試驗已陸續開展,并初步證實該方案可行、安全、有效。目前關于不同數量hUC-MSC移植治療MS的臨床試驗還很少。本研究對比使用不同劑量hUC-MSC移植治療MS的效果,結果發現,治療后A、B、C三組EDSS均較治療前、對照組降低,且hUC-MSC移植治療劑量越高DESS評分降低越顯著;治療后A、B、C三組病灶數量及病灶體積均較治療前、對照組減少,且hUC-MSC移植治療劑量越高病灶數量及病灶體積減少越顯著。因此,在最新公約[4]認為的最佳移植劑量基礎上適當增加hUC-MSC移植劑量,治療MS效果更優。但由于本研究樣本小,未能探討求證達到最佳治療效果的移植劑量,尚需大樣本的臨床試驗進一步探討求證。hUC-MSC移植治療可能產生不良反應,常見的有發熱、中性粒細胞減少、注射部位疼痛、瘙癢等。本研究僅B、D組各出現1例低等發熱,其他兩組均無明顯不良反應發生。 綜上所述,應用hUC-MSC移植治療MS時,應根據患者自身情況制定個體化治療方案,根據患者的耐受情況,在hUC-MSC≤15×106/kg范圍內逐步增加其劑量,在盡可能降低并發癥發生率的同時達到更好的治療效果。 [1] Li JF, Zhang DJ, Geng T, et al. The potential of human umbilical cord-derived mesenchymal stem cells as a novel cellular therapy for multiple sclerosis[J]. Cell Transplant, 2014,23(Suppl 1):113-122. [2] 季興,李波,李瓊,等.臍帶間充質干細胞聯合利妥昔單抗治療多發性硬化癥30例臨床觀察[J].現代生物醫學進展,2013,13(17):3307-3310. [3] 張敏,楊萬章,盛佑祥,等.臍血源神經干細胞治療多發性硬化的療效及安全性評價[J].實用預防醫學,2008,15(4):1186-1188. [4] Freedman MS, Bar-Or A, Atkins HL, et al. The therapeutic potential of mesenchymal stem cell transplantation as a treatment for multiple sclerosis: consensus report of the International MSCT Study Group[J]. Mult Scler, 2010,16(4):503-510. [5] Polman CH, Reingold SC, Banwell B, et al. Diagnostic criteria for multiple sclerosis: 2010 revisions to the Mc Donald criteria[J]. Ann Neurol, 2011,69:292-302. [6] Kurtzke JF. Rating neurologic impairment in multiple sclerosis: an expanded disability status scale (EDSS)[J]. Neurology, 1983,33(11):1444-1452. [7] 周紅雨,許瑞琴.用EDSS系統評價多發性硬化急性期糖皮質激素療效[J].華西醫學,2003,18(2):198-199. [8] 劉瑩.間充質干細胞移植治療多發性硬化的研究進展[J].中國組織工程研究,2012,16(10):1889-1892. [9] Martino G, Franklin RJ, van Evercooren AB, et al. Stem cell transplantation in multiple sclerosis: current status and future prospects[J]. Nat Rev Neurol, 2010,6(5):247-255. [10] Karussis D, Karageorgiou C, Vaknin-Dembinsky A, et al. Safety and immunological effects of mesenchymal stem cell transplantation in patients with multiple sclerosis and amyotrophic lateral sclerosis[J]. Arch Neurol, 2010,67(10):1187-1194. [11] Yamout B, Hourani R, Salti H, et al. Bone marrow mesenchymal stem cell transplantation in patients with multiple sclerosis: a pilot study[J]. J Neuroimmunol, 2010,227(1-2):185-189. [12] Kassis I, Grigoriadis N, Gowda-Kurkalli B, et al. Neuroprotection and immunomodulation with mesenchymal stem cells in chronic experimental autoimmune encephalomyelitis[J].Arch Neurol, 2008,65(6):753-761. [13] Tyndall A, EULAR Stromal Cell Translational Group. Mesenchymal stem cells for multiple sclerosis: can we find the answer[J]. Mult Scler, 2010,16(4):386. [14] Mohyeddin BM, Yazdanbakhsh S, Lotfi J, et al. Does mesenchymal stem cell therapy help multiple sclerosis patients? Report of a pilot study[J]. Iran J Immunol, 2007,4(1):50-57. [15] Mikaeili AE, Parivar K, Joghataei MT. Therapeutic effect of transplanted human Wharton's jelly stem cell-derived oligodendrocyte progenitor cells (hWJ-MSC-derived OPCs) in an animal model of multiple sclerosis[J]. Mol Neurobiol, 2014,49(2):625-632. [16] Munoz JR, Stoutenger BR, Robinson AP, et al. Human stem/progenitor cells from bone marrow promote neurogenesis of endogenous neural stem cells in thehippocampus of mice[J]. Proc Natl Acad Sci U S A, 2005,102(50):18171-18176. [17] Endo Y, Beauchamp E, Woods D, et al. Wnt-3a and Dickkopf-1 stimulate neurite outgrowth in Ewing tumor cells via a Frizzled3- and c-Jun N-terminal kinase-dependent mechanism[J]. Mol Cell Biol, 2008,28(7):2368-2379. [18] Neuhuber B, Timothy Himes B, Shumsky JS, et al. Axon growth and recovery of function supported by human bone marrow stromal cells in the injured spinal cord exhibit donor variations[J]. Brain Res, 2005,1035(1):73-85. 河南省醫學科技攻關計劃項目(201503089)。 楊霄鵬(E-mail:yaxipe39@126.com) 10.3969/j.issn.1002-266X.2017.37.021 R744.51 B 1002-266X(2017)37-0062-03 2017-07-06)1 資料與方法
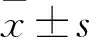
2 結果
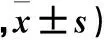
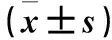
3 討論

