硫化銅微球電化學儲鋰性能研究
魏艷萍,張 穎,周 亞,李 婕,楊鵬舉
(河北工業大學化工學院,天津300130)
硫化銅微球電化學儲鋰性能研究
魏艷萍,張 穎,周 亞,李 婕,楊鵬舉
(河北工業大學化工學院,天津300130)
以硝酸銅[Cu(NO3)2·3H2O]和硫代乙酰胺(TAA)為原料,通過溶劑熱法制備中空球狀結構硫化銅。研究了中空微球樣品作為鋰離子電池負極材料的電化學性能。討論了焙燒溫度和焙燒時間等條件對硫化銅樣品的物相結構和電化學性能的影響。研究發現,焙燒后的硫化銅樣品的電化學性能表現良好,在0.1C電流密度下首次充放電比容量均超過了理論比容量(560mAh/g),其中焙燒溫度為150℃、焙燒時間為1 h的硫化銅樣品,其首次放電比容量達到682.8mAh/g,且循環25次后其比容量仍能保持在106.7mAh/g,表現出了良好的循環穩定性。
硫化銅;溶劑熱法;鋰離子電池;負極;中空球狀
Abstract:The copper sulfide(CuS)samples of hollow spheres were prepared by solvothermal synthesis method,with Cu(NO3)2·3H2O and TAA as raw materials.The electrochemical performance of hollow spheres samples was studied as anode materials for lithium ion batteries.The hollow calcinated samples composite exhibited a relative high reversible capacity and good cycling stability.The initial discharge specific capacity of the prepared CuS anode materials was 682.8mAh/g,even beyond the theoretical capacity(560mAh/g).After 25 cycles,the capacity remained 106.7mAh/g,and showed a good capacity retention during 0.1Crate cycles.
Key words:copper sulfide;solvothermal synthesis method;lithium-ion batteries;anode;hollow sphere
近二十年來,鋰離子電池作為一種新型能源,研究十分廣泛,與其他鋰離子電池相比,CuS具有高比能量、循環壽命長等優點[1]。硫化銅(CuS)材料作為一種重要的p型半導體,表現出很多的電子性能、光催化性能[2]及其他物理化學性能,在光學濾光片、超離子材料、太陽能控制器、太陽輻射吸收體及催化劑、納米級交換機及高容量的鋰離子電池負極材料[2-4]等很多應用中具有很大的潛力。CuS有較高的理論比容量為560mAh/g[5]和電導率(10-3S/cm)[6],價格低廉,制備簡單,備受關注。但因為其復雜的化學計量數所以種類很多,因此包含多種反應機理[7]。以Cu(NO3)2·3H2O和硫代乙酰胺為原料,通過溶劑熱法制備中空結構硫化銅,通過對其電化學性能的研究,對其進行相應改進。
1 實驗
1.1 CuS樣品的制備
分別稱取一定量的Cu(NO3)2·3H2O(分析純)和硫代乙酰胺(分析純),用無水乙醇溶解,然后將其轉移至高壓反應釜中,在120℃下恒溫一定時間(A為6 h,B為16 h)。然后將其進行離心分離,80℃干燥即得CuS樣品。
1.2 CuS樣品的改性
將制得的CuS樣品(S0)置于N2氣氛下焙燒,在90、120、150℃溫度下焙燒1 h得樣品S1,S2,SI,在150℃下焙燒樣品1、1.5、2 h 得 SI,SⅡ,SⅢ。
1.3 CuS/Li模擬電池的制備
按m(活性物質)∶m(乙炔黑)∶m(聚偏氟乙烯)=65∶20∶15準確稱取各物質,活性物質和乙炔黑混合研磨后。與溶于N-甲基吡咯烷酮的粘結劑聚偏氟乙烯(PVDF)充分攪拌至糊狀,均勻地涂覆在銅箔上。105℃下干燥1 h,經100 MPa碾壓3次,然后再經105℃烘1 h,100 MPa碾壓3次沖成10 mm的圓片。以研究樣品作為工作電極,金屬鋰片作為對電極,以1mol/L的LiPF6/(EC+DMC+EMC)(體積比為1∶1∶1)為電解液。Celgard2400雙層微孔聚丙烯膜為隔膜,在相對濕度5%以下的手套箱中組裝模擬電池。
1.4 材料表征和電化學性能測試
使用D8 Foucas型X射線衍射儀可以對樣品進行物相分析[Cu靶Kα衍射,λ=1.54056nm,管電壓為40.0 kV,管電流為40.0 mA,掃描速率為12(°)/min,2θ=10°~80°]。Nova Nano SEM450掃描樣品表面及內部形貌;分析樣品元素組成(15 kV 1.0nm;1 kV 1.4nm)。使用CT2001A LAND型電池測試系統對模擬電池進行恒流充放電測試 (電壓范圍為0.01~3.0 V)。使用CHI660C型電化學工作站進行電化學阻抗(EIS)和循環伏安(CV)測試,電化學阻抗測試頻率范圍為10 mHz~100 kHz,振幅5 mV,循環伏安測試電壓范圍0.01~3.0 V,掃描速率為0.1 mV/s。
2 結果與討論
2.1 反應時間
分別考察反應時間為6 h和16 h下的CuS樣品的XRD和SEM。CuS樣品特征衍射峰均與PDF卡片中CuS的標準譜圖 (JCPDS No.06-0464)一致,屬于六方晶系,空間群為P63/mmc,且沒有出現其他物質的特征衍射峰,說明該方法制得的CuS樣品純度較高。CuS晶體以(110)晶面為擇優取向生長。樣品B的衍射峰強要明顯高于樣品A,樣品B的結晶度優于樣品A。CuS晶體選擇這個晶面作為擇優生長方向有利于Li+的嵌入和脫出,如圖1所示[8]。樣品的a,c值均與標準樣品的值相近,誤差范圍在2.14%以內,這同樣表明樣品純度在該范圍內較高,如表1所示。
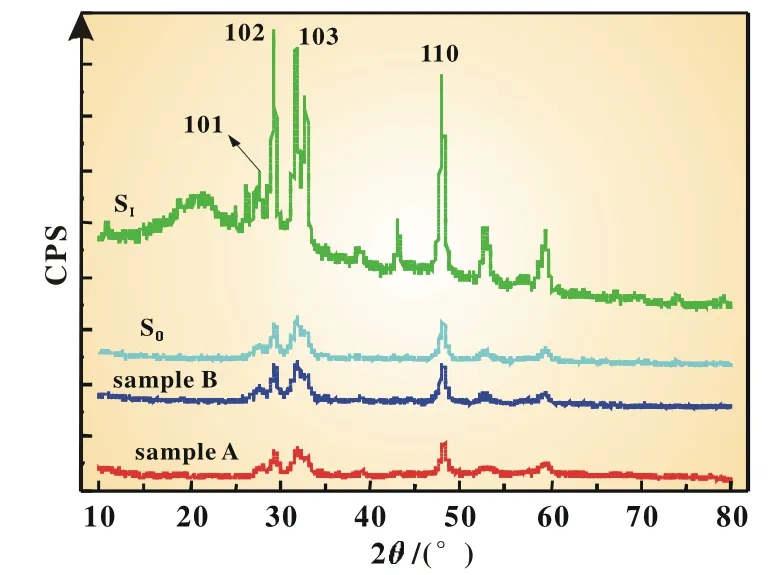
圖1 不同條件下制備CuS樣品的XRD圖
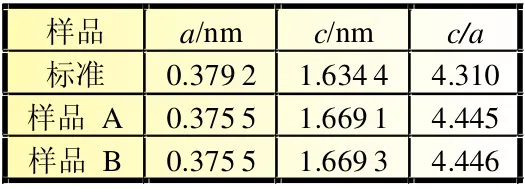
表1 CuS系列材料晶格參數
反應時間為6 h和16 h的CuS樣品一樣是有規則的幾何形狀,表現為中空微球結構。這說明所得產物具有完整的晶體結構,晶化程度較高[9]。其中樣品B的微球表面附著一些微小顆粒,這可能是因為隨著反應時間的延長,發生了團聚現象。其中有一些破裂的微球,這有利于鋰離子進入微球內部,并充分利用其內部的表面,有利于鋰離子的嵌入和脫出,提高電池容量,不同反應時間下CuS的SEM如圖2所示。

圖2 不同反應時間下CuS的SEM圖
AB兩個樣品的兩個放電平臺,分別對應以下電化學反應過程[10]:
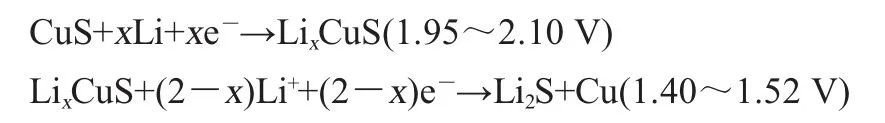
不同反應時間制得的兩種樣品的放電平臺都為2.0 V和1.5 V,這說明制得的樣品純度較高,這與XRD表征結果相符,如圖3所示。樣品B的循環性能要比樣品A穩定,容量衰減速率慢,這表明樣品B的穩定性較好,如圖4所示。
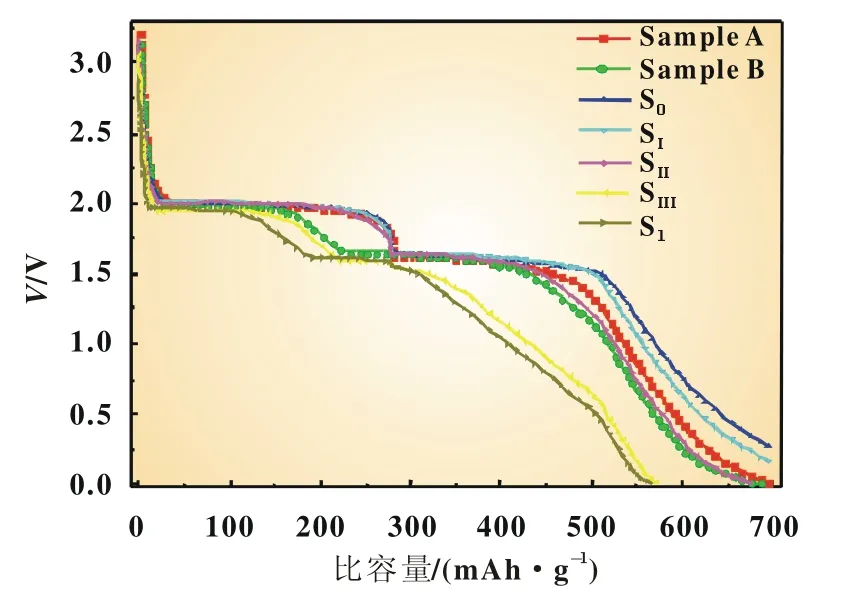
圖3 不同反應條件下CuS的首次放電曲線
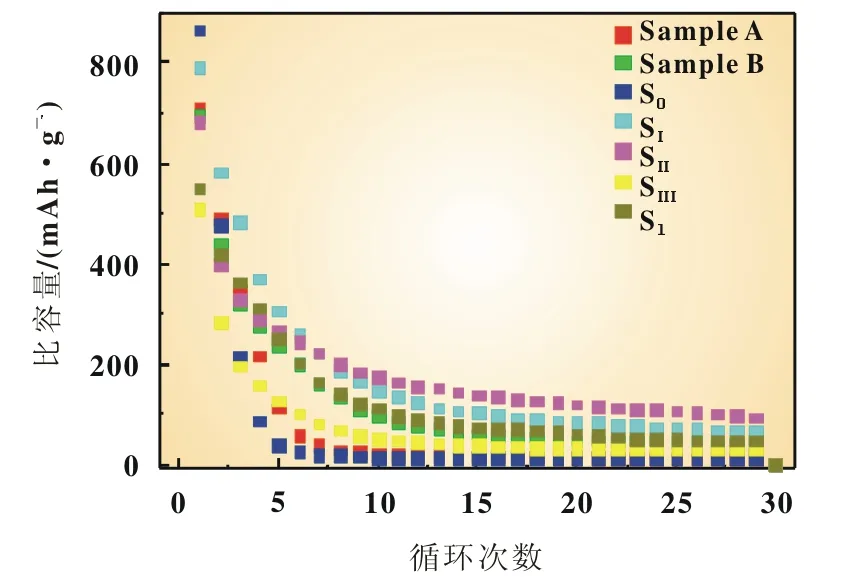
圖4 不同反應條件下CuS的循環性能
典型的CuS負極材料的電化學阻抗圖由四部分組成,分別是電解液電阻Re,電極表面膜電阻Rs,電化學反應電荷轉移阻抗Rct及鋰離子在活性材料體相的固體擴散過程相關的阻抗,即Warburg阻抗W[5]。反應時間為6 h(樣品A)和16 h(樣品B)的CuS樣品,在中頻區出現的壓縮半圓的半徑較小,也就是說電荷轉移的阻抗較小。兩個樣品的低頻區出現的直線斜率越接近45°,電化學阻抗較小,較為有利于鋰離子的擴散,如圖5所示。
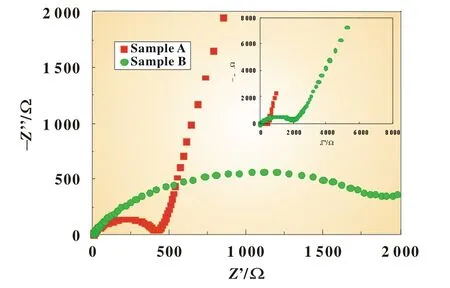
圖5 為不同反應時間下CuS的交流阻抗
為進一步考察電化學阻抗對電極材料的性能影響,對其進行擬合,電化學阻抗譜擬合所用等效電路如圖6所示。擬合數據如表2所示。
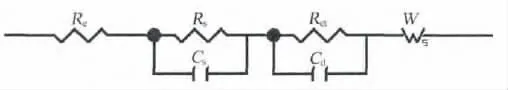
圖6 電化學阻抗譜擬合所用等效電路

表2 等效電路擬合所得動力學參數
兩個樣品的Re值都較為接近,且其值均較小,即表明鋰離子在電解液中的擴散阻抗較小。樣品B的Rct值和W值均較小,較為適合Li+的嵌入和脫出,也有利于電荷轉移,但其Rs值較大,即電極表面膜電阻較大,還有待改善,如表2所示。
圖7是CuS樣品在氮氣氣氛下,室溫~800℃的熱分析曲線,升溫速率為10℃/min。在100℃左右是第一個失重階段,TG曲線有少量的質量損失,對應DTA曲線出現相應的吸熱峰,這可能是失去吸附水造成的,失重率在3%左右。100~200℃是第二個失重階段,此階段可能是失去結晶水造成的。200℃以上時,失重率增加,這可能是因為CuS發生分解(分解溫度為220℃)造成的。鑒于以上數據,焙燒溫度不能超過200℃。
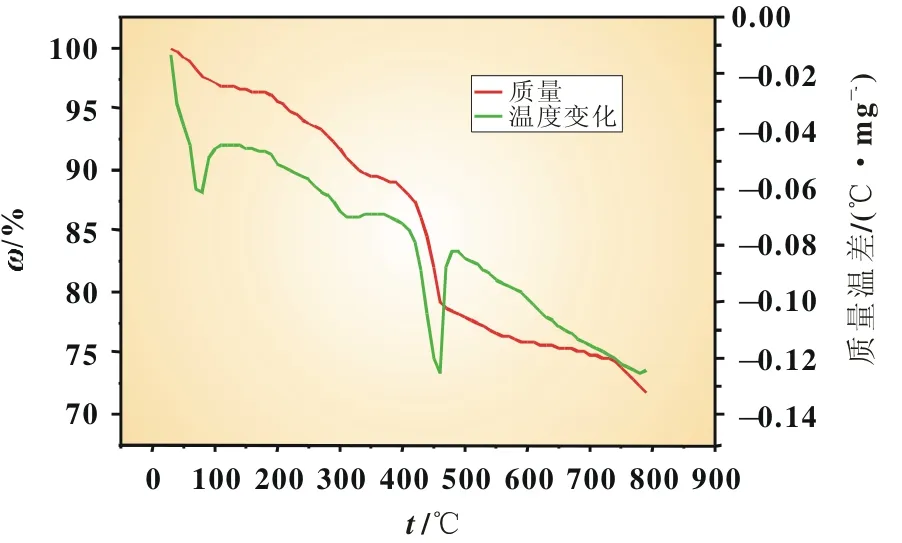
圖7 CuS樣品的TG-DTA曲線
2.2 焙燒溫度的影響
分別考察焙燒溫度為90℃(S1),120℃(S2)和150℃(SI)下CuS樣品的電化學性能。焙燒后的CuS樣品的首次放電比容量都較高,如圖3所示,在2.0 V和1.5 V附近有明顯平臺,未焙燒材料(S0)處于相同電位,說明焙燒未影響放電平臺,未引進其他雜質。前25周充放電測試,如圖4所示,樣品S3首次放電比容量為682.8mAh/g,但是第3、4、5次放電比容量下降較快,第6次后趨于穩定,這是由于所制備的硫化銅空心結構還不穩定,鋰離子的嵌入和脫出引起了結構不可逆的變化[11]。但在其后期循環性能良好,容量保持率較高,穩定性較好。循環至25次時,其比容量仍能保持在106.7mAh/g,明顯優于其他樣品。有報道認為,在硫化銅脫嵌鋰過程中,S8、Sx2和聚硫化物的生成存在隨機性并且多硫化物可溶于液態電解質[3,12],會導致循環性能的衰減,對其循環性能的改善還需進行更深入的研究。
典型的CuS負極材料的電化學阻抗圖由四部分組成,分別是電解液電阻Re,電極表面膜電阻Rs,電化學反應電荷轉移阻抗Rct及鋰離子在活性材料體相的固體擴散過程相關的Warburg阻抗W[13]。焙燒溫度為120℃(S2)和150℃(SI)的CuS樣品,在中頻區出現的壓縮半圓的半徑較小,也就是說電荷轉移的阻抗較小。兩個樣品的低頻區出現的直線斜率越接近45,電化學阻抗較小,較為有利于鋰離子的擴散,如圖8所示。
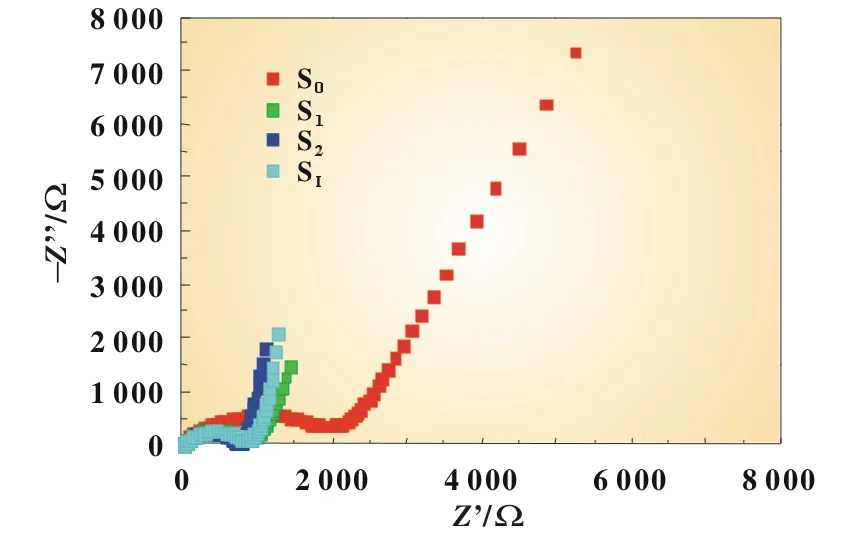
圖8 不同焙燒溫度下CuS的電化學阻抗
四個樣品的Re值都較為接近,且其值均較小,即表明鋰離子在電解液中的擴散阻抗較小。樣品S3的Rs值和Rct值均較小,較為適合Li+的嵌入和脫出,也有利于電荷轉移,但其W值較大,即鋰離子在固體中的擴散阻抗較大,還有待改善,如表3所示。
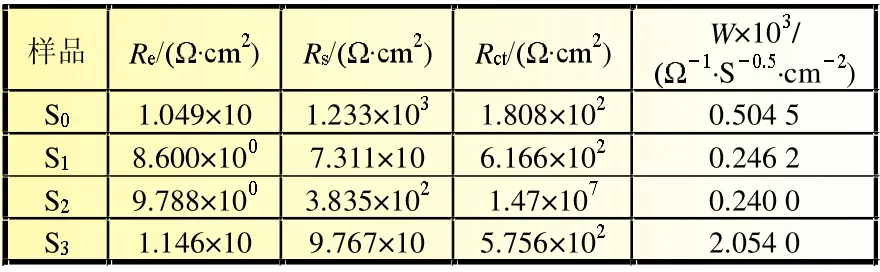
表3 等效電路擬合所得動力學參數
2.3 焙燒時間的影響
焙燒時間為1 h的CuS樣品(SI)的首次放電比容量較高,且其放電平臺明顯,分別在2.0 V和1.5 V附近。且兩個放電平臺都較長,有利于Li+的嵌入,如圖3所示。SⅡ和SⅢ兩個樣品的循環性都優于S0,衰減速率都比較緩慢,即容量保持率較好,其中焙燒時間為1 h的樣品容量保持效果更為良好,如圖4所示。綜合考慮,焙燒時間為1 h的CuS樣品的效果更佳。
2.4 焙燒前后結構和性能對比
分別考察了焙燒溫度、焙燒時間對CuS電極材料的電化學性能的影響。得出焙燒溫度為150℃,焙燒時間為1 h的樣品的電化學性能最佳即樣品SI。
比較未焙燒樣品S0和SI的CV曲線如圖9所示,可知兩個樣品的出峰位置相似,氧化峰均在1.3~2.1 V之間,還原峰均在1.8~2.5 V之間,二者峰電流都較小,但峰電位差較大,即表明電池存在一定的不可逆容量。其中的不可逆容量損失主要是由SEI膜的形成及CuS負極材料自身充放電機理造成的。在充電過程中,SEI膜覆蓋在電極材料表面,阻礙了鋰離子有效脫出,同時,SEI膜的不可逆分解以及CuS+2 Li→Cu+Li2S反應的不可逆性,均影響了鋰離子電池內部可逆反應的進行。在隨后的循環中,電解液不斷分解,SEI膜的厚度逐漸增加,阻礙電荷傳遞,減緩電化學反應,當SEI膜厚度達到平衡態時,Li+嵌入/脫出逐步穩定[8],結果與循環性能圖4表現一致。
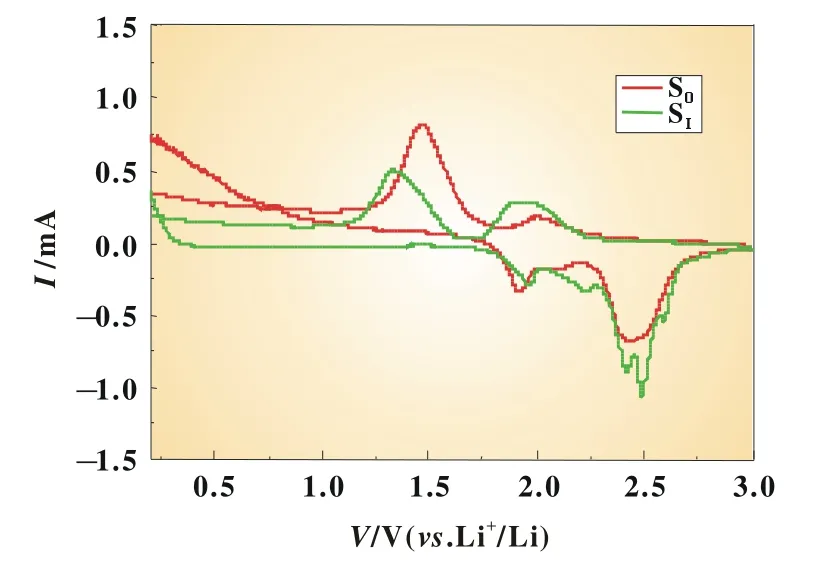
圖9 S0和SⅠ兩個樣品的循環伏安曲線
分別考察S0和SI兩個樣品的XRD和SEM圖。兩個樣品的特征衍射峰均與PDF卡片中CuS的標準譜圖 (JCPDS No.06-0464)一致,屬于六方晶系,空間群為P63/mmc,樣品SI雖出現一些其他物質的特征衍射峰,但其強度并不強,說明該方法制得的CuS樣品純度較高。樣品SI的衍射峰強要明顯高于樣品S0,表明焙燒提高樣品結晶度。CuS晶體以(102)(103)(110)晶面為擇優取向生長。此外,(102)的晶面間距要小于其他晶面的間距,CuS晶體選擇這個晶面作為擇優生長方向顯然縮短了Li+的擴散路徑,更為有利于Li+的嵌入和脫出,如圖1所示。樣品的a,c值均與標準樣品的值相近,誤差范圍在2.14%以內,這同樣表明樣品純度在該范圍內較高,如表4所示。
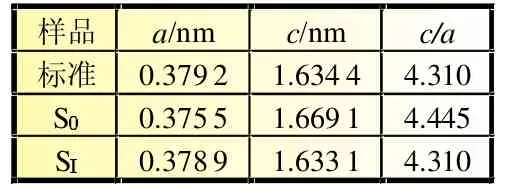
表4 CuS系列材料晶格參數
焙燒后的樣品與焙燒前的樣品一樣,如圖10所示,有規則的幾何形狀,表現為中空微球結構,中空結構由大小較為均一的顆粒構成。焙燒后的樣品伴隨團聚現象,顆粒尺寸由焙燒前的~85nm變成焙燒后的~80nm,這可能是因為失水造成結構的些許塌陷。因為粘接劑PVDF和電解液是非水體系的,所以對水比較敏感,150℃的焙燒溫度會使一些吸附水甚至是結晶水失去,結論與TG-DTA曲線一致,這對于非水體系而言是有利的。

圖10 焙燒后樣品的SEM圖
3 結論
以Cu(NO3)2·3H2O和TAA為原料,通過溶劑熱法制備中空結構硫化銅操作簡單,產品純度高,焙燒溫度和焙燒時間的改變均能影響樣品的電化學性能。其中,焙燒溫度為150℃,焙燒時間為1 h的CuS樣品的循環性能表現較為突出,并且其首次放電比容量(682.8mAh/g)較高,循環25次以后其比容量仍能保持在106.7mAh/g,循環穩定性較好,容量保持率(15.6%)較好。
[1]WANG X,WANG Y,LI X,et al.A facile synthesis of copper sulfides composite with lithium-storage properties[J].Journal of Power Sources,2015,281:185-191.
[2]周蕾.硫化銅微米花狀結構材料的合成及其光催化性能的研究[D].上海:復旦大學,2013.
[3]HAN Y,WANG Y,GAO W,et al.Synthesis of novel CuS with hierarchical structures and its application in lithium-ion batteries[J].Powder Technology,2011,212(1):64-68.
[4]LI F,WU J,QIN Q,et al.Controllable synthesis,optical and photocatalytic properties of CuS nanomaterials with hierarchical structures[J].Powder Technology,2010,198(2):267-274.
[5]WANG Y,ZHANG X,CHEN P,et al.In situ preparation of CuS cathode with unique stability and high rate performance for lithiumion batteries[J].Electrochimica Acta,2012,80:264-268.
[6]CHEN G Y,WEI Z Y,JIN B,et al.Hydrothermal synthesis of copper sulfide with novel hierarchical structures and its application in lithium-ion batteries[J].Applied Surface Science,2013,277:268-271.
[7]JACHE B,MOGWITZ B,KLEIN F,et al.Copper sulfides for rechargeable lithium batteries:Linking cycling stability to electrolyte composition[J].Journal of Power Sources,2014,247:703-711.
[8]李菁,張穎,韓恩山,等.氧化銅作鋰離子電池負極材料的制備及性能研究[J].無機鹽工業,2013,45(2):60-62.
[9]楊麗娟,金頭男,李于華.Al摻雜對尖晶石型LiMn2O4結構及循環性能的影響[J].鹽湖研究,2006(3):29-33.
[10]朱翔.錫基合金及其復合材料作為鋰離子電池負極材料的研究[D].南京:南京航空航天大學,2010.
[11]杜奉娟,張穎,劉軍.溶劑熱法合成硫化銅及其電化學性能[J].電源技術,2015,39(6):1263-1265.
[12]DéBART A,DUPONT L,PATRICE R,et al.Reactivity of transition metal(Co,Ni,Cu)sulphides versus lithium:the intriguing case of the copper sulphide[J].Solid State Sciences,2006,8(6):640-651.
[13]吳潔帆,劉紅光,葉學海,等.不同鋁源對LiNi1/3Co1/3Mn1/3O2材料的包覆改性研究[J].無機鹽工業,2015,47(7):71-74.
Preparation and performance of hollow sphere copper sulfide as anode materials for lithium-ion batteries
WEI Yan-ping,ZHANG Ying,ZHOU Ya,LI Jie,YANG Peng-ju
(School of Chemical Engineering and Technology,Hebei University of Technology,Tianjin 300130,China)
TM 912.9
A
1002-087X(2017)09-1261-03
2017-03-21
國家自然科學基金項目(21206027)
魏艷萍(1988-),女,河北省人,碩士,主要研究方向為無機材料化學。

