N,N,N'-三甲基-N'-羥乙基乙二胺的合成工藝研究
葉小明,魏夢怡,張琪,錢超,陳新志*
(1.浙江大學化學工程與生物工程學院,浙江杭州310027;2.四川之江高新材料股份有限公司,四川遂寧629100)
精細化工
N,N,N'-三甲基-N'-羥乙基乙二胺的合成工藝研究
葉小明1,2,魏夢怡1,張琪1,2,錢超1,陳新志1*
(1.浙江大學化學工程與生物工程學院,浙江杭州310027;2.四川之江高新材料股份有限公司,四川遂寧629100)
以羥乙基乙二胺、多聚甲醛為主要原料,經催化加氫反應生成目標產物,分別考察了催化劑、原料配比、溫度、氫氣壓力、pH值等影響因素。研究結果表明,以Raney Ni為催化劑,原料配比n(多聚甲醛):n(羥乙基乙二胺)=3,溫度100℃,氫氣壓力1.6 MPa和pH=10的條件下,羥乙基乙二胺的轉化率為100%,產品選擇性98.2%,收率93.6%,研究結果為該產品生產工藝的優化與生產放大提供了重要的基礎數據。
N,N,N'-三甲基-N'-羥乙基乙二胺;羥乙基乙二胺;甲基化;聚氨酯泡沫催化劑
N,N,N’-三甲基-N’-羥乙基乙二胺(簡稱:TMAEEA),是一種性能良好的通用型聚氨酯發泡催化劑,在催化硬球模塑的聚醚類軟質、硬質包裝材料的發泡過程中應用廣泛[1-2]。其結構中羥基上的氫很活潑,能夠和異氰酸酯發生反應,并結合到體系中難于揮發,是近年來重點發展的環保型催化劑之一[3-4],在日本、歐美等國家已經得到廣泛應用,市場需求量較大。
目前,文獻報道的主要方法有甲酸還原胺化法和鹵化物親核取代法。Doege Ulrica,Eger Kurt等人采用甲酸還原胺化法,以羥乙基乙二胺為原料,在甲醛、甲酸的作用下,N-甲基化反應生成TMAEEA[5]。但是,該方法以甲酸為氫供體,需要消耗大量的甲酸,原子經濟性差并釋放溫室氣體二氧化碳。同時,由于產品容易與甲酸、二氧化碳發生反應,因此副產物多,分離困難,產品質量較差。Vander Stelt C等人采用了鹵化物親核取代法,以N,N-二甲基氯乙胺和N-甲基乙醇胺為原料,在路易斯堿的作用下反應生成TMAEEA[6]。親核取代反應過程中需要加入縛酸劑,會生成摩爾量的氯化鈉鹽,對反應設備的腐蝕性強,反應后處理困難,同時該法原子經濟性差,原料成本較高,故限制了工業化規模應用。由于目前的合成工藝存在著原子經濟性差、生成鹵鹽腐蝕設備、副產物多和成本高等問題,制約了TMAEEA的產品市場競爭力。因此,開發TMAEEA的綠色工藝具有重大意義。
作者等人通過研究N-甲基化反應[7-10],提出了一種以羥乙基乙二胺和多聚甲醛為原料,氫氣為還原劑,在催化劑的作用下反應生成TMAEEA的合成工藝,系統地考察了不同的催化劑、原料配比、溫度、壓力、pH值等工藝條件對轉化率和選擇性的影響,研究結果能為該產品生產工藝的改進與工業化應用提供有用的數據。該法工藝簡單,原子經濟性高,副產物為水,具有環境友好、適宜工業化等特點。

1 實驗部分
1.1 實驗裝置及方法
合成TMAEEA裝置如圖1,電子天平(上海浦春),氣相色譜儀(安捷倫1790F氫火焰檢測器,30 m長SE54毛細管色譜柱),氣相-質譜聯用儀(Thermo Quest公司)等。化學品均為市售分析純試劑,未精制直接使用。
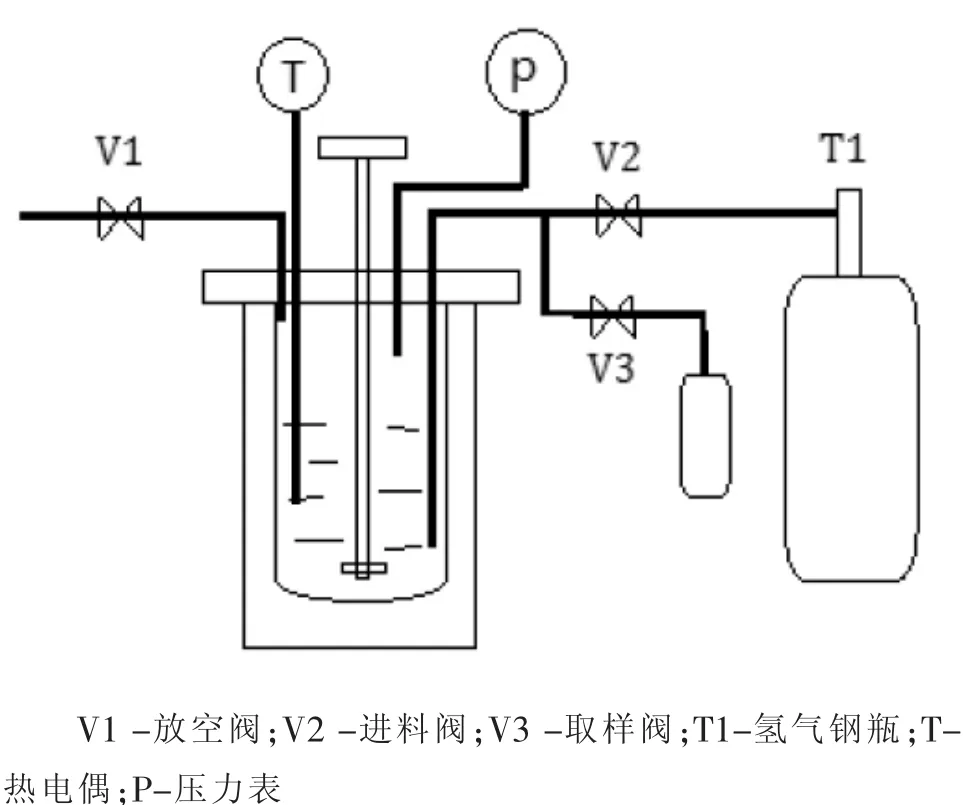
圖1 高壓釜示意圖Figure 1 The schematic ofhigh-pressure autoclave
1.2 實驗步驟
(1)于高壓釜中加入所需的多聚甲醛、羥乙基乙二胺、催化劑和甲醇,N2檢漏并置換空氣三次,再用H2置換三次,然后充入氫氣至壓力1.60 MPa;
(2)開啟攪拌,緩慢升溫至100℃,保溫100℃反應;
(3)期間,釜內壓力緩慢降低,需向釜內充入氫氣,使釜內壓力穩定在1.40~1.60 MPa之間,至壓力不再改變,即反應結束,停止加熱;
(4)降溫至室溫,泄壓,靜置1 h,吸出上層反應液;
1.3 分析方法
氣相色譜條件:氮氣壓力100 KPa,氫氣壓力100 kPa,空氣壓力30 kPa,進樣量0.2μL,進樣溫度260℃,檢測溫度260℃,初始溫度100℃,初始時間2 min,升溫速率20℃/min,終止溫度260℃。
1.4 結構表征
GC/MS,44:N(CH3)2,58:CH2N(CH3)2,71:CH2N(CH3)C2H4OH,88:(CH3)2NC2H4N(CH3)CH2;1H NMR,(400 MHz,CDCl3)δ4.04(s,0H),3.62(dt,J=29.0,5.1 Hz,3H),2.62~2.46(m,4H),2.46~2.37(m,2H),2.27(dd,J=25.5,9.6 Hz,9H)。
2 結果與討論
2.1 催化劑選擇與用量
第Ⅷ族過渡金屬元素的金屬催化劑,如鉑、鈀、鎳、鈷以及其負載催化劑在有機還原反應中使用最為廣泛[11]。本文在溫度100℃,壓力1.6 MPa的反應條件下,以羥乙基乙二胺(1.0 mol)和多聚甲醛(3.0 mol)為原料,甲醇(50 mL)為溶劑,催化劑用量7.8 g(4 wt.%),考察了不同金屬催化劑的影響,結果如表1所示。
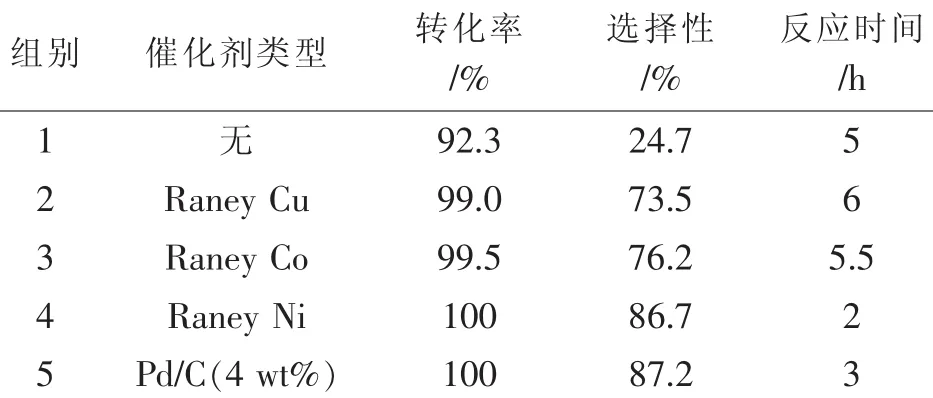
表1 催化劑種類對羥乙基乙二胺N,N,N'-三甲基化反應的影響Table 1 The effects ofseveral kinds ofcatalysts on the reactions
由表1可知,在第一組沒有催化劑的實驗中,在沒有催化劑的存在下,氫氣的還原活性很低,大多生成了與甲醛的加成產物,產物選擇性低。第二組的Raney Cu和第三組Raney Co催化劑催化還原活性較弱,反應時間長,選擇性低,收率較低。第五、六組結果表明,Raney Ni較Pd/C(4 wt.%)催化活性高,且價格便宜。因此,本文以Raney Ni為催化劑進行反應條件的考察。
本文在溫度100℃,壓力1.6 MPa的反應條件下,以羥乙基乙二胺(1 mol)和多聚甲醛(3 mol)為原料,甲醇(50 mL)為溶劑的條件考察了不同的催化劑用量對選擇性的影響,結果如圖2所示。
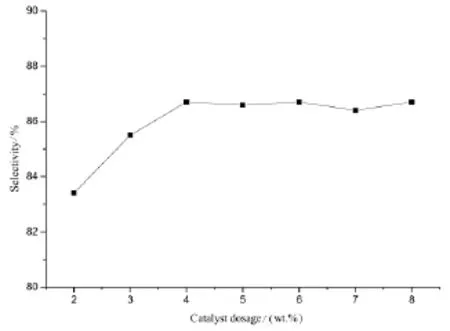
圖2 催化劑用量對選擇性的影響Figure2 Effectof catalystdosage on selectivity
由圖2可知,當催化劑用量由2 wt.%上升至4 wt.%,產物的選擇性隨著催化劑用量的增加而上升;而催化劑用量大于4 wt.%后,隨著催化劑用量的增加,產物的選擇性略微下降。考慮催化劑的消耗,本文以4 wt.%作為適宜的催化劑用量。
2.2 原料配比
為了得到適宜的原料配比,本文在溫度100℃,壓力1.6 MPa的反應條件下,以甲醇(50 mL)為溶劑,催化劑用量4 wt.%,考察了原料配比對選擇性的影響,結果如圖3所示。
由圖3可知,當n(多聚甲醛):n(羥乙基乙二胺)大于3.3時,選擇性隨著原料配比的增大而減小。在摩爾比3.0~3.3之間,選擇性維持在較高水平。考慮原料的消耗,本文以n(多聚甲醛):n(羥乙基乙二胺)=3作為適宜的原料配比。
2.3 反應溫度
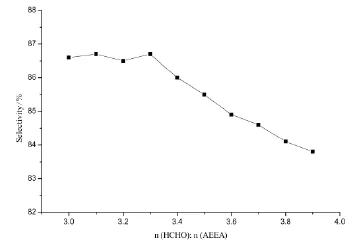
圖3 原料配比對選擇性的影響Figure 3 Effect ofraw material ratio on selectivity
反應溫度對反應速度以及產品選擇性有重大的影響,本文在壓力1.6 MPa,催化劑用量4 wt.%,n(多聚甲醛):n(羥乙基乙二胺)=3,甲醇為溶劑的條件下,考察了反應溫度對選擇性的影響,結果如圖4所示。
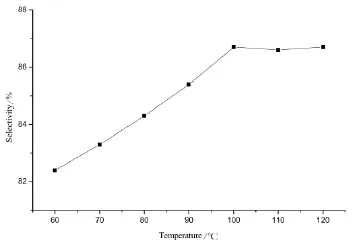
圖4 反應溫度對選擇性的影響Figure 4 Effectofreaction temperature on selectivity
由圖4可知,當溫小于100℃時,隨著溫度的上升選擇性上升,當溫度達到100℃時,選擇性為86.7%;隨著溫度的繼續提高,選擇性稍有下降。綜合考慮能耗,本文以100℃作為適宜的反應溫度。
2.4 壓力
體系壓力主要由氫氣提供,直接影響了產物的選擇性。本文在溫度100℃,催化劑用量4 wt.%,n(多聚甲醛):n(羥乙基乙二胺)=3,甲醇為溶劑的條件下,考察了體系壓力對選擇性的影響,結果如圖5所示。
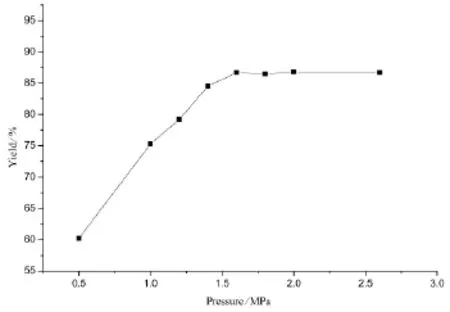
圖5 反應壓力對選擇性的影響Figure 5 Effect of reaction pressure on selectivity
由圖5可知,當壓力低于1.0 MPa時,選擇性低;提高體系壓力,選擇性上升明顯,當壓力達到1.6 MPa之后,繼續提高壓力對選擇性基本沒影響。綜合考慮氫氣消耗及工藝安全,適宜的反應壓力為1.6 MPa。
2.5 pH值
由于pH值對多聚甲醛的解聚有著重要影響[12],故本文通過加入pH調節劑(如:有機酸、無機堿、強酸弱堿鹽、強堿弱酸鹽等)的方式,在催化劑用量4 wt.%,n(多聚甲醛):n(羥乙基乙二胺)=3,溫度100℃,壓力1.6 MPa,甲醇為溶劑的條件下,考察了pH值對選擇性的影響,結果如圖6所示。
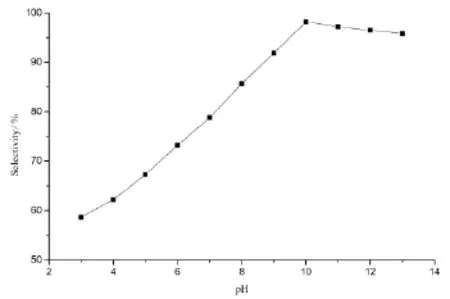
圖6 pH值對選擇性的影響Figure 6 Effect of pH on selectivity
由圖6可知,體系pH值在3~10之間,選擇性隨著pH值的增大而增加;體系pH值在10~13之間,選擇性隨著pH值的增大而減小,當pH=10時,選擇性最高可達98.2%。這可能是由于該反應從伯胺經N-甲基化反應生成叔胺,隨著反應的進行,溶液的pH值逐漸降低,影響了多聚甲醛的解聚和胺的活性,從而造成了產物選擇性的下降。且若要保持pH=10,只需加入少量的強堿弱酸鹽(如甲酸鈉、Na2CO3等)即可,故本文適宜的pH值為10。將此條件得到的產物進行減壓精餾提純,得到產品的含量為99.9%,收率為93.6%。
2.6 合成工藝的比較
將本工藝與甲酸還原胺化法[5]和鹵化物親核取代法[6]進行比較,如表2所示,由表2可知,本工藝具有如下特點:(1)原料來源廣、工藝簡單;(2)收率高,原子經濟性高;(3)副產物為水,工藝清潔環保。
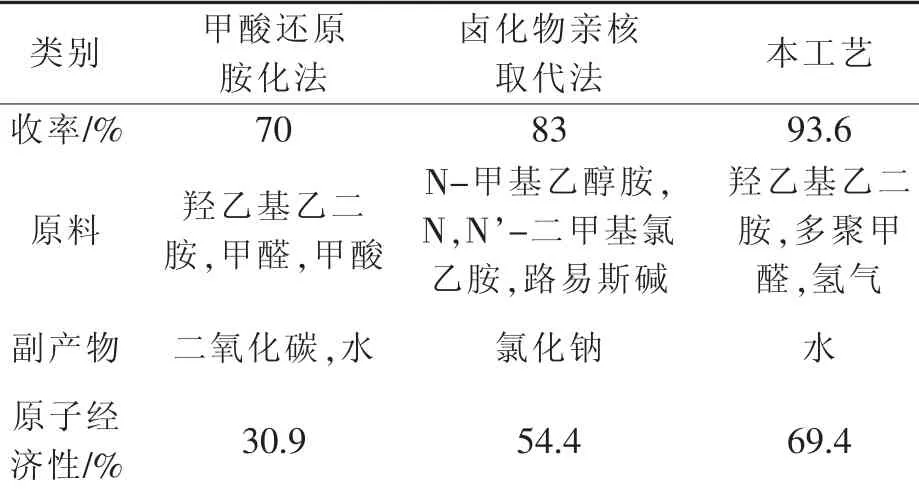
表2 合成工藝的比較Table 2 Comparison of the synthesis prosess
3 結論
(1)本文采用羥乙基乙二胺和多聚甲醛為原料,經催化加氫還原生成TMAEEA,產物經GC/ MS、1H NMR結構鑒定正確;該工藝路線清潔環保、工藝簡單,適合工業化生產。
(2)較優的合成TMAEEA工藝條件:采用Raney Ni為催化劑,催化劑用量4 wt%,n(多聚甲醛):n(羥乙基乙二胺)=3,反應溫度為100℃,氫氣壓力1.6 MPa,pH=10。在此條件下,羥乙基乙二胺的轉化率100%,產物選擇性達到98.2%,收率可達93.6%。
[1]李人粹.聚氨酯用胺催化劑組成物[J].聚氨酯,2006,(6):72-74.
[2]孫剛,劉預,馮芳.聚氨酯泡沫材料的研究進展[J].材料導報,2006,20(3):29-32.
[3]譚美軍.聚氨酯泡沫有機胺類催化劑[J].湖南化工,1991,21(1):21-23.
[4]李偉.環保聚氨酯彈性體催化劑[J].橡膠參考資料,2014,44(6):56-56.
[5]Doege U,Eger K.A simple HPLC-UV method for the determination of dimenhydrinate and related substances-identification of an unknown impurity[J].Pharmazie,2007, 62(3),174-178.
[6]Stelt C,Tersteege H.Synthesis and properties of a number of alkyl-substituted diphenylmethyldialkylaminoethoxyethyl ethers and some related substances[J].Arzneimittel-Forschung,1964,14(9),1053-1055.
[7]駱晨希.基于催化加氫N-甲基化工藝研究[D].杭州:浙江大學,2014.
[8]Roe A,Montgomery J A.Kinetics of the catalytic hydrogenation of certain schiff bases[J].Journal of the America Chemistry Society,1953,75(4):910-912.
[9]Shen J W,Qin D G,Zhang H W,et al.Studies on the synthesis of(2S,3R)-3-hydroxy-3-methylproline via C-2-N bond formation[J].Journal of Organic Chemistry,2003,68(19):7479-7484.
[10]Ge X,Luo C X,Qian C,et al.Raneynickel-catalyzed reductive N-methylation of amines with paraformaldehyde: theoretical and experimental study[J].Rsc Adv,2014,4(81),43195-43203.
[11]Angelovski G,Eilbracht P.Synthesis of hydroquinonebiphenol and binaphthol-containing azamacroheterocycles via regioselectivehydroformylation and reductive amination [J].Tetrahedron,2003,59(41):8265-8274.
[12]伍艷輝,白素松,譚露璐,等.多聚甲醛的解聚實驗研究[J].實驗室研究與探索,2008,27(6):69~71.
[13]沈玉龍,曹文華.綠色化學[M].北京:中國環境出版社,2004.
Synthesis of N,N,N’-trimethylamino-N’-ethylethanolamine
YE Xiao-ming1,2,WEIMeng-yi1,ZHANG Qi1,2,QIAN Chao1,CHEN Xin-zhi1*
(1.Zhejiang University,College of Chemical and Biological Engineering,Hangzhou,Zhejiang 310027,China;2.Sichuan Z-river High-tech Material Co.,Ltd.,Suining,Sichuan 629100,China)
2-[(2-Aminoethyl)amino]ethanol and polyoxymethylene were employed as the main reagents to synthesize TMAEEA via catalytic hydrogenation.The effects of a series of factors like catalyst,feeding ratio,reaction temperature,hydrogen pressure and pH value on the preparation of TMAEEA in a stainless steel autoclave were investigated.The optimum reaction conditions obtained were:n(paraformaldehyde):n(AEEA)=3,reaction temperature=100℃,hydrogen pressure 1.6 MPa,pH value=10,with Raney Nias catalyst.accordingly,a conversion of 2-[(2-Aminoethyl)amino]ethanol=100%with a selectivity of TMAEEA=98.2%was achieved,yield 93.6%.The result of the research provided important basic data for the process optimization and production enlargement.
N,N,N’-trimethylamino-N’-ethylethanolamine;2-[(2-aminoethyl)amino]ethanol;methylation;polyurethane foam catalyst
1006-4184(2017)7-0027-05
深圳先進院研發出新型低成本雙碳鉀離子電池技術
2017-05-24
國家自然科學基金(21376213,21476194);四川省省級科技計劃項目(2016GZ0382)。
葉小明(1982-),男,浙江杭州人,在讀碩士研究生,工程師,主要從事精細化學品合成研究。E-mail:xiaoming1256@163.com。
*通訊作者:陳新志,E-mail:xzchen@zju.edu.cn。
結合鉀離子電池與雙碳電池各自的優點,中國科學院深圳先進技術研究院集成所功能薄膜材料研究中心研究員唐永炳及其團隊成員季必發、張帆等人成功研發出一種新型高性能、低成本、環保友好的雙碳鉀離子電池。該電池采用中間相碳微球為負極,膨脹石墨作為正極;電解液采用廉價易得的六氟磷酸鉀作為鉀鹽電解質溶于有機溶劑中。其反應機理為:充電時,電解液中的鉀離子運動到中間相碳微球負極表面,并嵌入至石墨層中,同時六氟磷酸根陰離子插層到正極石墨中;放電時,鉀離子從負極石墨層中脫出,同時正極石墨中的六氟磷酸根脫嵌回到電解液中。研究表明,該新型廉價雙碳鉀離子電池的放電中值電壓高達4.5 V,單個紐扣電池就能同時點亮兩顆LED燈,并且電池充放電循環100圈后,容量幾乎沒有衰減,使得其可以滿足高電壓器件的要求。
(來源:http://www.cas.cn/syky/201707/t20170724_4609493.shtml)

