造影增強超聲內鏡對上消化道及毗鄰占位的診斷價值
鄧 巍,姜海行,覃山羽△
(1.廣西壯族自治區欽州市第二人民醫院消化內科 535000;2.廣西醫科大學第一附屬醫院消化內科,南寧 530021)
造影增強超聲內鏡對上消化道及毗鄰占位的診斷價值
鄧 巍1,姜海行2,覃山羽2△
(1.廣西壯族自治區欽州市第二人民醫院消化內科 535000;2.廣西醫科大學第一附屬醫院消化內科,南寧 530021)
目的 探討造影增強超聲內鏡(CE-EUS)對上消化道及毗鄰占位的診斷價值。方法 收集廣西醫科大學第一附屬醫院2014年6月至2015年3月收治的上消化道及毗鄰占位性病變180例,均進行CE-EUS檢查,通過觀察實性占位的血流灌注增強特征作出初步診斷,并與超聲內鏡引導下細針穿刺細胞學(EUS-FNA)和(或)組織病理學結果、膽道刷檢細胞學涂片結果、手術病理結果、CT、磁共振成像(MRI)及隨訪結果的綜合判斷結果進行對比分析,全面總結分析各實性占位內鏡超聲造影特點。結果 180例上消化道及毗鄰占位中,CE-EUS與最終診斷符合169例,不符合11例,診斷符合率為93.9%。結論 CE-EUS可引導EUS-FNA穿刺,提高EUS-FNA陽性率。
體層攝影術,X線計算機;造影劑;造影增強超聲內鏡檢查術;上消化道及毗鄰占位;血流灌注特征;診斷
常規超聲內鏡是診斷上消化道及毗鄰占位的準確手段之一,但它未能顯示病灶血流灌注特征,不能對腫瘤良惡性提供客觀依據,僅依據常規超聲內鏡影像判斷占位病變性質有較大局限性[1]。而造影增強超聲內鏡術(contrast-enhanced endoscopic ultrasonography,CE-EUS)檢查與超聲內鏡(endoscopic ultrasonography,EUS)相結合,能清晰顯示消化道管壁、毗鄰結構病變及占位血流灌注特征,是超聲影像診斷學領域一個重要進展[2]。如同時行超聲內鏡引導下細針抽吸術(endoscopic ultrasonography-guided fine needle aspiration,EUS-FNA),還可獲取占位組織細胞,為臨床提供病理學依據,進一步提高確診率[3]。
1 資料與方法
1.1 一般資料 本研究觀察對象為2014年6月至2015年3月廣西醫科大學第一附屬醫院收治的180例患者,經胃鏡、EUS、腹部B超、CT、磁共振成像(MRI)、上消化道鋇餐等發現或疑有上消化道及毗鄰占位。其中男114例(63.3%),女66例(36.7%),年齡19~82歲,中位年齡 52 歲。所有患者行CE-EUS前均完善凝血功能、心電圖、胸片、電解質等相關檢查,排除有嚴重心、肺疾病難以耐受內鏡操作或麻醉的患者和凝血功能障礙的患者。所有患者均事先簽署知情同意書。
1.2 儀器與試劑 CE-EUS采用Prosound F75主機及GF-UCT260電子凸陣掃描超聲胃鏡,超聲胃鏡掃描范圍可達180°,支持造影諧波功能,能幫助評估可疑占位,能同時進行EUS-FNA,穿刺針選用Wilson-Cook 22G。采用六氟化硫微泡(Sono Vue)超聲造影增強劑,它包含SF6氣體59 mg及凍干粉25 mg。使用時向小瓶內注入5.0 mL生理鹽水并用力振搖后形成微泡混懸液,隨后將2.4 mL混懸液抽至注射器并勻速注入淺靜脈,注射完畢后予5.0 mL生理鹽水進行沖管。
1.3 方法
1.3.1 術前準備 所有接受CE-EUS檢查患者,術前禁食8 h以上,檢查前常規口服二甲硅油散及利多卡因膠漿,建立靜脈通道。如需同時進行內鏡黏膜下剝離術(endoscopic submucosal dissection,ESD)或EUS-FNA,應準備患者近3 d凝血功能、血常規、生化6項、心電圖等檢查結果,準備EUS-FNA、ESD手術用物,如穿刺針、載玻片、ESD配件、黏膜下注射劑、鈦夾等。
1.3.2 檢查方法 對于上消化道占位患者,先行胃鏡直接觀察病灶情況,如部位、大小、形態等,后在EUS下觀察目標病灶管壁的層次結構、邊界、回聲、切面大小,判斷病灶的起源及有無浸潤。對于上消化道毗鄰占位,如縱膈、壺腹部、腎上腺、腹腔等,直接在EUS下觀察病灶情況。鎖定目標病灶后注射Sono Vue,同時對EUS彩色多普勒圖像進行全程錄像,錄像至增強效應基本消失為止,以備結果分析,同時密切觀察占位的血流灌注情況,觀察內容包括增強模式、增強時相及增強強度,對多發占位患者應選擇1~2個病灶進行重點觀察。全過程由2~3名經驗豐富的醫師對造影結果進行綜合分析并作出診斷。如需獲取細胞學、組織病理學結果,隨后行EUS-FNA、ESD、膽道刷檢等。
1.3.3 觀察指標 回放受檢病灶的彩色多普勒圖像錄影,仔細觀察血流灌注的增強情況,內容包括增強模式、增強時相及增強強度。(1)增強模式根據造影增強達到峰值時EUS彩色血流信號的形態特征,分為以下3型:Ⅰ型為點狀增強;Ⅱ型為棒狀增強;Ⅲ型為斑塊狀增強。(2)增強時相根據占位與周圍正常組織在注射Sono Vue后血流信號出現增強和開始消退的先后,從而判斷病灶增強時相的特點。主要有快進快退、快進慢退、慢進快退及慢進慢退4種類型。(3)增強強度根據造影增強達峰值時血流信號面積所占比例分為4級:1級,<25%;2級,≥25%~<50%;3級,≥50%~<75%;4級,≥75%。

2 結 果
2.1 各部位占位構成比 180例患者經胃鏡、EUS、腹部B超、CT、MRI發現占位,其中46例(25.6%)為食管占位,48例(26.7%)為胃占位,12例(6.7%)為十二指腸占位,26例(14.4%)為肝臟占位,8例(4.4%)為腎上腺占位,16例(8.9%)為縱膈占位,24例(13.3%)為腹腔占位。180例患者均行CE-EUS,以超聲內鏡引導下細針穿刺細胞學和(或)組織病理學結果、膽道刷檢細胞學涂片結果、手術病理結果、CT結果、MRI結果及隨訪結果的綜合判斷為最終診斷。
2.2 CE-EUS初步診斷結果 食管病變46例:平滑肌瘤23例,食管癌22例,結核1例。胃病變48例:間質瘤20例,胃癌14例,異位胰腺12例,胃腔外壓迫2例。十二指腸病變12例:間質瘤8例,脂肪瘤4例。肝臟病變26例:肝細胞癌20例,血管瘤4例,肝膿腫2例。腎上腺病變8例:腎上腺轉移癌6例,囊腫2例。縱膈病變16例:淋巴結轉移癌12例,淋巴結結核4例。腹腔病變24例:淋巴結轉移癌17例,淋巴結結核6例,畸胎瘤1例。
2.3 最終診斷結果 本研究180例患者均行CE-EUS檢查,以病理、影像學、隨訪結果綜合判斷為最終診斷。其中行病理活檢確診30例,行ESD術后病理確診60例,行EMR術后病理確診12例,行EUS-FNA確診48例,行ERCP膽道刷檢確診6例,外科手術病理確診10例,行常規影像學CT、MRI、EUS檢查并隨訪患者已達臨床確診14例。最終確診97例為惡性病變, 83例為良性病變。食管病變中CE-EUS初步診斷食管平滑肌瘤23例,其中1例行ESD術后病理為食管平滑肌肉瘤。診斷食管結核1例,病理活檢提示食管癌。胃病變中CE-EUS初步診斷胃癌14例,其中2例ESD術后病理為淋巴瘤,另1例行EUS-FNA病理為惡性間質瘤,已行外科手術,術后病理同EUS-FNA診斷。診斷胃間質瘤20例,其中1例ESD術后病理為類癌。肝臟病變中CE-EUS初步診斷肝細胞癌20例,其中1例外科術后病理為膽管細胞癌。診斷肝膿腫2例,1例行EUS-FNA病理為膽管細胞癌,另1例行ERCP膽道刷檢確診為膽管細胞癌。縱膈病變中CE-EUS初步診斷淋巴結結核4例,其中1例行EUS-FNA,所取材行細胞塊及免疫組織化學,結果提示肺癌縱膈淋巴結轉移。腹腔病變中CE-EUS初步診斷淋巴結結核6例,其中1例經EUS-FNA取材后行細胞塊及免疫組織化學,結果提示肝癌腹腔淋巴結轉移。其余病例CE-EUS初步診斷均與最終診斷相符。CE-EUS總診斷符合率為93.9%(表1)。各部位占位CE-EUS特點見表2。

表1 各部位占位CE-EUS初步診斷與最終診斷比較

表2 各部位占位CE-EUS特點
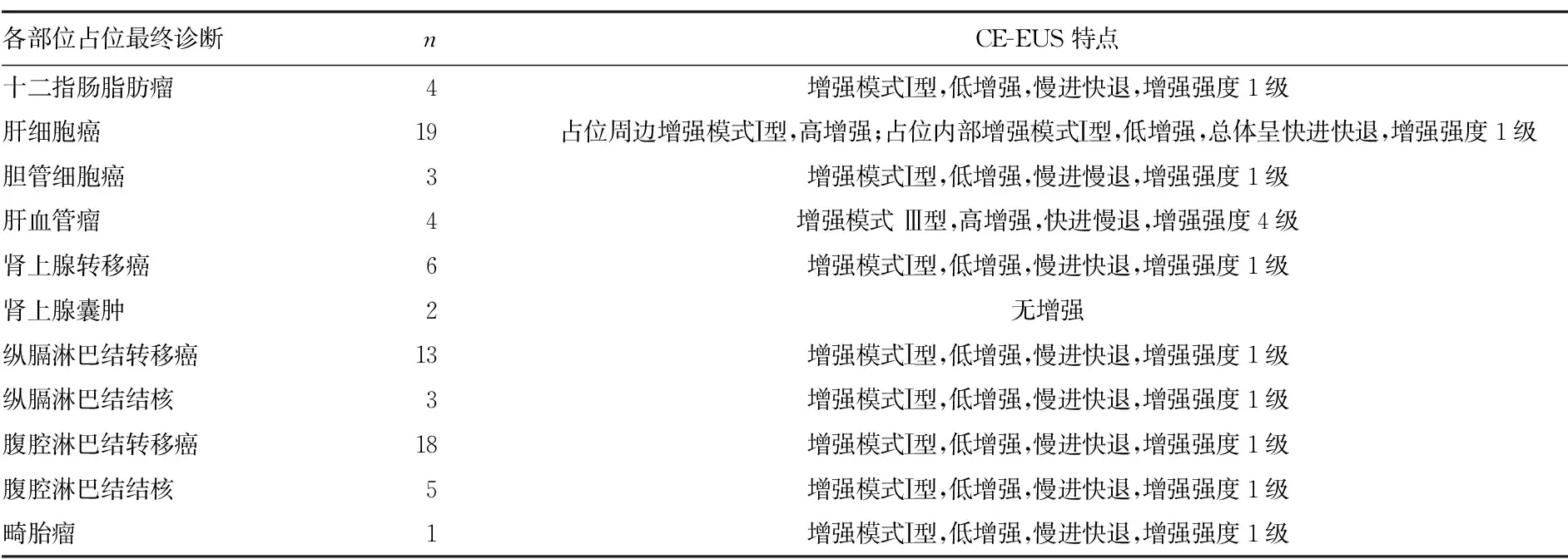
續表2 各部位占位CE-EUS特點
2.4 典型病例 病例1,女,24歲,因“反復上腹部悶脹、發熱2個月”入院,行胃鏡檢查示“胃體前壁見一大小約3.0 cm×3.0 cm隆起,表面形成淺潰瘍,診斷為胃體隆起性質待查”(圖1),EUS示“胃體對應病變起源于黏膜層,低回聲,回聲不均勻,擬診胃體黏膜隆起:胃息肉?胃癌?”(圖2),CE-EUS示“高增強,呈快進慢退型,擬診胃體黏膜隆起:淋巴瘤可能性大”(圖3),遂行ESD術(圖4、5),大體標本送檢。術后病理及免疫組化結果提示“瘤細胞表達Ki67陽性率約90%,CD20(+),CD79a(+),CD3(-),Bcl-6(+),CD10(-),CK(-),診斷B細胞淋巴瘤”(圖6)。
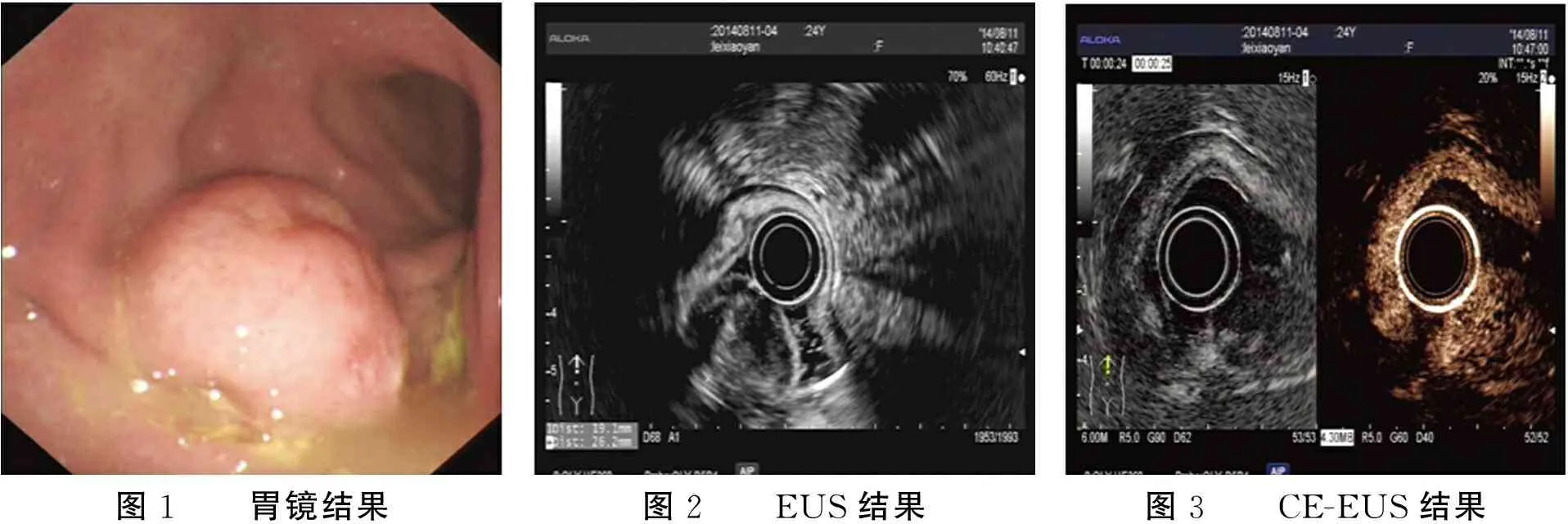
圖1 胃鏡結果圖2 EUS結果圖3 CE-EUS結果
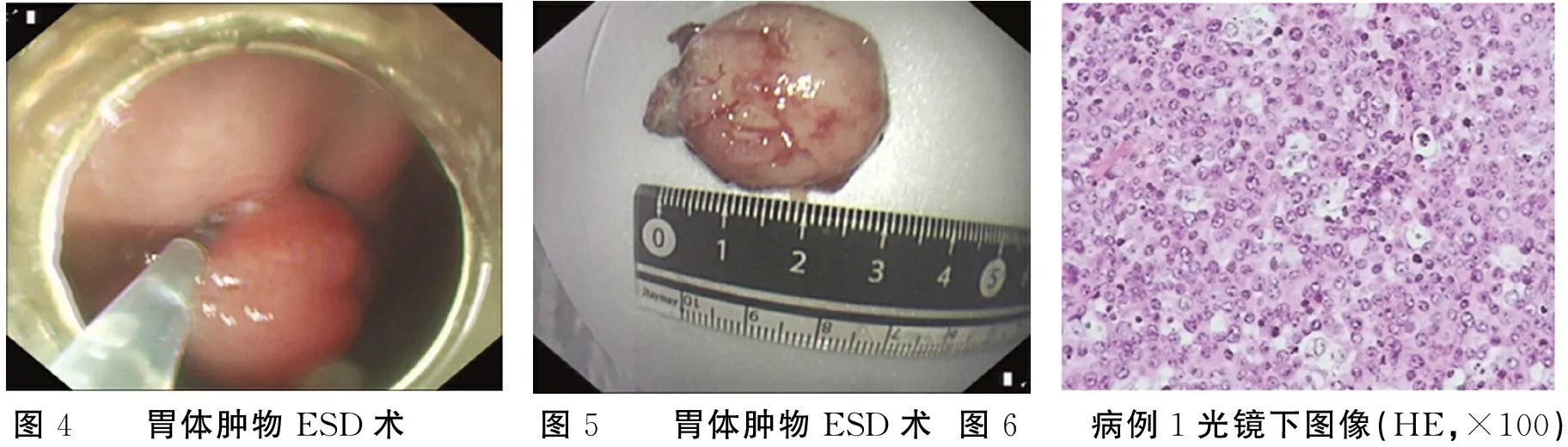
圖4 胃體腫物ESD術圖5 胃體腫物ESD術圖6 病例1光鏡下圖像(HE,×100)
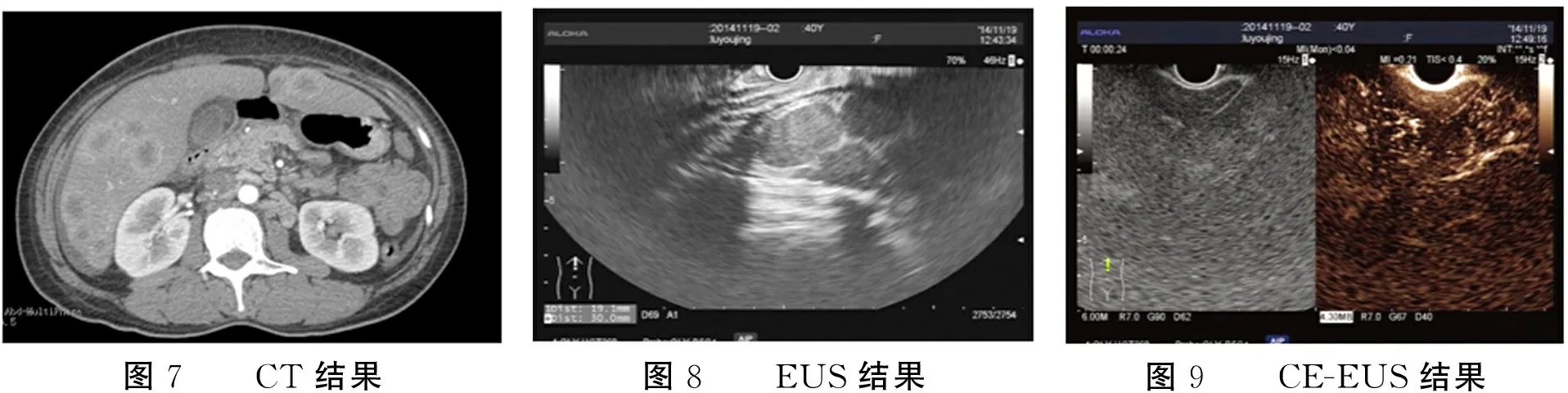
圖7 CT結果圖8 EUS結果圖9 CE-EUS結果
病例2,女,40歲,因“右上腹脹痛3月余”入院,本院增強CT 提示“肝實質內可見多發大小不等的類圓形低密度影,考慮為肝轉移瘤可能性大”(圖7);EUS提示“肝左葉見多個大小不等的類圓形低密度影,邊緣較清晰,較大病灶直徑約3.0 cm×2.5 cm,考慮為肝轉移瘤”(圖8);CE-EUS示“肝占位呈低增強,慢進慢退型,擬診肝轉移瘤”(圖9);遂行EUS-FNA(圖10);細胞學涂片及免疫組織化學結果提示“可見核異形細胞,CK18(+),CK19(+),CK20(-),CD20(-),CD79a(-),CD4(-),診斷膽管上皮來源癌”(圖11)。
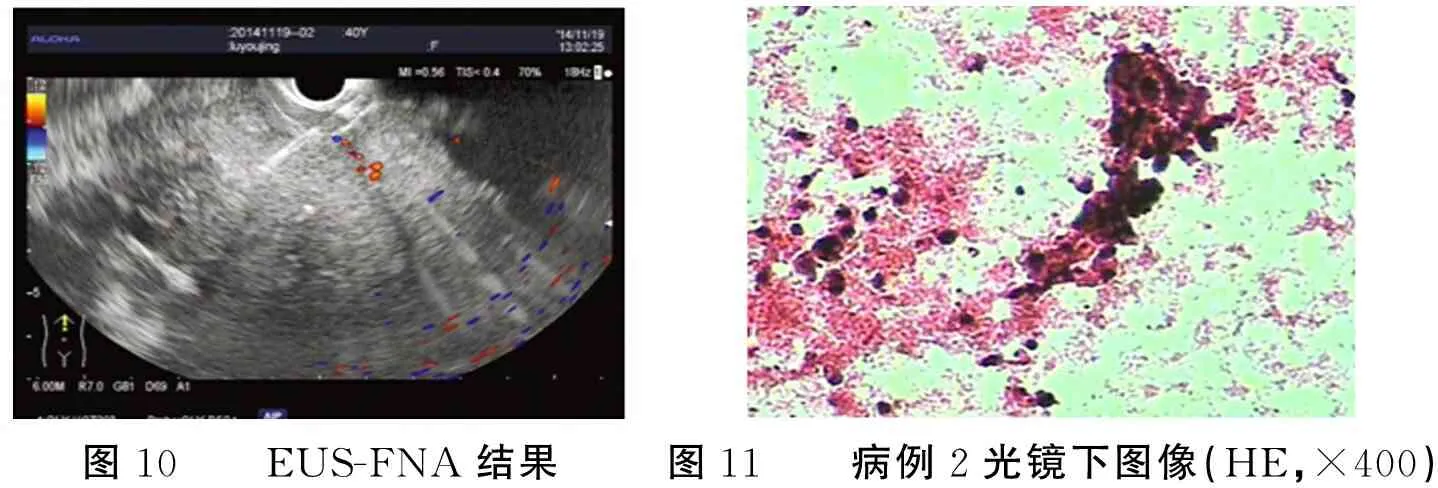
圖10 EUS-FNA結果圖11 病例2光鏡下圖像(HE,×400)
3 討 論
超聲內鏡是目前診斷消化道黏膜下病變較為準確的方法[4-6],如能與超聲造影增強技術相結合,通過利用微氣泡導致被掃查對象界面回聲的聲阻抗差改變,就能觀察占位血流灌注特征,判別病變血管結構,有助于占位病變性質的鑒別[7],進而提高超聲診斷和鑒別診斷的能力。
普通胃鏡觀察上消化道占位多表現為黏膜或黏膜下隆起,菜花樣或半球狀,寬基底,邊界清,黏膜層病變通過常規活檢一般可以確診,但對于黏膜下病變,內鏡取檢多不滿意,往往因取材表淺或取材過少而無法判斷病變性質。對于上消化道毗鄰占位及腔外生長病變,胃鏡下可為陰性表現。腹部B超常受胃腸腔氣體及腹壁脂肪組織等因素干擾,造成誤診、漏診。因此,對非局限于或非來源于黏膜層病變的大小、來源、性質及累及深度,常規內鏡、影像學檢查手段無法判斷,極易導致漏診、誤診及延診,限制了進一步治療措施的選擇、開展與實施,尤其是腫瘤的內鏡下治療[8]。對黏膜下層病變診斷有優勢的普通超聲內鏡,主要顯示病灶起源、大小、形態、回聲,無法提供其血流灌注特征,在良惡性判斷上有局限,不能指導EUS-FNA的靶向穿刺活檢。而本研究的CE-EUS診斷方法則彌補了上述不足,清晰顯示病灶血流灌注特征,對占位良惡性的檢測和區分提供客觀依據。本研究還將腔外壓迫納入討論范圍,嚴格意義上說,腔外壓迫不屬于消化道腫瘤范疇,但常規內鏡往往難以鑒別,需要借助其他手段,如CE-EUS進一步明確。
CE-EUS能使病灶內部血流異常灌注區清晰顯示,它如同超聲彈性成像學一樣[9],在EUS-FNA前獲取病灶性質初步判斷,更好地引導EUS-FNA對上消化道及毗鄰占位穿刺,成功獲取組織行病理及免疫組織化學等檢查,提高陽性率,可更好地確定病變性質,對指導治療具有非常重要的意義[10-13]。對于某些穿刺部位不理想,血管橫跨,穿刺距離太遠而不適合行EUS-FNA的病灶,CE-EUS提供的客觀依據是對診斷的進一步補充。該技術的發展主要應用于胰腺疾病的診斷中,目前已逐漸應用于上消化道及毗鄰占位的診斷[14-17]。
本組研究病例以食管、胃、肝臟、腹腔病例數居多,這是臨床上最常見、最多發的病種。食管病變中以平滑肌瘤的發生率最高,胃則以間質瘤最為常見,CE-EUS示食管平滑肌瘤多起源于黏膜肌層,低增強,而胃低度惡性間質瘤多起源于固有肌層,整個瘤體呈現高增強,如為高度惡性間質瘤則表現在瘤體周邊高增強,內部低增強表現,這與腫瘤滋養血管多位于瘤體周邊,距離血管越近,腫瘤細胞生長越活躍,而遠離血管的腫瘤中央細胞容易壞死相關。此外,Okai 等[18]發現腫瘤周邊有聲暈、回聲相對較高多的為間質瘤,平滑肌瘤無此聲暈。肝臟病變中以肝細胞癌發病率最高,腹腔病變以肝癌并腹腔淋巴結轉移多見,肝細胞癌(HCC)超聲造影增強特點為低增強,快進快退,這與HCC在增強CT上的表現類似[19-21]。而肝癌腹腔淋巴結轉移超聲造影特點亦為低增強,但呈慢進快退型。相對于經腹超聲造影在肝占位的應用,CE-EUS不僅避免了腹壁及腸氣干擾所致部分切面觀察不清,還能引導EUS-FNA,對穿刺物采取細胞塊的制作和免疫細胞化學的輔助診斷,有助于確定病變的良惡性質及確定病變的類型[3]。
本研究發現,對普通內鏡或常規影像學檢查發現的占位存在可疑時,常規行CE-EUS可減少漏診及誤診的發生率,且六氟化硫微泡極其穩定,在血液中存留時間較長,為超聲檢查提供足夠時間,安全有效,無明顯不良反應[22]。CE-EUS能在無法進行EUS-FNA或因穿刺取材太少無法明確病灶性質時提供另一種診斷依據,也能引導EUS-FNA在病灶血流相對豐富的區域進行穿刺取檢。因此,CE-EUS可提高EUS-FNA單次穿刺陽性率。
綜上所述,CE-EUS能對上消化道及毗鄰占位進行初步定性診斷及引導EUS-FNA穿刺活檢,提高EUS-FNA單次穿刺陽性率,為患者的診治方案提供有力參考,在臨床中有較高的應用價值。
[1]Kahl S,Schütte K,Malfertheiner P.Pancreatic cancer-Endosonography[J].中德臨床腫瘤學雜志,2007,6(2):123-128.
[2]呂明德,楊建勇.腹部外科影像與介入治療學[M].北京:人民衛生出版社,2003:131-185.
[3]覃山羽,姜海行,李萍,等.細胞塊結合免疫組化在內鏡超聲引導下穿刺診斷胰腺實性占位中的應用價值[J].中華消化內鏡雜志,2014,31(6):312-316.
[4]胡凱風,梅俏,許建明.超聲內鏡對上消化道黏膜隆起性病變的診斷價值[J].安徽醫學,2011,32(1):83-85.
[5]Keter D,Melzer E.Endoscopic ultrasound in clinical practice[J].Acta Gastroenterol Latinoam,2008,38(2):146-151.
[6]陳浩,林李淼,夏宣平.電子胃鏡和超聲內鏡在上消化道黏膜下病變中診斷比較的研究[J].安徽醫學,2008,29(3):288-290.
[7]諸琦,熊回訪,徐凱.造影增強超聲內鏡對胰腺占位病變的鑒別診斷初步探討[J].中華消化內鏡雜志,2008,25(3):126-130.
[8]徐美東,姚禮慶,周平紅,等.經黏膜下隧道內鏡腫瘤切除術治療源于固有肌層的上消化道黏膜下腫瘤初探[J].中華消化內鏡雜志,2012,28(11):606-610.
[9]Giovannini M,Hookey LC,Bories E,et al.Endoscopic ultrasound elastogmphy:the first step towards virtual biopsy? Preliminary results in 49 patients[J].Endoscopy,2006(38):344-348.
[10]Shah JN,Ahmad NA,Beilstein MC,et al.Clinical impact of endoscopic ultrasonography on the management of malignancie[J].Clin Gastroenterol Hepatol,2004,2(12):1069-1073.
[11]夏璐,戴欣,袁勤.超聲內鏡引導下細針穿刺在消化系占位性病變診斷中的價值[J].中華消化雜志,2009,29(5):296-299.
[12]丁祥武,高山,廖曉鋒.內鏡超聲引導下細針穿刺活檢術在消化道管壁及其周圍器官疾病診斷中的應用價值[J].中華消化內鏡雜志,2011,28(9):497-501.
[13]袁德強,史維,孫曉濱.內鏡超聲介入技術診治上消化道及其壁外占位病變的價值分析[J].中華消化內鏡雜志,2010,27(4):212-214.
[14]Rickes S,Monkemuller K,Malfertheiner P.Echo-enhanced ultrasound with pulse inversion imaging:a new imaging modality for the differentiation of cvstic pancreatic tumours[J].World J Gastmenterol,2006,12(14):2205-2208.
[15]Rickes S,Uhle C,Kahl S,et al.Echo enhanced ultmsound:a new valid initial imaging appmach for severe acute pancreatitis[J].Gut,2006,55(1):74-78.
[16]Yang W,Chen MH,YaJ K,et al.Differential diagnosis of nonfunctional islet cell tumor and pancreatic carcinoma with sonography[J].Eur J Radiol,2007,62(3):342-351.
[17]嚴昆,戴瑩,王艷濱,等.超聲造影對胰腺占位病變的診斷應用價值[J].中華超聲影像學雜志,2006,15(5):361-364.
[18]Okai T,Minamoto T,Ohtsubo K,et al.Endosonographic evaluation of c-kit-positive gastrointestinal stromal tumor[J].Abdominal Imaging,2003,28(3):301-307.
[19]Quaia E,Calliada F,Bertolotto M,et al.Characterization of focal liver lesions with contrast-specific US modes and a sulfur hexafluoride-filled microbubble contrast agent:diagnostic performance and confidence[J].Radiology,2004,232(2):420-430.
[20]Brannigan M,Burns PN,Wilson SR.Blood flow patterns in focal liver lesions at microbubble-enhanced US[J].Radiographics,2004,24(4):921-935.
[21]Solbiati L,Martegani A,Leen E,et al.Contrast-enhanced ultrasound of liver diseases[M].Milan:Springer,2003:44-87.
[22]楊永生.應用六氟化硫微泡超聲造影劑診斷肝血管瘤[J].山西醫藥雜志,2014,43(8):881-882.
Diagnostic value of contrast-enhanced ultrasound endoscopy for upper gastrointestinal tract and adjacent lesions
DengWei1,JiangHaixing2,QinShanyu2△
(1.DepartmentofGastroenterology,QinzhouMunicipalSecondPeople′sHospital,Qinzhou,theGuangxiZhuangAutonomousRegion535000,China;2.DepartmentofGastroenterology,theFirstAffiliatedHospital,GuangxiMedicalUniversity,Nanning,theGuangxiZhuangAutonomousRegion530021,China)
Objective To investigate the diagnostic value of contrast-enhanced ultrasound endoscopy(CE-EUS) for the upper gastrointestinal tract and adjacent lesions.Methods One hundred and eighty samples of upper gastrointestinal tract and adjacent lesions in the First Affiliated Hospital of Guangxi Medical University from June 2014 to March 2015 were collected and performed CE-EUS.The preliminary diagnosis was taken by observing the features of various kinds of solid mass,which was conducted the contrastive analysis with the results of fine needle aspiration cytology(EUS-FNA) and (or) histopathology, biliary brush cytology smear results,operative pathologic findings,and CT,MRI scans and follow-up results.Results In 180 cases of gastrointestinal tract and adjacent placeholder,169 cases of CE-EUS were in line with the final results,while 11 cases were not consistent,and the diagnostic consistency rate was 93.9%.Conclusion CE-EUS can guide EUS-FNA puncture for increasing its positive rate..
tomography,X-ray computed;contrast media;contrast-enhanced ultrasound endoscopy;upper gastrointestinal tract and adjacent lesion;blood perfusion features;diagnosis
10.3969/j.issn.1671-8348.2017.14.021
鄧巍(1984-),主治醫師,碩士,主要從事消化道早期癌診治的研究。△
,E-mail:qsy0511@163.com。
R735
A
1671-8348(2017)14-1933-05
2016-12-02
2017-01-20)

