避免疫苗中有色物質(zhì)干擾的甲醛殘留量測定法
于曉輝,馬秋冉,張璐,董玲玲,戴青,楊秀玉
(中國獸醫(yī)藥品監(jiān)察所,北京 100081)
?
避免疫苗中有色物質(zhì)干擾的甲醛殘留量測定法
于曉輝,馬秋冉,張璐,董玲玲,戴青,楊秀玉*
(中國獸醫(yī)藥品監(jiān)察所,北京 100081)
建立了一種能有效避免疫苗中有色物質(zhì)干擾的甲醛殘留量測定法。采用乙酰丙酮分光光度法,利用“本底扣除”的方式,在410 nm波長處對疫苗中甲醛的殘留量進(jìn)行測定。結(jié)果顯示,酚紅、中性紅等有色物質(zhì)均不會對測定結(jié)果產(chǎn)生干擾;在0.002~0.2 mg/mL范圍內(nèi),吸光度與濃度呈良好的線性關(guān)系(r=0.9999,n=7);在0.005、0.05、0.15 mg/mL三種添加濃度下,該方法的平均回收率分別為110.5%、97.5%和101.3%;對24批含有有色物質(zhì)的疫苗進(jìn)行測定,所得結(jié)果與專屬性較強(qiáng)的HPLC法一致。該方法專屬性強(qiáng)、準(zhǔn)確度好、適用范圍寬,可以作為疫苗中甲醛殘留量的檢測方法。
甲醛;疫苗;有色物質(zhì)干擾;分光光度法
甲醛溶液作為滅活劑被廣泛應(yīng)用于獸用疫苗的生產(chǎn)中,由于其具有致癌性和致畸性, 因而必須對制劑中游離甲醛的含量進(jìn)行準(zhǔn)確控制,以提高產(chǎn)品的安全性,進(jìn)而保證動物源性食品的安全性。目前,國內(nèi)獸用疫苗甲醛殘留量測定的法定標(biāo)準(zhǔn)是《中國獸藥典》[1]三部,該標(biāo)準(zhǔn)中明確規(guī)定“本法僅適用于不含酚紅的產(chǎn)品”,即該方法無法準(zhǔn)確測定含有酚紅的疫苗中甲醛的殘留量,主要是因為該方法的測定波長是在可見光區(qū),疫苗中含有的酚紅會在測定波長處(410 nm)產(chǎn)生吸收,使得最終的測定結(jié)果偏高,造成測定不準(zhǔn)確。經(jīng)查閱得知,現(xiàn)行《中國藥典》[2]、《美國藥典》[3]、《歐洲藥典》[4]和《英國藥典》[5]中甲醛殘留量的測定波長均在可見光區(qū),且測定方法中均未就如何避免疫苗中有色物質(zhì)的干擾給出明確的操作建議。
1 材 料
1.1 主要儀器 紫外-可見分光光度計:TU1901,北京普析通用儀器有限責(zé)任公司;電子天平:AE240,瑞士METTLER-TOLEDO公司;恒溫水浴鍋:DK-S22型,上海精宏實(shí)驗設(shè)備有限公司。
1.2 主要試劑 甲醛對照品溶液:國藥集團(tuán)化學(xué)試劑有限公司(經(jīng)標(biāo)定其含量為37.0%);水為純化水;其余試劑均為分析純。供試疫苗樣品的相關(guān)信息見表1(供試疫苗均以編號表示)。
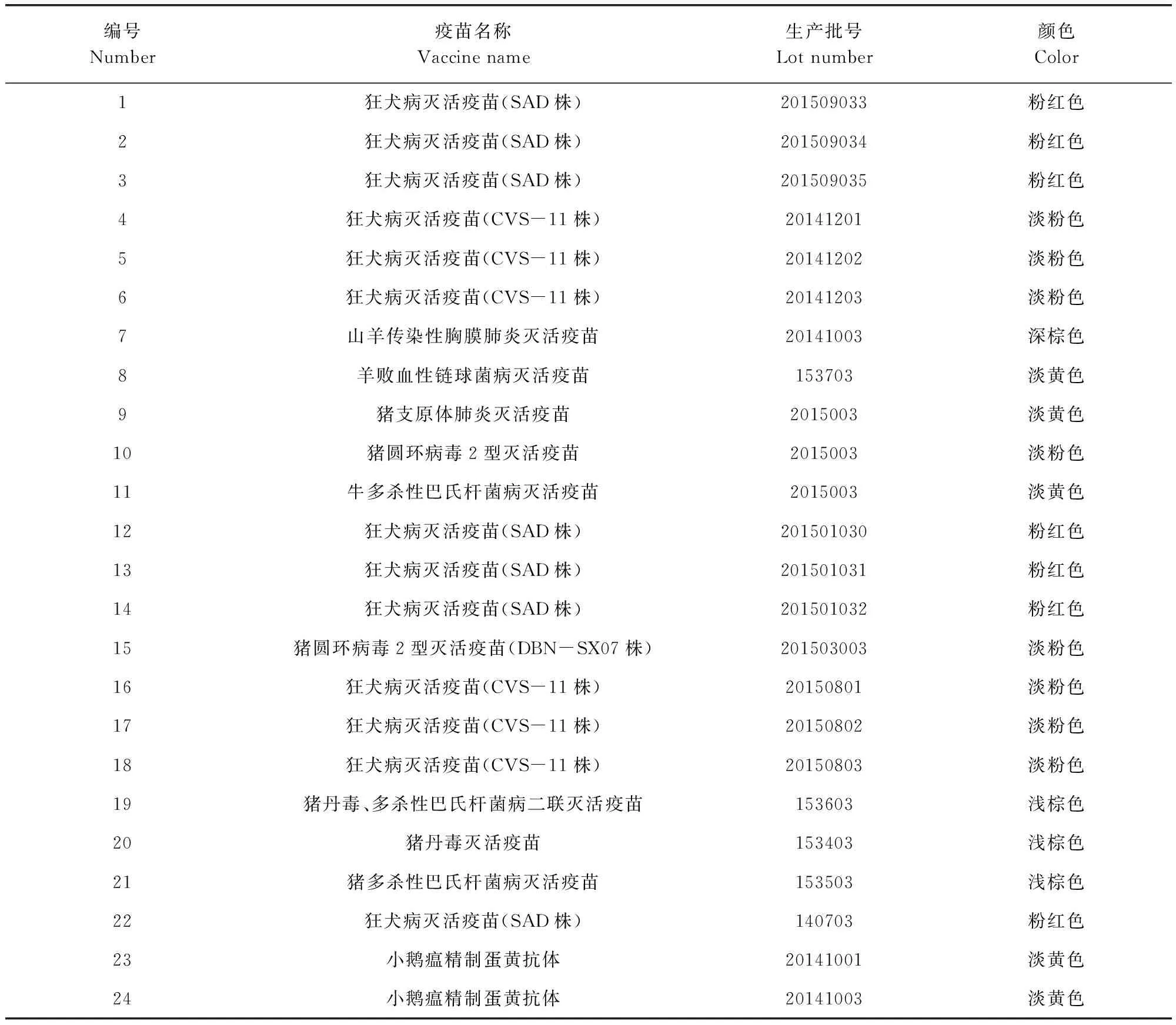
表1 供試疫苗樣品信息Tab 1 Information of tested vaccines
2 方法與結(jié)果
2.1 溶液制備 乙酰丙酮試液:量取乙酰丙酮7.0 mL,加乙醇14 mL,混勻,加水至1000 mL。醋酸-醋酸銨緩沖液:量取醋酸5.2 mL,加水至40 mL;稱取醋酸銨173.4 g,加水至1000 mL,使溶解;將上述兩種溶液混勻,即得。對照儲備液:精密稱定甲醛對照品溶液約140 mg,置于50 mL量瓶中,加水稀釋至刻度,搖勻,即得每1 mL含甲醛1.0 mg的對照儲備液。對照溶液:精密量取對照儲備液5 mL,置50 mL量瓶中,加水稀釋至刻度,搖勻。供試溶液:量取被測疫苗樣品5.0 mL,置50 mL量瓶中,加水稀釋至刻度,搖勻。
2.2 實(shí)驗方法 步驟1:分別量取對照溶液、供試溶液、水各0.5 mL,置具塞試管中,加醋酸-醋酸銨緩沖液10 mL,乙酰丙酮試液10 mL,置60 ℃水浴15 min,冷水冷卻5 min,放置20 min后,以空氣為參比,在410 nm的波長處測定吸光度,即得A對照、A供試、A空白-1。步驟2:分別量取供試溶液和水各0.5 mL,置具塞試管中,加醋酸-醋酸銨緩沖液20 mL,置60 ℃水浴15 min,冷水冷卻5 min,放置20 min后,以空氣為參比,在410 nm的波長處測定吸光度,即得A本底、A空白-2。
2.3 計算方法 根據(jù)Lambert-Beer定律和吸光度具有可加和性的特性得知,待測溶液的總吸光度等于溶液中各組分吸光度之和,即:
A供試=樣品中甲醛吸光度+樣品本底吸光度+乙酰丙酮吸光度+10 mL緩沖液吸光度
(1)
A本底=樣品本底吸光度+20 mL緩沖液吸光度
(2)
A對照=對照液中甲醛吸光度+0.5 mL水的吸光度+乙酰丙酮吸光度+10 mL緩沖液吸光度
(3)
A空白-1=0.5 mL水的吸光度+乙酰丙酮吸光度+10 mL緩沖液吸光度
(4)
A空白-2=0.5 mL水的吸光度+20 mL緩沖液吸光度
(5)
將式(1)、式(2)與式(3)、式(4)兩兩合并同類項加減,得到:
A供試- A本底=樣品中甲醛吸光度+乙酰丙酮吸光度-10 mL緩沖液吸光度
(6)
A空白-1- A空白-2=乙酰丙酮吸光度-10 mL緩沖液吸光度
(7)
將式(6)、式(7)合并同類項加減,即得:

2.4 專屬性 本研究采用的方法是乙酰丙酮法,即甲醛和顯色劑乙酰丙酮在pH值約為6的環(huán)境下,迅速生成穩(wěn)定的黃色化合物。該法選擇性強(qiáng),共存的其他化合物不易參與反應(yīng)。酚紅和中性紅作為指示劑,經(jīng)常用于培養(yǎng)基和細(xì)胞維持液的制備中,成為疫苗顏色的主要來源。焦亞硫酸鈉作為滅活阻斷劑,也會用于疫苗生產(chǎn)過程中。
本研究以酚紅、中性紅和焦亞硫酸鈉為考察對象,驗證了這三種化合物均不會參與甲醛與乙酰丙酮的反應(yīng),即這些化合物產(chǎn)生的干擾都可以通過“本底扣除”的方式抵消。具體實(shí)驗過程如下:分別配制0.02%酚紅溶液、0.002%酚紅溶液、0.1%中性紅溶液和0.4%焦亞硫酸鈉溶液,按照2.2項中的步驟1和步驟2操作,即得A1和A2,具體結(jié)果見表2。
根據(jù)表2的結(jié)果得知,當(dāng)反應(yīng)液中含有乙酰丙酮時(步驟1),酚紅、中性紅、焦亞硫酸鈉的吸光度值與不含乙酰丙酮時(步驟2)的吸光度值幾乎完全一致,表明這三種化合物的吸光度值均為自由顏色吸收,不是與乙酰丙酮反應(yīng)的結(jié)果,即這三種化合物均不會參與甲醛與乙酰丙酮的反應(yīng),它們產(chǎn)生的干擾可以通過“本底扣除”的方式抵消。實(shí)驗結(jié)果證明,該方法的專屬性良好。

表2 專屬性驗證結(jié)果Tab 2 Results of specificity
2.5 線性、范圍及定量限 量取2.1項下的對照儲備液適量,用水稀釋,制得濃度為0.0005、0.001、0.002、0.005、0.01、0.02、0.05、0.1、0.2、0.3 mg/mL的對照溶液,按照2.2項下的方法操作,測定吸光度值,以濃度X對吸光度Y作圖(圖1),得到甲醛的線性回歸方程為Y=6.7497X-0.0081(r=0.9999,n=7),線性范圍為0.002~0.2 mg/mL。
實(shí)驗結(jié)果表明,當(dāng)對照溶液濃度大于等于0.3 mg/mL時,吸光度值不穩(wěn)定,無法準(zhǔn)確測定。當(dāng)對照溶液濃度小于等于0.001 mg/mL時,吸光度值小于A空白-1,所以,本法的定量限為0.002 mg/mL。

圖1 甲醛線性關(guān)系圖Fig 1 Linear relationship of formaldehyde
2.6 回收率 以22號樣品為考察對象,向其中添加濃度為0.005、0.05、0.15 mg/mL的甲醛對照溶液,每種濃度平行制備3份樣品,按照2.2項下的方法操作,測定吸光度值,按照2.3項下的方法計算,結(jié)果見表3。
根據(jù)表3的結(jié)果得知,在0.005、0.05、0.15 mg/mL三種添加水平下,該方法的回收率在96.95%~116.19%之間,結(jié)果令人滿意,表明方法的準(zhǔn)確度良好。
2.7 精密度和溶液穩(wěn)定性 量取對照儲備液適量,分別配制濃度為0.005 mg/mL和0.02 mg/mL的甲醛對照溶液,每種濃度各配制5份,按照2.2項下的方法操作,測定吸光度值。結(jié)果,濃度為0.005 mg/mL時,RSD=1.8%;濃度為0.02 mg/mL時,RSD=0.3%,表明方法的精密度良好。
取上述兩種濃度的對照溶液,分別于0、0.5、1.5、3.5 h,按照2.2項下的方法操作,測定吸光度值。結(jié)果表明,兩種濃度下,吸光度值的RSD分別為0.2%和0.1%。實(shí)驗表明,溶液在3.5 h內(nèi)保持穩(wěn)定。
2.8 方法應(yīng)用 按照2.2項下的方法,對24批含有有色物質(zhì)的疫苗進(jìn)行測定,并將測定結(jié)果與已經(jīng)經(jīng)過驗證的高效液相色譜法[6]進(jìn)行比較,結(jié)果見表4。
從上述測定結(jié)果得知,本研究新建立的甲醛殘留量測定法的測定結(jié)果,與經(jīng)過驗證的高效液相色譜法的測定結(jié)果幾乎完全一致;新建方法設(shè)定了定量限,保證了測定結(jié)果更客觀。現(xiàn)行《中國獸藥典》中甲醛殘留量測定法的測定結(jié)果均比新建方法高,其中,偏差最大的甚至高達(dá)228%,這其中的原因主要是因為疫苗中的有色物質(zhì)對測定結(jié)果產(chǎn)生了干擾,尤其當(dāng)疫苗中甲醛含量較低時,干擾就更顯著。
3 討論與小結(jié)
本研究2.2項下步驟1的操作源自現(xiàn)行版《中國獸藥典》三部,而步驟2中的方法則是本研究的創(chuàng)新點(diǎn),即通過只添加緩沖液、不添加顯色劑乙酰丙酮,得到供試疫苗本底吸光度值。為了保證步驟1UV-新:本研究新建立的甲醛殘留量測定法;UV-原:《中國獸藥典》[1]中甲醛殘留量測定法;ND:低于方法的定量限。
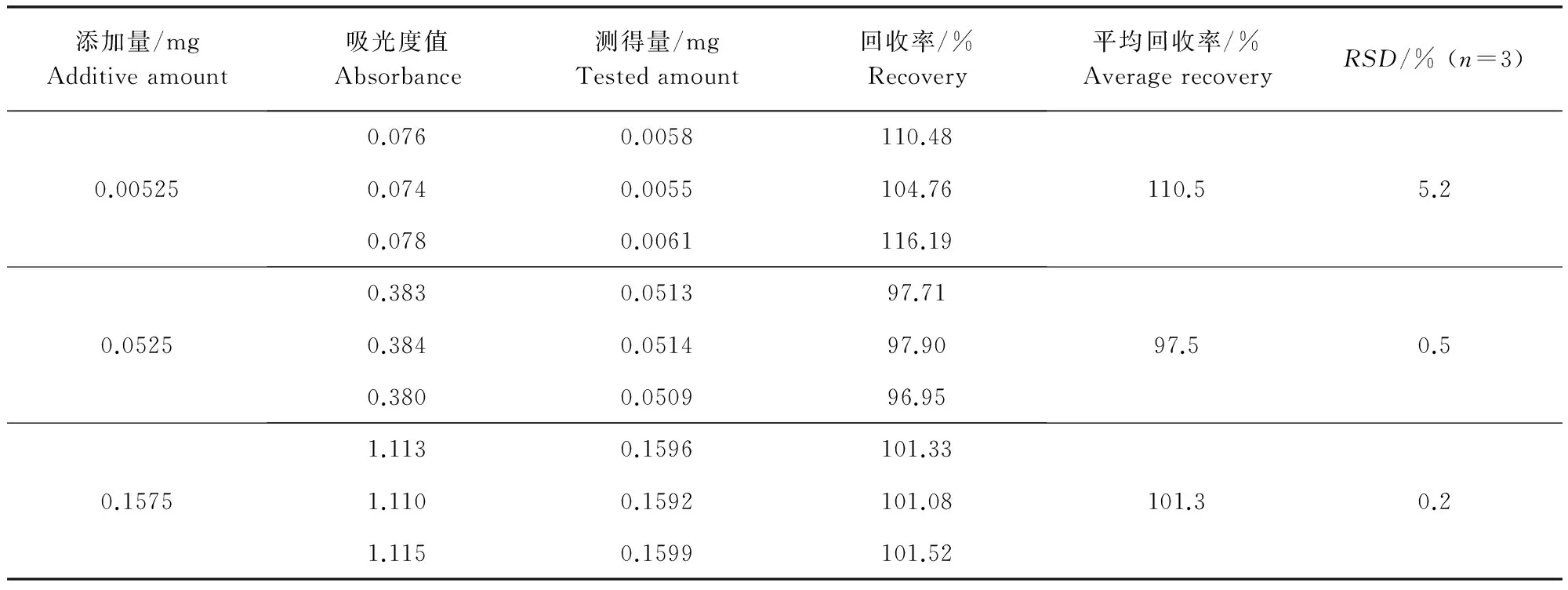
表3 回收率測定結(jié)果Tab 3 Tesults of recoveries

表4 24批疫苗樣品測定結(jié)果Tab 4 Results of 24 batches of vaccines
和步驟2中制備的溶液體積一致(即濃度一致),步驟2中緩沖液的加入量為20 mL。本研究對現(xiàn)行《中國獸藥典》中甲醛殘留量的測定方法進(jìn)行了改進(jìn),應(yīng)用新建立的方法對24批含有酚紅等多種有色物質(zhì)的疫苗進(jìn)行了測定,并將測定結(jié)果與專屬性較強(qiáng)的高效液相色譜法[6]進(jìn)行了比較和驗證。本研究創(chuàng)新采用了“本底扣除”的檢測技術(shù)成功解決了疫苗中有色物質(zhì)干擾測定結(jié)果的問題。經(jīng)文獻(xiàn)查閱得知,目前國內(nèi)外尚未見應(yīng)用該方法測定疫苗中甲醛殘留量的相關(guān)報道。相比于HPLC法,“本底扣除”的方法不但結(jié)果準(zhǔn)確,而且操作簡便、成本低廉。
通過上述實(shí)驗得知,本研究建立的方法專屬性強(qiáng)、準(zhǔn)確度高,可以作為各類疫苗(含有色物質(zhì)疫苗和不含有色物質(zhì)疫苗)中甲醛殘留量的測定方法。本研究為擴(kuò)大現(xiàn)行《中國獸藥典》的適用范圍提供了有力的技術(shù)支持,也為更好的控制獸用疫苗質(zhì)量提供了可靠的實(shí)驗依據(jù)。
[1] 中國獸藥典委員會.中華人民共和國獸藥典.三部[M].北京:中國農(nóng)業(yè)出版社,2010.
Commission of Chinese veterinary pharmacopoeia. Veterinary Pharmacopoeia of the People's Republic of China. Volume III[M]. Beijing: China Agriculture Press, 2010.
[2] 國家藥典委員會.中華人民共和國藥典.二部[M].北京:中國醫(yī)藥科技出版社,2010.
Commission of Chinese pharmacopoeia. Pharmacopoeia of the People's Republic of China. Volume II[M]. Beijing: China Medical Science Press, 2010.
[3] The United States Pharmacopeial Convention. U.S.P38-NF33 [S].
[4] European Pharmacopoeia Commission. EP 8 [S].
[5] British Pharmacopoeia Commission. BP 2015[S].
[6] 馬秋冉,張 璐,戴 青,等. 柱前衍生化-高效液相色譜法檢測疫苗中游離甲醛含量[J]. 中國獸藥雜志. 2016,50(8):20-23.
Ma Q R,Zhang L,Dai Q,et.al.Determination of Free Formaldehyde Content in Vaccine by Pre-column Derivatization HPLC[J]. Chinese Journal of Veterinary Drug, 2016, 50(8): 20-23.
(編輯:侯向輝)
Detection of Free Formaldehyde in Vaccines Avoiding Interference from Colored-Substances
YU Xiao-hui,MA Qiu-ran,ZHANG Lu,DONG Ling-ling,DAI Qing,YANG Xiu-yu*
(China Institute of Veterinary Drug Control, Beijing 100081,China)
YANG Xiu-yu, E-mail: yxyyang0903@163.com
To establish a method for the detection of free formaldehyde in vaccines that can avoid the interference from colored substances, the analysis was performed by acetyl acetone spectrophotometric method with the means of "deducting background" at 410 nm. Phenol red and neutral red did not interfere with the result; the linearity range was 0.002~0.2 mg/mL (r=0.9999,n=7) , and under 0.005, 0.05, 0.15 mg/mL levels of accession, the average recoveries were respectively 108.6%, 97.5% and 101.3%; 24 batches of sample were detected by the new established method, and the results were in agreement with HPLC. The method is characterized by good specificity and accuracy with wide adaptive range. It can be used for the formaldehyde detection in vaccines.
formaldehyde; vaccines; colored-substance interference; spectrophotometry
10.11751/ISSN.1002-1280.2017.5.05
于曉輝,碩士,副研究員,從事獸藥檢測工作。
楊秀玉,E-mail:yxyyang0903@163.com
2016-11-25
A
1002-1280 (2017) 05-0022-06
S859.797

