卵裂期凍融復蘇胚胎進一步發育情況對臨床結局的影響
惠董娜,任文娟,雷鑫,劉建榮,王懷秀,李弘
(山西省人民醫院生殖醫學科,太原 030012)
卵裂期凍融復蘇胚胎進一步發育情況對臨床結局的影響
惠董娜,任文娟,雷鑫,劉建榮,王懷秀,李弘*
(山西省人民醫院生殖醫學科,太原 030012)
目的 探討卵裂期凍融復蘇胚胎過夜培養后胚胎生長個數及卵裂球增殖情況對臨床結局的影響。 方法 回顧性分析我中心268個卵裂期FET周期,根據過夜培養后復蘇胚胎的生長個數分為0個生長組(A1,n=46)、1個生長組(A2,n=48)和2個及以上生長組(A3,n=174);根據卵裂球增殖情況分為<8細胞組(B1,n=39)、8~16細胞組(B2,n=57)和含融合細胞組(B3,n=126);比較各組間的種植率、妊娠率和多胎率。 結果 A3組妊娠率、種植率(分別為55.17%、34.29%)顯著高于A1組(分別為15.22%、6.67%)、A2組(分別為29.17%、16.00%)(P<0.01),且A2組妊娠率、種植率顯著高于A1組(P<0.01),A3組多胎率顯著高于A2組(36.46% vs.7.14%)(P<0.01),A1組無多胎妊娠;B2組妊娠率顯著高于B1組(52.63% vs.27.59%)(P<0.01),B2組種植率顯著高于B1組(31.15% vs.10.71%)(P<0.05),而B2組與B3組妊娠率、種植率均無顯著差異(P>0.05),三組間多胎率無顯著差異(P>0.05),但B3組多胎率有所升高。 結論 卵裂期凍融胚胎經過夜培養后,有2個及以上生長的胚胎,且卵裂球發育到8~16細胞或有融合細胞階段者,能獲得更好的臨床結局;對移植含2個及以上生長的胚胎,可考慮選擇單胚胎移植,以降低多胎妊娠長方案及拮抗劑方案中HCG日孕酮水平對IVF-ET妊娠結局的影響。
卵裂期胚胎; 凍胚移植; 過夜培養; 種植率; 臨床妊娠率; 多胎率
(JReprodMed2017,26(1):19-23)
凍融胚胎移植(FET)作為輔助生殖中一項重要的衍生技術,可避免卵巢過度刺激綜合征(OHSS),使患者一次促排卵周期形成的胚胎實現最大限度的利用,有效地提高了臨床累積妊娠率[1]。FET能否取得較好的臨床結局與解凍復蘇后的胚胎質量密切相關[2-3]。通過觀察過夜培養后胚胎進一步發育情況評估胚胎質量,為選擇具有高種植潛力和發育潛能的胚胎提供了一個重要指標[4],并以此達到改善臨床結局的目的。本文回顧性分析我中心268個FET周期,依據凍融復蘇后移植胚胎生長個數以及卵裂球增殖情況探討胚胎質量對FET臨床結局的影響。
資料與方法
一、臨床資料
收集2013年6月至2014年12月在本院生殖醫學科行全胚冷凍或新鮮周期移植失敗的患者234例,268個周期。女方年齡21~48歲,不孕年限1~20年。
納入標準:卵裂期凍融胚胎移植周期;女方因盆腔輸卵管、排卵障礙等因素不孕,男方少、弱、畸精、無精癥等因素不育,以及免疫因素、原因不明致不孕;內膜準備方案均為人工周期。
排除標準:移植單個卵裂期胚胎;女方子宮內膜異位癥、宮腔粘連等影響著床的因素。
二、方法
1.冷凍胚胎的選擇:胚胎質量評分按我科標準進行評級:Ⅰ級≥8細胞,卵裂球大小均勻,碎片<5%,無空泡,無多核;Ⅱ級≥7細胞,卵裂球大小均勻或大致均勻,碎片10%~20%,無空泡,無多核;Ⅲ級4~7細胞或≥8細胞,卵裂球大小不均勻,碎片≤20%,有少量空泡,無多核;Ⅳ級4~7細胞或≥8細胞,碎片>20%,卵裂球大小不均勻,有多核;Ⅴ級<4細胞或大量碎片,半數卵裂球為多核。D3選擇Ⅰ、Ⅱ、Ⅲ級胚胎進行冷凍。
2.胚胎凍融、培養與移植:按上述標準冷凍保存D3胚胎。胚胎冷凍采用玻璃化法冷凍試劑盒(Kitazato,日本),操作按說明書進行,每載桿放置2~3枚胚胎,置于最前端,快速放入液氮中保存;于移植前一天下午解凍,根據患者情況選擇解凍胚胎的數量,一般2或3枚胚胎,采用玻璃化解凍試劑盒(Kitazato,日本),具體操作按說明書進行;解凍后胚胎轉入含人血清替代品的1026中(Quinn’s, SAGE,美國),過夜培養17 h,第2天早上觀察胚胎、評級并做輔助孵化,再行移植。解凍后未移植的胚胎,根據其質量決定繼續凍存或廢棄。
3.內膜準備:內膜準備方案均采用人工周期。月經周期第2~3天行陰道超聲,根據患者既往內膜厚度決定戊酸雌二醇(補佳樂,拜耳,德國)的起始用量及持續用量,待子宮內膜≥8 mm并出現三線征時,加用黃體酮并誘導內膜向分泌期轉化,3 d后移植。
4.研究分組:(1)根據過夜培養后,胚胎復蘇生長情況分為0個生長組(A1,n=46)、1個生長組(A2,n=48)、2個及以上生長組(A3,n=174);(2)在胚胎生長組中,根據卵裂球生長情況分為≤8細胞組(B1,n=39)、8~16細胞組(B2,n=57)、含融合細胞(Compaction,CP)組(B3,n=126)。
5.隨訪及確定妊娠:移植后12~14 d檢測血清?-HCG,若血清?-HCG>25 U/L提示妊娠,則繼續黃體支持;若血清?-HCG<0.5 U/L,則未妊娠,停止黃體支持。移植后30 d超聲檢查見孕囊、胚芽,移植后35 d超聲檢查心管搏動者確定為臨床妊娠,繼續黃體支持至妊娠10~12周。
三、統計學分析

結 果
一、患者一般資料
本研究共納入268個卵裂期FET周期。共解凍胚胎632枚,存活胚胎599枚,胚胎存活率94.78%;移植胚胎587枚,種植154枚,種植率26.24%;妊娠117個周期,平均妊娠率43.66%,多胎妊娠36個周期,多胎妊娠率30.77%。
根據過夜培養后移植胚胎生長個數分為:0個生長組(A1);1個生長組(A2);2個及以上生長組(A3)。三組患者的年齡、不孕年限、原發不孕比率、ICSI比率以及移植日內膜厚度均無統計學差異(P>0.05);2個及以上生長組(A3)全胚冷凍比例高于0個生長組(A1)及1個生長組(A2),但無統計學差異(P>0.05)(表1)。
二、過夜培養后胚胎生長情況對臨床結局的影響
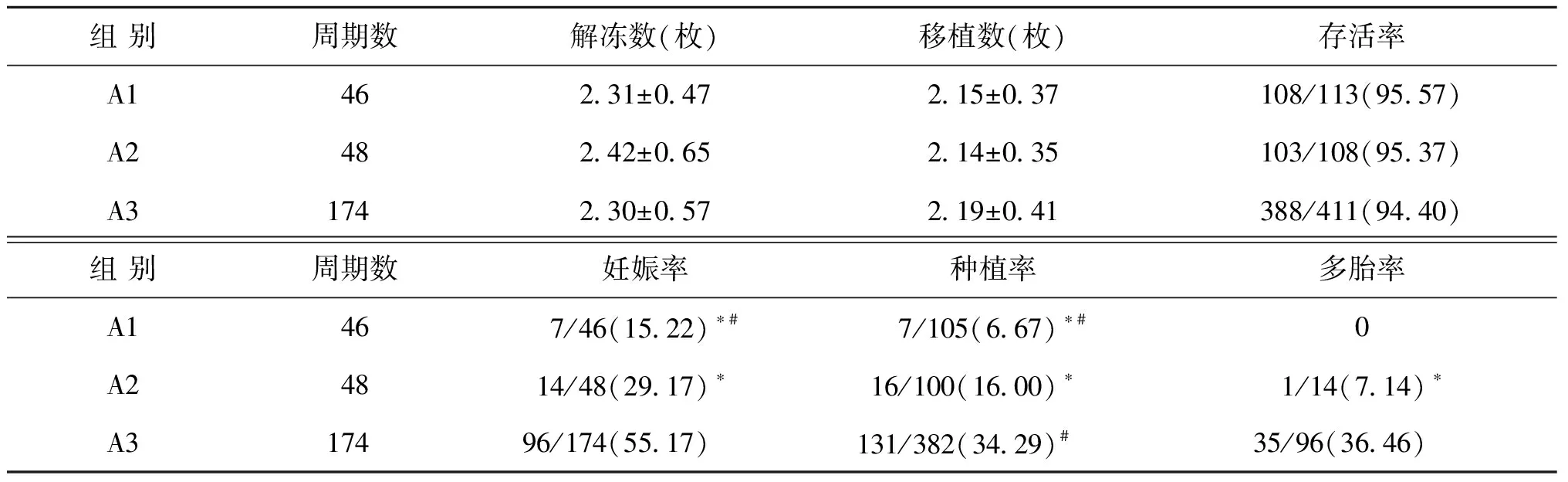
過夜培養后,A1組46個周期,妊娠率15.22%,種植率6.67%,無多胎妊娠;A2組48個周期,妊娠率29.17%,種植率為16.00%,多胎率7.14%;A3組174個周期,妊娠率55.17%,種植率34.29%,多胎率36.46%。三組間解凍個數、移植個數及存活率無顯著差異(P>0.05)。A3組妊娠率、種植率顯著高于A1、A2組(P<0.01),A2組妊娠率、種植率顯著高于A1組(P<0.01)。A3組多胎率顯著高于A2組(P<0.01),A1組無多胎妊娠(表2)。


組別周期數年齡(歲)不孕年限(年)原發不孕比例A1463028±485341±24833/46(7174)A2482868±391382±31040/48(8333)A31742934±449370±314130/174(7471)組別周期數ICSI比例全胚冷凍比例移植日內膜厚度(cm)A1465/46(1087)20/46(4348)093±085A24813/48(2708)22/48(4583)094±090A317439/174(2241)101/174(5805)095±110

組別周期數解凍數(枚)移植數(枚)存活率A146231±047215±037108/113(9557)A248242±065214±035103/108(9537)A3174230±057219±041388/411(9440)組別周期數妊娠率種植率多胎率A1467/46(1522)?#7/105(667)?#0A24814/48(2917)?16/100(1600)?1/14(714)?A317496/174(5517)131/382(3429)#35/96(3646)
注:與A3組比較,*P<0.01;與A2組比較,#P<0.01
三、卵裂球生長情況對臨床結局的影響
過夜培養17 h后,根據卵裂球生長情況分組比較。B1組39個周期,妊娠率27.59%,種植率10.71%、多胎率11.11%;B2組57個周期,妊娠率52.63%,種植率31.15%、多胎率27.59%;B3組126個周期,妊娠率52.94%,種植率36.23%、多胎率37.50%。三組間解凍個數、移植個數及存活率無顯著性差異(P>0.05)。B2、B3組種植率顯著高于B1組 (P<0.01);B2組妊娠率顯著高于B1組(P<0.05);B3組妊娠率顯著高于B1組(P<0.01)。三組間多胎率比較無顯著差異(P>0.05),但B3組多胎妊娠率有所升高(表3)。


組別周期數解凍數(枚)移植數(枚)存活率B139231±047215±03786/91(9451)B257242±065214±035127/138(9203)B3126230±057219±041278/290(9586)組別周期數妊娠率種植率多胎率B1398/29(2759)?#9/84(1071)?Δ1/9(1111)B25730/57(5263)38/122(3115)8/29(2759)B312672/136(5294)100/276(3623)27/72(3750)
注:與B3組比較,*P<0.01;與B2組比較,#P<0.05,ΔP<0.01
討 論
FET因其可避免卵巢過度刺激、減少再次促排卵操作等優點成為一些患者臨床治療的選擇方案。有研究表明胚胎質量是影響FET臨床結局的重要因素之一[2-3]。目前對FET周期中胚胎體外培養時間的選擇多在解凍后2~4 h或是經過夜培養后,而是否要延長凍融胚胎的體外培養時間,各個中心的標準不同[5-8],且對凍融胚胎體外培養時間和臨床結局關系的認識也不同[6,8]。近來的一些研究顯示,凍融復蘇的胚胎經過夜培養,通過觀察其是否恢復分裂并有增殖的細胞,可作為評價凍融復蘇胚胎質量的一個指標,從而選擇出具有高發育潛能的胚胎,以提高臨床妊娠率[4,9-10]。
本研究所納入的FET周期中解凍的胚胎經過夜培養后移植,根據移植時胚胎生長個數分為0個生長組、1個生長組、2個及以上生長組,各組間患者的年齡、不孕年限、原發不孕比例以及移植日內膜厚度等臨床資料均無統計學差異,且內膜準備方案均采用人工周期,避免了其它影響FET臨床結局的因素。結果顯示,移植含2個及以上生長的胚胎組,其妊娠率和種植率顯著高于0個生長組及1個生長組,差異具有統計學意義,且1個生長組的妊娠率及種植率顯著高于0個生長組。說明復蘇胚胎經過夜培養,能夠恢復分裂生長的胚胎具有更好的發育潛能,可作為選擇移植胚胎的一個關鍵指標,且移植含有2個及以上生長個數的胚胎能獲得更好的臨床結局。
解凍復蘇的胚胎經過夜培養后進一步生長,具體表現為卵裂球數目的增加,即細胞的增殖。有研究表明復蘇4 h已分裂的胚胎其臨床妊娠率和單胚著床率都顯著大于未分裂組[11],而復蘇后24 h未有卵裂球分裂生長的胚胎往往表現為染色體異常,僅有20%的胚胎為正常的二倍體[12],說明復蘇后胚胎能快速恢復有絲分裂是其具有良好發育潛能的一項重要指標。本研究中復蘇后繼續生長的8~16細胞組及含CP細胞組的妊娠率、種植率顯著高于<8細胞組胚胎,而8~16細胞組和含CP細胞組的妊娠率及種植率無顯著差別,提示復蘇胚胎的卵裂球數目增加大于8細胞或已至融合階段的會有更好的種植率及妊娠率,可能是由于8~16細胞或含CP的胚胎在隨后發育中更容易形成囊胚,打破發育阻滯的情況,且發生細胞融合的胚胎促進了基因調控由母型調節向胚胎型調節的轉化,對囊胚腔的形成、內細胞團及胚層分化發揮著積極作用,預示著較好的臨床結局[13-14]。
多胎妊娠是輔助生殖技術中最為關注的問題之一,其所造成的妊娠高風險,以及對圍產兒及新生兒健康等方面的影響, 成為輔助生殖領域亟待解決的問題。為降低多胎妊娠的風險,選擇合適的單胚胎移植成為研究的焦點[15]。有研究表明,與多胎妊娠相關的因素包括年齡、獲卵數、可利用胚胎數、移植胚胎數量、移植胚胎質量以及冷凍胚胎數[16]。本文對解凍后復蘇胚胎質量與多胎妊娠的關系進行分析,結果顯示含2個及以上生長胚胎組的多胎率顯著高于0個生長組及1個生長組,差異顯著有統計學意義,而0個生長組無多胎妊娠,提示過夜培養后,有2個及以上生長的胚胎需考慮選擇單胚胎移植以降低多胎妊娠。同時,比較了有卵裂球增殖的胚胎,發現含CP組多胎率較高,但與<8細胞組及8~16細胞組比較并無顯著差異,可能與樣本量有關,仍需進一步研究。
綜上所述,胚胎質量是影響卵裂期凍融胚胎移植臨床結局的重要因素。復蘇胚胎經過夜培養,能快速恢復有絲分裂并有增殖細胞者,預示有較好的發育潛能。移植中含有2個及以上生長的胚胎,且卵裂球數目在8~16細胞或含融合細胞的可獲得更好的臨床結局。對復蘇后繼續生長含有2個及以上生長的胚胎,可考慮選擇單胚胎移植,并充分告知患者,以減少多胎妊娠的風險。
[1] 李媛.人類輔助生殖實驗技術[M].第一版.北京:科學出版社,2008:139-140.
[2] Zdravka V, Mauri O, Sinikka NH, et al. Factors affecting the outcome of frozen-thawed embryo transfer[J]. Hum Reprod, 2013, 28: 2425-2431.
[3] 李榮,丘映,江莉,等.玻璃化凍融胚胎移植結局的相關因素分析[J].中國計劃生育和婦產科,2015,7:31-34.
[4] 丁錦麗,楊菁,張艷,等.卵裂期胚胎凍融后發育速度可能作為胚胎植入潛能的評估參數[J].生殖醫學雜志,2015,24:606-610.
[5] 羅金,楊菁,徐望明. 胚胎凍融后體外培養時間對妊娠結局的影響[J].生殖與避孕,2011,31:97-100.
[6] 駱榮,胡慧,洪焱,等. 玻璃化凍融胚胎提前解凍與當日解凍移植結局比較[J].生殖醫學雜志,2015,24:17-20.
[7] 趙杰,陳秀娟,劉芳,等.冷凍胚胎解凍后質量對臨床妊娠結局的影響[J].生殖醫學雜志,2014,23:981-985.
[8] Sole M, Santalo J, Rodriguez I, et al. Correlation between embryological factors and pregnancy rate: development of an embryo score in a cryopreservation programme[J]. J Assist Reprod Genet,2011,28:129-136.
[9] 李榮,許常龍,譚秀群,等.凍融卵裂期胚胎移植中過夜培養對臨床妊娠結局的影響[J].實用醫院臨床雜志,2015,12:55-57.
[10] 李偉,施文浩,李明昭,等.玻璃化凍融后胚胎卵裂球的損傷與生長融合對移植結局的影響[J].生殖醫學雜志,2015,24:542-545.
[11] 孫貽娟,馮云,張愛軍,等.凍融胚胎移植周期中胚胎因素的分析研究[J].生殖與避孕,2007,27:577-580.
[12] Laverge H, VanderElst J, DeSutter P, et al. Fluorescent in-situ hybridization on human embryos showing cleavage arrest after freezing and thawing[J].Hum Reprod, 1998,13:425-429.
[13] Blake DA,Farquhar CM. Cleavage stage versus blastocyst stage embryo transfer in assisted conception[J/DB].Cochrane Database Syst Rev,2007,17: CD002118.
[14] Iwata K, Yumoto K, Sugishima M,et al. Analysis of compaction initiation in human embryos by using time-lapse cinematography[J]. J Assist Reprod Genet, 2014, 31:421-426.
[15] Murray SR,Norman JE. Multiple pregnancies following assisted reproductive technologies-a happy consequence or double trouble? [J]. Semin Fetal Neonatal Med, 2014, 19:222-227.
[16] Hernandez-Nieto CA, Mendez-Lozano DH, Fraustro-Avila ME, et al. Analysis of factors associated with multiple pregnancies in assisted reproduction treatment complex[J].Ginecol Obstet Mex., 2016, 84:27-30.
[編輯:谷炤]
Impact of further development of frozen-thawed embryo on clinical outcome
HUI Dong-na, REN Wen-Juan, LEI Xin, LIU Jian-rong,WANG Huai-xiu,LI Hong*
DepartmentofReproductiveMedicine,ShanxiProvincialPeople’sHospital,Taiyuan030012
Objective: To explore the impact of the number of grown embryos and the blastomere proliferation after overnight culture in frozen-thawed embryos at cleavage stage on the clinical outcome.Methods: A total of 268 frozen-thawed cycles were analyzed retrospectively. According to the number of grown embryos after overnight culture, the cycles were divided into three groups: no grown embryo group (A1,n=46); one grown embryo group (A2,n=48) and more than two grown embryos group (A3,n=174). According to the proliferation of blastomere, the cycles were divided into three groups: blastomeres<8-cell group (B1,n=39), blastomeres 8 to 16-cell group (B2,n=57) and blastomeres compacted group (B3,n=126). The implantation rate, pregnancy rate and the multiple pregnancy rate were compared among the groups.Results: The pregnancy rate (55.17%) and implantation rate (34.29%) in group A3 were significantly higher than those in group A1 (15.22%, 6.67% respectively) or group A2 (29.17%, 16.00% respectively) (P<0.01), and those of group A2 were significantly higher than group A1 (P<0.01).The multiple pregnancy rate in group A3 were significantly higher than that in group A2 (36.46% vs.7.14%,P<0.01). There were no multiple pregnancy in group A1. The pregnancy rate (52.63% vs. 27.59%,P<0.01) and the implantation rate(31.15% vs.10.71%,P<0.05) in group B2 were significantly higher than those in group B1. The pregnancy rate and implantation rate between group B2 and B3 had no significant differences (P>0.05). There was no significant difference in multiple pregnancy rate among group B1, B2, and B3 (P>0.05), but multiple pregnancy rate was slightly higher in group B3.Conclusions: Frozen-thawed embryos at cleavage stage after overnight culture, which had more than two grown embryos and blastomeres developed to 8 to 16-cell or compaction formed, can obtain better clinical outcomes. Single embryo transfer can be considered for patients who have more than two grown embryos after frozen-thawed to reduce multiple pregnancies.
Cleavage embryo; Frozen-thawed embryo transfer; Overnight culture; Implantation rate; Clinical pregnancy rate; Multiple pregnancy rates
10.3969/j.issn.1004-3845.2017.01.004
2016-06-16;
2016-07-12
惠董娜,女,山西侯馬人,碩士,檢驗技師.(*

