立方體納米Cu2O表面熱力學函數的粒度及溫度效應
湯煥豐 黃在銀,2,* 肖 明
(1廣西民族大學化學化工學院,南寧530006;2廣西高校食品安全與藥物分析化學重點實驗室,南寧530006)
立方體納米Cu2O表面熱力學函數的粒度及溫度效應
湯煥豐1黃在銀1,2,*肖 明1
(1廣西民族大學化學化工學院,南寧530006;2廣西高校食品安全與藥物分析化學重點實驗室,南寧530006)
液相還原法合成了4種粒度在40-120 nm的立方體納米氧化亞銅(Cu2O)。利用X射線衍射儀(XRD)、顯微拉曼光譜儀和場發射掃描電子顯微鏡(FE-SEM)對納米Cu2O的物相組成及形貌結構進行了表征。采用原位微熱量技術實時獲取納米/塊體Cu2O與HNO3反應過程的熱動力學信息,結合熱化學循環及動力學過渡態理論計算得到納米Cu2O的表面熱力學函數。在薛永強等建立的無內孔球形納米顆粒的熱力學模型基礎上,發展了立方體納米顆粒的熱力學模型。最后由理論結合實驗結果分析了粒度和溫度對表面熱力學函數的影響規律及原因。結果表明,摩爾表面Gibbs自由能、摩爾表面焓和摩爾表面熵均隨粒度減小而增大,且與粒度的倒數呈線性關系,這與立方體熱力學模型規律一致;隨著溫度的升高,摩爾表面焓和摩爾表面熵均增大,摩爾表面Gibbs自由能則減小。本文不僅豐富和發展了納米熱力學基本理論,還為納米材料表面熱力學研究及應用提供了方法和思路。
表面熱力學函數;原位微熱量技術;熱力學模型;粒度效應;溫度效應;立方體納米Cu2O
Key Words:Surface thermodynamic function;In-situ microcalorimetry;Thermodynamic model; Particle size effect;Temperature effect;Cubic nano-cuprous oxide
1 引言
表面熱力學函數,包括Gibbs自由能、焓、熵等,是納米材料產生表面效應的熱力學特性,更是納米材料產生表面構效關系的直觀反映,極大地影響納米粒子多相反應過程的熱力學1,2、動力學3及電化學4、催化5、生物抗菌6、傳感7等過程。納米材料表面Gibbs自由能、表面焓、表面熵是聯系表面原子結構、電子結構和幾何結構的綜合體現,表面結構的調控實質就是調控表面能。因此,研究其粒度及溫度效應能為納米催化提供熱力學原理和技術方法,能更好理解納米表面反應的本質。然而,目前關于Cu2O的研究多圍繞在尺寸的精準調控及催化性能的改進等8,9,尚缺乏表面熱力學函數的粒度及溫度效應的深入研究。
減小粒度至納米尺度,可以顯著增大表面能,從而增強反應活性10。2016年Science最新報道Hutchings團隊11利用Pd-Sn高效催化生產H2O2,發現其高催化活性與粒度密切相關。最近,Jamshidian等12由密度泛函理論及連續介質理論證實表面能隨粒度減小而減小。Range等13發現當粒度d<20 nm時,表面能效應隨著粒度減小急劇增大,例如d= 0.9 nm時,表面能增大87%。上述研究的表面能多是理想模型的計算結果,相對于存在大量原子階梯和不飽和鍵的真實表面差異較大。因此,發展一種普適的實驗方法獲取表面能是當前納米表面科學亟待解決的關鍵問題。原位微熱量技術14,15是一種能實時在線監測體系熱動力學變化過程并結合熱動力學原理及動力學過渡狀態理論獲取表面能的實驗方法,具有高精度、高靈敏度,快速準確地獲取體系變化過程的熱力學和動力學精細信息的獨特優勢,廣泛應用于納米材料生長、反應、吸附、溶解過程熱動力學研究及表面能測定,具有普適性和科學性。
本文采用原位微熱量技術獲取Cu2O與HNO3反應過程熱動力學參數,結合化學熱化學循環及熱力學基本理論,計算獲得立方體納米Cu2O的表面熱力學函數,并建立熱力學模型討論了粒度及溫度對納米Cu2O摩爾表面Gibbs自由能、摩爾表面焓和摩爾表面熵的影響規律及原因。
2 實驗部分
2.1試劑與儀器
CuSO4·5H2O(純度≥99.0%),NaOH(純度≥96.0%)購于國藥集團化學試劑有限公司;檸檬酸三鈉(純度≥99.0%),抗壞血酸(純度≥99.7%),HNO3(純度為65%-68%)均購于廣東西隴化工股份有限公司;塊體Cu2O(純度≥99.0%)購于阿拉丁試劑有限公司;不同粒度納米Cu2O為實驗室自主合成。
微量電子天平(XS3DU,瑞士梅特勒-托利多國際股份有限公司);手動移液器(Research plus,德國艾本德股份公司);X射線衍射儀(XRD,Ultima IV,日本理學株式會社);顯微拉曼光譜儀(Raman,InVia,英國雷尼紹公司);場發射掃描電子顯微鏡(FE-SEM,SUPRA 55 Sapphire,德國卡爾蔡司公司);微熱量儀(RD 496-CK 2000,綿陽中物熱分析儀器有限公司)。
2.2不同粒度立方體納米Cu2O的制備
量取200 mL去離子水和一定量的檸檬酸三鈉于燒杯中,在30°C水浴池以恒定速率攪拌20 min;快速注入0.5 mL、1.2 mol·L-1CuSO4,反應5 min后,滴加0.5 mL、4.8 mol·L-1NaOH,繼續反應5 min,滴加0.5 mL、1.2 mol·L-1抗壞血酸,反應30 min得到橙紅色沉淀;靜置后,分別用去離子水和無水乙醇離心洗滌3次,通N2保存于無水乙醇中。其中0.3,0.6,0.9和1.2 mol·L-1檸檬酸三鈉分別對應平均粒度為42,55,67和116 nm的立方體Cu2O。
2.3Cu2O微熱量實驗
微量電子天平準確稱取1.500 mg納米/塊體Cu2O置于15 mL樣品池,然后使用移液器手動移取1.0 mL、2.0 mol·L-1的HNO3溶液于小玻璃管中。設定微熱量儀參數,分別恒溫至298.15、308.15和318.15 K。待基線平穩后捅破小玻璃管,使Cu2O和HNO3混合發生反應,得到反應過程的原位熱譜曲線。經計算可獲得不同粒度納米Cu2O的表面熱力學函數。
3 結果與討論
3.1Cu2O的表征
圖1(a)的XRD圖譜顯示產物所有的衍射峰均與氧化亞銅面心立方晶系Cu2O(JPCDS卡片No. 05-0667)相對應,各衍射峰強度較強,峰寬較窄且未見其他雜質峰,表明它們結晶度良好,晶體較純。圖1(b)產物的拉曼特征峰均與文獻報道的Cu2O相符16,17,沒有出現CuO的特征峰18。其中,112 cm-1拉曼位移屬于Γ-振動模式,150和632
12cm-1處的振動屬于Γ-
紅外活性模式,218和304
15cm-1歸屬為二階倍頻2Γ-振動模式,而414和506
12cm-1則分屬于四階倍頻4Γ-
振動模式和Γ+雙聲子模
1225式19,20。218 cm-1處峰型尖銳表明納米Cu2O結晶度好,并佐證了XRD結果。由圖2(a-d)納米Cu2O的SEM圖可看出,該Cu2O為不同納米尺寸下的立方體形貌,其形貌規則,表面光滑和棱角分明。粒度分布直方圖顯示納米Cu2O分布集中且粒度均勻,通過Nano Measurer對納米Cu2O的電鏡圖進行統計,其平均粒度依次為(42±6)、(55±7)、(67± 8)和(116±17)nm。
3.2立方體納米Cu2O熱力學理論模型
在恒溫恒壓下,各相中物質的量不變時,根據文獻21-23推導的無內孔球形納米顆粒熱力學模型,可以得摩爾表面Gibbs自由能為:
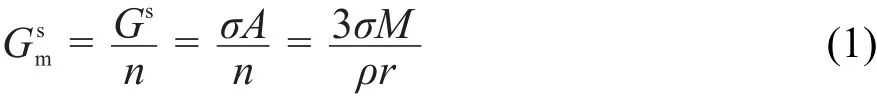
式中,Gs為表面Gibbs自由能,n、σ、A、M、ρ和r分別為納米顆粒的物質的量、表面張力、表面積、摩爾質量、密度和顆粒半徑。
對于立方體納米顆粒,其總面積和總物質的量分別為:
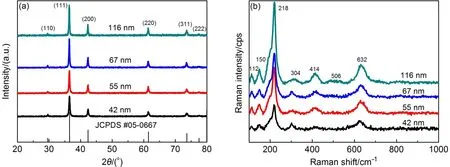
圖1 不同粒度納米氧化亞銅的(a)XRD圖譜和(b)拉曼光譜Fig.1 (a)XRD patterns and(b)Raman spectra of nano-Cu2O with different sizes
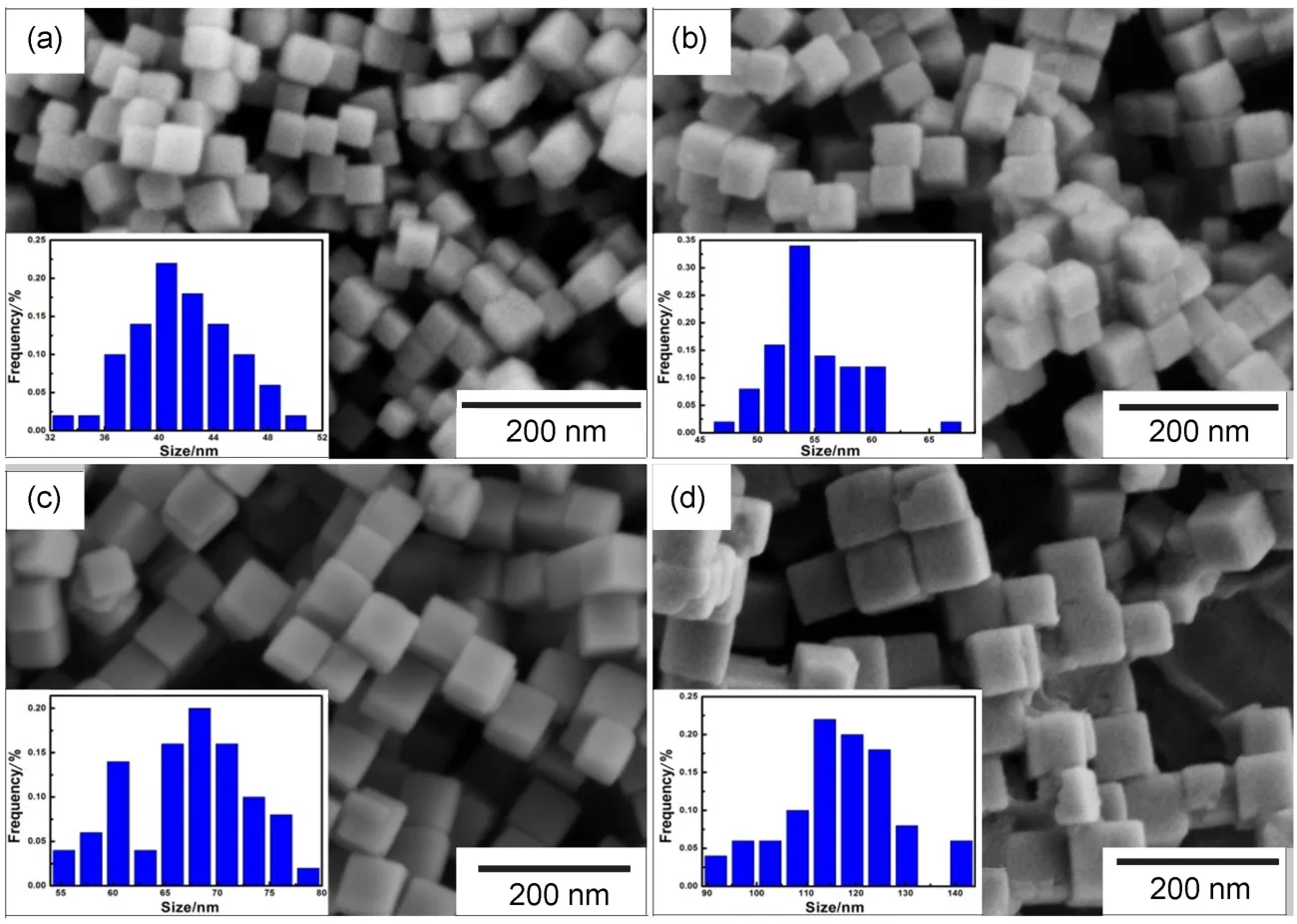
圖2 不同粒度納米氧化亞銅的SEM圖譜和粒徑分布直方圖Fig.2 SEM image and the distribution histograms of nano-Cu2O with different sizes

式中,N、V和l分別為納米顆粒的顆粒數、單個顆粒的體積和邊長。
將式(2)和(3)代入式(1),即可得到立方體納米顆粒的摩爾表面Gibbs自由能為:

由于化學反應過程粒度發生改變,其偏摩爾表面Gibbs自由能不等于摩爾表面Gibbs自由能。所以,對于立方體納米顆粒,其偏摩爾表面Gibbs自由能表達式為:
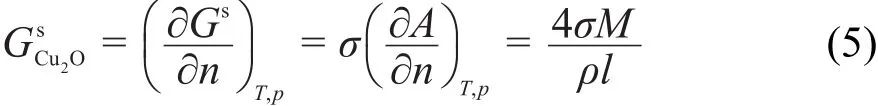
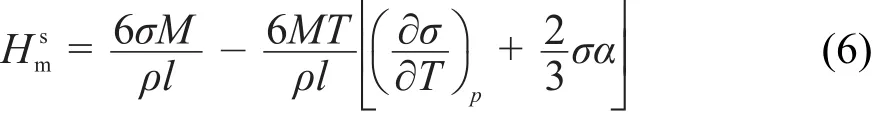
式中,α為等壓體積膨脹系數。
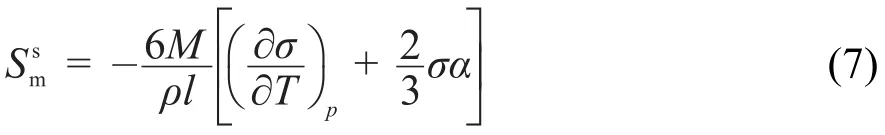
當納米顆粒的粒徑大于10 nm時,表面張力可近似為常數24。由式(4)可知,摩爾表面Gibbs自由能隨著粒度的減小而增大;對于固體顆粒α的數值很小,溫度不是很高時可以忽略,又因為普通固體物質,所以,式(6)中摩爾表面焓隨著粒度的減小而增大;同理,由式(7)可知,摩爾表面熵隨著粒度的減小而增大。
3.3立方體納米Cu2O表面熱力學函數的獲取
納米體系化學反應的摩爾Gibbs函數及摩爾焓由體相和表面相兩部分組成,而塊體化學反應的摩爾Gibbs函數及摩爾焓幾乎只有體相部分,因此納米與塊體體系的差值就是表面熱力學函數。根據文獻25,26,結合圖3的熱化學循環及過渡態理論,可獲得納米的摩爾表面焓,偏摩爾表面Gibbs自由能及摩爾表面熵(Ssm)計算公式為:
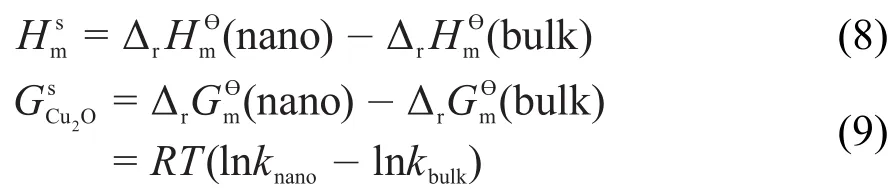
式中,knano和kbulk分別為納米和塊體Cu2O的反應速率常數,T為溫度,ΔrH?m為摩爾反應焓。
根據《物理化學中的量、單位和符號》27規定,采用過渡態理論由速率常數得到的是而非。但由式(4)及(5)可知,和Gsm之間有明確的關系且二者之比為2:3。
故由式(9)及二者的關系,可得納米Cu2O的摩爾表面Gibbs自由能為:
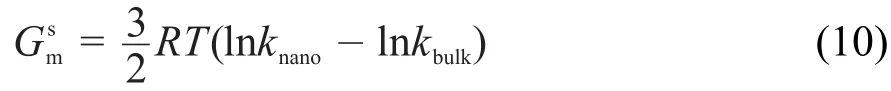
由(8)及(10)可得納米Cu2O的摩爾表面熵為:

3.4粒度及溫度對納米Cu2O表面熱力學函數的影響
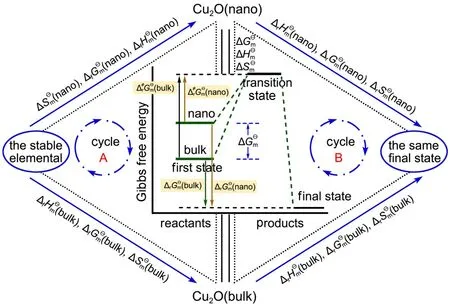
圖3 納米與塊體Cu2O的熱化學循環及過渡態理論Fig.3 Thermochemical cycle and transition state theory of nano-and bulk Cu2O
ΔrHm?(nano)和ΔrHm?(bulk)數值由微熱量儀直接測得,將高勝利等28報道的等溫等壓不可逆反應的熱動力學方程進行線性回歸,可求得反應速率常數k值,平均三次實驗的測量值見表1。
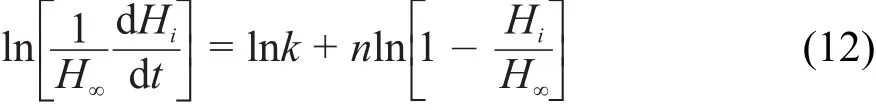
式中,H∞為整個反應過程的焓變,Hi為反應時間t時的瞬時焓變;dHi/dt為熱焓變化率。
將表1中反應速率常數k代入式(10),可得不同溫度下的立方體Cu2O納米反應體系的摩爾表面Gibbs自由能(Gms),結合式(8)和(11)得相應的摩爾表面焓(Hms)和摩爾表面熵(Sms)(見表2),相應的關系曲線見圖4(a-c)。
納米材料與塊體材料的本質區別在其表面相的高比表面能。如圖4(a-c)所示,同一溫度下,立方體納米Cu2O反應體系的均隨著粒度的減小而增大且與粒度的倒數成線性關系,這不僅與文獻26,27,29報道的規律一致,還與式(4)、(6)和(7)建立的立方體熱力學模型吻合。因為氧化亞銅超細化至納米尺度后,比表面積急劇增加,表面相的活性原子密度隨之增加,于是表面原子間相互作用力增強,其表面吸附和活化能力增強,亦即增大了納米Cu2O的;但由于原子受力不均勻和存在大量活躍的懸掛鍵,導致表面相的勢能增大,表面原子的混亂度隨之增大,因此,增大。
同一粒度下,Cu2O納米反應體系的均隨著溫度升高而增大,則減小。當溫度升高時,納米粒子熱運動加劇,表面原子間及表面與內部原子間的間距增大,使它們之間相互作用力減弱,因此表面張力減小,即減小;但是熱運動加快了分子間的碰撞,粒子動能、勢能均增大,體系的混亂度增加,因此和增大。
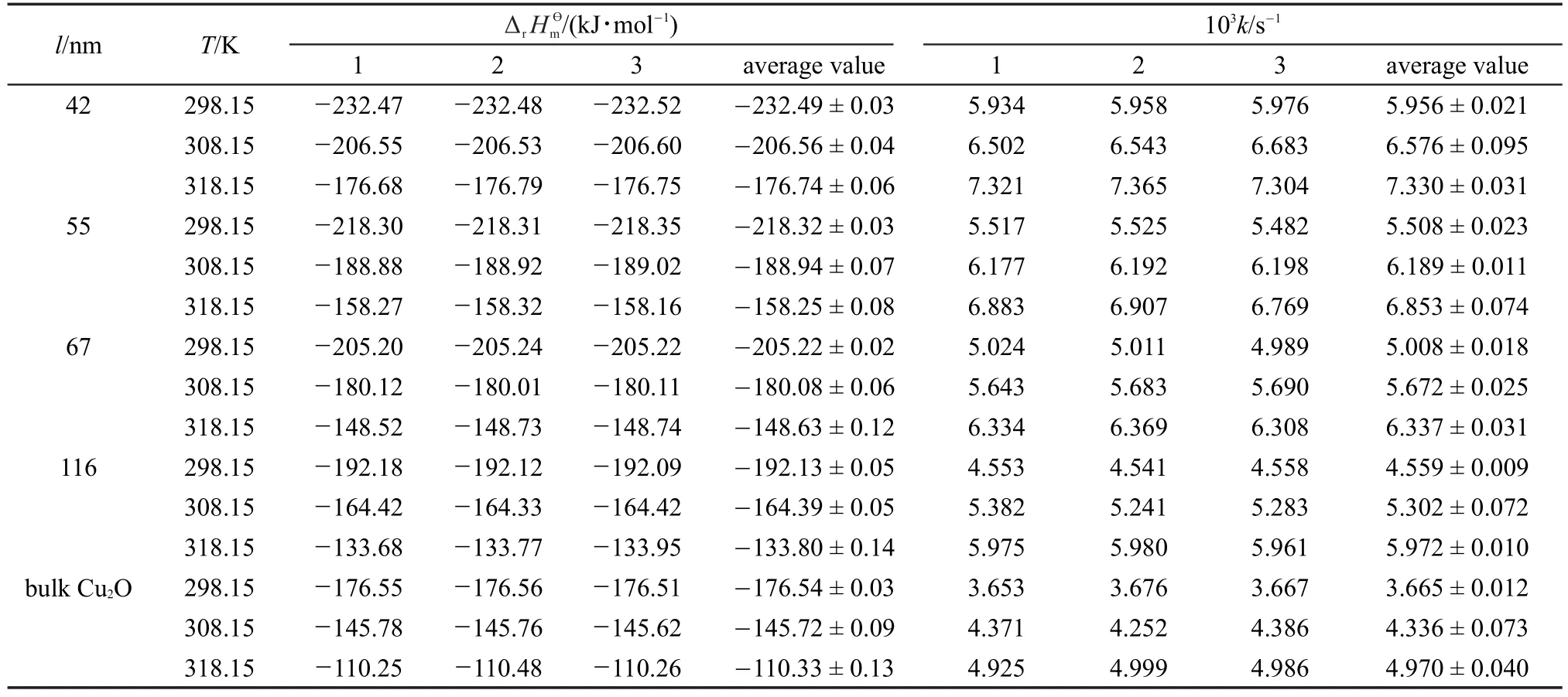
表1 不同粒度和溫度下納米/塊體Cu2O與HNO3反應體系的速率常數k和反應焓ΔrHm?Table 1 Rate constants(k)and reaction enthalpies(ΔrHm?)of nano-and bulk Cu2O(s)in HNO3(aq)at different particle sizes and temperatures
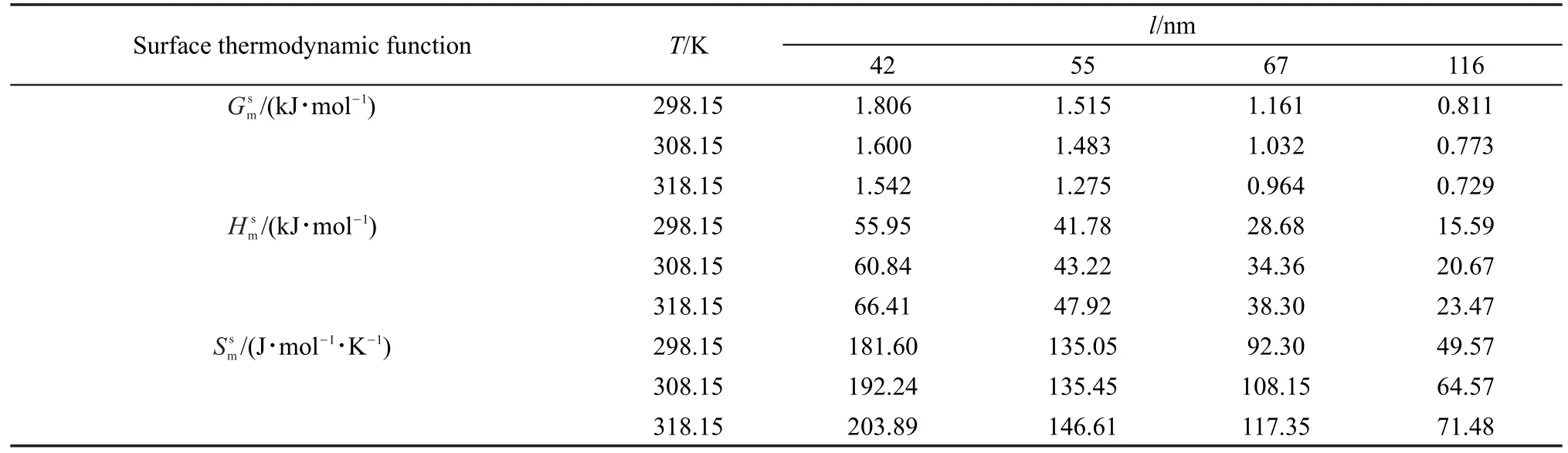
表2 不同粒度和溫度下立方體納米Cu2O的表面熱力學函數Table 2 Surface thermodynamical functions of cubic nano-Cu2O(s)at different particle sizes and temperatures
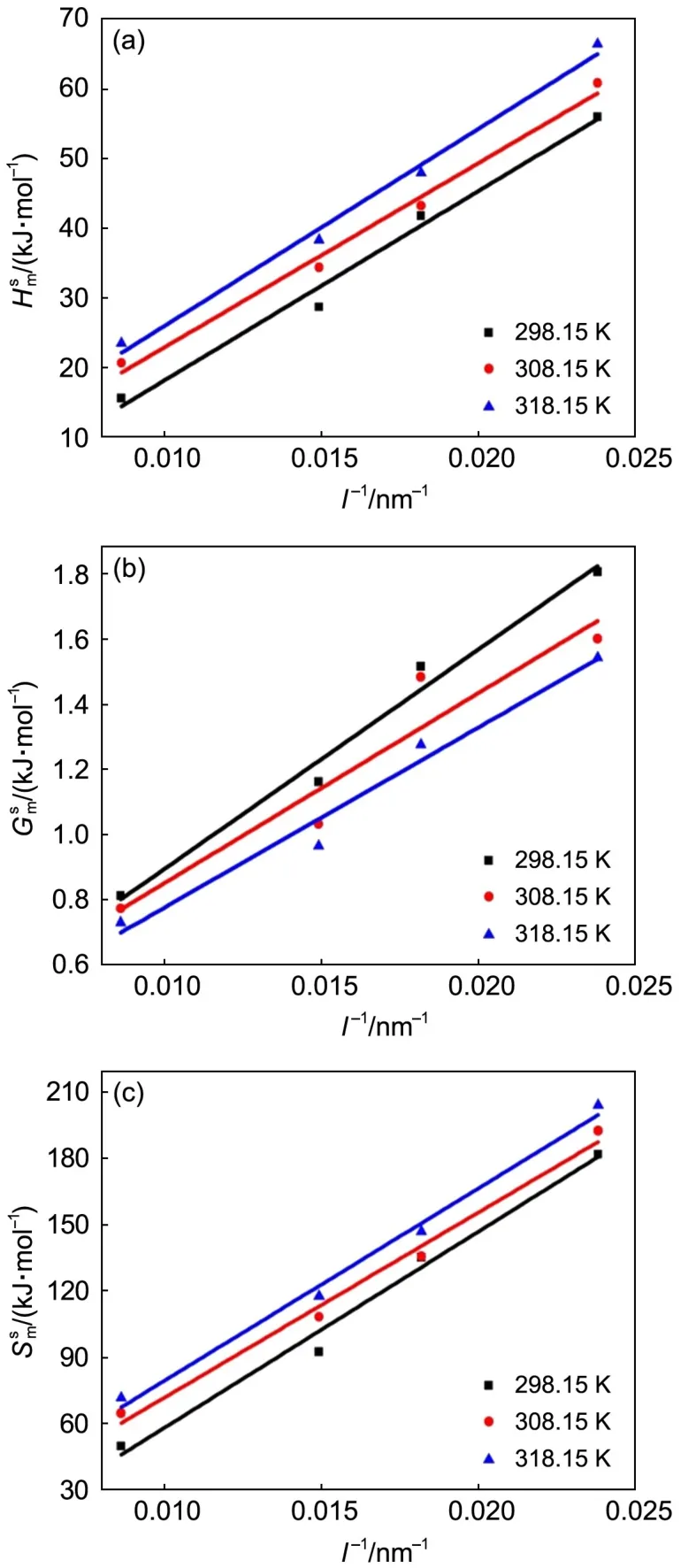
圖4 不同溫度下納米Cu2O表面熱力學函數與粒度的倒數的關系曲線Fig.4 Relationships between surface thermodynamical functions and the reciprocal of particle sizes(l-1)of nano-Cu2O for different temperatures(T)
4 結論
綜上所述,本文采用原位微熱量技術獲取了Cu2O與HNO3反應過程的熱力學精細信息,基于納米與塊體Cu2O表面相的差別,結合熱化學循環、熱動力學原理及過渡態理論計算獲得立方體納米Cu2O的表面熱力學函數。由建立的立方體熱力學模型結合實驗結果討論了粒度及溫度對表面熱力學函數的影響規律。結果表明,摩爾表面Gibbs自由能,摩爾表面焓和摩爾表面熵均隨著粒度的減小而增大,不僅與粒度的倒數成線性關系,且與立方體熱力學模型規律吻合;隨著溫度的升高,摩爾表面焓和摩爾表面熵增大,摩爾表面Gibbs自由能則減小。本文有望為納米材料表面熱力學函數的獲取及其粒度和溫度效應的研究提供新的思路和方法。
(1) Wen,Y.Z.;Xue,Y.Q.;Cui,Z.X.;Wang,Y.J.Chem. Thermodyn.2015,80,112.doi:10.1016/j.jct.2014.08.013
(2) Lai,W.P.;Xue,Y.Q.;Lian,P.;Ge,Z.X.;Wang,B.Z.;Zhang, Z.Z.Acta Phys.-Chim.Sin.2007,23(4),508.[來蔚鵬,薛永強,廉 鵬,葛忠學,王伯周,張志忠.物理化學學報,2007,23 (4),508.]doi:10.3866/PKU.WHXB20070411
(3) Lee,S.;Liang,C.W.;Martin,L.W.ACS Nano 2011,5(5), 3736.doi:10.1021/nn2001933
(4) Yang,Y.F.;Xue,Y.Q.;Cui,Z.X.;Zhao,M.Z.Electrochim. Acta 2014,136,565.doi:10.1016/j.electacta.2014.05.067
(5) Chakravarty,A.;Bhowmik,K.;Mukherjee,A.;De,G.Langmuir 2015,31(18),5210.doi:10.1021/acs.langmuir.5b00970
(6) Pang,H.;Gao,F.;Lu,Q.Y.Chem.Commun.2009,9,1076. doi:10.1039/B816670F
(7) Zhu,H.T.;Wang,J.X.;Xu,G.Y.Cryst.Growth.Des.2008,9 (1),633.doi:10.1021/cg801006g
(8) Song,J.H.;Rodenbough,P.P.;Xu,W.Q.;Senanayake,S.D.; Chan,S.W.J.Phys.Chem.C 2015,119(31),17667. doi:10.1021/acs.jpcc.5b04121
(9) Tsai,Y.H.;Chanda,K.;Chu,Y.T.;Chiu,C.Y.;Huang,M. H.Nanoscale 2014,6(15),8704.doi:10.1039/C4NR02076F
(10) Kuang,Q.;Wang,X.;Jiang,Z.Y.;Zhao,X.X.;Zheng,L.S. Acc.Chem.Res.2013,47(2),308.doi:10.1021/ar400092x
(11) Freakley,S.J.;He,Q.;Harrhy,J.H.;Lu,L.;Crole,D.A.; Morgan,D.J.;Ntainjua,E.N.;Edwards,J.K.;Carley,A.F.; Borisevich,A.Y.;Kiely,C.J.;Hutchings,G.J.Science 2016, 351(6276),965.doi:10.1126/science.aad5705
(12) Jamshidian,M.;Thamburaja,P.;Rabczuk,T.Phys.Chem. Chem.Phys.2015,17(38),25494.doi:10.1039/C5CP04375A
(13) Range,S.;Bernardes,C.E.S.;Simoes,R.G.;Epple,M.; Piedade,M.M.J.Phys.Chem.C 2015,119(8),4387. doi:10.1021/jp5124772
(14) Hu,R.Z.;Zhao,F.Q.;Gao,H.X.;Song,J.R.Fundamentals and Applications of Calorimetry;Science Press:Beijing,2011; pp 1-10.[胡榮祖,趙鳳起,高紅旭,宋紀蓉.量熱學基礎與應用.北京:科學出版社,2011:1-10.]
(15) Rychly,R.;Pekarek,V.J.Chem.Thermodyn.1977,9(4),391. doi:10.1016/0021-9614(77)90060-X
(16) Pan,L.;Zou,J.J.;Zhang,T.R.;Wang,S.B.;Wang,L.;Zhang, X.W.J.Phys.Chem.C 2013,118(30),16335.doi:10.1021/ jp408056k
(17) Li,C.;Li,Y.B.;Delaunay,J.J.ACS Appl.Mater.Interfaces 2013,6(1),480.doi:10.1021/am404527q
(18) Wu,L.L.;Tsui,L.K.;Swami,N.;Zangari,G.J.Phys.Chem.C 2010,114(26),11551.doi:10.1021/jp103437y
(19) Solache-Carranco,H.;Juarez-Díaz,G.;Esparza-García,A.; Biseo-García,M.;Galvan-Arellano,M.;Martínez-Juárez,J.; Romero-Paredes,G.;Pea-Sierra,R.J.Lumin.2009,129(12), 1483.doi:10.1016/j.jlumin.2009.02.033
(20) Sun,D.;Yin,P.G.;Guo,L.Acta Phys.-Chim.Sin.2011,27(6), 1543.[孫 都,殷鵬剛,郭 林.物理化學學報,2011,27(6), 1543.]doi:10.3866/PKU.WHXB20110619
(21) Fu,Q.S.;Cui,Z.X.;Xue,Y.Q.Eur.Phys.J.Plus 2015,130 (10),212.doi:10.1140/epjp/i2015-15212-4
(22) Wang,S.S.Study on the Size Effect of Nanoparticles on the Surface Thermodynamic Properties by Solubility Method.M.S. Dissertation,Taiyuan University of Technology,Taiyuan,2015. [王珊珊.溶解度法研究粒度對納米顆粒表面熱力學性質的影響[D].太原:太原理工大學,2015.]
(23) Guo,S.H.The Effect of Particle Size and Shape on the Thermodynamic Properties:a Theoretical Study and Quantum Chemistry Calculation.M.S.Dissertation,Taiyuan University of Technology,Taiyuan,2015.[郭少輝.粒度和形貌對納米顆粒熱力學性質影響的理論研究和量化計算[D].太原:太原理工大學,2015.]
(24) Xue,Y.Q.;Yang,X.C.;Cui,Z.X.;Lai,W.P.J.Phys.Chem.B 2011,115(1),109.doi:10.1021/jp1084313
(25) Li,X.X.;Huang,Z.Y.;Zhong,L.Y.;Wang,T.H.;Tan,X.C. Chin.Sci.Bull.2014,59(25),2490.[李星星,黃在銀,鐘蓮云,王騰輝,譚學才.科學通報,2014,59(25),2490.]doi:10.1360/ N972014-00332
(26) Fan,G.C.;Ma,Z.;Huang,Z.Y.;Tan,X.C.;Yao,X.C.Chem. J.Chin.Univ.2014,35(5),1007.[范高超,馬 昭,黃在銀,譚學才,姚先超.高等學校化學學報,2014,35(5),1007.] doi:10.7503/cjcu20140062
(27) International Union of Pure andApplied Chemistry.Chemistry Quantities,Units and Symbols in Physical Chemistry;Scientific and Technical Documentation Press:Beijing,1991;pp 56-57; translated by Qi,D.Y.,Jin,Z.D.,Zhuang,Y.L.[國際純粹化學與應用化學聯合會.物理化學中的量,單位和符號,漆德瑤,金宗德,莊云龍,譯.北京:科學技術文獻出版社,1991:56-57.]
(28) Gao,S.L.;Chen,S.P.;Hu,R.Z.;Li,H.Y.;Shi,Q.Z.Chin.J. Inorg.Chem.2002,18(4),362.[高勝利,陳三平,胡榮祖,李煥勇,史啟禎.無機化學學報,2002,18(4),362.]
(29) Piloyan,G.O.;Bortnikov,N.S.;Boeva,N.M.J.Mod.Phys. 2013,4(7),16.doi:10.4236/jmp.2013.47A2003
Effects of Particle Size and Temperature on Surface Thermodynamic Functions of Cubic Nano-Cu2O
TANG Huan-Feng1HUANG Zai-Yin1,2,*XIAO Ming1
(1College of Chemistry and Chemical Engineering,Guangxi University for Nationalities,Nanning 530006,P.R.China;2Guangxi Colleges and Universities Key Laboratory of Food Safety and Pharmaceutical Analytical Chemistry,Nanning 530006,P.R.China)
Cubic nano-cuprous oxides,with four types of particle sizes ranging from 40 to 120 nm,were synthesized via a liquid-phase reduction method.The composition,morphology and structure of the nano-Cu2O particles were characterized by X-ray diffractometry(XRD),Raman microscopy and field emission scanning electronic microscopy(FE-SEM).In-situ microcalorimetry was used to obtain thermodynamic information about the reaction between HNO3and bulk Cu2O or nano-Cu2O.The surface thermodynamic functions of cubic nano-Cu2O were calculated by a combination of thermodynamic principle and kinetic transition state theory.We develop a thermodynamic model for the cubic nanoparticles based on the thermodynamic model of spherical nanoparticles without bore developed by XUE Yong-Qiang et al.The particle size and temperature effects of surface thermodynamic functions are discussed by comparing the theoretical model with the experimental results.The molar surface Gibbs free energy,molar surface enthalpy and molar surface entropy increased with decreasing particle sizes.Linear trends were found between the reciprocal of particle size and surface thermodynamic functions,which agreed well with the theoretical model for a cube.The molar surface enthalpy and molar surface entropy were increased with rising temperature,whereas the molar surface Gibbs free energy decreased.This work not only enriches and develops the basic theory of nano-thermodynamics,but also provides a novel method and idea for investigating surface thermodynamic functions of nanomaterials and their applications.
O642
10.3866/PKU.WHXB201608084
Received:July 14,2016;Revised:August 4,2016;Published online:August 8,2016.
*Corresponding author.Email:huangzaiyin@163.com;Tel:+86-771-3267010.
The project was supported by the National Natural Science Foundation of China(21273050,21573048).
國家自然科學基金(21273050,21573048)資助項目

