響應(yīng)面法優(yōu)化α-淀粉酶酶解木薯淀粉的工藝及動(dòng)力學(xué)模型研究
高義霞 路宛如 楊金龍 周向軍
(天水師范學(xué)院生命科學(xué)與化學(xué)學(xué)院,天水 741001)
響應(yīng)面法優(yōu)化α-淀粉酶酶解木薯淀粉的工藝及動(dòng)力學(xué)模型研究
高義霞 路宛如 楊金龍 周向軍
(天水師范學(xué)院生命科學(xué)與化學(xué)學(xué)院,天水 741001)
以葡萄糖值(DE)為考察指標(biāo),在單因素試驗(yàn)基礎(chǔ)之上,利用響應(yīng)面法研究時(shí)間、溫度及酶與底物比(E/S)對(duì)α-淀粉酶酶解木薯淀粉的影響。利用Lineweaver-Burk和Wilkinson統(tǒng)計(jì)法求解米氏常數(shù)(Km)和最大反應(yīng)速度(Vm),并建立相應(yīng)動(dòng)力學(xué)模型。結(jié)果表明:α-淀粉酶酶解木薯淀粉制備葡萄糖的最佳參數(shù)為:溫度60 ℃,E/S=0.1 U/mg、時(shí)間130 min。在此條件下,DE驗(yàn)證值為(82.91±1.32)%。在pH 6.0,50 ℃條件下,Km=12.077 mg/mL,Vm=0.218 mg/(mL·min)。在37~52 ℃范圍內(nèi),Ea=44.611 kJ/mol,ΔH=110.847 kJ/mol。
木薯 酶解 動(dòng)力學(xué) 響應(yīng)面
木薯(Manihot utilissima)是全球三大薯類作物之一,廣泛分布在我國(guó)海南、廣西和廣東等地區(qū)。木薯淀粉具有資源豐富、黏度高、糊化溫度低,成膜性好等特點(diǎn),在淀粉加工行業(yè)具有較大優(yōu)勢(shì)[1]。生物能源具有可再生性、環(huán)保性等特點(diǎn),當(dāng)今資源和能源日益緊張,無論是利用非糧糖質(zhì)原料發(fā)酵生產(chǎn)燃料乙醇,還是利用油料作物、微藻等生產(chǎn)具有更突出優(yōu)勢(shì)的生物柴油[2],均具有巨大的吸引力,將成為國(guó)家可持續(xù)發(fā)展戰(zhàn)略的必然要求。目前,微藻異氧培養(yǎng)已被用于制備生物柴油,但葡萄糖占整個(gè)成本的80%[3],致使培養(yǎng)基成本太高,但有關(guān)響應(yīng)面法優(yōu)化木薯淀粉酶解工藝及動(dòng)力學(xué)研究鮮見報(bào)道。淀粉的酶解與其種類和濃度、pH、溫度、酶的類型及離子強(qiáng)度等均有關(guān),常規(guī)的米氏方程難以真實(shí)描述反應(yīng)過程[4],因此,在實(shí)際生產(chǎn)中,需進(jìn)一步探討酶促反應(yīng)條件,以最大化發(fā)揮酶的催化作用[5-6]。
隨生淀粉酶等新型淀粉酶的出現(xiàn),直接選擇淀粉顆粒作為底物進(jìn)行水解成為一種趨勢(shì),本試驗(yàn)以溫度、E/S及時(shí)間為因素,通過響應(yīng)面法優(yōu)化α-淀粉酶酶解木薯淀粉制糖的最佳工藝,同時(shí)對(duì)酶解動(dòng)力學(xué)模型進(jìn)行了研究,為降低微藻生產(chǎn)生物柴油成本提供參考。
1 材料與方法
1.1 材料與試劑
木薯淀粉,質(zhì)量分?jǐn)?shù)為(86.167±1.137)%:山東棗莊三畝糧田;α-淀粉酶(58.7 U/mg): Sigma公司(Lot:STBB0510,來自枯草芽孢桿菌);苯酚:天津市紅巖化學(xué)試劑廠;葡萄糖:天津登豐化學(xué)品有限公司。
1.2 主要儀器
TGL-20M型高速臺(tái)式冷凍離心機(jī):湖南湘儀離心機(jī)儀器有限公司;722型可見分光光度計(jì):上海欣茂有限公司。
1.3 試驗(yàn)方法
1.3.1 標(biāo)準(zhǔn)曲線的制作及木薯淀粉的酶解
參考3,5-二硝基水楊酸(DNS)法[7]。0.4 mg/mL葡萄糖溶液0、0.1、0.2、0.3、0.4、0.5、0.6 mL,加蒸餾水至2 mL,混勻,加入1.5 mL DNS,沸水浴加熱5 min,冷卻后補(bǔ)至3.5 mL。540 nm測(cè)定吸光值。Y=2.425 4X-0.090 1,r=0.992(X為葡萄糖質(zhì)量/mg,Y為OD)。稱取木薯淀粉0.1 g,加入20 mL 0.05mol/L pH 6.0的磷酸緩沖液,攪拌10 min,80 ℃糊化5 min,冷卻,按E/S=0.02 U/mg加入α-淀粉酶液,振蕩混勻,45 min后迅速沸水滅活5min,5 000 r/min離心10 min,測(cè)定吸光值,計(jì)算葡萄糖值(DE)。
DE/%=還原糖量(mg)×100/淀粉(mg)

(1)
式中:v為反應(yīng)速率/mg/mL·min,m/V為還原糖含量/mg/mL;t為反應(yīng)時(shí)間/min。
1.3.2 單因素試驗(yàn)
按1.3.1,考察溫度(30、40、50、60、70 ℃)、E/S(0.005、0.01、0.02、0.04、0.08 U/mg)、時(shí)間(10、20、40、60、80、100、120、150、180 min)及pH(4、5、6、7、8)對(duì)DE的影響。
1.3.3 酶促反應(yīng)動(dòng)力學(xué)模型
Michaelis和Menten根據(jù)快速平衡學(xué)說建立米氏方程,Briggs和Haldane用穩(wěn)態(tài)代替快速平衡態(tài),對(duì)米氏方程做了修正,得到更合理的酶促反應(yīng)動(dòng)力學(xué)過程。推導(dǎo)過程[8]:
(2)

(3)

(4)
vm=k3E總
(5)

(6)
式中:k1為ES生成速率;k2、k3分別為ES分解為E+S和P+E的速率;k4為E+P生成ES的速率(反應(yīng)初期忽略不計(jì));[S]為底物質(zhì)量濃度/mg/mL;E總(U/mL)=[E]+[ES]。將式(6)線性化處理,得Lineweaver-Burk方程:

(7)
求Km和Vm;利用Wilkinson統(tǒng)計(jì)法求Km和Vm。
1.3.4 響應(yīng)面法優(yōu)化酶解工藝
參考李忠海等[9]的方法,固定pH為6.0,以溫度、E/S、時(shí)間為因子,各因子最優(yōu)點(diǎn)為基準(zhǔn)點(diǎn),確定適度步長(zhǎng),DE為響應(yīng)值,利用Design-Expert 8.06設(shè)計(jì)試驗(yàn),見表1。

表1 Box-Benhnken試驗(yàn)因素水平及編碼
1.4 數(shù)據(jù)處理

2 結(jié)果與分析
2.1 單因素試驗(yàn)
時(shí)間對(duì)DE的影響見圖1a,在該條件下,在0~120 min范圍內(nèi),DE隨時(shí)間的增加而增大,隨后趨于平緩,甚至出現(xiàn)下降,這是因?yàn)樵诿附膺^程中,不僅發(fā)生淀粉的水解反應(yīng),同時(shí)還存在較弱的復(fù)合反應(yīng)[10]。DE在28%以下,復(fù)合糖幾乎不能生成,但隨著DE的進(jìn)一步增加,復(fù)合糖生成速率逐漸超過淀粉水解速率,因此,DE將不斷減少。溫度對(duì)DE的影響見圖1b(P<0.05),溫度為50 ℃時(shí),DE達(dá)到最大,表明最適溫度為50 ℃。一方面,溫度升高,分子間碰撞次數(shù)增加,反應(yīng)速率增加;另一方面,作為蛋白質(zhì),酶隨溫度逐漸升高而逐漸變性失活,導(dǎo)致反應(yīng)速率下降,因此溫度在50~60 ℃范圍內(nèi)選擇。E/S對(duì)DE的影響見圖1c(P<0.05),反應(yīng)初期,隨E/S的增大,酶解速率幾乎呈線性增大,這是因?yàn)椋诘孜镞^量的情況下,酶促反應(yīng)速率與酶量成正比;隨反應(yīng)的進(jìn)行,雖然E/S進(jìn)一步增大,但由于底物出現(xiàn)不足,反應(yīng)速率的增大程度將會(huì)變得緩慢,甚至出現(xiàn)下降趨勢(shì)[11]。E/S選擇0.08 U/mg。pH對(duì)DE的影響見圖1d(P<0.05),pH 6.0時(shí),DE達(dá)到最大值,表明酶的最適pH為6.0。pH可影響酶分子活性中心上必需基團(tuán)的離子化程度,也可影響底物的解離程度,從而影響酶與底物的結(jié)合[12]。
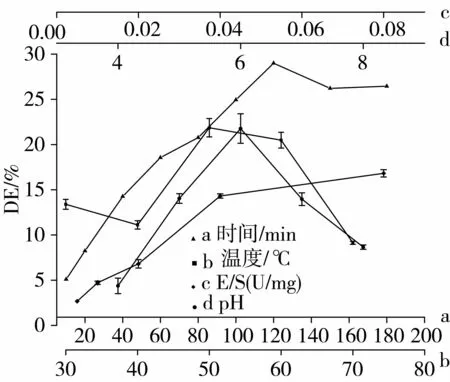
圖1 單因素試驗(yàn)
2.2 響應(yīng)面分析

Y=58.46-0.008 75X1+5.2X2+3.4X3+2.39X1X2+3.02X1X3+1.89X2X3+2.7X12-2.1X22+8.56X32
E/S和時(shí)間的P<0.000 1,表明其對(duì)DE影響極顯著;溫度的P>0.05,影響不顯著。各因素影響大小依次為E/S、時(shí)間及溫度。二次項(xiàng)X12、X22、X32影響極顯著,交互項(xiàng)的影響大小依次為X1X3、X1X2、X2X3,均達(dá)到極顯著水平,表明響應(yīng)值Y的變化相當(dāng)復(fù)雜,各因素對(duì)DE的影響并非簡(jiǎn)單的線性關(guān)系,而是呈二次關(guān)系,且3個(gè)因素間存在交互作用。去掉不顯著因素則有:
Y=58.46+5.2X2+3.4X3+2.39X1X2+3.02X1X3+1.89X2X3+2.7X12-2.1X22+8.56X32
最優(yōu)工藝:溫度60 ℃,E/S0.1 U/mg和時(shí)間130 min,預(yù)測(cè)DE為83.53%。驗(yàn)證結(jié)果見表4。

表2 Box-Benhnken試驗(yàn)設(shè)計(jì)表及結(jié)果

表3 回歸模型系數(shù)顯著性檢驗(yàn)及其方差分析

表4 回歸模型的6組參數(shù)及其驗(yàn)證結(jié)果
驗(yàn)證試驗(yàn)平均值(82.91±1.32)%,n=6,RSD=1.59%,表明模型有效,可用于木薯淀粉酶解參數(shù)的優(yōu)化。
2.3 Lineweaver-Buck法求解參數(shù)
V-S曲線及1/V-1/S作圖見圖2a和圖2b,Y=74.8X+3.722,r=0.991,方程極顯著。計(jì)算得Vm=0.269 mg/(mL·min),Km=20.097 mg/mL。

圖2 底物濃度與反應(yīng)速率的關(guān)系
2.4 Wilkinson統(tǒng)計(jì)法求解參數(shù)
2.4.1 最小二乘法求估算解
Wilkinson統(tǒng)計(jì)法求估算解見表5。表5可知,Δ=αε-γδ=0.000 000 000 007 585 3。Vm0=(βε-δ2)/Δ=0.122 mg/(mL·min),Km0=(βγ-αδ)/Δ=7.323 mg/mL。
式中:Vm0和Km0分別為最大反應(yīng)速度和米氏常數(shù)估算值。
2.4.2 泰勒展開式求精校解

(8)
表6,Δ′=α′β′-γ′2=0.000 000 004 190 58,b1=(β′δ′-γ′ε′)/Δ′=1.785,b2=(α′ε′-γ′δ′)/Δ′=8.485。求得精確解為Vm=Vm0b1=0.218 mg/(mL·min);Km=Km0+b2/b1=12.077 mg/mL;式中:b1和b2分別為Vm和Km計(jì)算過程中修正常數(shù)。

表5 Wilkinson統(tǒng)計(jì)法求估算解

表6 Wilkinson法精校解
2.4.3 Lineweaver-Buck法和Wilkinson統(tǒng)計(jì)法的比較


表7 Lineweaver-Buck法和Wilkinson統(tǒng)計(jì)法數(shù)據(jù)比較
2.5 Ea及ΔH計(jì)算
在37~52 ℃范圍內(nèi),反應(yīng)速率隨溫度的增加而增大,以lnv對(duì)1/T(×103)作圖,見圖3,呈直線關(guān)系,用阿累尼烏斯(Arrhenius)方程擬合:

圖3 lnv-1/T

圖4 lnKs-1/T

(9)
式中:R為氣體常數(shù)8.31{J/(molK)};Ea為活化能(kJmol);B為積分常數(shù)。將式(9)寫成指數(shù)形式,K3=A×exp(-Ea/RT),A為指前因子{mg/(mL·min)},Y=10.079 48-5.368 31X,r=0.994。求得Ea= 44.611 kJ/moL,A=23 848.581 mg/(mL·min),r=0.994,表明Arrhenius方程對(duì)該數(shù)據(jù)的擬合是極顯著的。平衡常數(shù)Ks與溫度T服從范特柯夫方程:lnKs=-ΔH/RT+lnC(10),K3≥K2,Ks≈Km,以不同溫度下Km與1/T回歸[16],見圖4,Y=44.053-13.339X,r=0.983,ΔH=110.847 kJ/mol。
3 結(jié)論
利用響應(yīng)面法優(yōu)化α-淀粉酶酶解木薯淀粉,對(duì)酶解動(dòng)力學(xué)進(jìn)行研究。結(jié)果表明:酶解模型為:Y=58.46+5.2X2+3.4X3+2.39X1X2+3.02X1X3+1.89X2X3+2.7X12-2.1X22+8.56X32。酶解工藝為:溫度60 ℃,E/S=0.1 U/mg和時(shí)間130 min,在此條件下,DE驗(yàn)證值為(82.91±1.32)%,RSD=1.59%。在pH 6.0,50 ℃條件下,Km=12.077 mg/mL,Vm=0.218 mg/(mL·min)。在37~52 ℃范圍內(nèi),Ea=44.611 kJ/moL,ΔH=110.847 kJ/mol。
[1]許青華,李偉漢,徐中岳,等. 酶法制備木薯淀粉糊精的理化性質(zhì)研究[J]. 食品科技,2010,35(12):13-16
[2]Buaban B, Inoue H, Yano S, et al. Bioethanol production from ball milled bagasse using an on-site produced fungal enzyme cocktail and xylose-fermenting Pichia stipitis. Journal of bioscience and bioengineering, 2010, 110(1):18-25
[3]Li X F,Xu H, Wu Q Y. Large-scale biodiesel production from microalga chlorella protothecoides through heterotrophic cultivation in bioreactors[J]. Biotechnology and Bioengineering, 2007, 98(4):764-771
[4]黎金,張國(guó)權(quán),羅勤貴. 蕎麥蛋白的堿性蛋白酶酶解動(dòng)力學(xué)研究[J]. 中國(guó)糧油學(xué)報(bào),2009,24(6):41-46
[5]張國(guó)權(quán),史一一,魏益民,等. 蕎麥淀粉的真菌淀粉酶酶解動(dòng)力學(xué)研究[J]. 農(nóng)業(yè)工程學(xué)報(bào),2007,23(5):42-46
[6]張樹河,李海明,潘世明,等. 木薯淀粉酶解糖化工藝研究[J]. 福建農(nóng)業(yè)學(xué)報(bào),2011,26(5):818-821
[7]張惟杰. 糖復(fù)合物生化研究技術(shù)[M]. 杭州:浙江大學(xué)出版社(第二版),1999,10-11
[8]鐘昔陽(yáng),楊積東,湯玉清,等. α-淀粉酶酶解小麥面粉動(dòng)力學(xué)模型研究[J]. 食品科學(xué),2012,33(7):96-100
[9]李忠海,劉建軍,鐘海雁,等. 響應(yīng)面法優(yōu)化甘薯淀粉酶解條件的研究[J]. 中國(guó)糧油學(xué)報(bào),2009,24(10):64-69
[10]齊明,房書,沙同勝,等. 葡萄糖收率-糖化反應(yīng)的研究[J]. 牡丹江醫(yī)學(xué)院學(xué)報(bào),1993(S1):29-31
[11]鄭寶東. 食品酶學(xué)[M]. 南京:東南大學(xué)出版社,2006,88
[12]蔡麗華,馬美湖. 4種常用蛋白酶對(duì)牛骨蛋白的酶解動(dòng)力學(xué)研究[J]. 食品科學(xué),2010,31(5):150-154
[13]袁亞宏,蔡露陽(yáng),岳田利,等. 胺基化磁性殼聚糖微球?qū)μO果渣多酚的吸附條件優(yōu)化[J]. 農(nóng)業(yè)工程學(xué)報(bào),2012,28(11):279-286
[14]趙燕,涂勇剛,郭建軍,等. 玉米淀粉的β-淀粉酶酶解動(dòng)力學(xué)研究[J]. 食品科學(xué),2009,30(17):190-194
[15]鐘穗生,劉生玉,張林香. 馬鈴薯淀粉糖化動(dòng)力學(xué)的研究[J]. 中國(guó)糧油學(xué)報(bào),1998,13(1):21-25
[16]任省濤,程可可,宋安東,等. 蒸汽爆破玉米秸稈酶解動(dòng)力學(xué)[J]. 生物工程學(xué)報(bào),2011,27(4):592-597.
Enzymolysis Technology of Cassava Starch Using Response Surface Method and Its Kinetics Modeling
Gao Yixia Lu Wanru Yang Jinlong Zhou Xiangjun
(Life Science and Chemistry Department, Tianshui Normal Colleage, Tianshui 741001)
Dextrose equivalent value (DE) has been utilized as an index; the effects of time, temperature and the ratio of enzyme to substrate concentration (E/S) on enzymolysis of cassava starch with α-amylase have been explored based on Single Experiment and Response Surface Method. The michaelis constant (Km), maximum velocity (Vm) and its corresponding kinetics modeling were also researched. The results indicated that the optimal parameters were as follows: temperature of 60 ℃,E/S=0.1 U/mg and time of 130 min. The verification DE could reach (82.91±1.32)%. On condition of pH 6.0 and temperature at 50 ℃,Km,Vm could be 12.077 mg/mL and 0.218 mg/(mL·min) respectively.Ea and ΔHwere 44.611 and 110.847 kJ/mol in the temperature range of 37 to 52 ℃ respectively.
cassava starch, enzymolysis, kinetics, response surface method
TS201.1
A
1003-0174(2016)02-0013-05
天水師范學(xué)院“青藍(lán)”人才工程(75201406)
2014-07-01
高義霞,女,1982年出生,碩士,食品化學(xué)
周向軍,男,1980年出生,講師,食品酶學(xué)

