琥珀酸索利那新片自研制劑與原研制劑溶出曲線的相似性評價
龔俊強,陳 仙,徐彩虹,張 霞,吳春梅,王 萍,傅旭春(1.浙江大學藥學院,杭州 10058;.浙江華義醫藥有限公司,浙江義烏 000;.華東醫藥生物工程研究所,杭州 10011)
琥珀酸索利那新片自研制劑與原研制劑溶出曲線的相似性評價
龔俊強1,2*,陳 仙2,徐彩虹2,張 霞3,吳春梅2,王 萍2,傅旭春1#(1.浙江大學藥學院,杭州 310058;2.浙江華義醫藥有限公司,浙江義烏 320002;3.華東醫藥生物工程研究所,杭州 310011)
目的:考察琥珀酸索利那新片自研制劑與原研制劑溶出曲線的相似性,為前者的處方和工藝篩選以及與后者的質量一致性評價提供參考。方法:采用槳法,轉速為50 r/min,分別以水、pH1.2鹽酸溶液、pH4.5乙酸鹽緩沖液和pH6.8磷酸鹽緩沖液為溶出介質進行溶出度試驗,采用高效液相色譜法(HPLC)測定琥珀酸索利那新片自研制劑與原研制劑中主成分在不同時間點的累積溶出度,并繪制溶出度曲線,進而采用相似因子(f2)法評價二者溶出曲線的相似性。結果:在4種溶出介質中,琥珀酸索利那新片自研制劑與原研制劑的f2均>50,說明二者溶出曲線具有相似性。結論:所建立的HPLC法適用于琥珀酸索利那新片的溶出度測定;自研制劑與原研制劑的溶出行為基本一致,一定程度說明自研制劑的處方和工藝具有可行性。
琥珀酸索利那新片;自研制劑;原研制劑;高效液相色譜法;溶出曲線;相似因子法;評價
琥珀酸索利那新(Solifenacin succinate)是由日本安斯泰來制藥公司開發,其片劑商品名為衛喜康(Vesicare),2004年8月首次在歐洲上市,同年11月獲美國食品與藥品管理局(FDA)許可在美國上市,2009年9月在我國獲得上市許可。該藥通過阻滯膀胱平滑肌的毒蕈堿M3受體來抑制逼尿肌的過度活動,從而緩解膀胱過度活動癥(OAB)伴隨的急迫性尿失禁、尿急和尿頻癥狀。該藥具有高度膀胱選擇性和M3受體選擇性,臨床療效確切,口干等副作用相對較少,患者耐受性好[1]。因此,包括中國、美國等多個國家的泌尿外科疾病診斷治療指南都已將該藥列為治療OAB的一線藥物[2-3]。
本研究中,筆者參考國家食品藥品監督管理總局(CFDA)發布的《普通口服固體制劑溶出度試驗技術指導原則》[4]和FDA溶出度方法數據庫[5]等,對琥珀酸索利那新片自研制劑與原研制劑在水、pH1.2鹽酸溶液、pH4.5乙酸鹽緩沖液和pH6.8磷酸鹽緩沖液4種溶出介質中溶出曲線的相似性進行了評價,旨在為其自研制劑的處方和工藝篩選以及與原研制劑的質量一致性評價提供參考。
1 材料
1.1 儀器
e2695型高效液相色譜儀,含自動進樣器、光電二極管陣列檢測器[沃特世科技(上海)有限公司];XS205DU型電子分析天平[梅特勒-托利多儀器(上海)有限公司];ZRS-8L型智能溶出試驗儀(天津市天大天發科技有限公司)。
1.2 藥品與試劑
琥珀酸索利那新對照品(埃斯特維華義制藥有限公司,批號:13-601,純度:99.9%);琥珀酸索利那新原料藥(埃斯特維華義制藥有限公司,批號:130401,純度:99.2%);琥珀酸索利那新片原研制劑[商品名:衛喜康,安斯泰來制藥(中國)有限公司,批號:12I22/03,規格:5 mg];琥珀酸索利那新片自研制劑(浙江華義醫藥有限公司,批號:130901,規格:5 mg);鹽酸、氫氧化鈉、乙酸、乙酸鈉、磷酸氫二鉀、磷酸二氫鉀、磷酸(均為分析純,國藥集團化學試劑有限公司);乙腈(色譜純,默克股份兩合公司);試驗用水為純化水。
2 方法與結果
2.1 色譜條件
色譜柱:Symmetry Shield RP18(150 mm×4.6 mm,5 μm);流動相:0.05 mol/L磷酸氫二鉀緩沖液(pH6.0)-乙腈(65∶35,V/V);流速:1 ml/min;柱溫:40℃;檢測波長:210 nm;進樣量:50 μl。
2.2 溶液的制備
2.2.1 對照品溶液 取琥珀酸索利那新對照品約25 mg,精密稱定,置于50 ml量瓶中,以水-乙腈(70∶30,V/V)溶解并稀釋至刻度,搖勻,得質量濃度為0.5 mg/ml的對照品貯備液。精密量取上述貯備液1.0 ml,置于100 ml量瓶中,用水-乙腈(70∶30,V/V)稀釋至刻度,制成質量濃度為5 μg/ml的對照品溶液。
2.2.2 供試品溶液 取自研制劑樣品,按2015年版《中國藥典》(四部)“溶出度與釋放度測定法”第二法(槳法)[6],以900 ml水為溶出介質,轉速為50 r/min,溫度(37.0±0.5)℃,依法操作,經30 min后,取溶出液適量,濾過,取續濾液3.5 ml與1.5 ml乙腈混勻,作為供試品溶液。
2.2.3 陰性對照溶液 按自研制劑處方取空白輔料適量,按“2.2.2”項下方法進行操作,制成陰性對照溶液。
2.2.4 溶出介質的制備 水:純化水;pH1.2鹽酸溶液:取鹽酸7.65 ml,加水稀釋至1 000 ml,搖勻,即得;pH4.5乙酸鹽緩沖液:取2 mol/L乙酸溶液(取120.0 g冰乙酸用水稀釋至1 000 ml,即得)14.0 ml和乙酸鈉2.99 g,加水溶解并稀釋至1 000 ml,搖勻,即得;pH6.8磷酸鹽緩沖液:取0.2 mol/L磷酸二氫鉀溶液(取27.22 g磷酸二氫鉀,用水溶解并稀釋至1 000 ml,即得)250 ml和0.2 mol/L氫氧化鈉溶液(取8.00 g氫氧化鈉,用水溶解并稀釋至1 000 ml,即得)112.0 ml,加水稀釋至1 000 ml,搖勻,即得。
2.3 專屬性試驗
取“2.2”項下對照品溶液、供試品溶液、陰性對照溶液各適量,按“2.1”項下色譜條件進樣測定,記錄色譜,詳見圖1。結果表明,對照品與供試品的主峰保留時間一致,陰性對照在此波長下無干擾。
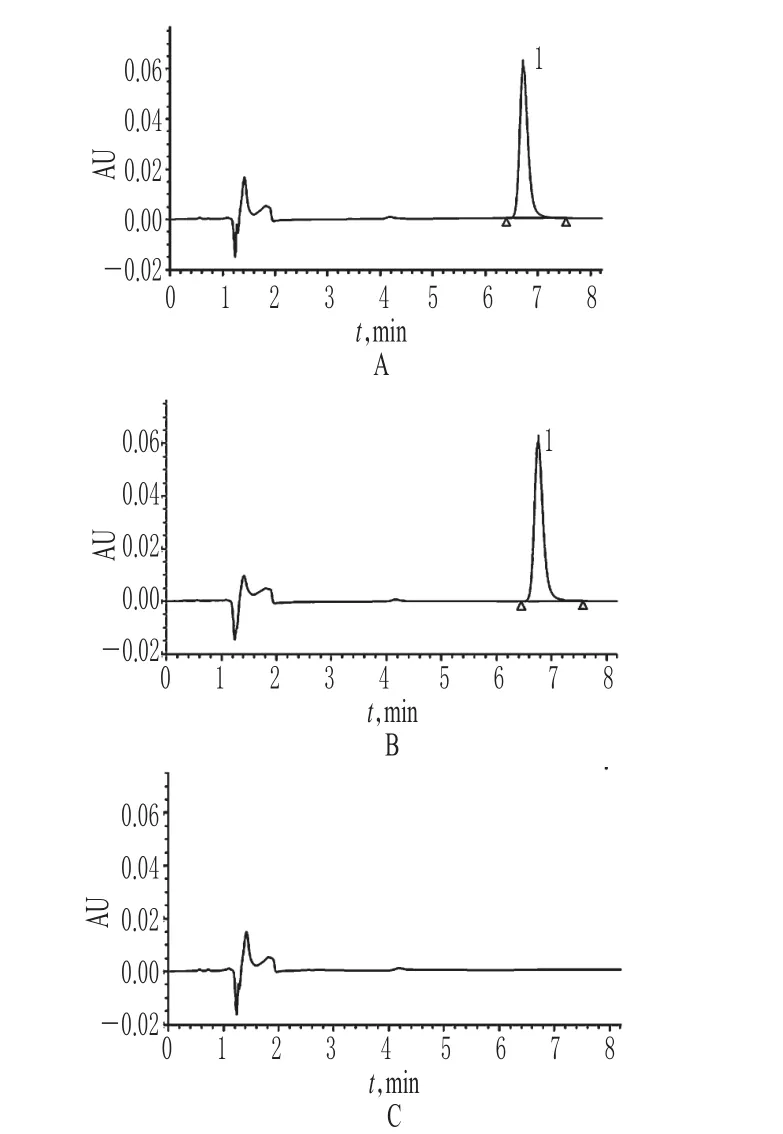
圖1 高效液相色譜圖A.對照品溶液;B.供試品溶液;C.陰性對照溶液;1.琥珀酸索利那新Fig 1 HPLC chromatogramsA.reference substance solution;B.test sample solution;C.negative control solution;1.solifenacin succinate
2.4 線性關系考察
取“2.2.1”項下對照品貯備液適量,用水-乙腈(70∶30,V/V)稀釋成質量濃度約為0.4、0.8、2.0、3.2、4.0、4.8和5.6 μg/ml的系列對照品溶液,按“2.1”項下色譜條件進樣測定。以待測成分質量濃度(x,μg/ml)為橫坐標、峰面積(y)為縱坐標進行線性回歸,得回歸方程為y=133 495x-6 840(r=0.999 9)。結果表明,琥珀酸索利那新檢測質量濃度線性范圍為0.4~5.6 μg/ml。
2.5 精密度試驗
取“2.4”項下0.4、4.0、5.6 μg/ml 3種質量濃度的琥珀酸索利那新對照品溶液適量,分別按“2.1”項下色譜條件連續進樣測定6次,記錄峰面積。結果,琥珀酸索利那新峰面積的RSD分別為0.88%、0.20%、0.17%(n=6),表明儀器精密度良好。
2.6 穩定性試驗
取自研制劑樣品,以水、pH1.2鹽酸溶液、pH4.5乙酸鹽緩沖液和pH6.8磷酸鹽緩沖液4種溶出介質,分別按“2.2.2”項下方法進行溶出度試驗并制備供試品溶液,分別于室溫下放置0、2、4、6、12 h時按“2.1”項下色譜條件進樣測定,記錄峰面積。結果,4種溶出介質中琥珀酸索利那新峰面積的RSD分別為0.45%、0.68%、0.70%和1.08%(n=5),表明供試品溶液在室溫下放置12 h內穩定性良好。
2.7 重復性試驗
取自研制劑樣品,每次6片,按“2.2.2”項下方法進行溶出度試驗并制備供試品溶液,再按“2.1”項下色譜條件進樣測定并計算其溶出度,重復測定6次。結果,琥珀酸索利那新溶出度的平均值為97.60%,RSD=0.89%(n=6),表明本方法重復性良好。
2.8 回收率試驗
根據自研制劑處方,按處方量50%、80%、100%精密稱取琥珀酸索利那新對照品,輔料按處方量100%稱取,每個水平各3份,按“2.2.2”項下方法進行溶出度試驗并制備供試品溶液;另取琥珀酸索利那新對照品適量,精密稱定,以水-乙腈(70∶30,V/V)溶解并稀釋制成與供試品溶液質量濃度相近的對照品溶液。分別取上述兩種溶液各適量,按“2.1”項下色譜條件進樣測定,記錄峰面積,以外標法計算回收率,結果見表1。
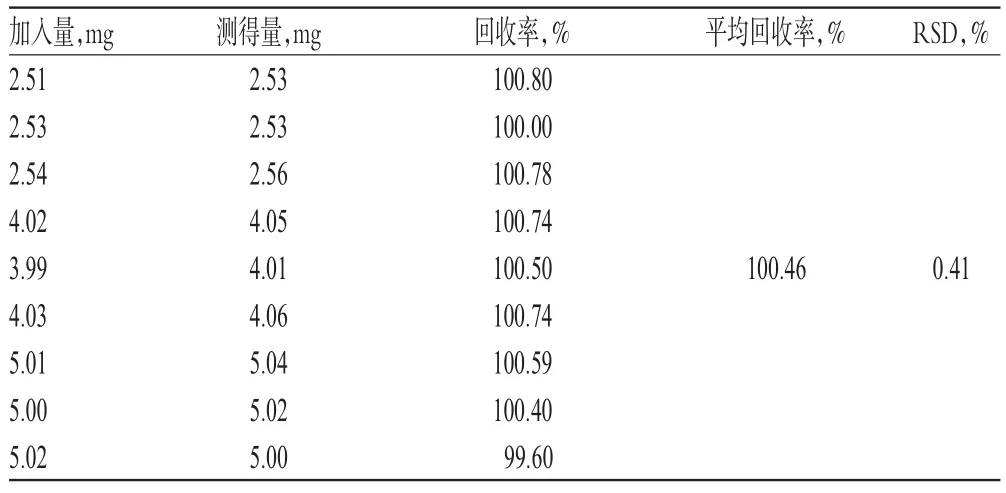
表1 回收率試驗結果(n=9)Tab 1 Results of recovery tests(n=9)
2.9 溶出度測定及溶出曲線繪制
按2015年版《中國藥典》(四部)“溶出度與釋放度測定法”第二法(槳法)進行溶出試驗[6],分別以900 ml水、pH1.2鹽酸溶液、pH4.5乙酸鹽緩沖液和pH6.8磷酸鹽緩沖液作為溶出介質,轉速50 r/min,溫度(37.0±0.5)℃,依法操作,分別于5、10、15、20、30、45 min時取溶出液10 ml(即時在溶出杯中補加10 ml溶出介質),經0.45 μm微孔濾膜濾過后,取續濾液3.5 ml與1.5 ml乙腈混勻,制成供試品溶液;另取琥珀酸索利那新對照品適量,按“2.2.1”項下方法制成對照品溶液。分別取上述兩種溶液各適量,按“2.1”項下色譜條件進樣測定,記錄峰面積,以外標法計算各時間點的累積溶出度,繪制溶出曲線,結果見表2和圖2。
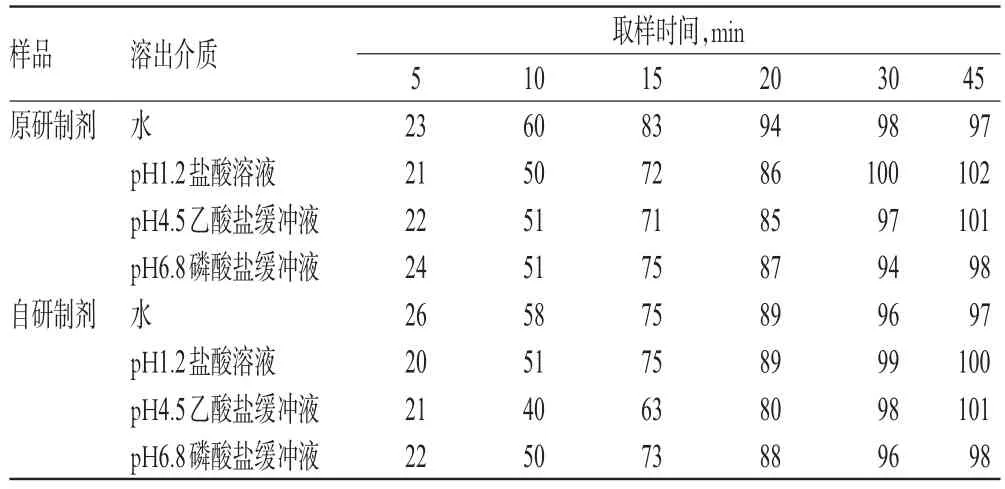
表2 琥珀酸索利那新片自研制劑與原研制劑在各溶出介質中的平均累積溶出度(n=12,%)Tab 2 Average cumulative dissolution of self-development and original preparations of Solifenacin succinate tablet in each dissolution medium(n=12,%)
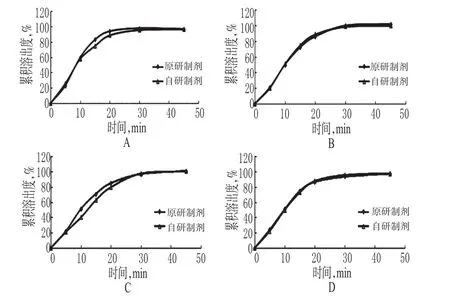
圖2 琥珀酸索利那新片自研制劑與原研制劑在各溶出介質中的溶出曲線(n=12)A.水;B.pH1.2鹽酸溶液;C.pH4.5乙酸鹽緩沖液;D.pH6.8磷酸鹽緩沖液Fig 2 The cumulative dissolution profiles of self-development and original preparations of Solifenacin succinate tablet in each dissolution medium(n=12)A.water;B.pH1.2 hydrochloric acid solution;C.pH4.0 acetate buffer solution;D.pH6.8 phosphate buffered solution
2.10 溶出曲線的相似性評價
采用FDA推薦的相似因子(f2)法,分別考察在4種溶出介質中琥珀酸索利那新片自研制劑與原研制劑溶出曲線的相似性。f2計算公式為:
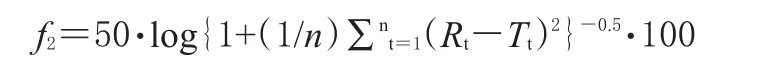
式中,Rt為原研制劑(參比制劑)t時間的平均累積溶出度;Tt為自研制劑(受試制劑)t時間的平均累積溶出度;n為取樣時間點個數(n=3~5,且Rt>85%的點不超過1個,因此本研究選取5、10、15、30 min時的平均累積溶出度進行計算)。f2取值在0~100之間,FDA規定當f2值在50~100之間時,表明兩種制劑的溶出曲線相似,且值越大相似度越高。經計算,琥珀酸索利那新片自研制劑與原研制劑在4種溶出介質中溶出曲線的f2均>50,說明二者溶出曲線具有相似性。琥珀酸索利那新片自研制劑與原研制劑在各溶出介質中溶出曲線的見表3。
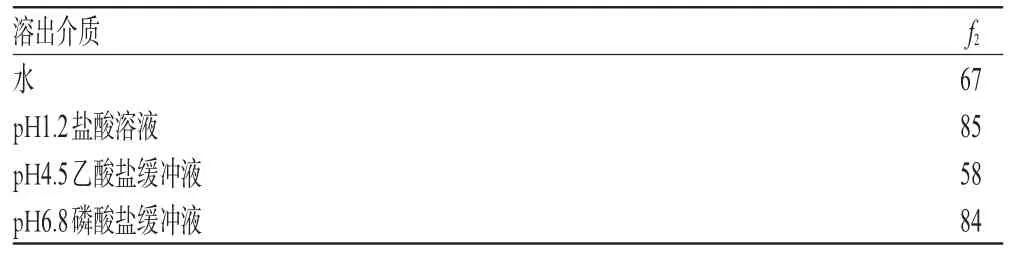
表3 琥珀酸索利那新片自研制劑與原研制劑在各溶出介質中溶出曲線的f2(n=4)Tab 3 The f2of dissolution profiles of self-development and original preparations of Solifenacin succinate tablet in each dissolution medium(n=4)
3 討論
體外溶出度試驗常用于指導藥物制劑的研發,評價制劑批間、批內質量的一致性,以及評價藥品處方工藝變更前后質量和療效的一致性等。已有數據表明,若仿制制劑體外多條溶出曲線與原研制劑皆一致,則二者體內生物利用度一致的概率高[7]。琥珀酸索利那新血藥峰濃度(cmax)在口服后3~8 h達到[8],該藥體內生理pH介質下30 min已經完全溶出,故其體外溶出曲線更重要的意義在于為制劑處方和工藝的開發及優化提供參考。尤其對于小規格口服固體制劑而言,原輔料的混合均勻性、片重和硬度差異等均會對溶出曲線和片間溶出差異產生較大影響。
3.1 溶出介質的選擇
固體制劑口服給藥后,藥物的吸收取決于藥物從制劑中的溶出或釋放、藥物在生理條件下的溶解以及在胃腸道的滲透。溶出度試驗應盡可能在生理條件下進行,這樣可以從藥品體內行為的角度,更好地理解體外溶出數據[9],且溶出介質中藥物溶解性應滿足漏槽條件的要求。預試驗中,取琥珀酸索利那新原料藥約1 g,分別加入1 ml水、pH1.2鹽酸溶液、pH4.5乙酸鹽緩沖液和pH6.8磷酸鹽緩沖液中,37℃恒溫,均迅速溶解,呈無色透明黏稠狀溶液,表明琥珀酸索利那新在所選取的不同pH介質中均易溶,溶解性為非pH依賴型,完全滿足漏槽條件。故參考CFDA發布的《普通口服固體制劑溶出度試驗技術指導原則》,最終選擇水、pH1.2鹽酸溶液、pH4.5乙酸鹽緩沖液和pH6.8磷酸鹽緩沖液作為溶出介質。
3.2 溶出方法和轉速的選擇
3.2.1 溶出方法的選擇 取原研制劑(12片),按2015年版《中國藥典》(四部)“溶出度與釋放度測定法”項下第一法(籃法)與第二法(槳法)進行溶出試驗[6],以水為溶出介質,溶出介質體積為900 ml,轉速為50 r/min,分別在5、10、15、20、30、45 min時取溶出液10 ml(即時在溶出杯中補加10 ml溶出介質),經0.45 μm微孔濾膜濾過,取續濾液3.5 ml與1.5 ml乙腈混勻,按“2.1”項下色譜條件進樣測定,記錄峰面積并計算各取樣時間點琥珀酸索利那新的累積溶出度。結果表明,采用籃法與槳法在各取樣時間點的平均累積溶出度基本一致,因片劑溶出度測定一般采用槳法,故本試驗最終選用槳法。
3.2.2 轉速的選擇 取原研制劑(12片),按2015年版《中國藥典》(四部)“溶出度與釋放度測定法”項下第二法(槳法)[6],以水為溶出介質,溶出介質體積為900 ml,轉速分別為50、75 r/min,余按“3.2.1”項下方法操作,進樣測定并計算各取樣時間點琥珀酸索利那新的累積溶出度。結果表明,轉速為75 r/min時溶出偏快,15 min時間點平均累積溶出度>85%,導致溶出曲線的區分能力較差;而當轉速為50 r/min時,溶出速率較為合適,故本試驗最終選擇轉速為50 r/min。
3.3 本研究的成果
本研究建立了琥珀酸索利那新片溶出度測定的HPLC法。經驗證,本方法準確性好、靈敏度高,適用于琥珀酸索利那新片的溶出度測定。同時,本研究建立了具有區分力的琥珀酸索利那新片的溶出試驗方法[10],為琥珀酸索利那新片自研制劑的處方和工藝篩選以及與原研制劑的質量一致性評價提供了試驗依據。研究結果表明,自研制劑與原研制劑溶出行為基本一致,一定程度說明自研制劑的處方和工藝具有可行性,但二者的體內生物利用度和生物等效性是否一致還有待進一步考察。
[1] 鄭建洪,黃紅萍.治療膀胱過度活動癥的新藥索利那新[J].中國新藥與臨床雜志,2013,32(10):771.
[2]那彥群,葉章群,孫穎浩,等.中國泌尿外科疾病診斷治療指南:2014版[M].北京:人民衛生出版社,2013:330-333.
[3] Apostolidis A.Antimuscarinics in the treatment of OAB:is there a first-line and a second-line choice?[J].Current Drug Targets,2015,16(11):1 187.
[4]國家食品藥品監督管理總局.普通口服固體制劑溶出度試驗技術指導原則[EB/OL].(2015-02-05)[2015-06-06]. http://www.sda.gov.cn/WS01/CL0087/114286.html.
[5]FDA.Dissolution Methods Database:Solifenacin Succinate Tablets[EB/OL].(2008-02-19)[2015-07-06].http:// www.accessdata.fda.gov/scripts/cder/dissolution/index.cfm.
[6]國家藥典委員會.中華人民共和國藥典:四部[S].2015年版.北京:中國醫藥科技出版社,2015:121-124.
[7]林蘭,牛劍釗,許明哲,等.國外仿制藥一致性評價比較分析[J].中國新藥雜志,2013,22(21):2 470.
[8]劉軍,姚建.新型毒蕈堿受體拮抗劑solifenacin治療膀胱過動癥[J].世界臨床藥物,2006,27(1):39.
[9]張啟明,謝沐風,寧保明,等.采用多條溶出曲線評價口服固體制劑的內在質量[J].中國醫藥工業雜志,2009,40(12):946.
[10]謝沐風.具有區分力的溶出曲線[J].中國醫藥工業雜志,2014,45(7):687.
(編輯:周 箐)
Similarity Evaluation of Dissolution Profiles of Self-development and Original Preparation of Solifenacin Succinate Tablet
GONG Junqiang1,2,CHEN Xian2,XU Caihong2,ZHANG Xia3,WU Chunmei2,WANG Ping2,FU Xuchun1(1.College of Pharmacy,Zhejiang University,Hangzhou 310058,China;2.Zhejiang Huayi Pharmaceutical Co.,Ltd.,Zhejiang Yiwu 320002,China;3.Huadong Biological Engineering Research Institute,Hangzhou 310011,China)
OBJECTIVE:To explore the similarity of dissolution profiles of self-development and original preparation of Solifenacin succinate tablet,and provide reference for the prescription and process screening of the former one and the quality similarity evaluation of the latter one.METHODS:The paddle method was adopted with rotational speed of 50 r/min,using water,pH1.2 hydrochloric acid solution,pH4.0 acetate buffer solution and pH6.8 phosphate buffer solution as dissolution media,HPLC was used to determine the cumulative dissolution of main components of self-development and original preparation of Solifenacin succinate tablet at different time points,dissolution profile was drew,then f2was used to evaluate its similarity.RESULTS:In the 4 dissolution media,the f2of both self-development and original preparation of Solifenacin succinate tablet was higher than 50,which indicated that the dissolution profiles showed similarity.CONCLUSIONS:The established HPLC is suitable for the dissolution determination of Solifenacin succinate tablet;the dissolution profiles of the self-development and original preparations are basically similar,which indicates the prescription and technology of self-development preparation are feasible.
Solifenacin succinate tablet;Self-development;Original preparation;HPLC;Dissolution profiles;f2similarity factor;Evaluation
R927
A
1001-0408(2016)30-4311-04
2015-11-04
2016-09-14)
*工程師,碩士研究生。研究方向:藥物制劑研發。E-mail:47160688@qq.com
#通信作者:教授,博士。研究方向:新藥研發和藥動學。E-mail:fuxc@zucc.edu.cn
DOI 10.6039/j.issn.1001-0408.2016.30.44

