芳綸原料制備中尾氣氯化氫回收制氯清潔工藝
王農躍
(上海方綸新材料科技有限公司,上海 200122)
芳綸原料制備中尾氣氯化氫回收制氯清潔工藝
王農躍
(上海方綸新材料科技有限公司,上海200122)
闡述了氯化氫污染現狀、以及伴隨著有機氯產品的發展而產生更多的副產氯化氫情況。介紹了芳綸制造中副產氯化氫的現有處理方法及特點,重點介紹了最具工業化前景的氯化氫催化氧化制氯氣清潔工藝,并通過工藝之間的比較,分析了上海方綸開發的氯化氫氧化工藝的優勢與發展前景。
氯化氫;催化氧化;氯氣
1 氯化氫污染現狀
氯氣主要應用于生產PVC、聚氨酯環氧樹脂、硅材料、合成橡膠、氟氯烴、TiO2,涂料及一些農用化學品、建筑材料和一些醫藥制劑[1~2]。1998年,美國和歐洲年消耗氯2 500萬t,我國消耗量達到576萬t,居世界第二位[3]。2008年我國氯氣消費量達到1 700萬t,約占世界氯氣消費總量的1/3[4]。
然而在有氯氣參與的工業生產中,主要進行的是有機物的氯取代反應,氯資源的原子利用率最高不超過50%,另外一半的氯成為大量的副產氯化氫。1986年,日本副產HCl就達47萬t之多,全世界副產HCl約達1 650萬t之多[5]。2011年,我國工業副產氯化氫總量達到了380萬t[6],隨著MDI、TDI、甲烷氯化物等涉氯產品的大規模擴產和氯堿行業的發展,預計5年內(2012 ~2016年)副產HCl的總量將達到500萬t/年。
2 有機氯產品的發展
有機氯是指結構中含有氯元素的有機化合物。目前,我國主要的有機氯產品的生產能力已經穩居世界第1位[7]。國內規模以上氯產品有數十個品種,根據2011年的產能估算[8],其中聚氯乙烯、甲烷氯化物、環氧氯丙烷、MDI/TDI等產能規模較大,約占國內有機氯產品產能的70%以上。
2.1聚氯乙烯(PVC)
聚氯乙烯是氯堿行業耗氯量最大的有機氯產品,其耗氯量約占行業總耗氯量的35%~40%[9]。2005年,我國聚氯乙烯產量為688萬t,2014年增至1 630萬t,年均增長率達10.4%。近年中國聚氯乙烯產量情況見圖1。并且,未來幾年中國聚氯乙烯新建項目較多,據不完全統計,新增產能將達到400萬t/年左右[10]。
2.2甲烷氯化物
甲烷氯化物包括一氯甲烷、二氯甲烷、三氯甲烷(氯仿)和四氯化碳,是有機氯產品中僅次于聚氯乙烯的最大宗產品。
2003年,我國甲烷氯化物總生產能力接近40萬t[11],2010年產能約為116萬t/年,2010~2011年新增產能約30萬t,達到146萬t/年,2013年產能超過200萬t/年。目前,國內尚有部分企業正在或計劃擴建甲烷氯化物項目[8]。
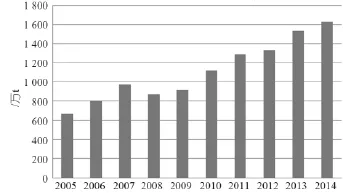
圖1 聚氯乙烯產量情況
2.3環氧氯丙烷
環氧氯丙烷是生產環氧樹脂、合成甘油和氯醇橡膠的重要原料,近年環氧氯丙烷產能增長情況見下圖2。

圖2 環氧氯丙烷產能情況
2015年我國環氧氯丙烷產能繼續增長,產能有些過剩,市場需求面臨考驗,但是長期來看,隨著經濟復蘇,需求釋放,屆時我國環氧氯丙烷的消費也將進入一個新的發展時期[12]。
2.4MDI/ TDI
2.4.1MDI(二苯基甲烷-4,4′-二異氰酸酯)
據不完全統計,2015年我國MDI產能達到261萬t/年。且德國拜耳計劃在上海新建50.0 萬t/年生產裝置;巴斯夫公司在重慶新建的40.0 萬t/年MDI項目;上海聯恒異氰酸酯有限公司在上海啟動了新建24.0萬t/年MDI生產裝置項目。此外,甘肅銀光聚銀化工有限公司、滄州大化集團有限責任公司、天脊集團等公司也有新建MDI生產裝置的初步意向和前期規劃。如果這些項目能夠按照計劃實施,預計到2018年,我國MDI的總生產能力將達到約375.0萬t/年,繼續領先世界產能潮流[13]。
2.4.2TDI(甲苯二異氰酸酯)
2012年,我國TDI產能為82萬t/年[8],2014年產能為88.5萬t/年,預計,到2020年國內TDI產能將達到131萬t/年[14]。
有機氯產品產能近年來快速增長,從上述列出的幾類有機氯產品的產能/產量增長情況可以窺見一斑。伴隨著國內氯產品產能的快速增長,氯氣的消耗量進一步加大,副產氯化氫量也將隨之快速增長。因此,亟待開發一種環保、節能、充分利用副產氯化氫資源的技術。
3 氯化氫制氯氣工藝
傳統的副產HCl處理方法一是用水吸收制成鹽酸被回收利用或低價出售,因其中含有一定量的有機雜質,其用途受到了較大的限制,造成副產鹽酸漲庫,直接影響主導產品的生產;二是用堿液中和后直接排空,這不僅影響氯產品生產的經濟效益,還會造成嚴重的環境污染。
而許多產生副產氯化氫的工藝同時又是大量消耗氯氣的過程,將氯化氫重新轉化為氯氣,可以實現氯化氫的循環利用。目前,氯化氫制備氯氣的方法主要可以分為三類:電解法,直接氧化法和催化氧化法。
3.1電解法
氯化氫電解法分為濕法和干法,而濕法又分為隔膜電解和氧陰極電解。
3.1.1隔膜電解法
隔膜電解法要求氯化氫氣體通過吸收使氯化氫變為鹽酸,鹽酸經過精制除去雜質后在隔膜電解槽中電解,生成氫氣和氯氣,反應方程式為:2HCl=H2↑+Cl2↑。隔膜電解法工藝是由赫斯特、 拜耳公司和伍德公司合作開發的, 已對世界上一百余家氯堿廠提供該技術。但是該方法能耗大,沒有發展潛力。
3.1.2氧陰極電解法
氧陰極電解法也是需要氯化氫氣體通過吸收變成鹽酸,鹽酸經過深度精制除去雜質后,在離子膜電解槽中電解,陰極通入氧氣,從而生產出氯氣和水,化學方程式為:4HCl+O2=2H2O+2Cl2↑。拜耳公司是世界上利用鹽酸電解方法生產氯氣的最大生產商,目前在德國有40萬t/年生產能力,其中2萬t/年采用的是最新的ODC氧陰極鹽酸電解工藝。該方法比傳統的隔膜法電解節電35%,但是投資大、離子膜電解槽對材質要求高、氧陰極要求高且要求有純氧供給。
3.1.3干法電解
美國杜邦公司在 20 世紀 90 年代中期發明了干電解氯化氫生產氯的工藝用于乙烯氯化。該方法延長了隔膜的使用壽命,但是對雜質敏感,電解氯化氫前,一般需先將氣體用加熱的方法進行預處理,脫除有機物和其他雜質,然后加入電解槽陽極一側,氯化氫轉化成氯氣,質子通過全氟陽離子交換膜轉移到陰極,轉化成含水氫氣,該工藝能耗高,成本高。
3.2直接氧化法
直接氧化法是利用 NO2、SO3、NOHSO4和混合酸HNO3/H2SO4等無機氧化劑直接氧化HCl制備Cl2的一種方法,典型工藝為杜邦公司20世紀60年代開發的硝酸氧化法Kel-Chlor工藝[15],該工藝使用硝酸和硫酸的混合物氧化氯化氫。反應方程式為:
NO2+2HCl?NO+Cl2+H2
NO+ NO2+H2SO4?2NOHSO4+H2O
NOHSO4+HCl?NOCl+ H2SO4
2NOCl?2 NO+Cl2
2 NO+ O2?2 NO2
直接氧化法由于存在反應過程中產生腐蝕性物質、產物分離困難、能耗較大、廢液處理難等問題,難以實現工業化。
3.3催化氧化法
1868年,英國人Deacon首先采用負載在載體沸石上的銅或錳鹽等作為催化劑,氧氣或空氣作為氧化劑,使氯化氫氧化生成氯氣,并發表了一系列專利[16~20],其反應方程式可表述為:4HCl(g)+O2?2H2O+Cl2+114.48(kJ),人們習慣上將以上反應稱為Deacon反應。在工程應用中存在的問題包括:①受反應平衡的限制,氯化氫轉化率只有60%~70%;②反應溫度過高(430~475℃之間),活性組分氯化銅在400℃以上容易揮發,導致催化劑流失、活性迅速降;③未反應的氯化氫與可能凝結的水蒸氣結合生成鹽酸,帶來嚴重的設備腐蝕問題。
1962年,美國Shell Oil Company[21~23]采用SiO2負載銅鹽催化劑,并開發了采用該催化劑的固定床工藝[24],于1965年分別在荷蘭和印度建成了30 000 t/年的裝置,由于催化劑活性組分流失及轉化率無法提高等因素,該裝置已經關停。
日本住友化學工業株式會社研制公開了以氧化釕為活性組份、氧化鈦為載體的催化劑體系[25~27]以及使用氧化釕催化劑的列管式反應器,見圖3,在列管中將催化劑分成2~4個串聯排列的反應段進行裝填,其中至少有一個反應段的溫度控制所用的熱交換介質為50%~55%硝酸鉀、37%~43%亞硝酸鈉和5%~10%的硝酸鈉所組成的熔鹽。其氯氣產能為12萬t/年規模的固定床反應器已先后在日本三菱公司、拜耳上海公司和萬華寧波工業園等地實際應用[28]。該方法中催化劑成本過于昂貴,投資成本高。
Benson小組[29]為了改善固定床反應器氯化氫轉化率較低的問題,開發了雙流化床二段法工藝。這種工藝流程將反應分為低溫氯化(氧化銅和氯化氫在200~280℃下反應)和高溫氧化(氯化銅和氧氣在340~380℃下反應)兩個步驟,催化劑在2個反應器之間通過固體催化劑循環裝置進行交互傳遞。反應方程式為:CuO+2HCl→CuCl2+H2O CuCl2+1/2O2→CuO+Cl2,工藝示意圖見圖4,該工藝的缺點在于兩個反應器中的壓力不一樣,固體催化劑容易從高壓的氧化反應器進入壓力低的氯化反應器,而不容易從低壓的氯化反應器進入高壓的氧化反應器,難以實現催化劑顆粒循環。

圖3 日本住友固定床反應器

圖4 Benson雙流化床工藝示意圖

圖5 單塔二段流化床
清華大學[30]在Beason工藝的基礎上,開發了單塔二段流化床催化氧化工藝,特點是在流化床提升管中設置氣固分布板形成二段流化床反應器,上段為進行氯化反應的氯化反應器,下段為發生氧氯化反應的氧化反應器,催化劑的轉移靠氣流推動和重力完成,見圖5,雖然全過程HCl的轉化率能接近100%,但在“氧氯化”段氯化氫的轉化率未超過60%,且過程操作復雜,控制困難。清華大學和煙臺萬華共同合作采用該流化床裝置在寧波建成了中試裝置,但尚未有商業化應用的報道[31]。清華大學在后續對該裝置進行了進一步的改進[32],采用氣固分布板將流化床反應器主體分為上下兩段,上段為氯化段,下段為氧氯化段,氯化氫氣體入口設置在氧氯化段的中部,另外通過在氧氯化段設置多層錯排氣固逆流擋板等措施,進一步提高氯化氫的轉化率。
德國巴斯夫公司開發了氯化氫的兩階段固定床催化氧化法[33],第一階段為氯化,向反應器中通入HCl氣體,使HCl與催化劑反應生成水和固定在催化劑上的氯化物,排出水,完成后用惰性氣體沖洗反應器;第二階段為氧化,將氣態氧化劑送入反應器,與前面生成的含氯化合物反應,釋放出氯氣,并排出反應器,隨后用惰性氣體沖洗反應器。其中,催化劑采用陶瓷材料為載體,用浸漬法將銅、鐵、堿金屬氯化物等負載于載體上制得。可以用一固定床反應器或多個相連的固定床反應器來實施,圖6為5個相連的固定床反應器工藝圖。雖然該兩階段固定床反應工藝可以打破氯化氫氧化的化學平衡限制,氯化氫轉化率高,但在氧化混合氣中仍存在大量的氧氣及氮氣,難以直接利用。

圖6 巴斯夫固定床反應器示意圖
南京工業大學提出了一種流化床與絕熱固定床串聯的氯化氫氧化反應工藝[34],可以利用流化床良好的移熱性能,避免在列管式固定床反應器中因放熱反應產生的飛溫現象,圖7為流化床反應器與4臺絕熱反應器串聯工藝圖。不過,由于固定床與流化床操作氣速、催化劑粒度與壓降差異均很大,一般很少串聯操作使用[35~36],為了滿足強放熱反應的移熱與轉化率的要求,可以串聯操作,但需要考慮前面的流化床出口夾帶的顆粒對后面固定床中催化劑磨損的影響,在0.212~0.424 m/s氣速下,固定床中顆粒質量損失可達3%~4%[37];以及后面固定床層對前面流化床催化劑的進一步磨損,并同時關注固定床的允許氣速與流化床中細顆粒的機械強度。
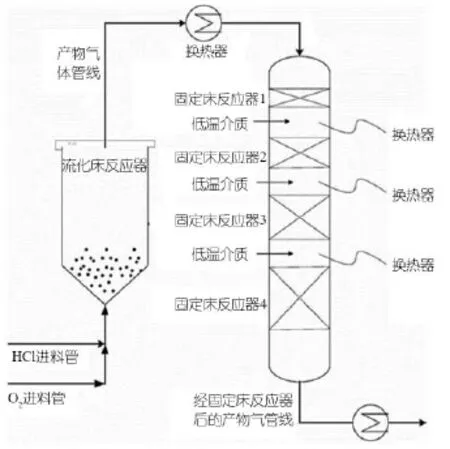
圖7 流化床與絕熱反應器串聯工藝圖
萬華聚氨酯股份有限公司寧波分公司在生產聚氨酯過程中,每年要產生45萬t氯化氫,為此萬華也加快了催化氧化制氯技術的研究工作,開發了采用微反應器進行氯化氫氧化制備氯氣的工藝[38],微反應器結構示意圖見圖8。以及一種利用磁穩流化床進行氯化氫氧化制備氯氣的工藝[39],磁穩流化床結構示意圖見圖9。微反應器容易出現微通道堵塞、以及檢測與控制難等問題;磁穩流化床的應用需要相應合適的磁性催化劑并確定磁穩流化床的穩定操作區域,磁穩流化床的磁場發生裝置在產生磁場的過程中會釋放出大量的熱量,易對磁性載體和反應過程產生影響。目前來說,這些方法技術都不成熟,工業化困難。
上海氯堿化工股份有限公司,對催化劑進行了改進[40],采用以二氧化硅包覆的氧化鋁為載體制備催化劑,并將其應用于固定床工藝,減少了反應過程中催化劑的流失,但是氯化氫轉化率低,不到80%。
4 上海方綸新材料開發的氯化氫制氯回收工藝
盡管國內外的企業與科研單位均在加快氯化氫催化氧化制氯技術的開發和改進工作,但是通過前述介紹我們可以看出目前催化氧化工藝仍存在各種問題,其中最大的問題在于:①反應溫度較高,催化劑揮發導致活性迅速降低,需要不斷更換或者補加催化劑,從而導致生產成本過高;②催化氧化后反應所得氣體的分離困難;③成本高,技術不成熟,操作控制難,導致難于實現工業化。

圖8 微反應器結構示意圖

圖9 磁穩流化床結構示意圖
針對該情況,上海方綸新材料科技有限公司開發了一種關于氯化氫催化氧化制備氯氣的新工藝,該工藝已申請了中國發明專利[41],并提交了PCT國際申請[42]。
上海方綸開發的新工藝可以通過一個或多個串聯或并聯的裝填有催化劑的反應器(優選絕熱反應器)來實現。以三個反應器串聯、多段進氧為例,工藝流程如圖10所示。
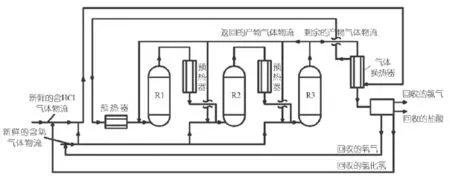
圖10 上海方綸材料氯化氫氧化工藝流程
4.1具體工藝步驟
(1)向第一反應器提供含氯化氫氣體物流以及用于氧化所述含氯化氫氣體物流的含氧氣體物流,向第二、第三反應器提供用于氧化所述含氯化氫氣體物流的含氧氣體物流,以進行催化氧化氯化氫的反應。
(2)將來自第三反應器的經過催化氧化反應的產物氣體物流的一部分不經分離直接返回至任意一個或任意多個反應器。
(3)將來自第三反應器的剩余的產物氣體物流部分分離以獲得氯氣,并將分離回收的氯化氫和氧氣循環至反應器中繼續參與反應。
4.2該工藝具有下列優點
(1)將來自最后一個反應器的經過催化氧化反應的產物氣體物流的一部分不經分離返回至反應器,直接利用催化氧化后產物氣體物流部分的熱能加熱含氯化氫氣體物流和/或用于氧化含氯化氫氣體物流的含氧氣體物流,從而使得進入第一反應器的氣體物流達到適宜的反應溫度,而不必全部使用外部熱源對含氯化氫氣體物流和/或用于氧化含氯化氫氣體物流的含氧氣體物流體進行加熱到適宜的反應溫度。
(2)由于未經分離的產物氣體物流再次經過催化劑床層時不再釋放反應熱,也即這些氣體成為只含氯化氫、氧、氯氣和水蒸氣的不含其他氣體成分的相對反應的“惰性”氣體,摻混有產物氣體物流的氣體物流在經過反應器時,反應器中的催化劑床層溫度比現有工藝具有更好的可控性。
(3)在返回產物氣體物流對反應熱的控制作用下,和依次向下游反應器提供含氧氣體物流等方式的共同作用下,催化劑壽命得到顯著延長。
(4)所返回的產物氣體物流與經催化氧化反應得到的產物氣體物流成分相同,這大大降低了后續分離操作的難度和對設備的要求;特別地,當選擇氧氣過量至能夠保證氯化氫基本被氧化時,產物氣體物流更易于分離。因為氧氣過量,使得氯化氫殘余量小,甚至可以忽略。因此產物氣體物流通過冷凝后,反應形成的水即可以將氯化氫基本吸收,深度脫除水份后,只需要分離氯氣和氧氣,即可得到氯氣,后續分離操作可以進一步簡化。
5 氯化氫制備氯氣的工藝比較
由于電解法存在著投資大、能耗高、對裝置要求高及產品純度不高等不足之處、而直接氧化法又難以實現工業化,因此,催化氧化法最具工業化潛力,成為氯化氫轉化為氯氣的主要發展方向。
從工業化能力比較來說:
(1)電解法,能源消耗太大,且離子膜也需要經常更換,成本非常高,每噸氯氣回收成本>4 000元。
(2)直接氧化法,回收率低,不可工業化。
(3)催化氧化過程最具工業化潛力,部分工藝已經實現工業化,但是仍然存在氯化氫轉化率低,投資成本高等問題。其中固定床催化氧化法,設備投資太大,每噸氯氣回收成本>1 200元,萬噸氯化氫處理裝置投資>10億,且沒有解決系統中由于氯化氫、氧氣、水汽、氯氣的混合氣體,在400℃以上操作溫度下的設備腐蝕問題以及反應巨大的放熱引起的傳熱問題;而國內由高校與企業共同研發的流動床工藝一直受到反應溫度高、體系材質耐腐蝕等問題的困擾。
(4)上海方綸新材料科技有限公司研發的氯化氫氧化過程,采用多級進氧、反應氣循環的絕熱反應工藝,既解決了設備腐蝕問題也解決了傳熱問題,單程轉化率達到90%以上,并用吸附與解吸附工藝回收氯氣,氯氣成本降至400元/t。
氯化氫回收制備氯氣的各種工藝的具體比較見表1。

表1 氯化氫制備氯氣方法比較
6 上海方綸新材料氯化氫制氯工藝的發展前景
近年來,我國氯堿產能的快速增長帶動和刺激了氯產品的發展,與此同時,國內外市場對氯的需求量越來越大,特別是國內外市場對聚氯乙烯和異氰酸酯的強勁需求,使得有機氯產品快速發展,隨之而來的是大量的副產氯化氫。除此之外,化肥、輕工、電鍍、制藥及冶金等行業的生產過程也會產生大量廢鹽酸,這也是副產氯化氫的重要組成部分,以化肥行業為例,僅僅年產約600萬t硫基氮磷鉀復合肥,就要副產鹽酸約200萬t[6]。
大量副產HCl的出路和利用問題已成為制約聚氨酯、氯堿、有機氟、農藥、醫藥化工等眾多行業發展的共性難題。因此有效的綜合利用副產氯化氫,通過氯化氫的綜合利用提供下游有機氯產品賴以發展的原料氯將十分有意義。
但是目前國內僅萬華化學在寧波建成了氯化氫催化氧化制氯氣工業化裝置,雖然其自身也在積極研發氯化氫氧化制氯技術,不過其工業化裝置卻是引進日本住友的技術。此外,上海氯堿化工股份有限公司自主研發的氯化氫催化氧化制氯氣技術已建成千噸級中試裝置并平穩運行,但是從上海氯堿公開的技術來看,其氯化氫轉化率較低,不到80%。
基于國內的氯化氫催化氧化技術現狀并結合副產氯化氫量持續增長的情況來看,上海方綸新材料開發的氯化氫氧化清潔工藝市場前景廣闊,其將廉價量大的氯化氫綜合利用并高附加值化,實現了氯元素的閉路循環和反應過程的零排放,這將徹底改變整個行業的格局,帶來巨大的經濟效益和社會效益。參照現有文獻[43]估算,如果將我國目前副產的500余萬t/年的氯化氫制成氯氣或下游產品循環利用,每年可節電約121.3億kW.h(折標煤425萬t/年),間接減排1 000萬t各類有機廢水,經濟效益和社會效益巨大。目前中國產業調整政策已涉及副產氯化氫的綜合利用,并列入了國家 2011 年產業結構調整鼓勵類名錄。因此,上海方綸新材料公司開發的氯化氫催化氧化制氯清潔工藝,也順應了國家的政策導向,符合循環經濟的發展模式,必將得到發展和應用。
[1] 吳玉龍,魏飛,韓明漢,等.回收利用副產氯化氫制氯氣的研究進展[J].過程工程學報, 2004,4(3):269~275.
[2]Committee on Medical and Biologic Effects of Environmental Pollutants.Chlorine and Hydrogen Chloride [M]. Washington:National Academy 0f Sciences.1976:282.
[3] 張泗文.世界氯堿產業動向及其對我國市場的影響[J].氯堿工業, 2002,3:1~11.
[4]葉田忠.國內外燒堿市場展望[J].氯堿工業, 2009,45(11):1~7.
[5]萬永周.氯化氫催化氧化制氯氣工藝研究[D].南京工業大學.2004.
[6]劉建路,何家海,潘玉強,等.我國副產氯化氫的現狀和綜合利用[J].廣州化工, 2011,39(9): 25~28.
[7]何如浩.氯化氫氣體在離子液體中溶解性能的研究[D].北京化工大學, 2012.
[8] 劉鵬.氯產品發展建議及主要產業鏈搭建[J].氯堿工業. 2013.4:1~8.
[9]蔡杰.國內氯產品現狀與發展趨勢分析(上)[J].觀察市場. 2012.1:51~53.
[10]田升江.2014年中國聚氯乙烯市場分析及前景展望[J].中國石油和化工經濟分析. 2015.8:55~57.
[11]張鑫.我國甲烷氯化物行業現狀及發展趨勢[J].中國農藥. 2011.7:21~28.
[12]屈葉青.環氧氯丙烷的生產技術及國內外市場分析[J].石油化工技術與經濟. 2015.31(4): 26~30.
[13] 李玉芳,伍小明.MDI生產技術進展及國內外市場分析[J].上海化工. 2015.40(10):33~38.
[14] 張悅,張寶輝,宗茂森.甲苯二異氰酸酯產品競爭環境分析[J].化學工業. 2014.32(9):16~18.
[15] Van Kijk C P,Schreiner W C.Hydrogen Chlorine to Chlorine via the Kel.Chlor Process. Chemical Engineering Process. 1973(69)4:57~63.
[16] BP1403(1868).H.Deacon.
[17] Henry Deacon.Manufacture of chlorine:US85370,1 868.
[18] Henry Deacon.Improvement in the manufacture of chlorine:US141333.1873.
[19] Henry Deacon.Improvement in the manufacture of chlorine:US165802.1875.
[20] Henry Deacon.Improvement in apparatus for the manufacture of chlorine:US118209.1871.
[21] W.F.Engel, M.J.Waale, Recent Developments in the Oxidative Recovery of Chlorine from Hydrochloric Acid. Chemistry and Industry. Jan.13.1962:76~83.
[22] WillemF.Engel,FreddyWattimena. Process for the production of chlorine:US3210158.1965.
[23] F.Engel,Freddy Wattimena.Catalyst composition,particularly for catalyzing oxidation of hydrogen chloride to chlorine: US3260678,1996.
[24] Alphonsus M. Alkemade, Johannes H.De Groot. Hydrochloric acid recovery: US3242647.1966.
[25] 西田洋之,阿部川宏明.氯的制造方法:CN1145328.1997.
[26] 阿部川宏明,伊藤禎昭,日比卓男.氯的生產方法:CN1176223.1998.
[27] 鈴田哲也,石野勝,巖永清司.制備氯氣的方法:CN1201013.1998.
[28] 郭楊龍,孫宇,盧冠忠,等. 用于氯化氫催化氧化制氯氣的銅基催化劑及其制備方法和應用:CN104923239.2015.
[29] R.C. Minet, S.W. Benson, and T.T. Tsotsis. Recovery of chlorinr from hydrogen chloride by carrier catalyst process:US4994265.1991.
[30] 韓明漢,魏飛,金涌,等.氯化氫催化氧化生產氯氣的工藝方法及裝置:CN1417107.2003.
[31] 張鈞鈞.氯化氫催化氧化制氯氣技術進展[J].中國氯堿. 2013,5:6~10.
[32] 魏飛,陳智濤,韓明漢.一種氯化氫催化氧化生產氯氣的裝置及方法:CN101293637.2008.
[33] O.瓦森伯格,D.阿加爾,C.W.里克,等.氯的制備:CN1156121.1996.
[34] 喬旭,陳獻,戴勇,等.一種流化床與絕熱固定床串聯的HCl氧化反應工藝及系統: CN104030247.2014.
[35] 時鈞,汪家鼎,金國綜,等.化學工程手冊,第2版[M].北京:化學工業出版社, 1996. 25~69.
[36] 金涌,祝京旭,汪展文,等.流態化工程原理[M].北京:清華大學出版社, 2001.334.
[37] 惲松,騫偉中,魏飛.流化床與固定床耦合反應器中的顆粒磨損[J].過程工程學報. 2010.10(1):17~22.
[38] 陳斌,羅務習,孫鯤鵬,等. 一種采用微反應器進行氯化氫氧化制備氯氣的方法: CN102101650.2011.
[39] 陳斌,羅務習,張宏科,等.一種利用磁穩流化床進行氯化氫氧化制備氯氣的方法: CN103145099.2013.
[40] 孫策,馬斌全,繚暉,等.氯化氫催化氧化制氯氣的催化劑及其制備方法和應用:CN105289631.2015.
[41] 王農躍,瞿雄偉,李國華,趙全忠,邵建明,聞國強. 一種二(三氯甲基)苯和二(氯甲酰基)苯的制備方法: CN104447188.2013.
[42] 王農躍,瞿雄偉,李國華,趙全忠,邵建明,聞國強.一種三氯甲基取代苯的制備方:WO2015/035937.
[43] 俞志宏,王明亮.氯化氫綜合利用現狀及展望[J],化工時刊,2012,26(8):56~58.
(R-03)
可吸收納米復合人工骨材料研究獲進展
2016年8月,中國科學院長春應用化學研究所牽頭承擔的“可吸收納米復合人工骨材料與器件的產業化關鍵技術研究”項目順利通過由省科技廳組織的專家驗收。該項目是吉林省“雙十工程”重大科技攻關項目,專家組一致認為該項目在可吸收納米復合人工骨材料方面的研究達到了國內領先水平,并建議進一步加快產品的臨床應用和商業化進程,拓寬其應用領域。
該項目通過科研人員的不懈努力,圓滿完成了從可降解原材料合成到自主開發可吸收納米復合人工骨材料的研究任務,獲得了系列具有自主知識產權的產業化關鍵技術,可指導規模化生產。該人工骨材料具有完全人工合成、降解時間可調以及具有骨傳導和誘導作用等諸多特點,其物理化學性能和生物學性能等技術指標均達到任務合同要求。
該項目取得的突出進展體現在,從系列生物醫用高分子材料PLGA原料的合成和制備出發,實現了LA與GA比例可控,降解時間可調;完成了LA/GA單體的開環聚合和批量制備,PLGA的純度達到醫用級要求;實現了公斤級聚乳酸改性納米羥基磷灰石(g-HA)原料的合成和制備;聚乳酸接枝率(質量百分比)可控,純度達到醫用級要求;開發了多種骨支架的制備方法和工藝,制備出了系列不同孔結構、孔隙率和孔徑的人工骨支架,孔隙率、孔尺寸與降解速度均可根據骨愈合需要進行調整;完成了支架材料和產品的物理/化學性能評價,以及生物學檢測和動物實驗,獲得了人工骨材料的組分、結構、機械性能等重要參數;實現了骨愈合過程中材料的實時成像追蹤;制備了與幾丁質、膠原等材料具有特異性結合能力的活性生長因子蛋白;創造性地實現了高強度可注射骨支架的制備,可更好地滿足臨床骨科缺損的微創治療。
在該項目執行期間,長春應化所與吉林大學骨科成立了聯合共建的“骨科生物材料工程研究中心”,進一步為骨科材料基礎與臨床的合作研究和完善“產學研”開發體系提供了有力保障。
該項目獲得了一系列重要成果。其中,獲得人工骨支架新產品1個,新建《可吸收人工骨》產品企業標準1項;申請專利6項,授權專利5項,在Biomacromolecules 等學術刊物發表論文9篇;并獲得可吸收釘板等配套器件產品注冊證2個(國械注準20153461863和國械注準20153461864)。
摘編自“中國聚合物網”
Chlorine cleaning process for recovering hydrogen chloride from tail gas in preparation of aromatic polyamide fi ber
Chlorine cleaning process for recovering hydrogen chloride from tail gas in preparation of aromatic polyamide fi ber
Wang Nongyue
(Shanghai Fanglun New Material Technology Co., LTD., Shanghai200122, China)
This paper expounds the hydrogen chloride pollution situation, and more by-product hydrogen chloride with the development of organic chlorine products. In this paper, the existing treatment methods and characteristics of hydrogen chloride in the production of aramid fi ber are introduced. This paper mainly introduces the clean process of catalytic oxidation of hydrogen chloride to chlorine gas which has the most industrialized foreground. By comparing the process, the advantages and development prospects of hydrogen chloride oxidation process by Shanghai Fanglun are analyzed in this paper.
hydrogen chloride; catalytic oxidation; chlorine gas
TQ124.42
1009-797X(2016)18-0020-09
BDOI:10.13520/j.cnki.rpte.2016.18.005
王農躍(1958-),男,教授級高工,工學博士,管理學博士,榮獲多項省部級科技進步一等獎及多項國家發明專利,發表多篇論文及著作。
2016-08-02

