HPLC法測定雙乙酰左旋多巴甲酯布洛芬的含量及其脂水分配系數
許崇搖 蔣偉哲 黃興振


[摘要] 目的 建立雙乙酰左旋多巴甲酯布洛芬的含量測定方法以及測定其脂水分配系數(LogP)。 方法 采用HPLC法和搖瓶法(正辛醇/水體系),Synergi Fusion-RP-C18色譜柱(4.6 mm×250 mm,4 μm);流動相為水-甲醇(25∶75,V∶V);流速0.8 mL/min,檢測波長226 nm,柱溫40℃,進樣量為20 μL。 結果 雙乙酰左旋多巴甲酯布洛芬質量濃度在8.5~340 μg/mL范圍內與峰面積線性關系良好,r=0.9999,平均回收率為99.81%,RSD為0.36%( n = 6)。樣品平均含量為98.26%,其LogP約為1.4。 結論 該檢測方法準確、簡便,精密度高,可用于雙乙酰左旋多巴甲酯布洛芬酯的含量測定。
[關鍵詞] 高效液相色譜法;雙乙酰左旋多巴甲酯布洛芬酯;脂水分配系數;含量測定
[中圖分類號] R927.2 [文獻標識碼] A [文章編號] 1673-7210(2016)03(c)-0149-04
[Abstract] Objective To establish a method for determine the content and partition coefficient (LogP) of diacetyl L-dopa methylester ibuprofen. Methods Shaking-flask method (n-Octanol/water system) and HPLC method were used. The Synergi Fusion-RP C18 column (4.6 mm×250 mm, 4 μm) was used and the mobile phase was H2O-CH3OH (25∶75,V∶V), the flow rate was 0.8 mL/min. The detection wavelength was 226 nm. The column temperature was 40℃ and the injective volume was 20 μL. Results A good linear relationship was observed in the concentration range of 8.5-340 μg/mL, with the correlation coefficient of 0.9999. The average recovery rate was 99.81% and RSD was 0.36% (n=6). The average content of diacetyl L-dopa methylester ibuprofen was 98.26%, and the LogP was about 1.4. Conclusion The determination method was accurate and sensitive with high precision, which can be applicable for the content assay of diacetyl L-dopa methylester ibuprofen.
[Key words] HPLC method; Diacetyl L-dopa methylester ibuprofen; Partition coefficient; Content determination
帕金森病是一種腦內的多巴胺能神經元病變為特征的神經元退化性疾病[1-2],目前臨床藥物治療仍以左旋多巴(L-dopa)為主,但是L-dopa在治療過程中會引起較多的副作用和生物利用度低等問題[3-5]。近年來有研究發現,布洛芬每周服用2~3次,患帕金森病的高齡人發生率減少30%左右;雖然布洛芬減少患帕金森病發病率的機制尚不清楚,但是目前認為,這可能與布洛芬的抗炎作用有利于降低導致帕金森病的細胞死亡有關[6]。這一發現將有助于帕金森病新治療藥物的研發。雙乙酰左旋多巴甲酯布洛芬(diacetyl L-dopa methylester ibuprofen)為L-dopa與布洛芬拼合得到的一個潛在的治療帕金森病的酰胺化合物,其化學名為4-[(2S)-2-(2-(4-異丁苯基)丙酰胺基]-3-甲氧基-3-氧代丙基)-1,2-苯二乙酸酯[4-((2S)-2-(2-(4 -isobutylphenyl)propanamido)-3-methoxy-3-oxopropyl)-1,2-phenylene diacetate],化學結構式見圖1。為了對雙乙酰左旋多巴甲酯布洛芬作進一步的研究和開發,筆者建立了其含量測定方法,并用HPLC法檢測了其脂水分配系數(LogP),該法可用于其質量控制和檢測分析,現報道如下:
1 儀器與試劑
EL204梅特勒-托利電子天平[梅特勒-托利多儀器(上海)有限公司];LC20AVP高效液相色譜儀(日本島津公司);SHA-CA數顯水浴恒溫振蕩器(金壇市易晨儀器制造有限公司);甲醇(Fisher公司,色譜純,批號:111773);蒸餾水自制;其他試劑均為分析純;雙乙酰左旋多巴甲酯布洛芬樣品(批號分別為20120101, 20120102和20120103),雙乙酰左旋多巴甲酯布洛芬對照品(經純化精制,其純度為98.80%,百分歸一化法)由實驗室合成精制。
2 方法與結果
2.1 色譜條件
色譜柱為Synergi Fusion-RP80A C18柱(4.6 mm×250 mm,4 μm),流動相使用水-甲醇(25∶75,V∶V),流速為0.8 mL/min,檢測波長為226 nm,柱溫40℃,自動進樣器進樣,進樣量為20 μL。
2.2 溶液配制
2.2.1 樣品溶液配制 取雙乙酰左旋多巴甲酯布洛芬對照品適量,精密稱定,置100 mL容量瓶中,以流動相溶解,定容至刻度,搖勻,配制成濃度約為340 μg/mL對照品儲備液,備用。取雙乙酰左旋多巴甲酯布洛芬樣品適量,精密稱定,置100 mL容量瓶中,以流動相溶解,定容至刻度,搖勻,配制成濃度約為136 μg/mL的供試品溶液,備用。以流動相作為空白對照溶液。
2.2.2 緩沖溶液配制 pH值1.3緩沖液:取0.2 mol/mL KCl 25 mL和0.2 mol/L HCl 33.6 mL,混合再加蒸餾水稀釋至100 mL,即得。
pH值5.0緩沖液:取0.2 mol/mL的NaH2PO4溶液,用NaOH試液調pH值至5.0,即得。(NaOH試液:NaOH 4.3 g,加水溶解成100 mL,即得。)
pH值7.4緩沖液:取KH2PO4 1.36 g,加0.1 mol/mL NaOH溶液79 mL用蒸餾水稀釋至200 mL,即得。
2.3 方法學考察
2.3.1 系統適應性試驗 按“2.2.1”項下方法配制對照品和樣品溶液,分別進樣20 μL,按“2.1”項下色譜條件測定,結果顯示,供試品溶液(圖2B)色譜峰與雙乙酰左旋多巴甲酯布洛芬對照品溶液(圖2A)色譜峰保留時間相一致,空白對照溶液(圖2C)顯示無干擾,理論塔板數以雙乙酰左旋多巴甲酯布洛芬峰計不低于5000,見圖2。
2.3.2 線性關系考察 精密吸取上述對照品貯備溶液(340 μg/mL)10、8、4、2、1、0.5、0.25 mL,置于10 mL容量瓶,以流動相稀釋至刻度,搖勻,制得濃度分別為340、272、204、136、68、34、17、8.5 μg/mL的對照品溶液,進樣20 μL,記錄色譜峰面積,以雙乙酰左旋多巴甲酯布洛芬濃度為橫坐標,峰面積為縱坐標,繪制標準曲線。結果,標準曲線方程為Y= 29 172X + 32 001,r =0.9999。
2.3.3 精密度試驗 取濃度為136 μg/mL的對照品溶液按色譜條件連續進樣6次,每次進樣20 μL,以峰面積考察其日內精密度。試驗結果顯示,平均峰面積為4 034 815.3,RSD為0.39%(n = 6),表明儀器進樣精密度較好。
2.3.4 穩定性試驗 取濃度為136 μg/mL的對照品溶液每隔一定時間(0、2、4、8、12 h)進樣20 μL測定,每次測定2針,平均峰面積為4 034 504.5,RSD為0.59%(n = 5),試驗表明對照品溶液在12 h內保持穩定。
2.3.5 重復性試驗 取同一批供試品(批號:20120102),按供試品溶液的配制方法平行配制3份,按色譜條件方法測定結果,3份樣品測定平均值為98.20%,RSD為0.04%(n = 3),表明重復性良好。
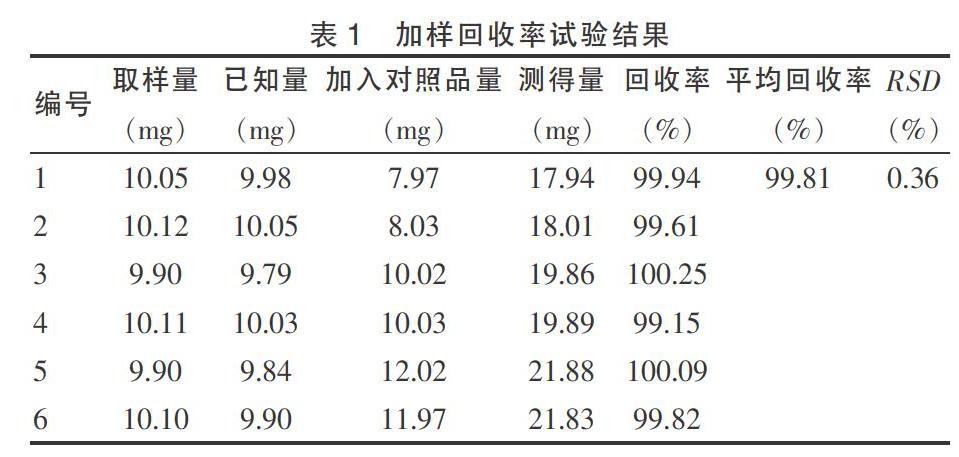
2.3.6加樣回收率試驗 取已知含量的雙乙酰左旋多巴甲酯布洛芬樣品約10 mg(批號:20120101)6份,精密稱定,置100 mL容量瓶中,每兩份中分別精密加入干燥至恒重的對照品約8、10、12 mg,以流動相溶解,定容至刻度,搖勻。按色譜條件方法測定,計算回收率[7-8]。結果,平均回收率為99.81%,RSD為0.36%(n = 6),表明加樣回收結果符合要求。結果見表1。
2.3.7 定量限及檢測限 在該色譜條件下,按信噪比(S/N)為3和10分別對檢測限和定量限進行測定。對照品溶液逐級稀釋后進樣,測定結果顯示,濃度為15.2 μg/mL進樣量為0.1 μL時,主峰信號約為噪音信號的3倍;進樣量為0.3 μL時,主峰信號約為噪音信號的10倍,即最低檢測限和定量限分別為1.52、4.56 ng。
2.3.8 脂水分配平衡時間考察 稱取雙乙酰左旋多巴甲酯布洛芬約5 mg,加正辛醇(水飽和)于250 mL容量瓶中溶解,定容。取20 mL含樣品的正辛醇(水飽和)溶液至錐形瓶,加入20 mL蒸餾水(正辛醇飽和),加塞密封,同樣處理5份,置25℃水浴恒溫振蕩器分別劇烈振搖0.25、0.5、1、1.5、2 h,轉入分液漏斗中靜置,分離出水相和有機相,以水相進樣20 μL,當含量不再增減時,即為平衡時間[9-11]。結果,振搖1 h時達到分配平衡。
3 結果
3.1 樣品含量測定
稱取3批樣品分別約為10 mg,精密稱定,置100 mL容量瓶,加流動相溶解并稀釋至刻度,搖勻,進樣20 μL,記錄色譜峰;另取對照品溶液,同法操作,以外標法峰面積計算。結果顯示,批號為20120101、 20120102和20120103樣品雙乙酰左旋多巴甲酯布洛芬的含量分別為98.40%、98.18%、98.20%,平均含量為98.26%。
3.2 LogP的測定
按“2.3”項下“脂水分配平衡時間考察”方法,準確量取20 mL含雙乙酰左旋多巴甲酯布洛芬的正辛醇(水飽和)溶液至錐形瓶,加20 mL蒸餾水、pH值7.4緩沖液、pH值5.0緩沖液和pH值1.3緩沖液(分別用正辛醇飽和),分別平行操作2份,加塞密封后振搖1 h(25℃),轉入分液漏斗中靜置,分離出水相和有機相,取有機層和水層溶液分別進樣,檢測分析樣品濃度,計算不同pH值溶液下的脂水分配系數,計算公式為
4 討論
雙乙酰左旋多巴甲酯布洛芬的甲醇溶液(80 μg/mL)在200~400 nm波長范圍內光譜掃描,有兩個最大吸收峰分別為210、226 nm,因此選取226 nm作為檢測波長;由于Synergi Fusion-RP 80A C18柱芯填充顆粒比較細(4 μm),柱溫在室溫時柱子壓力較高,柱溫在40℃條件下時柱壓較為理想,不影響結果的分析;流動相采用水-甲醇(25∶75,V∶V),流速為0.8 mL/min時出峰時間大約為11 min。在該分析條件下,雙乙酰左旋多巴甲酯布洛芬的檢測限和定量限分別為1.52、4.56 ng,3批樣品的平均含量為98.26%。
正辛醇-水為有機化合物測定脂水分配系數方法常用的溶液體系,有機化合物具有合適的LogP將有利于機體的吸收和轉運,發揮更好的療效[15]。筆者首先考察了雙乙酰左旋多巴甲酯布洛芬在正辛醇和水溶液中分配平衡時間,發現在該實驗條件下振搖60 min分配達到平衡。為了探討雙乙酰左旋多巴甲酯布洛芬在不同pH值緩沖溶液中的脂水分配情況[16-18],筆者還采用了蒸餾水、pH值7.4緩沖液、pH值5.0緩沖液和pH值1.3緩沖液作為水相,分別測定分析其LogP,發現其LogP分別為1.44、1.45、1.66和1.44(25℃),說明該化合物在不同pH值溶液中均具有較高的脂溶性[19-20]。其在不同pH值緩沖溶液中的LogP略有差別,可能與雙乙酰左旋多巴甲酯布洛芬在不同pH值條件下的穩定性情況不同有關。
本文建立了雙乙酰左旋多巴甲酯布洛芬的含量檢測方法,操作較為簡便、重復性好,可用于質量控制和分析檢測以及反應過程的動態監測。
[參考文獻]
[1] 安殿紅.美多巴聯合普拉克索治療帕金森病的臨床有效性及安全性[J].中國醫藥指南,2015,13(25):158.
[2] 秦皎嬌,張琦,丁斐.帕金森病的治療進展[J].南通大學學報:醫學版,2015,35(3):211-215.
[3] 蔣雨平.對左旋多巴長期治療帕金森病的評價[J].中國臨床神經科學,2014,22(1):19-21.
[4] Hagan JJ,Middlemiss DN,Sharpe PC,et al. Parkinson's disease: prospects for improved drug therapy [J]. Trends in Pharmacological Sciences,1997,18(5):156-163.
[5] Blandini F,Greenamyre JT. Protective and symptomatic strategies for therapy of Parkinson's disease [J]. Drugs of Today,1999,35(6):473-483.
[6] Gao X, Chen H, Schwarzschild MA,et al. use of ibuprofen and risk of parkinson disease [J]. Neurology,2011,76(10):854-869.
[7] 潘俏鳳.HPLC法測定鹽酸左旋多巴甲酯的含量研究[J].中國醫藥導報,2010,7(21):51-52.
[8] 鄭曉青,李浩.超高效液相色譜法測定復方止顫顆粒中二苯乙烯苷含量[J].安徽醫藥,2015,19(10):1885-1886.
[9] 于秀珍,何珺,錢一鑫,等.HPLC法測定大豆苷元的平衡溶解度和表觀油水分配系數[J].安徽農業科學,2009,37(10):4367-4368.
[10] 朱彧,劉夢源,劉培毅,等.γ2氨基丁酸脂溶性前體藥物合成及脂水分配系數測定[J].中國現代應用藥學雜志, 2008,25(4):275-278.
[11] 孫潔胤,周芝芳,劉放.苦參素油水分配系數及pH值對其的影響[J].浙江省醫學科學院學報,2006, 1:19-21.
[12] 鐘玲,臧志和,吳敏,等.蘆丁在不同介質中平衡溶解度的測定[J].時珍國醫國藥,2009,20(4):874-875.
[13] 王慶偉,梅其炳,劉雪英,等.染料木黃酮的物化常數測定[J].中國醫院藥學雜志,2003,23(12):729-730.
[14] 王弘,陳濟民,張清民.黃芩苷的物化常數測定[J].沈陽藥科大學學報,2000,17(2):105-106.
[15] 王艷玲,李婕,王任小.有機化合物脂水分配系數和溶解度的計算方法[J].物理化學學報,2010,26(7):1742-1754.
[16] Piera S,Antonio I,Laura SC,et al. New L-dopa codrugs as potential antiparkinson agents [J]. Arch Pharm Chem Life Sci,2008,341(7):412-417.
[17] 何翊,秦燕,范亞葦,等.槲皮素及其乙酸乙酯衍生物的平衡溶解度和油水分配系數的測定[J].食品科學,2015, 36(14):55-58.
[18] 涂瑤生,付建武,張建軍,等.姜黃素和胡椒堿溶解度和表觀油水分配系數的測定[J].按摩與康復醫學,2013, 4(12):114-117.
[19] 高旭,于悅,王亞靜,等.補骨脂酚平衡溶解度和表觀油水分配系數的測定[J].華西藥學雜志,2013,28(3):285-286.
[20] Jukka L,Juhani H,Tapio N,et al. Design and synthesis of a novel L-dopa-entacapone codrug [J]. J Med Chem,2002,45(6):1379-1382.
(收稿日期:2015-11-01 本文編輯:趙魯楓)

