四環素類金屬離子配合物應用研究進展
楊 旭,王建華
(重慶大學生物工程學院,重慶 400044)
?
四環素類金屬離子配合物應用研究進展
楊旭,王建華*
(重慶大學生物工程學院,重慶 400044)
四環素類抗生素是一類具有氫化駢四苯環的廣譜抗生素,由于這類抗生素帶有可配位活性基團和合適的空間構型,因而可與金屬離子配位形成穩定的配合物。研究表明四環素類金屬離子配合物與四環素具有著不同的生物、化學及物理性質。本文介紹了四環素類藥物與金屬離子的配位機制,綜述了其配位化學在分析檢測、藥物研發和環境評價等方面的應用,并對四環素金屬配合物研究發展方向進行了展望。
四環素,金屬配合物,應用
自20世紀40年代四環素類(Tetracyclines,TCs)抗生素被發現以來,它就作為高效的抑菌劑被廣泛地應用于畜牧生產活動。四環素類是由放線菌產生的廣譜抗生素,如金霉素、土霉素等天然四環素類抗生素以及多西環素、甘氨酰四環素等半合成四環素。這類抗生素能特異性地與細菌核糖體30S亞基的A位置結合,抑制肽鏈的增長和影響細菌蛋白質的合成,對革蘭氏陽性菌和陰性菌、衣原體、立克氏體等有著很好的抑制作用。
四環素類藥物具有四個六元環結構(見圖1),其中C2位酰胺基、C10~C12的共軛雙鍵系統、以及C4位的二甲氨基都屬于抑菌必需的活性基團,容易發生電離,具有3個電離平衡常數(Equilibrium constant,pKa)。因為有了這些含氧和含氮的官能團,金霉素可以在合適的溶劑和pH情況下,和金屬離子絡合形成1∶1、1∶2、2∶1的配合物。配合物作為自然界及機體中常見的形式,具有很重要的生物學意義,特別是在生命科學領域,從機體組織構成、生長發育到物質新陳代謝都有著至關重要的作用。而無機金屬離子作為核心與有機分子形成各式各樣的配合物,金屬離子、配體和配合物三者之間的平衡使它們相互作用會產生一定的生物學活性,如生物大分子藥物,本身具有的性質也因配位絡合物的產生而發生物理、化學性質改變,進而產生新的藥學活性和藥理影響。本文主要對四環素類藥物與金屬離子配位化學在檢測、生物活性、環境方面的研究成果進行綜述,為四環素藥物未來的發展提供一定的理論研究依據。
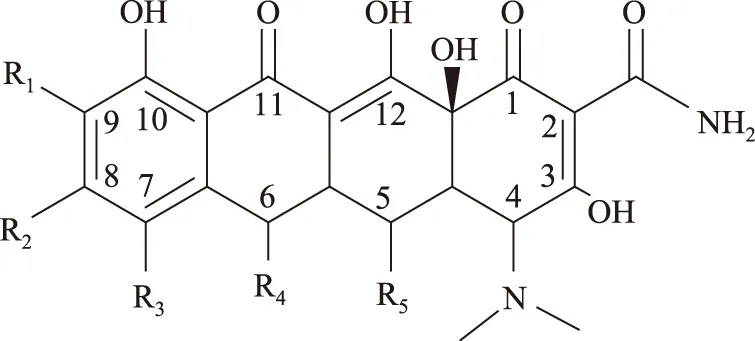
圖1 四環素類結構式Fig.1 Chemical Structure of Tetracyclines
1 四環素類藥物與金屬離子配位機制
四環素類帶有的C3-OH,C12-OH以及易質子化的二甲氨基基團,造成其存在質子化、中性兩性離子、陰離子和二陰離子4種離子化形式,電性隨pH增加從帶正電荷向負電荷過度,對金屬離子的親和性也逐步增強。Carlotti等人[1-2]研究發現,低pH時,金屬離子能取代氫連接到C3-O上;隨著pH增大,C3-O質子解離并帶負電荷,和金屬離子相互作用后導致C12-O位失去一個質子后形成1∶2的金屬離子配合物。即四環素A環C1-O,C3-O,C4-N以及BCD環的C10-O,C11-O,C12-O結合位點能與金屬離子形成1∶1,1∶2型配合物。而Bagheri等人[3]采用滴定法、分光光度法研究四環素配合物,確定Pd2+與四環素形成了2∶1型配合物(TC:Pd2+)。隨著計算化學的發展,Bruna[4]采用密度泛函理論(DFT)計算出四環素類與金屬離子在低pH或高pH環境下,傾向于在BC環的O1-O12-O11形成配位,而中性介質使其傾向于在O3-O2-O1形成一種延伸式的構象配位,限制分子構象旋轉,形成平面剛性結構,從而使分子更穩定。綜上所述,四環素金屬配合物的結構得到了確認。
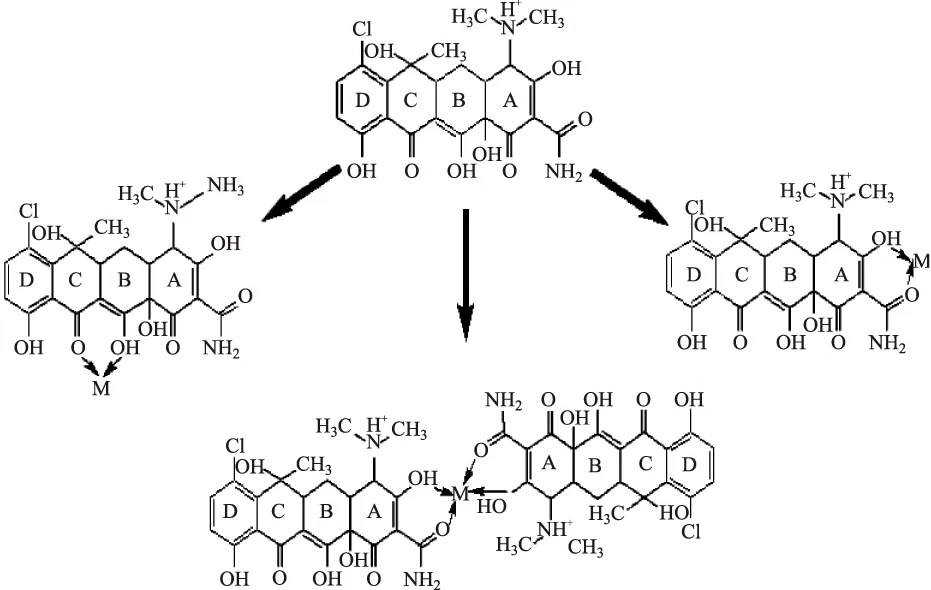
圖2 金霉素與金屬離子配位示意圖[2]Fig.2 The positions of chlortetracycline complexation with metal ions[2]
2 檢測應用
四環素本身屬于弱熒光物質,但是和金屬離子絡合后,熒光強度會增大,紫外吸收改變,激發態壽命延長。張紅漫等人[5]研究發現,鈣離子易與四環素(TC)形成氧橋型雜多核配合物,使吸收的能量通過鈣離子傳遞給TC,導致TC的特征熒光發射增強,以激發波長389 nm、發射波長504 nm測量TC熒光強度。當體系中鈣離子濃度達到3.0×10-5mol/L時,體系熒光強度穩定且達到最大值。Khan等人[6]用Na+研究四環素、金屬離子對DNA熒光強度的影響,發現0.05 mol/L的Na+可以使熒光淬滅減少27%,而0.2 mol/L的Na+可以使熒光淬滅減少42%,進一步驗證了金屬離子對四環素熒光的增益性,而四環素與金屬離子這方面的特性主要應用于以下方面。
2.1小分子檢測
四環素金屬熒光體系可以應用于銪、釤等鑭系元素的檢測,且檢測限低。李紅霞等人[7]利用四環素與金屬離子形成多核配合物的特性,篩選了Ca2+增敏TCs體系測定釤、銪的最佳測定條件,與普通的熒光測定法相比,Sm3+和Eu3+的檢測限分別由38.2、0.09 μg/L下降至7.9、0.015 μg/L,鑭系元素熒光強度增加最高可達30倍。此外,這種金屬元素配合物的強熒光性還可以用于四環素的定量檢測,張紅漫等人[5]提出了一種Ca2+和陽離子表面活性劑溴化十六烷基三甲銨(CTMAB)、四環素的三元配合物增敏體系來測定TC含量,Ca2+能使四環素熒光強度急劇增加,在8.0×10-9~1.0×10-5mol/L范圍內有良好線性關系,相關系數為0.988,檢出限2.65 μg/L,這與傳統的高效液相色譜法[8]四環素檢測限50~100 μg/L相比,檢測線低、靈敏度高、方便快捷,具有一定的優勢。
2.2生物大分子檢測
四環素金屬離子配合物具有一定的脂溶性。Teixeira等人[9]發現四環素和銪配合物在低密度脂蛋白(LDL)存在時,光強度和LDL濃度成正相關,制備出四環素-銪探針準確、靈敏的應用于檢測低密度脂蛋白,其中四環素-銪探針的檢測范圍是0~3 mg/mL,最低檢測限為0.23 mg/mL。而金霉素-銪探針(CT-Eu)檢測LDL的最低檢測限為0.49 mg/mL,且可為動態檢測低密度脂蛋白提供更寬的檢測范圍。此外,四環素-銪熒光探針還用來測定卵磷脂、三磷酸腺苷二鈉(ATP)等生物大分子,取得了良好的效果[10],其中ATP的測量線性范圍是3.0×10-7~4.5×10-6mol/L,檢出限為4.68×10-8mol/L;卵磷脂測量線性范圍為4.0×10-7~1.4×10-5mol/L,檢出限為3.9×10-8mol/L。
鹽酸四環素與鋅、釤的配合可以形成二元配合物增強其熒光強度,并能和DNA結合,利用其可以增強熒光強度的特性,建立測定DNA的方法。文志剛等人[11]提出Tc-Zn2+可以在1.0×10-6~5.0×10-5mol/L線性范圍內對小牛胸腺DNA(CT-DNA以及Calf Thymus DNA)進行檢測,相關系數為0.988,檢出限5.0×10-7mol/L,所以該方法可以用于痕量DNA的檢測。
3 生物研究
四環素類藥物在血液內傳遞主要是與Ca2+和Mg2+絡合的形式在體內運[2,12],以金屬配合物的形式透過生物體內膜系統,通過不同的絡合形式調節血液中藥物生物利用度,其作為離子載體有很重要的生物學意義。
3.1提高與RNA親和性
金屬離子的存在,提高了四環素類藥物對RNA和RNA的親和性,而抗生素本身對RNA或DNA的親和力是很弱的,比如抗生素和Cu2+絡合,這就增強了抗生素對核酶的親和力[12-13]。實驗證明,隨著Cu2+濃度從0~10 μmol/L,四環素-DNA-Cu2+(復合體的絡合常數也由1.16×107上升至4.76×107;但是銅配合物會導致DNA的N7和N3位的腺嘌呤和鳥嘌呤堿基烷化,以溝槽式形式與DNA相互作用[11],引起DNA二級結構變化[14]。也就是說,配合物可成為一種潛在的RNA或DNA靶向藥物。
3.2增加抑菌活性
Guerra等人[15]以1∶1的摩爾比使K2PtCl4與四環素類藥物(四環素、多西環素、金霉素)結合,最后推測Pt2+與A環上的O-3以及酰胺氧原子可以結合形成1∶1絡合物,在此基礎上通過抑菌實驗證實金屬絡合物對大腸埃希氏菌(ATCC25922)、大腸桿菌HB101以及大腸桿菌HB101(pBR322)等三種大腸桿菌均具有很好的抑制作用。實驗表明,對ATCC25922菌種的最小抑菌濃度值(MIC)為四環素4.16 μmol/L、配合物2.08 μmol/L;多西環素8.32 μmol/L、配合物4.16 μmol/L。對HB101/pBR322菌種四環素的MIC值為266.20 μmol/L、配合物16.60 μmol/L;多西環素為66.50 μmol/L、配合物為33.30 μmol/L,由此數據可以看出,金屬配合物確實提高了抑菌效果。且各種金屬對配位后抑菌能力的提升也是不同的,Guru等人[16]將鎳、鋅和四環素結合,采用濾紙片擴散法考查配合物對金黃色葡萄球菌、傷寒沙門氏菌、大腸桿菌、黃曲霉等的抑菌能力,發現鋅配合物都取得比較滿意的效果,體外抑菌實驗表明,0.01 mol/L鋅、鎳配合物的金黃色葡萄球菌的抑菌圈分別為9 mm和18 mm,鋅配合物的抗生活性大約是鎳配合物的2倍。這些研究表明金屬離子和抗生素類藥物結合不但可改變抗生素的性質,而且在細胞內可能同樣具有生物活性。
3.3緩控釋藥物
Jung等人[17]發現由微晶纖維素化學修飾而成的纖維素黃酸(Cellulose xanthate,CX),只有與金屬離子絡合后才具有攜帶四環素類藥物的能力,并達到緩釋目的。每克纖維素黃酸分別可以吸附0.36 mol Cu2+和0.26 mol Zn2+而制得CX-Cu2+和CX-Zn2+,該兩種配合體單位載藥量分別37.1 mg和21.6 mg,釋放過程高達7~22 d,且Cu2+的配合物緩釋效果要優于Zn2+。而未配位前的四環素在體內具有吸收快,代謝也快的特點,所以金屬離子與四環素類配位可以達到緩控釋的目的。
3.4減弱耐藥性
由于四環素類藥物大劑量的使用,造成了耐藥菌的產生。四環素阻遏蛋白TetR控制一個完整膜蛋白TetA的基因轉錄過程[18]。當四環素通過被動擴散進入細胞后,與Mg2+形成四環素鎂配合物,該復合物可以與TetR阻遏蛋白結合并改變其構象,使TerR阻遏蛋白從TetO操縱序列蛋白上解離下來,并開始轉錄TetA和TetR基因,產生TetA蛋白和TetR阻遏蛋白,最后細菌細胞膜上的TetA蛋白開始將四環素金屬離子復合物泵出細胞外,同時泵入氫離子,這樣四環素就無法發揮功能。但最新的研究表明[19],四環素與Mg2+結合,并不是四環素阻遏物發生變構效應的前提條件,所以耐藥性是否與四環素金屬配合物有關還有待驗證。不過四環素類和金屬離子配合會減少細菌對四環素類配體的吸收,限制四環素類穿過細菌細胞膜從而誘導激活耐藥基因,雖然可能會降低抑菌效果,但這個過程也能調節細菌生存環境,減少耐藥細菌的產生和富集[20]。
3.5抗腫瘤
基質金屬蛋白酶(Matrix metalloproteinase,MMPs)通過降解胞外基質蛋白,從而促進腫瘤細胞的侵襲和轉移,加速腫瘤生長,這種蛋白酶一般需要Ca2+、Zn2+作為輔助因子才具有活性;而四環素類藥物可以和參與酶活化所必須的金屬陽離子螯合,改變構象造成酶失活和碎片化,抑制金屬蛋白酶(MMPs)的產生。這種特性可以應用于調節MMPs的活性和表達,影響腫瘤細胞的增殖和凋亡行為,臨床上可以作為潛在的抗癌藥物[21]。特別是去除C4位基團可以增加四環素類藥物對非抗生目標的趨向性[22],而不會引起耐藥等副作用,即通過一定的化學性修飾能增加其對腫瘤細胞的親和性。王茜等人[23]利用MTT法、PCR測得四環素基因表達調控系統確實能夠調控HSV tk基因在HeLa細胞中的內表達以及殺傷腫瘤功能,在轉染強力霉素48 h后,基因表達水平達到最大值,對GCV殺傷細胞敏感性增強。而Priscila等人[24]制備了銅、四環素(多西環素)和鄰菲羅啉的三元配合物,通過Cu2+連接兩個配體,研究表明四環素、多西環素配合物抑制K562細胞的半數抑制濃度(IC50)分別為1.93、2.59 μmol/L,均強于配體,且抑制活性與細胞內的銅離子濃度相關,進一步證明了配合物在抗腫瘤方面的巨大潛力。
4 環境研究
四環素類抗生素由于具有價格低、抗菌譜廣的特點,廣泛應用于畜牧行業。雖然具有相對較短的半衰期,但由于連續引入到生態鏈中,作為一種藥物殘留在土壤中或是河流、地下水流中,成為一種間接污染物,對大自然有很大的影響。而金屬元素在整個生態系統中無處不在,鑒于四環素與金屬陽離子特殊的親和性,在環境中兩者的結合使得四環素類抗生素的化學物理性質都發生了改變,所以從環境生物學和化學的角度綜合評價四環素類抗生素與金屬離子共存對環境的影響顯得尤為重要。毒性分析表明[25-26],四環素類抗生素和重金屬絡合可能對生物體有很大的毒性,考慮到四環素的金屬絡合物相比較于四環素單體半衰期延長,強穩定性,難降解性以及重金屬、輕金屬與四環素絡合效果的差異,環境方面的研究主要集中在兩個方面:
4.1水環境
在水性環境中,四環素類(TCs)作為電子的提供者,和金屬離子配合時,電子從金屬躍遷到配合物,會造成TCs一定程度的氧化降解。Chen等人[26]以金霉素為研究對象,考察了pH6.0~pH9.0不同金屬離子和金霉素的相互作用,實驗表明pH升到中性的時Fe3+顯著增強了CTC的光降解,光降解量子產率從3.3×10-4上升到8.5×10-3,質譜分析顯示該過程主要是CTC的C7位脫氯、C4位去甲基、分子內脫水等一系列反應,而這類四環素的降解產物是具有毒性的[27],對水生物的生長發育會有很大影響。Lu等人[28]就考察了水溶液中四環素與Cu2+對鳳眼蓮生長造成的影響,發現單體TCs使鳳眼蓮的根數量減少21%,低含量的銅與四環素形成配合物會對生物量產生負效應,15 mg/L的Cu2+就會導致鳳眼蓮的根數量下降39%。Pulicharla等人[29]也研究了金霉素與金屬離子配位前后對革蘭氏細菌的毒性,結果表明金霉素與金屬離子配合后對革蘭氏陽性菌的毒性變大,而對革蘭氏陰性菌卻沒有變化,這種特性可能會打破水環境中的細菌生態平衡,也間接說明水環境下四環素和金屬離子配位確實會對水生態環境產生一定的影響。
但是金屬離子與四環素絡合,卻可以應用于含抗生素污水處理,趙斌等人[30]通過紫外分光度法,研究水環境下鎘(Cd2+)和鉛(Pb2+)對四環素超聲降解的影響,發現在低摩爾比時,金屬離子可以加快四環素的超聲降解,1.0×10-5mol/L四環素溶液24 h降解率為7.54%,而加入金屬離子Cd2+和Pb2+降解率升高至20.82%和18.75%。而作為普遍處理污水的活性法,是水處理去除四環素的主要方式,宋現財[31]通過運用紅外(FTIR)和X射線光電子能譜分析(xps)研究擬合四環素的吸附過程,發現Cu2+通過離子交換和表面絡合機制(包括金屬架橋和cation-π作用)明顯促進污泥中四環素的吸附過程,污泥吸附后不會產生毒性[29],這一發現可以應用于活性污泥處理法完成污水中抗生素的處理,這些實驗說明配合物在環保方面的應用具有一定的參考價值。
4.2土壤環境
四環素類抗生素主要用作獸用抗生素,由于生物體對抗生素的低吸收能力,使其以排泄物的形式大量轉移至土壤環境中,而土壤中大量金屬會以陽離子的形式存在,因此在土壤環境評價方面,四環素與金屬離子的共存影響對改善土壤環境有一定的指導意義。
Zhao等人[32]采用電位滴定法和光譜法,發現Cd2+、Cu2+和Pb2+三種金屬顯著增強了土壤對四環素的吸附,吸附強度Cu2+>Pb2+>Cd2+,與四環素和金屬離子的配位能力成正相關。此外,吸附能力還受土壤pH的影響,一般來說金屬離子在酸性土壤更容易增強四環素的土壤吸附力,pH升高,吸附能力下降,在pH>7的土壤中四環素就會傾向于以游離的形式在土壤中轉移[32-33]。
Duan等人[34]研究了納米金屬與四環素結合對土壤的影響。結果表明新型納米材料納米氧化鎳(NiO)會吸附四環素,這種親和性會因Cu2+在納米NiO表面和四環素分子之間形成鍵橋而加強,分配系數由104.2L/kg增大至105.5L/kg,增強了土壤中的吸附。但是Xing等人[35]在埃洛石納米管(HNTs)中摻雜金屬離子(Zn2+,Bi3+,Ni2+等),促使在光子能量下,帶電子活躍發生躍遷時生成的導帶電子(e-)和價帶空穴(h+)更好的分離,最終產生羥基自由基(·OH)和其它活性基團,有效降解土壤中的四環素,提高催化劑降解四環素的效率,減少土壤環境損害。這一研究表明四環素金屬離子配合物具有特殊的優點,可以用于環境處理。
5 結論和展望
藥物與金屬離子配位一直是生物、化學研究領域的熱點,而四環素類抗生素作為治療和促生長類生物藥,其與金屬離子之間的相互作用一直是抗生素領域關注的焦點問題,主要集中在分子檢測、生物活性以及環境等方面的研究。金屬配位后熒光、紫外特征吸收的特性,使其可應于分子檢測,提高檢測靈敏度,豐富檢測方法。構象改變后的金屬配合物,生物性質也區別于原配體,抑菌活性、非抗菌活性(即RNA靶向性)、耐藥機制也是近年來生物活性方面的主要研究內容。而作為食品添加劑,四環素類抗生素對環境的影響是亟待解決的難點,特別是納入金屬離子配位后的研究,是最具實用價值的科研思路。
隨著食品科技的發展,今后對配合物所開展的生物研究,還應考查其能否為生物體引入不同金屬離子的藥學特性,以及配位后的穩定性、毒理性等,便于進一步對其生物可靠性進行評估。此外,在非抗生活性方面,四環素金屬配合物與RNA、DNA的特異親和性是靶向藥物、抗腫瘤藥物方向值得深入研究的課題。而在環境方面,作為近幾年四環素金屬配位研究的重點,科學的研究可以為治理環境中的抗生素提供最具價值的理論依據,也是未來作為藥物、食品添加劑等整體生物、生態評價的衡量指標。隨著配位化學研究的不斷深入,四環素類藥物的金屬配位研究必將在生物、食品方面具有更廣闊的應用前景,也會在解決藥物對環境影響方面發揮更大的潛力。
[1]Carlotti B,Cesaretti A,Elisei F. Complexes of tetracyclines with divalent metal cations investigated by stationary and femtosecond-pulsed techniquesElectronic supplementary information(ESI)available[J]. 2011,14(2):823-834.
[2]Puicharla R,Mohapatra D P,Brar S K,et al. A persistent antibiotic partitioning and co-relation with metals in wastewater treatment plant-Chlortetracycline[J]. Journal of Environmental Chemical Engineering,2014,2(3):1596-1603.
[3]Bagheri A. Thermodynamic Studies of Metal Complexes of Tetracycline and its Application in Drug Analysis[J]. Pharmaceutical Chemistry Journal,2015,48(11):765-769.
[4]Marcial B L,Costa L A S,De Almeida W B,et al. Interaction of chemically modified tetracyclines with catalytic Zn(II)ion in matrix metalloproteinase:evidence for metal coordination sites[J]. Theoretical Chemistry Accounts,2011,128(3):377-388.
[5]張紅漫,顧銘燕,黃金戀,等. 四環素-Ca2+-CTMAB三元配合物體系熒光光譜的研究與應用[J]. 分析實驗室,2009,28(7):22-25.
[6]Khan M A,Musarrat J. Interactions of tetracycline and its derivatives with DNAinvitroin presence of metal ions[J]. International Journal of Biological Macromolecules,2003,33(1-3):49-56.
[7]李紅霞,張俊國,黃漢國. 鈣對釤、銪-四環素類體系熒光法測定釤和銪的增敏作用及其機理探討[J]. 分析化學,1996,24(7):844-847.
[8]王敏,馬玉龍,馬琳,等. 高效液相色譜法同時檢測藥渣中四環素及其衍生物[J]. 湖北農業科學,2014,53(6):1411-1414.
[9]Teixeira L d S,Grasso A N,Monteiro A M,et al. Enhancement on the Europium emission band of Europium chlortetracycline complex in the presence of LDL[J]. Analytical Biochemistry,2010,400(1):19-24.
[10]宋斯貞. 四環素-銪與卵磷脂的相互作用及卵磷脂的測定[J]. 分析實驗室,2008,27(5):109-111.
[11]文志剛,鐘才寧,柏任流. 鹽酸四環素-Zn(II)配合物與DNA的相互作用研究[J]. 分析實驗室,2009,28(5):101-104.
[12]Wrzesinski J,Brzezowska M,Szczepanik W,et al. Inhibition of the catalytic activity of trans-acting antigenomic δ ribozyme by selected antibiotics and their Cu2+complexes[J]. Biochemical and Biophysical Research Communications,2006,349(4):1394-1400.
[13]Chopra I,Roberts M. Tetracycline Antibiotics:Mode of Action,Applications,Molecular Biology,and Epidemiology of Bacterial Resistance[J]. Microbiology and Molecular Biology Reviews,2001,65(2):232-260.
[14]Khan M A,Mustafa J,Musarrat J. Mechanism of DNA strand breakage induced by photosensitized tetracycline-Cu(II)complex[J]. Mutation Research-Fundamental and Molecular Mechanisms of Mutagenesis,2003,525(1-2):109-119.
[15]Guerra W,de Andrade Azevedo E,de Souza Monteiro A R,et al. Synthesis,characterization,and antibacterial activity of three palladium(II)complexes of tetracyclines[J]. Journal of Inorganic Biochemistry,2005,99(12):2348-2354.
[16]Guru P. Microbial Studies on some Coordination Compound of Metals with Tetracycline[J]. International Journal of ChemTech Research,2009,1(2):291-297.
[17]Jung Y,Kim Y M. Evaluation of Cellulose Xanthate-Metal-Tetracycline Complexes as a Polymeric Antibacterial Agent with Prolonged Antibacterial Activity[J]. Drug Delivery,2008,15(1):31-35.
[18]Palm G J,Lederer T,Orth P,et al. Specific binding of divalent metal ions to tetracycline and to the Tet repressor/tetracycline complex[J]. JBIC Journal of Biological Inorganic Chemistry,2008,13(7):1097-1110.
[19]Werten S,Dalm D,Palm G J,et al. Tetracycline Repressor Allostery Does Not Depend on Divalent Metal Recognition[J]. Biochemistry,2014,53(50):7990-7998.
[20]Zhang Y,Boyd S A,Teppen B J,et al. Role of Tetracycline Speciation in the Bioavailability toEscherichia colifor Uptake and Expression of Antibiotic Resistance[J]. Environmental Science & Technology,2014,48(9):4893-4900.
[21]Gu Y,Walker C,Ryan M E,et al. Non-antibacterial tetracycline formulations:clinical applications in dentistry and medicine[J]. Journal of Oral Microbiology,2012,4(0):1-14.
[22]Nelson M L. Chemical and biological dynamics of tetracyclines[J]. Advances in Dental Research,1998,12(2):5-11.
[23]王茜,杜珍武,馬青山,等. 四環素調控 HSV-tk 基因在 HeLa 細胞內表達及抗腫瘤作用[J]. 中國實驗診斷學,2014,9):1396-1398.
[24]Silva P P,Guerra W,Silveira J N,et al. Two New Ternary Complexes of Copper(II)with Tetracycline or Doxycycline and 1,10-Phenanthroline and Their Potential as Antitumoral:Cytotoxicity and DNA Cleavage[J]. Inorganic Chemistry,2011,50(14):6414-6424.
[25]Zhang Y,Cai X,Lang X,et al. Insights into aquatic toxicities of the antibiotics oxytetracycline and ciprofloxacin in the presence of metal:Complexation versus mixture[J]. Environmental Pollution,2012,166:48-56.
[26]Chen Y,Li H,Wang Z,et al. Photolysis of Chlortetracycline in aqueous solution:Kinetics,toxicity and products[J]. Journal of Environmental Sciences,2012,24(2):254-260.
[27]Wammer K H,Slattery M T,Stemig A M,et al. Tetracycline photolysis in natural waters:Loss of antibacterial activity[J]. Chemosphere,2011,85(9):1505-1510.
[28]Lu X,Gao Y,Luo J,et al. Interaction of veterinary antibiotic tetracyclines and copper on their fates in water and water hyacinth(Eichhornia crassipes)[J]. Journal of Hazardous Materials,2014,280:389-398.
[29]Pulicharla R,Das R K,Brar S K,et al. Toxicity of chlortetracycline and its metal complexes to model microorganisms in wastewater sludge[J]. Science of The Total Environment,2015,532:669-675.
[30]趙斌,王風賀,包健,等. Cd2+和Pb2+對四環素超聲降解性能的影響[J]. 環境工程學報,2015,9(4):1599-1605.
[31]宋現財. 四環素類抗生素在活性污泥上的吸附規律及其機理研究[D].天津:南開大學,2014.
[32]Zhao Y,Tan Y,Guo Y,et al. Interactions of tetracycline with Cd(II),Cu(II)and Pb(II)and their cosorption behavior in soils[J]. Environmental Pollution,2013,180(0):206-213.
[33]Zhao Y,Gu X,Gao S,et al. Adsorption of tetracycline(TC)onto montmorillonite:Cations and humic acid effects[J]. Geoderma,2012,183-184(0):12-18.
[34]Duan L,Li L,Xu Z,et al. Adsorption of tetracycline to nano-NiO:the effect of co-existing Cu(ii)ions and environmental implications[J]. Environmental Science:Processes & Impacts,2014,16(6):1462-1468.
[35]Xing W,Ni L,Liu X,et al. Effect of metal ion(Zn2+,Bi3+,Cr3+,and Ni2+)-doped CdS/halloysite nanotubes(HNTs)photocatalyst for the degradation of tetracycline under visible light[J]. Desalination and Water Treatment,2013,53(3):794-805.
Research of current situations and development of the complexes of Tetracyclines with metal ions
YANG Xu,WANG Jian-hua*
(Bioengineering college of Chongqing University,Chongqing 400044,China)
Tetracyclines is a kind of broad-spectrum antibiotics with four hydrocarbon rings derivation,which have complexation group and appropriate spatial configuration,could chelate with various metal ions to form the stable complexes,and the current study showes that the complexes have different bioactivity,chemical and physical property compared with Tetracyclines. The mechanism of the complexes Tetracyclines with metal ions,and the application and advances on different type of Tetracyclines metal-ion complex for chemical analytical detection,pharmaceutical discovery and environmental assessment were overviewed in this paper. And the development tendency of this complexes and its prospect were also anaylsed.
Tetracyclines;metal complexes;application
2015-11-05
楊旭(1990-),男,碩士研究生,研究方向:藥物合成及制劑工程,E-mail:20131902095@cqu.edu.cn。
王建華(1962-),男,博士,教授,主要從事藥物合成與制劑工程方面的研究,E-mail:wjh@cqu.edu.cn。
四川省農業科技成果轉化資金項目(14NZ0027);重慶市應用開發計劃項目(cstc2013yykfB10013);重慶市自然科學基金重點項目(cstc2013jjB0011)。
TS201.1
A
1002-0306(2016)11-0362-05
10.13386/j.issn1002-0306.2016.11.066

