活性氧的生成與健康和疾病關(guān)系研究進(jìn)展
李興太,張春英,仲偉利,高明波(.大連民族大學(xué)生命科學(xué)學(xué)院,遼寧 大連 6600;.黑龍江大興安嶺地區(qū)農(nóng)業(yè)林業(yè)科學(xué)研究院,黑龍江 加格達(dá)奇 65000)
?
活性氧的生成與健康和疾病關(guān)系研究進(jìn)展
李興太1,張春英2,仲偉利2,高明波1
(1.大連民族大學(xué)生命科學(xué)學(xué)院,遼寧 大連 116600;2.黑龍江大興安嶺地區(qū)農(nóng)業(yè)林業(yè)科學(xué)研究院,黑龍江 加格達(dá)奇 165000)
摘 要:從歷史上看,活性氧(reactive oxygen species,ROS)被認(rèn)為只引起細(xì)胞損傷及生理功能障礙,ROS及其氧化損傷與多種疾病,包括神經(jīng)退行性疾病、糖尿病、癌癥和過(guò)早衰老相關(guān)。然而,近年來(lái),越來(lái)越多的證據(jù)顯示,ROS對(duì)健康至關(guān)重要。在生理?xiàng)l件下,低水平ROS的生成被認(rèn)為是信號(hào)分子。另一方面,ROS的過(guò)度生成,與ROS緩沖系統(tǒng)的功能障礙相關(guān),會(huì)導(dǎo)致慢性疾病的發(fā)展。因此,ROS的慢性釋放參與許多疾病的發(fā)病。而且,ROS生成過(guò)量誘導(dǎo)生物分子的氧化損傷,進(jìn)而導(dǎo)致衰老、癌癥和許多其他疾病。ROS已經(jīng)參與100多種疾病的發(fā)生,包括威脅人類健康的重大疾病癌癥、心血管疾病、糖尿病、神經(jīng)退行性疾病(如帕金森病和阿爾茨海默病)、獲得性免疫缺陷綜合征、中風(fēng)和衰老的發(fā)生。本文綜述了氧的出現(xiàn)與需氧真核生物的進(jìn)化、ROS的種類、ROS的生理病理多效性、機(jī)體內(nèi)主要的ROS、ROS的生成與反應(yīng)、ROS與線粒體氧化磷酸化、細(xì)胞凋亡、免疫防御和炎癥、腫瘤等方面的最新進(jìn)展,鑒于ATP和ROS對(duì)生命的重要性,提出,調(diào)控線粒體氧化磷酸化實(shí)現(xiàn)ATP與ROS生成的平衡將是健康的關(guān)鍵。
關(guān)鍵詞:活性氧;線粒體;信號(hào)傳導(dǎo);氧化還原平衡;健康
引文格式:
李興太, 張春英, 仲偉利, 等.活性氧的生成與健康和疾病關(guān)系研究進(jìn)展[J].食品科學(xué), 2016, 37(13): 257-270.
LI Xingtai, ZHANG Chunying, ZHONG Weili, et al.Advances in generation of reactive oxygen species associated with health and diseases[J].Food Science, 2016, 37(13): 257-270.(in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201613046. http://www.spkx.net.cn
近年來(lái),廣泛的研究顯示,體內(nèi)產(chǎn)生的活性氧(reactive oxygen species,ROS),在不同的細(xì)胞信號(hào)傳導(dǎo)通路中發(fā)揮重要作用。與慢性疾病(如癌癥)有關(guān)的絕大多數(shù)危險(xiǎn)因素,如應(yīng)激、煙草、環(huán)境污染物、輻射、病毒感染、膳食和細(xì)菌感染,均通過(guò)ROS的產(chǎn)生與細(xì)胞相互作用。ROS又可激活各種轉(zhuǎn)錄因子,例如,B細(xì)胞的核因子κ-輕鏈增強(qiáng)子(nuclear factor-kappa B,NF-κB)、活化蛋白-1、缺氧誘導(dǎo)因子-1α及信號(hào)轉(zhuǎn)導(dǎo)子與轉(zhuǎn)錄激活子3(signal transducer and activator of transcription 3,STAT3),導(dǎo)致調(diào)控炎癥、細(xì)胞轉(zhuǎn)化、腫瘤細(xì)胞存活、腫瘤細(xì)胞增殖與侵襲、血管生成和轉(zhuǎn)移的蛋白的表達(dá)。矛盾的是,ROS還控制各種腫瘤抑制基因(p53、Rb和PTEN基因)的表達(dá)。類似地,γ輻射和各種化學(xué)治療劑用于治療癌癥,是通過(guò)ROS的產(chǎn)生介導(dǎo)其效應(yīng)。有趣的是,ROS也參與源自水果、蔬菜、香料、和傳統(tǒng)醫(yī)學(xué)使用的其他天然產(chǎn)物的營(yíng)養(yǎng)保健品的化學(xué)預(yù)防和抗腫瘤作用[1-4]。ROS是細(xì)胞信號(hào)傳導(dǎo)途徑的組成部分,并已被證明能調(diào)節(jié)細(xì)胞轉(zhuǎn)化、存活、增殖、侵襲、血管生成和轉(zhuǎn)移。近年發(fā)現(xiàn),ROS的形成參與了食品的氧化變質(zhì),以及100多種人類疾病[5],如嚴(yán)重威脅人類健康的重大疾病心血管疾病(高血壓、動(dòng)脈粥樣硬化等)[6-8]、糖尿病[9]、慢性炎癥、神經(jīng)退行性疾病和癌癥[10]的發(fā)病機(jī)制及免疫[11]和衰老過(guò)程[12]。
氧化應(yīng)激被定義為ROS的產(chǎn)生與抗氧化防御之間的失衡。由于助氧化-抗氧化反應(yīng)平衡狀態(tài)的破壞,ROS過(guò)量引起氧化應(yīng)激,促進(jìn)活細(xì)胞中脂質(zhì)、蛋白質(zhì)、DNA和RNA的氧化損傷,抑制細(xì)胞的正常功能[13-14]。ROS生成與消除(由抗氧化酶和抗氧化劑)之間保持平衡(氧化還原平衡)對(duì)健康具有重要意義[15]。這意味著,過(guò)量的ROS造成機(jī)體損傷。然而,完全消除ROS會(huì)抑制機(jī)體適應(yīng)性應(yīng)答外部應(yīng)激因素反應(yīng)的能力[3]。在這個(gè)復(fù)雜的系統(tǒng)中,近年出現(xiàn)了一個(gè)新概念,ROS對(duì)能量平衡起關(guān)鍵作用。作為神經(jīng)信號(hào)的ROS途徑的損傷導(dǎo)致自主神經(jīng)系統(tǒng)和神經(jīng)內(nèi)分泌功能的改變,導(dǎo)致代謝性疾病,如肥胖和2型糖尿病[16]。ROS相關(guān)疾病可以是由于缺乏ROS(如慢性肉芽腫病,某些自身免疫性疾病)或ROS過(guò)剩(如心血管疾病和神經(jīng)退行性疾病)引起[17]。事實(shí)上,雖然長(zhǎng)時(shí)間暴露于高濃度ROS可能會(huì)導(dǎo)致蛋白質(zhì)、脂質(zhì)、核酸的非特異性損傷,低到中濃度ROS卻通過(guò)調(diào)節(jié)細(xì)胞信號(hào)級(jí)聯(lián)發(fā)揮效應(yīng)[17]。近幾十年的研究已經(jīng)凸顯出ROS在健康和疾病中的重要性。鑒于此,本文綜述了ROS的種類、機(jī)體內(nèi)主要的ROS、ROS的生成與反應(yīng)等研究進(jìn)展,為促進(jìn)健康、防治疾病及抗氧化研究提供參考。
1 ROS的概念、種類及生理病理多效性
1.1 氧的出現(xiàn)與需氧真核生物的進(jìn)化
由于藍(lán)藻的光合作用,大約22億年前,氧(O2)最初大量出現(xiàn)在地球上。首先,大部分O2與可溶性鐵(Fe)反應(yīng)生成不溶性氧化礦物[18]。該初始事件后,O2開(kāi)始大量積聚于周圍的環(huán)境和大氣中。大氣中氧濃度的急劇增加及形成各種礦物氧化物被稱為大氧合事件(Great Oxygenation Event)[19],O2的增加導(dǎo)致了地球第一次大規(guī)模物種滅絕,這一事件也被稱為大氧災(zāi)難。事實(shí)上,O2對(duì)厭氧生物有劇毒,O2的損傷效應(yīng)與其自由基特性有關(guān),其耗竭必要的硫醇并使Fe-S聚簇(厭氧生物代謝和大分子結(jié)構(gòu)的生物合成所需)解聚[20]。大約15億年前,需氧α-變形菌被原始真核細(xì)胞共生吞噬后,演變?yōu)榫€粒體,線粒體已進(jìn)化為具有多種細(xì)胞功能的特化細(xì)胞器。近年來(lái),線粒體因作為具有明顯自主性的動(dòng)態(tài)細(xì)胞器,密切參與策劃各種各樣的細(xì)胞活動(dòng),而成為舞臺(tái)中心。由于O2是線粒體電子傳遞系統(tǒng)中的最終電子受體,氧化是電子從一個(gè)原子到另一個(gè)原子的轉(zhuǎn)移,并代表有氧生活及新陳代謝的必須部分,以ATP的形式產(chǎn)生能量。氧狀態(tài)的波動(dòng),有助于增加ROS的生成,這可能對(duì)高能需求或含大量線粒體的組織,如胎盤、大腦、心臟和骨骼肌尤為相關(guān)[21]。
自由基是指“能夠獨(dú)立存在、含一個(gè)或多個(gè)未配對(duì)電子的任何物質(zhì)”,一個(gè)未配對(duì)電子自身占據(jù)一個(gè)原子軌道[18],是極不穩(wěn)定的分子。考慮到基態(tài)氧在其最外層反鍵軌道有兩個(gè)未配對(duì)電子,因此可歸類為自由基[22]。O2最外層軌道的兩個(gè)孤對(duì)電子具有相同的自旋量子數(shù),對(duì)接受電子產(chǎn)生自旋限制[23]。因此,當(dāng)其被還原為水時(shí),O2一次只能接受一個(gè)電子,便可以產(chǎn)生幾種自由基中間產(chǎn)物,即超氧陰離子(O·)、過(guò)氧化氫(H2O2)和羥自由基(·OH)[24]。這也使O2變得危險(xiǎn),因?yàn)槠鋯蝺r(jià)還原導(dǎo)致高活性中間產(chǎn)物的生成(圖1)。自由基是活性代謝物,可由外來(lái)物質(zhì)生成。由于電子“喜歡”配對(duì)形成化學(xué)鍵,自由基不能與親核試劑發(fā)生共價(jià)反應(yīng);相反,其與另一種自由基反應(yīng)形成共價(jià)鍵,從中性分子抽去氫原子,以生成一種新的自由基,或抽去一個(gè)電子形成陰離子并產(chǎn)生自由基陽(yáng)離子。自由基可發(fā)生在脂類、氨基酸、核苷酸和含氧化合物等中。氧自由基特別重要,因?yàn)榭梢杂|發(fā)所有其他自由基的形成[25-26]。有氧呼吸期間O2逐步還原為水。輻射誘導(dǎo)的水裂解產(chǎn)生·OH,這可解釋輻射療法的損傷效應(yīng)[26]。

適應(yīng)于氧化環(huán)境為生物提供了一個(gè)重要的選擇優(yōu)勢(shì),可使酶活性與氧的利用相偶聯(lián)[20,27]。在需氧細(xì)胞中,O2被許多酶系統(tǒng)利用,然而O2卻是有氧三磷酸腺苷(adenosine triphosphate,ATP)生成背后的主要驅(qū)動(dòng)力。在需氧真核生物中,O2在營(yíng)養(yǎng)物代謝中的利用最大化節(jié)約了能量,促使生物復(fù)雜性的增加,最終進(jìn)化出人類[28-29]。需氧真核生物氧化磷酸化產(chǎn)生ATP是發(fā)生在線粒體,該雙層膜細(xì)胞器起源于原核生物,含有O·依賴性ATP生成(從碳氧化)所需的必要酶系統(tǒng)[30-31]。
1.2 ROS的概念與機(jī)體內(nèi)ROS的種類
ROS可被定義為含氧中間代謝物,帶或不帶一個(gè)未成對(duì)電子,包括氧自由基(即以氧為中心的自由基),如O·、·OH、烷氧自由基(RO·)、過(guò)氧自由基(ROO·)和一氧化氮(NO·),與非自由基,如H2O2、次氯酸(HOCl)和單線態(tài)氧(1O2),其能夠氧化其他成分并將其轉(zhuǎn)變成自由基,往往引起連鎖反應(yīng),導(dǎo)致形成許多新的自由基[32-34]。·OH(半衰期10-9s)和RO·(半衰期數(shù)秒)非常活潑,并迅速攻擊附近細(xì)胞的分子,雖經(jīng)修復(fù)過(guò)程其所造成的損傷可能是不可避免的。另一方面,O·、脂質(zhì)氫過(guò)氧化物和NO·的活性較低[35]。ROS由機(jī)體的正常耗氧如呼吸和一些細(xì)胞介導(dǎo)的免疫功能連續(xù)生成[36]。在體內(nèi)可以形成的主要自由基包括相對(duì)穩(wěn)定的自由基,如尿酸自由基(UrH·-)、抗壞血酸自由基(Asc·-)、VE自由基(VE·)與苯氧自由基(Phl·)和活性自由基,包括碳中心自由基(如脂質(zhì)自由基(L·))和硫中心自由基(如谷胱甘肽自由基(GS·)),其中,在有氧介質(zhì)中,可導(dǎo)致具有較高氧化電位物質(zhì)(如脂質(zhì)過(guò)氧自由基(LOO·)、脂質(zhì)烷氧自由基(LO·)和硫自由基(GSOO·、GSO·和GSO2OO·))。自由基鏈反應(yīng)通常會(huì)繼續(xù),直到系統(tǒng)變得厭氧或底物(如膜脂肪酸(LH))被耗盡,但當(dāng)兩個(gè)自由基形成非自由基產(chǎn)物或存在鏈斷裂抗氧化劑(如VE和多酚類物質(zhì))時(shí),鏈反應(yīng)可被停止[33]。氧化劑和還原劑是化學(xué)術(shù)語(yǔ),在生物環(huán)境中,其通常分別被稱為“助氧化劑和抗氧化劑”[37]。助氧化劑,對(duì)各種生物靶如核酸、脂類和蛋白質(zhì),可誘導(dǎo)其氧化損傷的物質(zhì)。另一方面,抗氧化劑,可以有效地還原助氧化劑,同時(shí)生成無(wú)毒性或低毒性產(chǎn)物的物質(zhì)。人類生活在各種無(wú)處不在的環(huán)境應(yīng)激劑中,其中包括紫外線輻射、微生物、過(guò)敏原和各種污染物,如增多的臭氧、香煙煙霧和多環(huán)芳烴,可以增加機(jī)體ROS的產(chǎn)生[38-40]。
1.3 ROS的生理病理多效性
值得注意的是,ROS是一柄雙刃劍。ROS一直被視為有害分子,通過(guò)氧化損傷各種細(xì)胞內(nèi)分子并負(fù)責(zé)衰老和各種人類疾病。然而,最近的研究揭示細(xì)胞中產(chǎn)生的ROS的另一面,作為第二信使介導(dǎo)生理胞內(nèi)信號(hào)。ROS-效應(yīng)器蛋白的進(jìn)展性鑒定,揭示ROS在生理和病理細(xì)胞生物學(xué)中的多效性功能[41]。一方面,其具有重要的生理功能,例如,NO·是一種重要的血管保護(hù)因子和神經(jīng)系統(tǒng)的神經(jīng)遞質(zhì)[42],氧自由基是免疫防御,以及調(diào)節(jié)細(xì)胞生長(zhǎng)和基因表達(dá)必需的[43]。但是,過(guò)多的自由基,則是有害的,因?yàn)樽杂苫羌?xì)胞代謝產(chǎn)生的非常危險(xiǎn)的副產(chǎn)物[44]。氧化失衡,即ROS的生成與抗氧化防御系統(tǒng)之間平衡的破壞,被描述為氧化應(yīng)激狀態(tài)[45],這會(huì)導(dǎo)致細(xì)胞損傷,引起功能與完整性的喪失。不良影響包括直接與ROS化學(xué)反應(yīng)使NO·失活及細(xì)胞成分如DNA和蛋白質(zhì)的氧化損傷[46-47]。這些影響可能參與大量病理狀態(tài)的發(fā)展[12,48],包括心血管疾病、神經(jīng)系統(tǒng)疾病、癌癥和衰老過(guò)程[49-50]。
此外,在懷孕期間ROS生成的變化,強(qiáng)調(diào)了胎盤中氧化信號(hào)傳導(dǎo)的重要性,在人類懷孕的早期階段,胎盤循環(huán)的建立與胎盤內(nèi)氧水平的劇增相關(guān),導(dǎo)致ROS生成增加及氧化應(yīng)激,隨著胎齡增加,胎盤氧合作用的改變對(duì)胎盤發(fā)育產(chǎn)生影響[21]。因此,了解氧化應(yīng)激如何影響胎盤內(nèi)氧化還原敏感的轉(zhuǎn)錄因子可能闡明潛在的治療靶點(diǎn),糾正異常的胎盤血管生成及功能。
2 機(jī)體內(nèi)主要的ROS
ROS是由分子氧還原產(chǎn)生的高反應(yīng)性分子。最常見(jiàn)的ROS是O·、·OH、H2O2。這些ROS主要是由線粒體氧化磷酸化(電子沿呼吸鏈酶?jìng)鬟f并泄漏給分子氧)生成的。生理水平的ROS參與細(xì)胞信號(hào)通路,這對(duì)發(fā)育和細(xì)胞功能尤為重要。
H2O2是由兩個(gè)電子還原O2生成的,不是一種自由基,但卻是氧化劑。在O2和過(guò)渡金屬離子存在下,H2O2可通過(guò)Fenton反應(yīng)生成·OH。H2O2在生物體中作為氧化代謝的副產(chǎn)物自然產(chǎn)生,這是非自由基反應(yīng)性物質(zhì),并易于在活細(xì)胞之間擴(kuò)散,可被過(guò)氧化氫酶(catalase,CAT)有效地轉(zhuǎn)化為水,該過(guò)程決定其半衰期。一些證據(jù)表明,H2O2通過(guò)核因子κB和載脂蛋白-1的途徑調(diào)節(jié)基因的表達(dá)參與信號(hào)轉(zhuǎn)導(dǎo)[56-57]。
因此,重要的是存在不同營(yíng)養(yǎng)物和氧化還原環(huán)境改變時(shí),要客觀評(píng)價(jià)線粒體如何產(chǎn)生O·/H2O2,考慮到線粒體ROS排放對(duì)細(xì)胞通訊很重要。線粒體中有11 個(gè)潛在的O·/H2O2生成底物,其中5 種,即復(fù)合體Ⅰ、Ⅱ、Ⅲ、α-酮戊二酸脫氫酶(2-oxoglutarate dehydrogenase,ODH)、丙酮酸脫氫酶(pyruvate dehydrogenase,PDH)作為線粒體O·/H2O2的主要來(lái)源。其他6 種酶,分別是電子傳遞黃素蛋白氧化還原酶(electron transfer flavoprotein oxidoreductase,ETFQO)、二氫乳清酸脫氫酶(dihydroorotate dehydrogenase,DHODH)、脯氨酸脫氫酶(proline dehydrogenase,PRODH)、琥珀酸:醌還原酶(succinate:quinone reductase,SQR)、sn-甘油-3-磷酸脫氫酶(sn-glycerol-3-phosphate dehydrogenase,G3PDH)、支鏈酮酸脫氫酶(branched chain keto acid dehydrogenase),只能少量產(chǎn)生O·/H2O2,但當(dāng)高濃度的抑制劑和底物存在時(shí)生成量可增加[26]。然而,最近研究顯示,O·等ROS也可產(chǎn)生有益的效應(yīng),其通過(guò)作為(氧化還原)信號(hào)參與細(xì)胞調(diào)節(jié),且其有害作用主要是由于信號(hào)傳導(dǎo)受損的結(jié)果,而不是由于直接損傷敏感的靶標(biāo)。有趣的是,ROS也可作為促存活信號(hào)增加壽命[10]。
2.2 ·OH
·OH是由3 個(gè)電子還原O2生成的,是氫氧根離子(OH-)的中性形式,是最活潑的自由基,估計(jì)半衰期約10-9s。其可能會(huì)在體內(nèi)由高能量照射裂解體內(nèi)水分形成或金屬催化內(nèi)源性H2O2的過(guò)程中形成。紫外線不足以將水裂解,但卻可以分解H2O2,得到兩分子的·OH。該自由基的高反應(yīng)性暗示了在其產(chǎn)生的地方立即發(fā)生反應(yīng)[58]。
2.3 NO·與ONOO
NO·是哺乳動(dòng)物(包括人類)重要的細(xì)胞信號(hào)傳導(dǎo)分子,參與許多生理和病理過(guò)程[59]。NO·是一種信使,由精氨酸在酶作用下生成,并松弛血管壁的平滑肌導(dǎo)致血壓降低。其也被激活的巨噬細(xì)胞在免疫防御期間所產(chǎn)生,過(guò)量的NO·具有細(xì)胞毒性,其可能會(huì)直接與生物分子反應(yīng)或與O·結(jié)合生成過(guò)氧亞硝酸鹽(ONOO-)。ONOO-能夠誘導(dǎo)脂蛋白的脂質(zhì)過(guò)氧化(lipid peroxidation,LPO),但還可能通過(guò)硝化蛋白質(zhì)酪氨酸殘基干擾細(xì)胞信號(hào)傳導(dǎo)[60-61]。
2.4 ROO·與RO·
過(guò)氧自由基(ROO·)壽命較長(zhǎng),在生物系統(tǒng)中具有相當(dāng)長(zhǎng)的擴(kuò)散路徑。其可以產(chǎn)生于LPO反應(yīng)的過(guò)程中,該過(guò)程是由多不飽和脂肪酸(polyunsaturated fatty acid,PUFA)抽去H原子而起始,·OH能夠啟動(dòng)該序列反應(yīng)[62-63]。LPO反應(yīng)產(chǎn)生的進(jìn)一步產(chǎn)物是烷氧自由基(RO·)和有機(jī)氫過(guò)氧化物(ROOH)。后者可能重新排列為內(nèi)過(guò)氧化物中間產(chǎn)物,其裂解后產(chǎn)生醛類,醛與蛋白氨基反應(yīng)作為一種機(jī)制參與脂蛋白中蛋白部分的修飾[58]。
3 ROS的生成
ROS由細(xì)胞內(nèi)的多個(gè)室和多種酶生成,其中大多都位于線粒體環(huán)境(如呼吸鏈復(fù)合體),復(fù)合體Ⅰ、復(fù)合體Ⅱ、復(fù)合體Ⅲ、線粒體甘油磷酸脫氫酶(mitochondrial glycerophosphate dehydrogenase,mGPDH,位于α-酮戊二酸脫氫酶附近)、電子傳遞黃素蛋白(electron transfer flavoprotein,ETF)、ETF泛醌氧化還原酶、丙酮酸脫氫酶(pyruvate dehydrogenase,PDH)、順烏頭酸酶、替代氧化酶(alternative oxidase,AO)、復(fù)合體Ⅳ、DHODH,外部NADH脫氫酶(external NADH dehydrogenase,NADHDH)、蛋白質(zhì)p66Shc、細(xì)胞色素(cyt)b5還原酶、單胺氧化酶(monoamine oxidase,MAO)和一氧化氮合酶(nitricoxide synthase,NOS)。其他蛋白或細(xì)胞器也可以導(dǎo)致ROS的產(chǎn)生[64-66]。然而,每種酶的精確貢獻(xiàn)尚不清楚。線粒體呼吸鏈復(fù)合體被視為主要生產(chǎn)者,特別是復(fù)合體Ⅰ酶的幾個(gè)位點(diǎn),復(fù)合體Ⅲ與輔酶Q相互作用的亞基和低底物條件下的復(fù)合體Ⅱ[66]。ROS產(chǎn)生位點(diǎn)還包括NADPH氧化酶、黃嘌呤氧化酶、過(guò)氧化物酶、細(xì)胞色素P450、各種胞質(zhì)溶膠酶(如環(huán)氧合酶)、脂氧合酶、紅細(xì)胞中的血紅蛋白[9]等。雖然所有這些來(lái)源有助于總的氧化負(fù)擔(dān),約90%細(xì)胞中的ROS源自線粒體。作為主要的細(xì)胞ROS的來(lái)源,線粒體參與衰老和壽命的調(diào)控[67]。線粒體ROS的產(chǎn)生是氧化磷酸化(oxidative phophorylation,OXPHOS)的結(jié)果,該過(guò)程將利用NADH或黃素胺腺嘌呤二核苷酸(reduced flavin adenine dinuleotide,F(xiàn)ADH2)的控制氧化產(chǎn)生跨線粒體內(nèi)膜的質(zhì)子位能,然后,該位能通過(guò)F1F0ATP酶磷酸化ADP。在沿細(xì)胞色素鏈數(shù)個(gè)部位,來(lái)自于NADH或FADH2的電子可以直接與氧或其他電子受體反應(yīng),產(chǎn)生自由基。
由于ROS生成的確切機(jī)制未知,我們可以構(gòu)建一個(gè)可能全面描述線粒體ROS生成的簡(jiǎn)單關(guān)系。ROS的形成是環(huán)境氧濃度的函數(shù)[68],細(xì)胞和有機(jī)體應(yīng)答高濃度氧可能意味著應(yīng)激,以探討衰老的作用機(jī)制。雖然一般認(rèn)為,耗氧量增加使ROS產(chǎn)生增加,如果耗氧量增加相對(duì)于更高的組織氧分壓或“位點(diǎn)”(即功能線粒體)的數(shù)量增加是次要的,這種正相關(guān)關(guān)系才是正確的。與此相反,在恒定的組織氧濃度及固定數(shù)量的線粒體條件下,耗氧量增加則有利于降低ROS水平。對(duì)細(xì)胞高氧的反應(yīng)也支持細(xì)胞內(nèi)氧化劑,至少是決定培養(yǎng)的哺乳動(dòng)物細(xì)胞壽命一個(gè)重要的決定因素[69]。研究者已發(fā)現(xiàn)降低環(huán)境的氧濃度可以顯著延長(zhǎng)培養(yǎng)的原代細(xì)胞壽命[70]。增強(qiáng)抗氧化劑的水平可以實(shí)現(xiàn)類似的細(xì)胞壽命延長(zhǎng)。比如,增加SOD水平可延長(zhǎng)原代成纖維細(xì)胞的壽命,同時(shí)也降低端粒縮短速率[71]。線粒體通過(guò)產(chǎn)生過(guò)多的ROS(爆發(fā))從而損傷細(xì)胞組分,而在再灌注損傷中發(fā)揮關(guān)鍵作用,并啟動(dòng)細(xì)胞死亡。再灌注ROS的“爆發(fā)”,導(dǎo)致線粒體結(jié)構(gòu)和功能損傷,誘導(dǎo)細(xì)胞死亡信號(hào)傳導(dǎo),最終損傷組織[72]。
基于前期研究結(jié)果,有研究者提出總氧耗的約2%用于ROS生成[73]。該數(shù)值已被廣泛引用,盡管事實(shí)上,這些早期研究中ROS的測(cè)定是在人工條件下。隨后,在更符合生理?xiàng)l件下的研究中,該基礎(chǔ)值降至約0.2%[74-75]。這種較低的數(shù)值并不意味著ROS的基礎(chǔ)生成速率不重要,但確實(shí)提示,在大多數(shù)組織中線粒體ROS的負(fù)載可能不像一度被認(rèn)為的那么嚴(yán)重[69]。
4 生成ROS的反應(yīng)
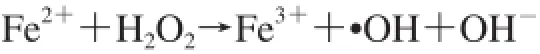
超氧化物作為還原劑,可以提供電子給Fe3+,經(jīng)Haber-Weiss反應(yīng)變成亞鐵狀態(tài),因此驅(qū)動(dòng)后續(xù)Fenton反應(yīng)并增加·OH生成:
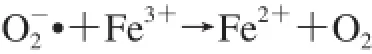
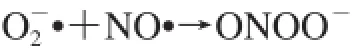
隨后的PN分解導(dǎo)致形成額外的高反應(yīng)性細(xì)胞毒自由基,包括二氧化氮(NO2·)和碳酸自由基(CO3·)。NO2·和CO3·是由PN質(zhì)子化為過(guò)氧亞硝酸(ONOOH)或由PN與CO2反應(yīng)以生成亞硝基過(guò)氧碳酸鹽(ONOOCO2)而形成。單獨(dú)分解ONOOH和ONOOCO2分別形成高活性的NO2·和·OH及NO2·和CO3·[76]。
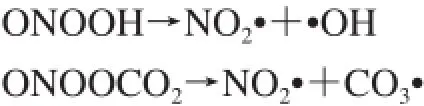
PN-衍生的自由基可誘導(dǎo)蛋白質(zhì)、脂類(細(xì)胞膜和線粒體膜)和核酸的氧化損傷[60,77],例如,PN-衍生的NO2·誘導(dǎo)蛋白硝化導(dǎo)致結(jié)合蛋白的酪氨酸翻譯后修飾為3-硝基酪氨酸(3-nitro tyrosine,3-NT),因此,3-NT作為ONOO-作用的生物標(biāo)志物[78-79];此外,PN產(chǎn)物可以引發(fā)脂質(zhì)過(guò)氧化(lipid peroxidation,LPO),進(jìn)一步引起氧化和不可逆的細(xì)胞損傷。
根據(jù)其所處的環(huán)境超氧化物化學(xué)性質(zhì)顯著不同,在水溶液中,超氧化物是一種弱氧化劑和較強(qiáng)的還原劑,由于在水溶液中的歧化反應(yīng),超氧化物迅速消失,形成H2O2與 O2[80]:

H2O2是一種弱氧化劑和弱還原劑,且不存在過(guò)渡金屬的情況下是相對(duì)穩(wěn)定的。然而,超氧化物和H2O2本身的氧化毒性低,其均為凈Haber-Weiss反應(yīng)的組成部分,容易由銅或亞鐵離子催化產(chǎn)生·OH:
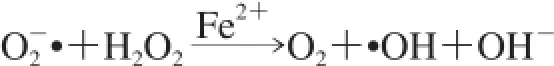
·OH非常活潑,其引起ROS對(duì)生物大分子產(chǎn)生的大部分損傷,生物·OH的主要來(lái)源是經(jīng)Fenton反應(yīng)(凈Haber-Weiss反應(yīng)的一半)由金屬催化H2O2的分解[80]:Mn++ H2O2→M(n+1)++·OH+OH-。
由于其半衰期短,·OH攻擊其生成部位附近的分子,由于具備非常高的反應(yīng)性,使得其幾乎不可能被清除。·OH與生物大分子的反應(yīng)產(chǎn)生新的自由基,通常具有較低的活性。
5 ROS與線粒體氧化磷酸化(oxidative phophorylation,OXPHOS)
細(xì)胞的生死存亡很大程度上取決于線粒體的功能。大部分細(xì)胞ROS,作為呼吸鏈正常能量生成的副產(chǎn)物,是在線粒體生成。ROS主要在OXPHOS的呼吸態(tài)4生成,線粒體在呼吸態(tài)3向呼吸態(tài)4轉(zhuǎn)換中,由于ADP耗盡,ATP積累,使O2消耗的主要途徑被切斷,導(dǎo)致O2濃度升高。而引起O2單電子還原的主要呼吸鏈成員都處于還原狀態(tài),高氧的環(huán)境和高還原態(tài)的呼吸鏈促使電子漏更易于生成O·。解偶聯(lián)作用使線粒體內(nèi)膜質(zhì)子漏(proton leak)增加,線粒體膜電位(Δψm)降低,刺激O2的消耗,減少O·的生成,所以,解偶聯(lián)抑制O2的單電子還原。解偶聯(lián)蛋白作為線粒體ROS生成和生物能學(xué)調(diào)節(jié)器,腺苷酸激酶在哺乳動(dòng)物雷帕霉素靶(mammalian target of rapamycin,mTOR,蛋白質(zhì)合成的主要調(diào)節(jié)器)上游作為一種能量傳感器[81]。轉(zhuǎn)化生長(zhǎng)因子-β(transforming growth factor-β,TGF-β)可激活mTOR途徑,其在某種程度上,通過(guò)mTOR增加Δψm和耗氧速率,導(dǎo)致ROS生成增多而起作用,這可能導(dǎo)致足細(xì)胞損傷,TGF-β1可刺激培養(yǎng)的鼠足細(xì)胞線粒體OXPHOS 及ROS的生成[82]。當(dāng)溫和的解偶聯(lián)不能阻止ROS的形成時(shí),積累ROS將激活線粒體上非特異的線粒體通透性轉(zhuǎn)換孔(mitochondrial permeability transition pore,MPTP)開(kāi)放,過(guò)高的ROS持續(xù)積累導(dǎo)致MPTP的持續(xù)開(kāi)放將引起細(xì)胞凋亡。
線粒體能量代謝,尤其是OXPHOS,受質(zhì)子電化學(xué)梯度(由還原燃料的氧化和跨線粒體內(nèi)膜的質(zhì)子漏產(chǎn)生)嚴(yán)格控制。同樣,線粒體ROS生成被描述為質(zhì)子電化學(xué)梯度的直接函數(shù),由經(jīng)質(zhì)子漏的溫和解偶聯(lián)所調(diào)控[83]。呼吸態(tài)3 H2O2的生成比呼吸態(tài)4低3~5 倍,這表明磷酸化線粒體H2O2生成比非磷酸化線粒體低幾倍。呼吸態(tài)4高質(zhì)子驅(qū)動(dòng)力由于增加了超氧化物形成的概率,而對(duì)細(xì)胞可能是危險(xiǎn)的[83]。ROS引起線粒體損傷時(shí),影響線粒體呼吸鏈復(fù)合體的活力,降低線粒體的效能,從而影響線粒體OXPHOS,減少胞內(nèi)ATP的合成,再經(jīng)系列反應(yīng)生成更多的ROS,使線粒體膜通透性增高,Δψm降低,從而形成ROS→線粒體損傷→ROS增多互為因果的惡性循環(huán),損傷線粒體直至細(xì)胞功能受損甚至凋亡。線粒體ROS生成增加可導(dǎo)致ATP合成功能障礙[84]。由于降低的ADP可用性和增加的分子氧,在呼吸態(tài)4形成的超氧化物量增多(與呼吸態(tài)3相比),而解偶聯(lián)可減少ROS的生成。低效線粒體呼吸條件下,由于復(fù)合體Ⅰ活性降低,ROS生成也可能增加[84]。
6 ROS與細(xì)胞凋亡
細(xì)胞凋亡對(duì)多細(xì)胞生物的組織分化、器官發(fā)育、維持機(jī)體穩(wěn)態(tài)具有重要意義。ROS是細(xì)胞信號(hào)通路中的重要中介體,在維持胞內(nèi)氧化還原平衡和細(xì)胞信號(hào)傳導(dǎo)通路上發(fā)揮重要作用。ROS生成過(guò)多會(huì)引起細(xì)胞損傷,這可能作為信號(hào)觸發(fā)凋亡信號(hào)轉(zhuǎn)導(dǎo)途徑,而在啟動(dòng)和調(diào)節(jié)細(xì)胞凋亡過(guò)程中扮演重要角色[85]。當(dāng)?shù)蛲鰡?dòng)后,ROS進(jìn)一步增多可能加速凋亡過(guò)程。ROS的作用方式與其濃度相關(guān),納摩爾水平的ROS可促進(jìn)細(xì)胞增殖,微摩爾水平的ROS可導(dǎo)致細(xì)胞凋亡,毫摩爾水平的ROS引起細(xì)胞的損傷死亡。細(xì)胞凋亡存在3 條途徑:線粒體通路、內(nèi)質(zhì)網(wǎng)通路和死亡受體通路,均與ROS密切相關(guān)[86]。
線粒體既是ROS產(chǎn)生的主要部位,又是ROS作用的主要靶點(diǎn)。通過(guò)呼吸鏈電子漏途徑,線粒體產(chǎn)生大量超氧陰離子,氧化應(yīng)激可對(duì)膜磷脂和膜蛋白過(guò)氧化修飾,造成線粒體通透性轉(zhuǎn)換(mitochondrial permeability transition,MPT),而引起線粒體損傷[87]。ROS激活MPTP開(kāi)放,釋放ROS、細(xì)胞色素c及凋亡誘導(dǎo)因子,從而使細(xì)胞進(jìn)入不可逆的凋亡過(guò)程[88]。MPTP孔道持續(xù)不可逆地開(kāi)放,引發(fā)線粒體內(nèi)膜的通透性非特異地增大,內(nèi)膜兩側(cè)的質(zhì)子梯度消失,Δψm降低,呼吸鏈OXPHOS脫偶聯(lián),ATP合成受到抑制,ROS大量爆發(fā)[87]。
MPT是細(xì)胞凋亡的中心事件,可以通過(guò)MPTP開(kāi)放介導(dǎo),ROS通過(guò)降低Δψm及促使MPTP開(kāi)放作為細(xì)胞凋亡信號(hào)分子。線粒體是影響細(xì)胞死亡和存活信號(hào)的一個(gè)關(guān)鍵集成點(diǎn),其中OXPHOS系統(tǒng)中一個(gè)關(guān)鍵的電子載體——細(xì)胞色素c,從線粒體膜間隙釋放到胞質(zhì)溶膠,作為細(xì)胞凋亡的誘導(dǎo)事件。在某些情況下,這些事件的發(fā)生似乎需要OXPHOS系統(tǒng)的功能,而在其他情況下,OXPHOS功能障礙本身敏化細(xì)胞凋亡,甚至可直接誘導(dǎo)凋亡[89]。總之,機(jī)體95%以上的ROS都來(lái)自線粒體電子漏,ROS水平升高可誘發(fā)Δψm降低和細(xì)胞凋亡,ROS、MPT與細(xì)胞凋亡之間的關(guān)系既復(fù)雜又微妙且密不可分。
7 ROS與免疫防御和炎癥
機(jī)體受細(xì)菌等致病微生物侵入后,通過(guò)先天性免疫和獲得性免疫調(diào)動(dòng)免疫效應(yīng)細(xì)胞和免疫分子清除病原體。先天免疫系統(tǒng)遇到病原體引發(fā)急性炎癥反應(yīng),伴隨著全身性血管擴(kuò)張,血管滲漏和白細(xì)胞遷移[90],從而在感染早期對(duì)機(jī)體進(jìn)行免疫干預(yù)。先天免疫防御系統(tǒng)在進(jìn)化過(guò)程中還形成了一套(100多種)模式識(shí)別受體(pattern recognition receptor,PRR)以識(shí)別各種入侵微生物(如病毒、細(xì)菌、真菌)的病原相關(guān)分子模式(pathogen associated molecular patterns,PAMP)的保守結(jié)構(gòu)域,包括鞭毛蛋白、糖類和各種微生物的細(xì)胞壁成分,如肽聚糖和脂多糖(lipopolysaccharide,LPS),以及受傷細(xì)胞釋放的危險(xiǎn)相關(guān)分子模式,如哺乳動(dòng)物雙鏈DNA和尿酸結(jié)晶。PRR家族包括膜結(jié)合受體,如Toll樣受體(toll-like receptor,TLR)和c-型凝集素受體,以及核苷酸寡聚區(qū)樣受體(nucleotide-oligomerization domain-like receptors,NLR)和維甲酸誘導(dǎo)基因Ⅰ樣受體(retinoic acid-inducible geneⅠ-like receptors,RLR)。PRR表達(dá)于多種免疫細(xì)胞,包括巨噬細(xì)胞、單核細(xì)胞、樹(shù)突狀細(xì)胞(dendritic cells,DCs),中性粒細(xì)胞,使早期檢測(cè)病原體成為可能[91]。
通過(guò)抗原呈遞細(xì)胞(巨噬細(xì)胞和樹(shù)突狀細(xì)胞)表面的PRR識(shí)別PAMP,誘導(dǎo)先天免疫反應(yīng),進(jìn)行抗原呈遞,募集并激活炎癥效應(yīng)細(xì)胞,釋放炎癥介質(zhì)(如白細(xì)胞介素(interleukin,IL)-1、干擾素(interferon,IFN)α、IL-6、趨化因子)以及免疫效應(yīng)因子(如IL-1、IL-5、IL-10、IL-12、轉(zhuǎn)化生長(zhǎng)因子(transforming growth factor,TGF)-β和IFNγ)等,同時(shí)激活獲得性免疫。炎癥是宿主對(duì)抗外來(lái)病原所產(chǎn)生的免疫防御應(yīng)答,脊椎動(dòng)物免疫系統(tǒng)已進(jìn)化了這一生存策略以促進(jìn)組織修復(fù)[92]。TLR家族是一類關(guān)鍵的病原PRR,通過(guò)識(shí)別自身及非自身分子模式調(diào)控先天免疫、抗原提呈和獲得性免疫等多個(gè)免疫環(huán)節(jié)。大多數(shù)哺乳動(dòng)物有10~14 種不同TLR,每一種識(shí)別不同的病原結(jié)構(gòu)。例如,TLR2是一種靶向細(xì)菌細(xì)胞壁的脂蛋白,而TLR3識(shí)別病毒的雙股RNA[93]。TLR4是其中重要成員之一,能夠通過(guò)激活NADPH氧化酶在內(nèi)的多個(gè)信號(hào)通路,上調(diào)TNF-α、IL-1、單核細(xì)胞趨化蛋白-1 (monocyte chemotactic protein-1,MCP-1)等炎癥因子的分泌,在調(diào)節(jié)先天免疫和炎癥反應(yīng)方面起到舉足輕重的作用。LPS是模式識(shí)別和促炎引發(fā)劑分子TLR4的微生物激活劑[94]。TLR4也是LPS的關(guān)鍵受體之一,LPS通過(guò)與TLR4結(jié)合后激活其下游信號(hào)通路,促進(jìn)炎癥因子釋放,從而擴(kuò)大炎癥反應(yīng)。
表達(dá)于上皮細(xì)胞以及吞噬細(xì)胞表面的PRR,如TLR家族的TLR1、2、4、5、6及CLR家族可識(shí)別細(xì)胞外病原體。而胞內(nèi)微生物則由表達(dá)于細(xì)胞質(zhì)內(nèi)吞體或溶酶體的TLR3、7、8、9、10以及NLR和RLR識(shí)別[91]。吞噬細(xì)胞經(jīng)過(guò)PRR識(shí)別入侵病原體的PAMP后,經(jīng)由絲裂原活化蛋白激酶(mitogen-activated protein kinases,MAPK)、髓樣分化因子88(myeloid differentiation factor 88, MyD88), Toll樣受體結(jié)構(gòu)域銜接蛋白(TLR adaptor molecule 1,TRIF)等通路激活NF-κB,分泌炎性細(xì)胞因子、趨化因子等募集血液循環(huán)中的單核細(xì)胞以及多形核中性粒細(xì)胞(polymorphonuclear neutrophils,PMN)至炎癥部位,從而啟動(dòng)吞噬過(guò)程[95]。而ROS可激活單核細(xì)胞、巨噬細(xì)胞等多種免疫細(xì)胞釋放大量炎性細(xì)胞因子(如TNF-α、IL-6等),引起全身炎癥反應(yīng)綜合征。增加ROS的水平可以觸發(fā)先天免疫,ROS與多種炎癥應(yīng)答相關(guān)[96],炎癥反應(yīng)也可以導(dǎo)致細(xì)胞凋亡或壞死[97]。
細(xì)胞凋亡信號(hào)調(diào)節(jié)激酶1(apoptosis signal-regulating kinase 1,ASK1),一種MAPK激酶(MAPK kinase kinase,MAP3K),在應(yīng)激反應(yīng)中扮演關(guān)鍵角色。此外,ASK1已成為PAMP和內(nèi)源性危險(xiǎn)信號(hào)引發(fā)的免疫應(yīng)答的關(guān)鍵調(diào)節(jié)器。在免疫細(xì)胞中LPS-刺激的細(xì)胞因子生成及胞外ATP-誘導(dǎo)的細(xì)胞凋亡需要ROS依賴的ASK1激活。ASK1參與先天免疫的激活,而這又依賴于ROS[96]。ROS的生成是許多炎性疾病進(jìn)程的核心。細(xì)胞產(chǎn)生的ROS參與寄主防御反應(yīng),如PMN,并通過(guò)關(guān)鍵細(xì)胞信號(hào)蛋白(如酪氨酸磷酸酶)的氧化,促進(jìn)內(nèi)皮功能障礙。ROS既是信號(hào)分子又作為炎癥介質(zhì)[92]。
氧化劑誘導(dǎo)炎癥的作用一直被各種實(shí)驗(yàn)?zāi)P退罅垦芯俊F鋸母旧蠀⑴c應(yīng)答已成共識(shí),但其如何應(yīng)答及抗氧化療法是否是治療炎癥病人的有效手段仍懸而未決[92]。越來(lái)越多的證據(jù)表明,促進(jìn)ROS的生成是TLR-介導(dǎo)的信號(hào)通路激活的中心。Ryan等[98]研究表明,ROS參與LPS/TLR4-介導(dǎo)的IL-8信號(hào)傳導(dǎo),抗氧化治療減少LPS-誘導(dǎo)的人單核細(xì)胞中NF-κB的核易位及IL-8的生成。Park等[99]提出了TLR4調(diào)節(jié)ROS生成的直接機(jī)制。
炎癥小體(inflammasome)是構(gòu)成先天免疫系統(tǒng)的重要組成部分,這些新發(fā)現(xiàn)的多蛋白寡聚物平臺(tái)是由胞內(nèi)傳感器(偶聯(lián)胱冬肽酶)和白介素激活系統(tǒng)構(gòu)成[100]。ROS是重要的炎癥小體激活信號(hào),ROS通過(guò)MAPK和胞外信號(hào)調(diào)節(jié)蛋白激酶1和2(extracellular signal-regulated protein kinases 1 and 2,ERK1/2)激活炎癥小體,炎癥小體的失調(diào)在各病理過(guò)程中起重要作用。病毒(如登革熱和呼吸道合胞病毒)感染亦可激活炎癥小體,矽肺和痛風(fēng)發(fā)病過(guò)程中的晶體化合物也激發(fā)ROS的生成[100]。
炎癥小體激活炎癥誘導(dǎo)細(xì)胞發(fā)生炎性凋亡(pyroptosis),其為不同于細(xì)胞凋亡的程序性細(xì)胞死亡過(guò)程[101],且炎癥小體的確切性質(zhì)取決于活化劑。微生物或非微生物所致的組織損傷后,主要源于微生物的PAMP和損傷相關(guān)分子模式(damage-associated molecular patterns,DAMP)的釋放是炎癥小體兩種常見(jiàn)的興奮劑,以誘導(dǎo)促炎細(xì)胞因子的成熟[102]。Nod樣受體蛋白(nod-like receptor protein,NLRP)3可能是研究最廣泛的炎癥小體,且被宿主源分子如過(guò)量的ATP、葡萄糖、ROS、鞘氨醇、神經(jīng)酰胺、氧化型低密度脂蛋白、尿酸和膽固醇結(jié)晶所激活[103-107]。
很顯然,ROS對(duì)炎癥和組織損傷的發(fā)病機(jī)制很重要,但ROS在生理上如何發(fā)揮免疫防御功能及其引發(fā)炎癥和組織損傷的機(jī)制還有待進(jìn)一步研究。
8 ROS在腫瘤細(xì)胞中亦作為一柄雙刃劍
生物體內(nèi)存在著一套完善的氧化、抗氧化體系,正常情況下可將ROS維持在穩(wěn)定范圍內(nèi),并在抗炎、抗菌等方面發(fā)揮積極作用。當(dāng)平衡打破,ROS持續(xù)升高,將可能促使細(xì)胞發(fā)生轉(zhuǎn)化、導(dǎo)致惡性腫瘤的發(fā)生。盡管大多數(shù)研究主要集中在氧化應(yīng)激參與癌癥起始,ROS也作用于腫瘤轉(zhuǎn)移并可能促進(jìn)腫瘤侵襲與轉(zhuǎn)移[108]。近年來(lái)ROS殺傷腫瘤細(xì)胞的作用也逐漸被認(rèn)識(shí)。
ROS對(duì)調(diào)節(jié)正常細(xì)胞過(guò)程很重要,ROS過(guò)量或不足所致的氧化還原失衡是疾病發(fā)病機(jī)制的誘因,包括癌癥的發(fā)生和進(jìn)展,ROS與細(xì)胞氧化應(yīng)激被認(rèn)為是癌癥發(fā)生的誘導(dǎo)物。然而,ROS與癌癥的相關(guān)性既復(fù)雜,有時(shí)又矛盾[109]。ROS的形成對(duì)癌細(xì)胞的生長(zhǎng)是必要且有益的事件,氧化還原失衡被認(rèn)為可導(dǎo)致腫瘤細(xì)胞死亡[109]。ROS在調(diào)節(jié)細(xì)胞信號(hào)傳導(dǎo)和體內(nèi)平衡中有重要作用,ROS失衡會(huì)引起各種疾病(包括癌癥)的發(fā)展。由于代謝加速,腫瘤細(xì)胞表現(xiàn)出增高的ROS水平(與正常細(xì)胞相比)[110],這使其更容易受到氧化應(yīng)激誘導(dǎo)的細(xì)胞死亡,這也是其Achilles之踵(致命弱點(diǎn))[111]。所以,進(jìn)一步增加細(xì)胞的氧化應(yīng)激已成為當(dāng)前抗癌療法的常見(jiàn)策略[111-112]。因?yàn)轶w內(nèi)總氧化還原平衡是由ROS生成和清除之間的平衡來(lái)維持,特別是,增加ROS的產(chǎn)生或抑制ROS清除的外源性化合物,有利于癌細(xì)胞ROS的積累,從而引起細(xì)胞損傷,一旦達(dá)到“耐受”閾值甚至可誘導(dǎo)癌細(xì)胞死亡[113]。
Wang[114]和Laurent等[115]提出了一個(gè)新的假說(shuō),稱為“ROS閾值概念”,進(jìn)一步描述細(xì)胞內(nèi)ROS在腫瘤細(xì)胞中的作用[116]。根據(jù)這一假說(shuō),細(xì)胞生存需要一定水平的ROS,但高濃度的ROS可以觸發(fā)細(xì)胞死亡,且腫瘤細(xì)胞的ROS水平通常遠(yuǎn)遠(yuǎn)高于正常細(xì)胞。進(jìn)一步增加ROS水平可使腫瘤細(xì)胞比正常細(xì)胞更早達(dá)到死亡閾值[117]。誘導(dǎo)ROS生成已成為癌癥治療一種新穎的方法[118-119]。這種策略激動(dòng)人心的優(yōu)勢(shì)在于其良好的選擇性,癌細(xì)胞通常處于氧化應(yīng)激,且因此具有相對(duì)較高的ROS基礎(chǔ)水平[113,120],腫瘤細(xì)胞ROS的輕微誘導(dǎo)可能推動(dòng)ROS水平超過(guò)細(xì)胞死亡閾值,而正常細(xì)胞因?yàn)槠漭^低的ROS基礎(chǔ)水平和較強(qiáng)的抗氧化能力,可以更好地耐受氧化攻擊[114,121]。
促進(jìn)ROS生成的藥物包括:1)線粒體電子傳遞鏈調(diào)節(jié)劑(如三氧化二砷、阿霉素、托泊替康等);2)氧化還原循環(huán)化合物(如莫特沙芬釓);3)破壞抗氧化防御機(jī)制的藥物,如GSH-耗竭藥物(如丁硫氨酸亞砜胺、β-苯乙基異硫氰酸酯(β-phenylethyl isothiocyanates,PEITC))、SOD抑制劑(如2-甲氧基雌二醇)和過(guò)氧化氫酶抑制劑(如3-氨基-1,2,4-三唑)[113,122-125]。3-甲基丙酮酸能激活人肺癌A549細(xì)胞和小鼠鱗狀細(xì)胞癌SCCVII細(xì)胞線粒體能量代謝,細(xì)胞接觸X射線后,用3-甲基丙酮酸預(yù)處理可顯著促進(jìn)這兩個(gè)細(xì)胞系輻射誘導(dǎo)的細(xì)胞死亡,并導(dǎo)致Δψm的升高和線粒體源ROS的生成[117]。
綜上,幾乎所有腫瘤細(xì)胞均有一個(gè)共同點(diǎn),氧化還原失衡、氧化應(yīng)激水平增高,表現(xiàn)出ROS水平的升高和抗氧化酶活性的降低。ROS通過(guò)脂質(zhì)過(guò)氧化、DNA損傷和蛋白質(zhì)破壞等過(guò)程介入腫瘤的形成,并且在腫瘤的轉(zhuǎn)移方面發(fā)揮重要的作用。細(xì)胞內(nèi)ROS對(duì)惡性腫瘤的誘發(fā)和治療具有雙重作用,降低細(xì)胞中ROS的含量似乎可用于腫瘤的預(yù)防,而提高腫瘤細(xì)胞中ROS的含量似乎可用于腫瘤的治療中,這將使ROS在腫瘤的防治中發(fā)揮更積極的作用。
隨著對(duì)ROS生理功能了解的深入,且閾值理論正被實(shí)驗(yàn),ROS不再僅僅被視為促腫瘤發(fā)生的分子。然而,促進(jìn)ROS生成的策略對(duì)癌癥治療是否可行仍有待觀察。誘導(dǎo)腫瘤細(xì)胞凋亡被認(rèn)為是一個(gè)有效的抗癌策略,而腫瘤與正常細(xì)胞之間治療的選擇性始終是一個(gè)挑戰(zhàn)。
增高的ROS水平和高糖酵解通量是腫瘤細(xì)胞的共同特征,這對(duì)癌癥的發(fā)生和發(fā)展尤為重要。在有氧條件下,正常細(xì)胞主要通過(guò)OXPHOS產(chǎn)生ATP,缺氧時(shí)則主要依賴糖酵解;而腫瘤細(xì)胞即使在有氧條件下,也主要通過(guò)糖酵解產(chǎn)生ATP,因此稱為“有氧糖酵解”(即Warburg效應(yīng)),Warburg假設(shè),腫瘤細(xì)胞以有氧糖酵解為主要產(chǎn)能方式是因?yàn)榫€粒體功能不可逆轉(zhuǎn)的損傷(線粒體能量代謝缺陷)所致[126]。但目前認(rèn)為,多數(shù)腫瘤的線粒體OXPHOS功能是完好的[127-128],并發(fā)現(xiàn)腫瘤細(xì)胞線粒體并沒(méi)有缺陷[129-130],是由于糖酵解抑制了OXPHOS,而非線粒體功能出現(xiàn)不可逆轉(zhuǎn)的損傷[131-132]。
與正常細(xì)胞的代謝相比,癌細(xì)胞經(jīng)常發(fā)生如下代謝重新編程(癌細(xì)胞的代謝特征):癌細(xì)胞呈現(xiàn)增加的糖酵解、磷酸戊糖途徑、谷氨酰胺消耗、合成代謝、Δψm和ROS的生成,以及降低的三羧酸循環(huán)通量、呼吸復(fù)合體活性、MPT和細(xì)胞凋亡[133]。可見(jiàn),腫瘤細(xì)胞的代謝異常并非單一代謝通路的簡(jiǎn)單調(diào)整,而是整個(gè)細(xì)胞代謝網(wǎng)絡(luò)顛覆性的改變,這也是癌邪峻烈難除的原因所在。
正常細(xì)胞與癌細(xì)胞之間線粒體功能的差異,可能為抗癌藥物的設(shè)計(jì)提供獨(dú)特的潛力,使藥物靶向于線粒體以選擇性殺死癌細(xì)胞。從癌癥相關(guān)性線粒體異常的發(fā)現(xiàn),到新穎的抗癌療法臨床探索的長(zhǎng)期過(guò)程,表明癌癥基本知識(shí)的積累最終產(chǎn)生醫(yī)療上可利用的信息是何等緩慢,成功地抗癌必須基于細(xì)胞能量代謝、線粒體的穩(wěn)定性及腫瘤細(xì)胞對(duì)死亡刺激抗性的其他機(jī)制的協(xié)同調(diào)節(jié)。
9 結(jié) 語(yǔ)
近50多年來(lái),ROS被視為有害物質(zhì),可以攻擊蛋白質(zhì)、脂質(zhì)和核酸。為了應(yīng)對(duì)ROS,線粒體進(jìn)化了復(fù)雜的防御系統(tǒng),以防止可能的傷害;ROS水平的增加可使防御系統(tǒng)受損,從而有助于闡明一些疾病的病理機(jī)制。然而,近年來(lái),ROS對(duì)許多細(xì)胞信號(hào)通路的重要性已經(jīng)被揭示,我們不應(yīng)再將ROS只看作是線粒體呼吸的有毒副產(chǎn)物了[66]。ROS作為主要免疫防御的一部分在生物體產(chǎn)生,吞噬細(xì)胞如中性粒細(xì)胞、單核細(xì)胞或巨噬細(xì)胞通過(guò)合成大量的O·或NO·作為其殺傷機(jī)制的一部分抵御外來(lái)生物。一些疾病伴隨著過(guò)多的巨噬細(xì)胞的激活導(dǎo)致組織損傷,至少部分是由于ROS的作用。而且,ROS生成過(guò)量誘導(dǎo)生物分子的氧化損傷,進(jìn)而導(dǎo)致衰老、癌癥和許多其他威脅人類健康的重大疾病[134]。此外,內(nèi)源性ROS形成的生物途徑是一整套反應(yīng)中間物及其生成方式的實(shí)例。應(yīng)當(dāng)進(jìn)一步指出,機(jī)體亦暴露于外源性ROS。在活生物體中,各種ROS可以以不同的方式生成。正常的有氧呼吸刺激多形核白細(xì)胞和巨噬細(xì)胞,及過(guò)氧化物酶體似乎是細(xì)胞產(chǎn)生氧化劑的主要內(nèi)源性來(lái)源。外源性ROS來(lái)源包括煙草煙霧、某些污染物、有機(jī)溶劑和農(nóng)藥。許多助氧化劑性質(zhì)的化合物,如苯醌具氧化還原循環(huán)能力,隨膳食進(jìn)入機(jī)體。一些自由基也隨香煙煙霧吸入,據(jù)報(bào)道,因空氣污染臭氧水平增加,臭氧是一種氧化脂質(zhì)的ROS。
ROS,由于各種內(nèi)源或外源因素產(chǎn)生于人體內(nèi)。越來(lái)越多的證據(jù)表明,ROS,如ROO·、·OH、O·和1O2,都參與衰老和多種疾病,如癌癥、阿爾茨海默病和帕金森病的病理生理學(xué)。ROS,通過(guò)UV光、X射線和γ射線在照射過(guò)程中產(chǎn)生,也是金屬催化反應(yīng)的產(chǎn)物;又在大氣污染物中存在,嗜中性粒細(xì)胞和巨噬細(xì)胞在炎癥過(guò)程中同樣產(chǎn)生,還是線粒體催化的電子傳遞反應(yīng)和其他機(jī)制的副產(chǎn)物。研究表明,α-生育酚保護(hù)角化細(xì)胞抵御紫外線A(ultraviolet A,UVA)輻射,可能是通過(guò)增加谷胱甘肽水平或減少脂質(zhì)過(guò)氧化和ROS生成的水平[135]。胰島素治療可抑制ROS過(guò)度生成,從而緩解糖尿病條件下鈦植入受損的骨生成(通過(guò)磷脂酰肌醇3-激酶/ Akt-依賴性機(jī)制),胰島素的抗氧化與代謝特性應(yīng)該使其成為一個(gè)可行的治療選擇以對(duì)抗糖尿病植入失敗[136]。尋找有效的方法以減少或抑制自由基在體內(nèi)的過(guò)量產(chǎn)生,對(duì)健康具有重要意義。
ROS作為信號(hào)分子在中樞神經(jīng)系統(tǒng),尤其是下丘腦,有強(qiáng)烈作用。由于下丘腦是參與體內(nèi)能量平衡調(diào)控的一個(gè)關(guān)鍵區(qū)域,下丘腦ROS在能量代謝和食物攝入量調(diào)節(jié)中起重要作用[16]。能量代謝和食物攝入量是一個(gè)非常復(fù)雜的過(guò)程,它包括由下丘腦網(wǎng)絡(luò)信號(hào)通路驅(qū)動(dòng)的穩(wěn)態(tài)機(jī)制。下丘腦ROS水平,由各種分子和燃料信號(hào)控制,在下丘腦控制能量平衡中扮演著重要角色。下丘腦ROS釋放的控制涉及到許多分子事件,如線粒體動(dòng)力學(xué)、NADPH氧化酶活性、突觸彈性、過(guò)氧化物酶體和內(nèi)質(zhì)網(wǎng)。高水平ROS使緩沖機(jī)制飽和,可能啟動(dòng)神經(jīng)元退化,并損傷體內(nèi)能量平衡,導(dǎo)致疾病,如肥胖和2型糖尿病[16]。抑制與減少底物的量、低氧與高氧、或內(nèi)源性與外源性應(yīng)激均可增加ROS。因此,對(duì)于不同的機(jī)體生理狀況或疾病狀態(tài)一定存在多種機(jī)制并導(dǎo)致不同的答案。此外,對(duì)ROS的生成、來(lái)源及機(jī)制尚有待進(jìn)一步充分研究。機(jī)體需要ROS是因?yàn)槠浔Wo(hù)最初的原核細(xì)胞在危險(xiǎn)的環(huán)境中生存?或是基于某種目的而后發(fā)展起來(lái)的?機(jī)體如何影響ROS的生成水平?我們?nèi)绾文軓钠渫猥@得什么?由于諸多原因,開(kāi)創(chuàng)了一個(gè)偉大的氧化還原生物學(xué)領(lǐng)域以進(jìn)一步揭示其中的奧秘,并將為人類的健康做出貢獻(xiàn)。
能量平衡是所有高等生物生存的主要決定因素,能量應(yīng)激又可導(dǎo)致氧化應(yīng)激。主要由線粒體ROS引起的蛋白質(zhì)、核酸與脂質(zhì)氧化,是決定健康和壽命的關(guān)鍵因素[137]。OXPHOS是線粒體一個(gè)關(guān)鍵的功能單位,并將電子傳遞與細(xì)胞呼吸和ATP的合成結(jié)合在一起,其不僅產(chǎn)生絕大部分細(xì)胞的能量,也參與了ROS的產(chǎn)生和細(xì)胞凋亡[138]。由線粒體的OXPHOS系統(tǒng)合成ATP是必需的以保持細(xì)胞活力,因?yàn)閹缀跛械募?xì)胞內(nèi)ATP都是在線粒體中生成,約1/3的細(xì)胞腺苷酸定位于該細(xì)胞器。因此,線粒體功能障礙具有多種功能后果,且發(fā)現(xiàn)于大多數(shù)的人類疾病[139-141],其特征是呼吸態(tài)3、呼吸控制率(respiratory control ratio,RCR)和Δψm降低,且呼吸態(tài)4和與氧化產(chǎn)物含量的增加相關(guān)的線粒體的大小和脆性增加。ROS介導(dǎo)的氧化是線粒體功能障礙和更替、細(xì)胞凋亡、組織功能及壽命的決定因素。線粒體不僅在生物能的供應(yīng)和ROS的“調(diào)節(jié)器”中發(fā)揮了重要作用,而且還控制細(xì)胞的生和死。細(xì)胞缺乏能量、ROS生成過(guò)多、細(xì)胞凋亡的失調(diào)被單獨(dú)或組合發(fā)現(xiàn)于大多數(shù)人類疾病,包括神經(jīng)退行性疾病、中風(fēng)、心腦血管疾病、缺血/再灌注損傷和癌癥等。大量且還在不斷增加的人類疾病都與OXPHOS功能障礙相關(guān)。所涉及的兩個(gè)不同的關(guān)鍵因素是缺乏能量及ROS產(chǎn)生增加。由于細(xì)胞功能中OXPHOS的核心作用,其組件的活性不得不經(jīng)過(guò)嚴(yán)密精細(xì)的調(diào)控,因?yàn)楹茱@然要考慮發(fā)育和組織特異性的能量需求[142]。線粒體通過(guò)操縱生物能學(xué)、MPT和ROS等因素而調(diào)控細(xì)胞的生與死[143]。如何控制線粒體內(nèi)ROS的生成并改善線粒體生物能學(xué),防護(hù)線粒體損傷將成為研究者關(guān)注的熱點(diǎn)。
綜上,筆者認(rèn)為,線粒體消耗人體約90%的氧,產(chǎn)生人體約90%的ROS和約90%的能量(ATP),線粒體控制細(xì)胞生死及整個(gè)生命過(guò)程(其本質(zhì)就是氧化還原),線粒體成為生命的主宰。這一切也許最終是通過(guò)操縱ATP與ROS的生成實(shí)現(xiàn)的,而ATP與ROS的生成又主要是線粒體呼吸鏈氧化磷酸化的結(jié)果,如何通過(guò)調(diào)控線粒體氧化磷酸化實(shí)現(xiàn)ATP與ROS生成的平衡將是健康的關(guān)鍵。
參考文獻(xiàn):
[1] RAY P D, HUANG B W, TSUJI Y.Reactive oxygen species (ROS)homeostasis and redox regulation in cellular signaling[J].Cellular Signalling, 2012, 24(5): 981-990.DOI:10.1016/j.cellsig.2012.01.008.
[2] CORDEIRO R M.Reactive oxygen species at phospholipid bilayers: distribution, mobility and permeation[J].Biochimica et Biophysica Acta (BBA)-Biomembranes, 2014, 1838(1): 438-444.DOI:10.1016/ j.bbamem.2013.09.016.
[3] SCHMEI?ER S, RISTOW M, BIRRINGER M.Recent reassessment of the role of reactive oxygen species (ROS)[J].Ernaehrungs Umschau International, 2013, 60(9): 162-167.
[4] GUPTA S C, HEVIA D, PATCHVA S, et al.Upsides and downsides of reactive oxygen species for cancer: the roles of reactive oxygen species in tumorigenesis, prevention, and therapy[J].Antioxidants & Redox Signaling, 2012, 16(11): 1295-1322.DOI:10.1089/ ars.2011.4414.
[5] FRANKEL E N, GERMAN J B.Antioxidants in foods and health: problems and fallacies in the field[J].Journal of the Science of Food and Agriculture, 2006, 86(13): 1999-2001.DOI:10.1002/jsfa.2616
[6] SANTOS C X C, NABEEBACCUS A A, SHAH A M, et al.Endoplasmic reticulum stress and Nox-mediated reactive oxygen species signaling in the peripheral vasculature: potential role in hypertension[J].Antioxidants & Redox Signaling, 2014, 20(1): 121-134.DOI:10.1089/ars.2013.5262.
[7] ZUO L, ROSE B A, ROBERTS W J, et al.Molecular characterization of reactive oxygen species in systemic and pulmonary hypertension[J].American Journal of Hypertension, 2014, 27(5): 643-650.DOI:10.1093/ajh/hpt292.
[8] GONCHAROV N V, AVDONIN P V, NADEEV A D, et al.Reactive oxygen species in pathogenesis of atherosclerosis[J].Current Pharmaceutical Design, 2015, 21(13): 1134-1146.DOI:10.2174/13816 12820666141014142557.
[9] FISHER-WELLMAN K, BELL H K, BLOOMER R J.Oxidative stress and antioxidant defense mechanisms linked to exercise during cardiopulmonary and metabolic disorders[J].Oxidative Medicine and Cellular Longevity, 2009, 2(1): 43-51.DOI:10.4161/oxim.2.1.7732.
[10] TAMURA M, MATSUI H, TOMITA T, et al.Mitochondrial reactive oxygen species accelerate gastric cancer cell invasion[J].Journal of Clinical Biochemistry and Nutrition, 2014, 54(1): 12-17.DOI:10.3164/ jcbn.13-36.
[11] NATHAN C, CUNNINGHAM-BUSSEL A.Beyond oxidative stress: an immunologist's guide to reactive oxygen species[J].Nature Reviews Immunology, 2013, 13(5): 349-361.DOI:10.1038/nri3423.
[12] LIOCHEV S I.Reactive oxygen species and the free radical theory of aging[J].Free Radical Biology and Medicine, 2013, 60(10): 1-4.DOI:10.1016/j.freeradbiomed.2013.02.011.
[13] GüL?IN ?, ELIAS R, GEPDIREMEN A, et al.Antioxidant activity of bisbenzylisoquinoline alkaloids from Stephania rotunda: cepharanthine and fangchinoline[J].Journal of Enzyme Inhibition and Medicinal Chemistry, 2010, 25(1): 44-53.DOI:10.3109/14756360902932792.
[14] GüL?IN ?, ELMASTA? M, ABOUL-ENEIN H Y.Antioxidant activity of clove oil:a powerful antioxidant source[J].Arabian Journal of Chemistry, 2012, 5(4): 489-499.DOI:10.1016/j.arabjc.2010.09.016.
[15] 李興太, 紀(jì)瑩.線粒體氧化應(yīng)激與天然抗氧化劑研究進(jìn)展[J].食品科學(xué), 2015, 36(7): 268-277.DOI:10.7506/spkx1002-6630-201507049.
[16] DROUGARD A, FOURNEL A, VALET P, et al.Impact of hypothalamic reactive oxygen species in the regulation of energy metabolism and food intake[J].Frontiers in Neuroscience, 2015, 9: 1-12.DOI:10.3389/fnins.2015.00056.
[17] BRIEGER K, SCHIAVONE S, MILLER F J, Jr, et al.Reactive oxygen species: from health to disease[J].Swiss Medical Weekly,2012, 142: w13659.DOI:10.4414/smw.2012.13659.
[18] HALLIWELL B.Reactive species and antioxidants.Redox biology is a fundamental theme of aerobic life[J].Plant Physiology, 2006, 141(2): 312-322.DOI:10.1104/pp.106.077073.
[19] CROWE S A, D?SSING L N, BEUKES N J, et al.Atmospheric oxygenation three billion years ago[J].Nature, 2013, 501: 535-538.DOI:10.1038/nature12426.
[20] ILBERT M, BONNEFOY V.Insight into the evolution of the iron oxidation pathways[J].Biochimica et Biophysica Acta, 2013, 1827(2): 161-175.DOI:10.1016/j.bbabio.2012.10.001.
[21] PEREIRA R D, de LONG N E, WANG R C, et al.Angiogenesis in the placenta: the role of reactive oxygen species signaling[J].Biomed Research International, 2015, 2015: 814543.DOI:10.1155/2015/814543.
[22] MURPHY M P.How mitochondria produce reactive oxygen species[J].Biochemical Journal, 2009, 417(1): 1-13.DOI:10.1042/BJ20081386.
[23] GILL S S, TUTEJA N.Reactive oxygen species and antioxidant machinery in abiotic stress tolerance in crop plants[J].Plant Physiology and Biochemistry, 2010, 48(12): 909-930.DOI:10.1016/ j.plaphy.2010.08.016.
[24] MAILLOUX R J, JIN X, WILLMORE W G.Redox regulation of mitochondrial function with emphasis on cysteine oxidation reactions[J].Redox Biology, 2014, 2(1): 123-139.DOI:10.1016/ j.redox.2013.12.011.
[25] ATTIA S M.Deleterious effects of reactive metabolites[J].Oxidative Medicine and Cellular Longevity, 2010, 3(4): 238-253.DOI:10.4161/ oxim.3.4.13246.
[26] MAILLOUX R J.Teaching the fundamentals of electron transfer reactions in mitochondria and the production and detection of reactive oxygen species[J].Redox Biology, 2015, 4: 381-398.DOI:10.1016/ j.redox.2015.02.001.
[27] HAREL A, BROMBERG Y, FALKOWSKI P G, et al.Evolutionary history of redox metal-binding domains across the tree of life[J].Proceedings of the National Academy of Sciences of the United States of America, 2014, 111(19): 7042-7047.DOI:10.1073/ pnas.1403676111.
[28] LANE N.Bioenergetic constraints on the evolution of complex life[J].Cold Spring Harbor Perspectives in Biology, 2014, 6: a015982.DOI:10.1101/cshperspect.a015982.
[29] WALLACE D C.Colloquium paper: bioenergetics, the origins of complexity, and the ascent of man[J].Proceedings of the National Academy of Sciences of the United States of America, 2010,107(Suppl 2): 8947-8953.DOI:10.1073/pnas.0914635107.
[30] FERNIE A R, CARRARI F, SWEETLOVE L J.Respiratory metabolism: glycolysis, the TCA cycle and mitochondrial electron transport[J].Current Opinion in Plant Biology, 2004, 7(3): 254-261.DOI:10.1016/j.pbi.2004.03.007.
[31] LANE N, MARTIN W.The energetics of genome complexity[J].Nature, 2010, 467: 929-934.DOI:10.1038/nature09486.
[32] RAMMAL H, BOUAYED J, SOULIMANI R.A direct relationship between aggressive behavior in the resident/intruder test and cell oxidative status in adult male mice[J].European Journal of Pharmacology, 2010,627(1): 173-176.DOI:10.1016/j.ejphar.2009.11.001.
[33] VALKO M, LEIBFRITZ D, MONCOL J, et al.Free radicals and antioxidants in normal physiological functions and human disease[J].The International Journal of Biochemistry & Cell Biology, 2007,39(1): 44-84.DOI:10.1016/j.biocel.2006.07.001.
[34] BOUAYED J, BOHN T.Exogenous antioxidants: double-edged swords in cellular redox state: health beneficial effects at physiologic doses versus deleterious effects at high doses[J].Oxidative Medicine and Cellular Longevity, 2010, 3(4): 228-237.DOI:10.4161/oxim.3.4.12858.
[35] AMES B N, SHIGENAGA M K, HAGEN T M.Oxidants,antioxidants, and the degenerative diseases of aging[J].Proceedings of the National Academy of Sciences of the United States of America,1993, 90(17): 7915-7922.DOI:10.1073/pnas.90.17.7915.
[36] GüL?IN ?.Antioxidant and antiradical activities of L-carnitine[J].Life Sciences, 2006, 78(8): 803-811.DOI:10.1016/j.lfs.2005.05.103.
[37] CAO G, PRIOR R L.Comparison of different analytical methods for assessing total antioxidant capacity of human serum[J].Clinical Chemistry, 1998, 44(6): 1309-1315.
[38] SPLETTSTOESSER W D, SCHUFF-WERNER P.Oxidative stress in phagocytes: “the enemy within”[J].Microscopy Research and Technique, 2002, 57(6): 441-455.DOI:10.1002/jemt.10098.
[39] SAUNDERS C R, DAS S K, RAMESH A, et al.Benzo(a)pyrene-induced acute neurotoxicity in the F-344 rat: role of oxidative stress[J].Journal of Applied Toxicology, 2006, 26(5): 427-438.DOI:10.1002/jat.1157.
[40] MAIESE K.Environmental stimulus package: potential for a rising oxidative deficit[J].Oxidative Medicine and Cellular Longevity, 2009,2(4): 179-180.DOI:10.4161/oxim.2.4.9733.
[41] MIKI H, FUNATO Y.Regulation of intracellular signalling through cysteine oxidation by reactive oxygen species[J].Journal of Biochemistry, 2012, 151(3): 255-261.DOI:10.1093/jb/mvs006.
[42] VANHOUTTE P M.How we learned to say NO[J].Arteriosclerosis,Thrombosis, and Vascular Biology, 2009, 29(8): 1156-1160.DOI:10.1161/ATVBAHA.109.190215.
[43] BEDARD K, KRAUSE K H.The NOX family of ROS-generating NADPH oxidases: physiology and pathophysiology[J].Physiological Reviews, 2007, 87(1): 245-313.DOI:10.1152/physrev.00044.2005.
[44] WINGLER K, SCHMIDT H.Good stress, bad stress: the delicate balance in the vasculature[J].Deutsches Arzteblatt International, 2009,106(42): 677-684.
[45] GUTTERIDGE J, HALLIWELL B.Antioxidants: molecules,medicines, and myths[J].Biochemical and Biophysical Research Communications, 2010, 393(4): 561-564.DOI:10.1016/ j.bbrc.2010.02.071.
[46] BECKMAN J S.Understanding peroxynitrite biochemistry and its potential for treating human diseases[J].Archives of Biochemistry and Biophysics, 2009, 484(2): 114-116.DOI:10.1016/j.abb.2009.03.013.
[47] MCNALLY J S, DAVIS M E, GIDDENS D P, et al.Role of xanthine oxidoreductase and NAD(P)H oxidase in endothelial superoxide production in response to oscillatory shear stress[J].American Journal of Physiology-Heart and Circulatory Physiology, 2003, 285(6): H2290-H2297.DOI:10.1152/ajpheart.00515.2003.
[48] DALLE-DONNE I, ROSSI R, COLOMBO R, et al.Biomarkers of oxidative damage in human disease[J].Clinical Chemistry, 2006,52(4): 601-623.DOI:10.1373/clinchem.2005.061408.
[49] AFANAS'EV I.Reactive oxygen species and age-related genes p66shc,Sirtuin, FOXO3 and Klotho in senescence[J].Oxidative Medicine and Cellular Longevity, 2010, 3(2): 77-85.DOI:10.4161/oxim.3.2.11050.
[50] ESSICK E E, SAM F.Oxidative stress and autophagy in cardiac disease, neurological disorders, aging and cancer[J].Oxidative Medicine and Cellular Longevity, 2010, 3(3): 168-177.DOI:10.4161/ oxim.3.3.12106.
[51] FRIDOVICH I.Superoxide dismutases[J].Advances in Enzymology & Related Areas of Molecular Biology, 1986, 58(6): 61-97.DOI:10.1002/9780470123041.ch2.
[52] HALLIWELL B.Commentary oxidative stress, nutrition and health.experimental strategies for optimization of nutritional antioxidant intake in humans[J].Free Radical Research, 1996, 25(1): 57-74.DOI:10.3109/10715769609145656.
[53] KINUTA Y, KIMURA M, ITOKAWA Y, et al.Changes in xanthine oxidase in ischemic rat brain[J].Journal of Neurosurgery, 1989, 71(3): 417-420.DOI:10.3171/jns.1989.71.3.0417.
[54] LIPTON P.Ischemic cell death in brain neurons[J].Physiological Reviews, 1999, 79(4): 1431-1568.
[55] HALLIWELL B.Oxidative stress and neurodegeneration: where are we now?[J].Journal of Neurochemistry, 2006, 97(6): 1634-1658.DOI:10.1111/j.1471-4159.2006.03907.x.
[56] SCHRECK R, BAEUERLE P A.Assessing oxygen radicals as mediators in activation of inducible eukaryotic transcription factor NF-кB[J].Methods in Enzymology, 1994, 234(1): 151-163.DOI:10.1016/0076-6879(94)34085-4.
[57] SEN C K, PACKER L.Antioxidant and redox regulation of gene transcription[J].The FASEB Journal, 1996, 10(7): 709-720.
[58] DIPLOCK A T, CHARLEUX J L, CROZIER-WILLI G, et al.Functional food science and defence against reactive oxidative species[J].British Journal of Nutrition, 1998, 80(Suppl 1): 77-112.DOI:10.1079/BJN19980106.
[59] HOU Y C, JANCZUK A, WANG P G.Current trends in the development of nitric oxide donors[J].Current Pharmaceutical Design, 1999, 5(6): 417-441.
[60] BECKMAN J S.Oxidative damage and tyrosine nitration from peroxynitrite[J].Chemical Research in Toxicology, 1996, 9(5): 836-844.DOI:10.1021/tx9501445.
[61] PACKER L.Nitric oxide.Part A: sources and detection of NO; NO synthase[J].Methods in Enzymology, 1996, 268: 331-340.
[62] ESTERBAUER H, GEBICKI J, PUHL H, et al.The role of lipid peroxidation and antioxidants in oxidative modification of LDL[J].Free Radical Biology and Medicine, 1992, 13(4): 341-390.DOI:10.1016/0891-5849(92)90181-F.
[63] REAVEN P D, WITZTUM J L.Oxidized low density lipoproteins in atherogenesis: role of dietary modification[J].Annual Review of Nutrition, 1996, 16(1): 51-71.DOI:10.1146/annurev.nu.16.070196.000411.
[64] VENDITTI P, di STEFANO L, di MEO S.Mitochondrial metabolism of reactive oxygen species[J].Mitochondrion, 2013, 13(2): 71-82.DOI:10.1016/j.mito.2013.01.008.
[65] QUINLAN C L, ORR A L, PEREVOSHCHIKOVA I V, et al.Mitochondrial complex Ⅱ can generate reactive oxygen species at high rates in both the forward and reverse reactions[J].Journal of Biological Chemistry, 2012, 287(32): 27255-27264.DOI:10.1074/jbc.M112.374629.
[66] HOLZEROVá E, PROKISCH H.Mitochondria: Much ado about nothing? How dangerous is reactive oxygen species production?[J].International Journal of Biochemistry & Cell Biology, 2015, 63:16-20.DOI:10.1016/j.biocel.2015.01.021.
[67] QUINLAN C L, PEREVOSHCHIKOVA I V, HEY-MOGENSEN M,et al.Sites of reactive oxygen species generation by mitochondria oxidizing different substrates[J].Redox Biology, 2013, 1(1): 304-312.DOI:10.1016/j.redox.2013.04.005.
[68] TURRENS J F.Mitochondrial formation of reactive oxygen species[J].The Journal of Physiology, 2003, 552(2): 335-344.DOI:10.1113/ jphysiol.2003.049478.
[69] BALABAN R S, NEMOTO S, FINKEL T.Mitochondria, oxidants, and aging[J].Cell, 2005, 120(4): 483-495.DOI:10.1016/j.cell.2005.02.001.
[70] PACKER L, FUEHR K.Low oxygen concentration extends the lifespan of cultured human diploid cells[J].Nature, 1977, 267: 423-425.DOI:10.1038/267423a0.
[71] SERRA V, von ZGLINICKI T, LORENZ M, et al.Extracellular superoxide dismutase is a major antioxidant in human fibroblasts and slows telomere shortening[J].Journal of Biological Chemistry, 2003,278(9): 6824-6830.DOI:10.1074/jbc.M207939200.
[72] SANDERSON T H, REYNOLDS C A, KUMAR R, et al.Molecular mechanisms of ischemia-reperfusion injury in brain: pivotal role of the mitochondrial membrane potential in reactive oxygen species generation[J].Molecular Neurobiology, 2013, 47(1): 9-23.DOI:10.1007/s12035-012-8344-z.
[73] CHANCE B, SIES H, BOVERIS A.Hydroperoxide metabolism in mammalian organs[J].Physiological Reviews, 1979, 59(3): 527-605.
[74] STANIEK K, NOHL H.Are mitochondria a permanent source of reactive oxygen species?[J].Biochimica et Biophysica Acta (BBA)-Bioenergetics, 2000, 1460(2): 268-275.DOI:10.1016/S0005-2728(00)00152-3.
[75] ST-PIERRE J, BUCKINGHAM J A, ROEBUCK S J, et al.Topology of superoxide production from different sites in the mitochondrial electron transport chain[J].Journal of Biological Chemistry, 2002,277(47): 44784-44790.DOI:10.1074/jbc.M207217200.
[76] BAINS M, HALL E D.Antioxidant therapies in traumatic brain and spinal cord injury[J].Biochimica et Biophysica Acta (BBA)-Molecular Basis of Disease, 2012, 1822(5): 675-684.DOI:10.1016/ j.bbadis.2011.10.017.
[77] RADI R.Peroxynitrite reactions and diffusion in biology[J].Chemical Research in Toxicology, 1998, 11(7): 720-721.DOI:10.1021/ tx980096z.
[78] HALL E D, OOSTVEEN J A, ANDRUS P K, et al.Immunocytochemical method for investigating in vivo neuronal oxygen radical-induced lipid peroxidation[J].Journal of Neuroscience Methods, 1997, 76(2): 115-122.DOI:10.1016/S0165-0270(97)00089-7.
[79] DENG Y, THOMPSON B M, GAO X, et al.Temporal relationship of peroxynitrite-induced oxidative damage, calpain-mediated cytoskeletal degradation and neuro-degeneration after traumatic brain injury[J].Experimental Neurology, 2007, 205: 154-165.DOI:10.1016/ j.expneurol.2007.01.023.
[80] KRIVORUCHKO A, STOREY K B.Forever young: mechanisms of natural anoxia tolerance and potential links to longevity[J].Oxidative Medicine and Cellular Longevity, 2010, 3(3): 186-198.DOI:10.4161/ oxim.3.3.12356.
[81] PUNG Y F.Mitochondria in cardiovascular physiology and disease: the role of mitochondrial bioenergetics and reactive oxygen species in coronary collateral growth[J].American Journal of Physiology-Heart and Circulatory Physiology, 2013, 305(9): H1275-H1280.DOI:10.1152/ajpheart.00077.2013.
[82] ABE Y, SAKAIRI T, BEESON C, et al.TGF-β1 stimulates mitochondrial oxidative phosphorylation and generation of reactive oxygen species in cultured mouse podocytes, mediated in part by the mTOR pathway[J].American Journal of Physiology-Renal Physiology,2013, 305(10): F1477-F1490.DOI:10.1152/ajprenal.00182.2013.
[83] JARMUSZKIEWICZ W, WOYDA-PLOSZCZYCA A, KOZIEL A,et al.Temperature controls the oxidative phosphorylation and reactive oxygen species production through uncoupling in rat skeletal muscle mitochondria[J].Free Radical Biology & Medicine, 2015, 83: 12-20.DOI:10.1016/j.freeradbiomed.2015.02.012.
[84] SHEERAN F L, PEPE S.Energy deficiency in the failing heart: linking increased reactive oxygen species and disruption of oxidative phosphorylation rate[J].Biochimica et Biophysica Acta (BBA)-Bioenergetics, 2006, 1757(5): 543-552.DOI:10.1016/ j.bbabio.2006.03.008.
[85] 趙云罡, 徐建興.線粒體, 活性氧和細(xì)胞凋亡[J].生物化學(xué)與生物物理進(jìn)展, 2001, 28(2): 168-171.DOI:10.3321/ j.issn:1000-3282.2001.02.010.
[86] 劉卉, 劉延香.細(xì)胞凋亡與活性氧[J].現(xiàn)代腫瘤醫(yī)學(xué), 2008, 16(10): 1830-1832.DOI:10.3969/j.issn.1672-4992.2008.10.077.
[87] 馬淇, 劉壘, 陳佺.活性氧、線粒體通透性轉(zhuǎn)換與細(xì)胞凋亡[J].生物物理學(xué)報(bào), 2012, 28(7): 523-536.
[88] 魏燕, 辛?xí)匝?活性氧調(diào)控的細(xì)胞凋亡信號(hào)[J].現(xiàn)代腫瘤醫(yī)學(xué), 2011,19(2): 371-373.DOI:10.3969/j.issn.1672-4992.2010.02.62.
[89] 李興太, 劉德文, 張新, 等.線粒體通透性轉(zhuǎn)換與細(xì)胞凋亡[J].中國(guó)公共衛(wèi)生, 2015, 31(4): 529-532.DOI:10.11847/zgggws2015-31-04-45.
[90] CLARK R, KUPPER T.Old meets new: the interaction between innate and adaptive immunity[J].Journal of Investigative Dermatology, 2005,125(4): 629-637.DOI:10.1111/j.0022-202X.2005.23856.x.
[91] TAKEUCHI O, AKIRA S.Pattern recognition receptors and inflammation[J].Cell, 2010, 140(6): 805-820.DOI:10.1016/ j.cell.2010.01.022.
[92] MITTAL M, SIDDIQUI M R, TRAN K, et al.Reactive oxygen species in inflammation and tissue injury[J].Antioxidants & Redox Signaling, 2014, 20(7): 1126-1167.DOI:10.1089/ars.2012.5149.
[93] WALMSLEY S R, McGOVERN N N, WHYTE M K B, et al.The HIF/VHL pathway: from oxygen sensing to innate immunity[J].American Journal of Respiratory Cell and Molecular Biology, 2008,38(3): 251-255.DOI:10.1165/rcmb.2007-0331TR.
[94] P?LSSON-MCDERMOTT E M, O'NEILL L A J.Signal transduction by the lipopolysaccharide receptor, Toll-like receptor-4[J].Immunology, 2004, 113(2): 153-162.DOI:10.1111/j.1365-2567.2004.01976.x.
[95] 朱瑩, 葉嘉, 李強(qiáng).下呼吸道固有免疫防御系統(tǒng)與下呼吸道感染[J].中國(guó)實(shí)用內(nèi)科雜志, 2015, 35(5): 455-458.
[96] YAMAUCHI S, NOGUCHI T, ICHIJO H.Molecular mechanism of reactive oxygen species-dependent ASK1 activation in innate immunity[J].Immune Network, 2008, 8(1): 1-6.DOI:10.4110/ in.2008.8.1.1.
[97] XU J, LUPU F, ESMON C T.Inflammation, innate immunity and blood coagulation[J].Hamostaseologie, 2010, 30(1): 5-6; 8-9.
[98] RYAN K A, SMITH M F, SANDERS M K, et al.Reactive oxygen and nitrogen species differentially regulate Toll-like receptor 4-mediated activation of NF-κB and interleukin-8 expression[J].Infection and Immunity, 2004, 72(4): 2123-2130.DOI:10.1128/iai.72.4.2123-2130.2004.
[99] PARK H S, JUNG H Y, PARK E Y, et al.Cutting edge: direct interaction of TLR4 with NAD(P)H oxidase 4 isozyme is essential for lipopolysaccharide-induced production of reactive oxygen species and activation of NF-κB[J].The Journal of Immunology, 2004, 173(6): 3589-3593.DOI:10.4049/jimmunol.173.6.3589.
[100] HARIJITH A, EBENEZER D L, NATARAJAN V.Reactive oxygen species at the crossroads of inflammasome and inflammation[J].Frontiers in Physiology, 2014, 5: 352.DOI:10.3389/fphys.2014.00352.
[101] FINK S L, COOKSON B T.Apoptosis, pyroptosis, and necrosis: mechanistic description of dead and dying eukaryotic cells[J].Infection and Immunity,2005, 73(4): 1907-1916.DOI:10.1128/iai.73.4.1907-1916.2005.
[102] SAVAGE C D, LOPEZ-CASTEJON G, DENES A, et al.NLRP3-inflammasome activating DAMPs stimulate an inflammatory response in glia in the absence of priming which contributes to brain inflammation after injury[J].Frontiers in Immunology, 2012, 3: 288.DOI:10.3389/fimmu.2012.00288.
[103] DUEWELL P, KONO H, RAYNER K J, et al.NLRP3 inflammasomes are required for atherogenesis and activated by cholesterol crystals[J].Nature, 2010, 464: 1357-1361.DOI:10.1038/nature08938.
[104] JIANG Y, WANG M, HUANG K, et al.Oxidized low-density lipoprotein induces secretion of interleukin-1β by macrophages via reactive oxygen species-dependent NLRP3 inflammasome activation[J].Biochemical and Biophysical Research Communications,2012, 425(2): 121-126.DOI:10.1016/j.bbrc.2012.07.011.
[105] LUHESHI N M, GILES J A, LOPEZ-CASTEJON G, et al.Sphingosine regulates the NLRP3-inflammasome and IL-1β release from macrophages[J].European Journal of Immunology, 2012, 42(3): 716-725.DOI:10.1002/eji.201142079.
[106] BANDYOPADHYAY S, LANE T, VENUGOPAL R, et al.MicroRNA-133a-1 regulates inflammasome activation through uncoupling protein-2[J].Biochemical and Biophysical Research Communications, 2013, 439(3): 407-412.DOI:10.1016/ j.bbrc.2013.08.056.
[107] FUKUMOTO J, FUKUMOTO I, PARTHASARATHY P T, et al.NLRP3 deletion protects from hyperoxia-induced acute lung injury[J].American Journal of Physiology-Cell Physiology, 2013, 305(2): C182-C189.DOI:10.1152/ajpcell.00086.2013.
[108] SCIOR T, ALEXANDER C, ZAEHRINGER U.Reviewing and identifying amino acids of human, murine, canine and equine TLR4/ MD-2 receptor complexes conferring endotoxic innate immunity activation by LPS/lipid A, or antagonistic effects by Eritoran,in contrast to species-dependent modulation by lipid IVa[J].Computational & Structural Biotechnology Journal, 2013, 5(6): 1-13.DOI:10.5936/csbj.201302012.
[109] LIN B, TAN X, LIANG J, et al.A reduction in reactive oxygen species contributes to dihydromyricetin-induced apoptosis in human hepatocellular carcinoma cells[J].Scientific Reports, 2014, 4: 7041.DOI:10.1038/srep07041.
[110] JUNG K H, LEE J H, QUACH C H T, et al.Resveratrol suppresses cancer cell glucose uptake by targeting reactive oxygen speciesmediated hypoxia-inducible factor-1α activation[J].Journal of Nuclear Medicine, 2013, 54(12): 2161-2167.DOI:10.2967/ jnumed.112.115436.
[111] NOGUEIRA V, HAY N.Molecular pathways: reactive oxygen species homeostasis in cancer cells and implications for cancer therapy[J].Clinical Cancer Research, 2013, 19(16): 4309-4314.DOI:10.1158/1078-0432.CCR-12-1424.
[112] WEIDNER C, ROUSSEAU M, PLAUTH A, et al.Melissa officinalis extract induces apoptosis and inhibits proliferation in colon cancer cells through formation of reactive oxygen species[J].Phytomedicine,2015, 22(2): 262-270.DOI:10.1016/j.phymed.2014.12.008.
[113] TRACHOOTHAM D, ALEXANDRE J, HUANG P.Targeting cancer cells by ROS-mediated mechanisms: a radical therapeutic approach?[J].Nature Reviews Drug Discovery, 2009, 8(7): 579-591.DOI:10.1038/nrd2803.
[114] WANG J, YI J.Cancer cell killing via ROS: to increase or decrease, that is the question[J].Cancer Biology & Therapy, 2008, 7(12): 1875-1884.DOI:10.4161/cbt.7.12.7067.
[115] LAURENT A, NICCO C, CHéREAU C, et al.Controlling tumor growth by modulating endogenous production of reactive oxygen species[J].Cancer Research, 2005, 65(3): 948-956.
[116] BENHAR M, ENGELBERG D, LEVITZKI A.ROS, stress-activated kinases and stress signaling in cancer[J].EMBO Reports, 2002, 3(5): 420-425.DOI:10.1093/embo-reports/kvf094.
[117] NISHIDA N, YASUI H, NAGANE M, et al.3-Methyl pyruvate enhances radiosensitivity through increasing mitochondria-derived reactive oxygen species in tumor cell lines[J].Journal of Radiation Research, 2014, 55(3): 455-463.DOI:10.1093/jrr/rrt142.
[118] CERNA D, LI H, FLAHERTY S, et al.Inhibition of nicotinamide phosphoribosyltransferase (NAMPT) activity by small molecule GMX1778 regulates reactive oxygen species (ROS)-mediated cytotoxicity in a p53- and nicotinic acid phosphoribosyltransferase1 (NAPRT1)-dependent manner[J].Journal of Biological Chemistry,2012, 287(26): 22408-22417.DOI:10.1074/jbc.m112.357301.
[119] WATSON J.Oxidants, antioxidants and the current incurability of metastatic cancers[J].Open Biology, 2013, 3(1): 120144.DOI:10.1098/rsob.120144.
[120] MAO L, WERTZLER K J, MALONEY S C, et al.HMGA1 levels influence mitochondrial function and mitochondrial DNA repair efficiency[J].Molecular and Cellular Biology, 2009, 29(20): 5426-5440.DOI:10.1128/MCB.00105-09.
[121] SUN X, AI M, WANG Y, et al.Selective induction of tumor cell apoptosis by a novel P450-mediated reactive oxygen species (ROS) inducer methyl 3-(4-nitrophenyl) propiolate[J].Journal of Biological Chemistry, 2013, 288(13): 8826-8837.DOI:10.1074/jbc.M112.429316.
[122] TRACHOOTHAM D, ZHOU Y, ZHANG H, et al.Selective killing of oncogenically transformed cells through a ROS-mediated mechanism by β-phenylethyl isothiocyanate[J].Cancer Cell, 2006, 10(3): 241-252.DOI:10.1016/j.ccr.2006.08.009.
[123] BARBIERI D, GRASSILLI E, MONTI D, et al.D-ribose and deoxy-D-ribose induce apoptosis in human quiescent peripheral blood mononuclear cells[J].Biochemical and Biophysical Research Communications, 1994,201(3): 1109-1116.DOI:10.1006/bbrc.1994.1820.
[124] CERUTI S, BARBIERI D, VERONESE E, et al.Different pathways of apoptosis revealed by 2-chloro-adenosine and deoxy-D-ribose in mammalian astroglial cells[J].Journal of Neuroscience Research, 1997, 47(4): 372-383.DOI:10.1002/(SICI)1097-4547(19970215)47:4%3C372::AID-JNR2%3E3.0.CO;2-B.
[125] XIAO D, LEW K L, ZENG Y, et al.Phenethyl isothiocyanate-induced apoptosis in PC-3 human prostate cancer cells is mediated by reactive oxygen species-dependent disruption of the mitochondrial membrane potential[J].Carcinogenesis, 2006, 27(11): 2223-2234.DOI:10.1093/ carcin/bgl087.
[126] WARBURG O.On the origin of cancer cells[J].Science, 1956, 123: 309-314.DOI:10.1126/science.123.3191.309.
[127] BONUCCELLI G, TSIRIGOS A, WHITAKER-MENEZES D, et al.Ketones and lactate “fuel” tumor growth and metastasis: Evidence that epithelial cancer cells use oxidative mitochondrial metabolism[J].Cell Cycle, 2010, 9(17): 3506-3514.DOI:10.4161/cc.9.17.12731.
[128] LIM H Y, HO Q S, LOW J, et al.Respiratory competent mitochondria in human ovarian and peritoneal cancer[J].Mitochondrion, 2011,11(3): 437-443.DOI:10.1016/j.mito.2010.12.015.
[129] FANTIN V R, ST-PIERRE J, LEDER P.Attenuation of LDH-A expression uncovers a link between glycolysis, mitochondrial physiology, and tumor maintenance[J].Cancer Cell, 2006, 9(6): 425-434.DOI:10.1016/j.ccr.2006.04.023.
[130] GOGVADZE V, ORRENIUS S, ZHIVOTOVSKY B.Mitochondria in cancer cells: what is so special about them?[J].Trends in Cell Biology,2008, 18(4): 165-173.DOI:10.1016/j.tcb.2008.01.006.
[131] SHYH-CHANG N, ZHU H, de SOYSA T Y, et al.Lin28 enhances tissue repair by reprogramming cellular metabolism[J].Cell, 2013,155(4): 778-792.DOI:10.1016/j.cell.2013.09.059.
[132] LIU W, BECK B H, VAIDYA K S, et al.Metastasis suppressor KISS1 seems to reverse the Warburg effect by enhancing mitochondrial biogenesis[J].Cancer Research, 2014, 74(3): 954-963.DOI:10.1158/0008-5472.CAN-13-1183.
[133] LI Xingtai, ZHAO Jia.Cancer-preventive mechanism from the perspective of effects of the Astragalus polysaccharides on mitochondrial energy metabolism improvement[M].Brisbane: iConcept Press, 2014: 141-180.
[134] SENA L A, CHANDEL N S.Physiological roles of mitochondrial reactive oxygen species[J].Molecular Cell, 2012, 48(2): 158-167.DOI:10.1016/j.molcel.2012.09.025.
[135] WU C M, CHENG Y L, DAI Y H, et al.α-Tocopherol protects keratinocytes against ultraviolet A irradiation by suppressing glutathione depletion, lipid peroxidation and reactive oxygen species generation[J].Biomedical Reports, 2014, 2(3): 419-423.
[136] WANG L, ZHAO X, WEI B Y, et al.Insulin improves osteogenesis of titanium implants under diabetic conditions by inhibiting reactive oxygen species overproduction via the PI3K-Akt pathway[J].Biochimie, 2015, 108: 85-93.DOI:10.1016/j.biochi.2014.10.004.
[137] de CAVANAGH E M V, INSERRA F, FERDER L.Angiotensin II blockade: a strategy to slow aging by protecting mitochondria?[J].Cardiovascular Research, 2011, 89(1): 31-40.DOI:10.1093/cvr/ cvq285.
[138] NAVARRO A, BOVERIS A.The mitochondrial energy transduction system and the aging process[J].American Journal of Physiology-Cell Physiology, 2007, 292(2): C670-C686.
[139] HUNT N D, HYUN D H, ALLARD J S, et al.Bioenergetics of aging and calorie restriction[J].Ageing Research Reviews, 2006, 5(2): 125-143.DOI:10.1016/j.arr.2006.03.006.
[140] HALESTRAP A P, CLARKE S J, KHALIULIN I.The role of mitochondria in protection of the heart by preconditioning[J].Biochimica et Biophysica Acta (BBA)-Bioenergetics, 2007, 1767(8): 1007-1031.DOI:10.1016/j.bbabio.2007.05.008.
[141] KIM J, WEI Y, SOWERS J R.Role of mitochondrial dysfunction in insulin resistance[J].Circulation Research, 2008, 102(4): 401-414.DOI:10.1161/CIRCRESAHA.107.165472.
[142] HüTTEMANN M, LEE I, SAMAVATI L, et al.Regulation of mitochondrial oxidative phosphorylation through cell signaling[J].Biochimica et Biophysica Acta (BBA)-Molecular Cell Research, 2007,1773(12): 1701-1720.DOI:10.1016/j.bbamcr.2007.10.001.
[143] FERNANDES M A S, MARQUES R J F, VICENTE J A F, et al.Sildenafil citrate concentrations not affecting oxidative phosphorylation depress H2O2generation by rat heart mitochondria[J].Molecular and Cellular Biochemistry, 2008, 309(1/2): 77-85.DOI:10.1007/s11010-007-9645-9.
大連民族大學(xué)人才引進(jìn)科研項(xiàng)目(20116126)
DOI:10.7506/spkx1002-6630-201613046 10.7506/spkx1002-6630-201613046 http://www.spkx.net.cn
中圖分類號(hào):Q505
文獻(xiàn)標(biāo)志碼:A
文章編號(hào):1002-6630(2016)13-0257-14
收稿日期:2015-05-10
基金項(xiàng)目:大連市科學(xué)技術(shù)計(jì)劃項(xiàng)目(2013E15SF131);大興安嶺地區(qū)科技計(jì)劃項(xiàng)目博士后基金資助項(xiàng)目(LRB10-316);
作者簡(jiǎn)介:李興太(1966—),男,副教授,博士,研究方向?yàn)楣δ苁称芳爸兴幘€粒體生化藥理。E-mail:xtli@dlnu.edu.cn
Advances in Generation of Reactive Oxygen Species Associated with Health and Diseases
LI Xingtai1, ZHANG Chunying2, ZHONG Weili2, GAO Mingbo1
(1.College of Life Science, Dalian Nationalities University, Dalian 116600, China;2.Heilongjiang Daxing'anling Academy of Agriculture and Forestry Sciences, Jiagedaqi 165000, China)
Abstract:Historically, reactive oxygen species (ROS) are thought to exclusively cause cellular damage and physiological dysfunctions.The accumulation of ROS and oxidative damage has been linked to multiple pathologies, including neurodegenerative diseases, diabetes, cancer, and premature aging.Accumulating evidence in recent years suggests that ROS are critical for health.In physiological conditions, ROS are considered as a signaling molecule produced at low level and in a transient manner.On the other hand, over-production of ROS, associated with the dysfunction of ROS buffering systems, can lead to the development of chronic diseases.Thus, chronic ROS release participates in the occurrence of over 100 kinds of diseases, including major diseases that threaten human health, such as cancer, cardiovascular diseases, diabetes,neurodegenerative diseases (Parkinson's and Alzheimer's diseases), acquired immune defciency syndrome, stroke and aging.This paper reviewes the latest progress in the presence of oxygen on earth and the evolution of aerobic eukaryotic organisms,ROS types, physiological and pathological pleiotropy of ROS, the major ROS in the body, the generation and reactions of ROS, the association of ROS with mitochondrial oxidative phosphorylation, apoptosis, immune defense, infammation and cancers.Given the importance of ATP and ROS to life, we propose that the balance between the generation of ATP and ROS by regulation of mitochondrial oxidative phosphorylation will be the key to human health.
Key words:reactive oxygen species; mitochondria; signal transduction; redox balance; health

