布洛芬緩釋片中布洛芬含量測(cè)定方法的優(yōu)化
王 博, 吳杰連, 吳明明
(江西科技師范大學(xué)藥學(xué)院,江西南昌 330013)
?
布洛芬緩釋片中布洛芬含量測(cè)定方法的優(yōu)化
王 博, 吳杰連*, 吳明明
(江西科技師范大學(xué)藥學(xué)院,江西南昌 330013)
摘要[目的]建立布洛芬緩釋片的含量測(cè)定的最佳方法。[方法]采用紫外分光光度法(檢測(cè)波長(zhǎng)為263 nm)和高效液相色譜法(色譜柱為Agilent C18,流速為1.0 mL/min,檢測(cè)波長(zhǎng)263 nm)測(cè)定布洛芬緩釋片中布洛芬的含量,最終確定布洛芬緩釋片中布洛芬含量的最佳質(zhì)量控制方法。[結(jié)果]以流動(dòng)相為乙酸銨緩沖液∶乙腈(40∶60)的HPLC方法最佳,布洛芬質(zhì)量在1.05~6.30 μg范圍內(nèi)線性關(guān)系很好(r=1.000 0),平均回收率為99.71%,RSD=1.14%,重現(xiàn)性好。[結(jié)論]采用高效液相色譜法測(cè)定布洛芬緩釋片含量最佳,該方法操作簡(jiǎn)單、分離效果好、重現(xiàn)性好、靈敏度高。
關(guān)鍵詞布洛芬緩釋片;紫外分光光度法;HPLC法;含量測(cè)定;優(yōu)化
布洛芬緩釋片在臨床上一般用于解熱鎮(zhèn)痛[1-2],其作用機(jī)理是通過(guò)抑制環(huán)氧化物酶作用而抑制前列腺素的合成與釋放,從而起到鎮(zhèn)痛和抗炎等作用[3-4]。目前,藥品中布洛芬含量的測(cè)定方法主要有化學(xué)計(jì)量法[5]、酸堿滴定法[6]、紫外分光光度法[7]、離子色譜法[8]、高效液相色譜法[9]等,每種方法均有其各自的優(yōu)缺點(diǎn),《中國(guó)藥典(二部)》中采用酸堿滴定法測(cè)定含量,此方法誤差較大,且操作過(guò)程易造成樣品損失。為了進(jìn)一步完善布洛芬的質(zhì)量控制方法,近幾年較多學(xué)者采用高效液相色譜和紫外分光光度法測(cè)定布洛芬的含量[7,9],并在藥物分析中得到日趨廣泛的應(yīng)用,但針對(duì)這2種方法沒有進(jìn)行系統(tǒng)的比較。筆者通過(guò)優(yōu)化HPLC的流動(dòng)相,確定最佳色譜條件測(cè)定布洛芬緩釋片中布洛芬的含量,并與紫外分光光度法比較,最終確定布洛芬緩釋片中布洛芬含量的最佳質(zhì)量控制方法。
1材料和方法
1.1材料布洛芬對(duì)照品(中國(guó)藥品生物制品檢定所,批號(hào)100179-200804,供HPLC測(cè)定,含量99.5%;供UV測(cè)定,含量為100.0%),布洛芬緩釋片(標(biāo)示量0.3g,西南藥業(yè)股份有限公司,批號(hào)為國(guó)藥準(zhǔn)字H20013193);Agilent1100高效液相色譜儀(美國(guó)),AgilentC18色譜柱(150mm×4.6mm,5μm);日本島津UV-265紫外分光光度計(jì);垂熔玻璃漏斗;堿式滴定管;乙腈和甲醇為色譜純,其他試劑均為分析純。
1.2方法
1.2.1色譜條件和系統(tǒng)適用性試驗(yàn)。色譜柱為AgilentC18柱(150mm×4.6mm,5μm),檢測(cè)波長(zhǎng)263nm,進(jìn)樣量10μL,流速1.0mL/min,柱溫25 ℃,流動(dòng)相分別為Ⅰ甲醇∶磷酸二氫鉀∶磷酸(700∶300∶0.1)、Ⅱ乙腈:0.01mol/L磷酸溶液(40∶60)、Ⅲ乙酸銨緩沖液(稱取乙酸銨5.762 2g,加水750mL,振動(dòng)溶解,用冰醋酸調(diào)pH至2.5)∶乙腈(40∶60)[10-11]。
1.2.2溶液制備。
1.2.2.1對(duì)照品溶液的制備及對(duì)照品處理方法的選擇。稱取布洛芬對(duì)照品10.50和5.68mg,分別置2個(gè)25mL容量瓶中,在分別用100%和60%甲醇稀釋至刻度,超聲濾過(guò)。分別吸取10μL,按“1.2.1”色譜條件,分別以Ⅰ、Ⅱ、Ⅲ 3種流動(dòng)相進(jìn)行試驗(yàn)。當(dāng)改用60%甲醇處理時(shí),以“1.2.1”色譜條件,乙酸銨緩沖液∶乙腈(40∶60)為流動(dòng)相,同樣進(jìn)樣10μL進(jìn)行試驗(yàn)。
1.2.2.2供試品溶液的制備。先取布洛芬10片,精密稱其總重量3.301g,其平均每片重為0.330g,再精密稱取布洛芬緩釋片5.50mg,置于10mL容量瓶中,加60%甲醇適量,超聲15min,用60%甲醇稀釋至刻度,搖勻?yàn)V過(guò),即得。
1.2.3高效液相色譜法。
1.2.3.1線性關(guān)系考察。以“1.2.1”色譜條件,將2種不同濃度甲醇制備好的對(duì)照品溶液分別精密量取2.5、5.0、7.5、10.0、12.5、15.0μL進(jìn)樣,以各溶液的進(jìn)樣體積為橫坐標(biāo)、峰面積積分值為縱坐標(biāo)繪制標(biāo)準(zhǔn)曲線,計(jì)算回歸方程。
1.2.3.2精密度試驗(yàn)。以“1.2.1”色譜條件,取對(duì)照品溶液連續(xù)進(jìn)樣5次,進(jìn)樣量為10μL,以外標(biāo)法計(jì)算樣品的含量。
1.2.3.3重復(fù)性試驗(yàn)。取同一批號(hào)樣品,精密稱量布洛芬緩釋片5份,各約15mg,按“1.2.1”色譜條件操作,平行進(jìn)樣5次,測(cè)其含量樣品進(jìn)行方法重現(xiàn)性試驗(yàn)。
1.2.3.4回收率試驗(yàn)。精密稱取已知布洛芬含量的樣品7份(相當(dāng)布洛芬10mg),每份加入布洛芬對(duì)照品10mg的溶液,按“1.2.2.2”供試品溶液制備方法制備,在“1.2.1”色譜條件下測(cè)定含量,計(jì)算回收率。
1.2.3.5樣品含量的測(cè)定。分別稱取布洛芬樣品5.03、5.19、5.24mg樣品,置10mL容量瓶中,用60%甲醇稀釋至刻度,超聲濾過(guò)。分別吸取10μL,在選定的色譜條件下測(cè)定布洛芬的峰面積,計(jì)算布洛芬的含量。標(biāo)示量(%)=Cx×D×w/W×B×100%,式中,Cx為樣品的濃度;D為稀釋體積;w為平均片重;W為供試品的稱取量;B為制劑的標(biāo)示量。
1.2.4紫外分光光度法。
1.2.4.1線性關(guān)系考察。精密稱取布洛芬對(duì)照品36.48mg,置于100mL容量瓶中,加0.4%氫氧化鈉溶液超聲并過(guò)濾。再量取濾液2、4、6、8、10mL分別置10mL量瓶中,加0.4%氫氧化鈉溶液稀釋至刻度,搖勻后按照“1.2.1”色譜條件測(cè)定吸光度[12]。
1.2.4.2精密度試驗(yàn)。在“1.2.1”色譜條件下,精密量取樣品溶液10μL,連續(xù)進(jìn)樣5次,測(cè)峰面積和RSD。
1.2.4.3重復(fù)性試驗(yàn)。取同一樣品7份,按“1.2.1”色譜條件操作,平行進(jìn)樣7次,評(píng)價(jià)試驗(yàn)重現(xiàn)性。
1.2.4.4樣品含量測(cè)定。精密稱取布洛芬樣品33.45、34.04、33.88mg,置于100mL容量瓶中,加入0.4%氫氧化鈉溶液超聲30min,稀釋至刻度,過(guò)濾,測(cè)定吸收值,按回歸方程計(jì)算含量。
2結(jié)果與分析
2.1流動(dòng)相的選取按照“1.2.1”色譜條件和方法,分別以Ⅰ甲醇:磷酸二氫鉀:磷酸(700∶300∶0.1)、Ⅱ乙腈:0.01mol/L磷酸溶液(40∶60)、Ⅲ乙酸銨緩沖液∶乙腈(40∶60)3種流動(dòng)相進(jìn)行試驗(yàn)。結(jié)果顯示(圖1),在其他色譜條件相同的情況下,乙酸銨緩沖液∶乙腈(40∶60)為流動(dòng)相效果最好,故以Ⅲ流動(dòng)相測(cè)定布洛芬含量。
2.2對(duì)照品處理方法的選擇由圖2可見,使用不同濃度的甲醇溶解對(duì)對(duì)照品主峰的峰形有一定的影響,對(duì)照品采用60%甲醇溶解測(cè)得峰面積大于純甲醇溶解的峰面積,故測(cè)得60%甲醇溶解的含量較高,說(shuō)明布洛芬在60%甲醇中的溶解率大于純甲醇,故采用60%甲醇作為對(duì)照品和樣品的前處理溶劑,能取得更佳的提取率。
2.3高效液相色譜試驗(yàn)
2.3.1方法學(xué)考察。按照線性范圍考查方法,測(cè)得回歸方程為Y=39.146x+0.359(r=1.000),說(shuō)明布洛芬質(zhì)量在1.05~6.30μg范圍內(nèi)線性關(guān)系良好(圖3)。按精密度試驗(yàn)方法,測(cè)得色譜峰面積平均值為357.71,RSD為0.576%,表明精密度很好。按重復(fù)性試驗(yàn)方法操作,得出RSD為0.56%,表明該方法重現(xiàn)性良好。按回收率試驗(yàn)方法測(cè)定,結(jié)果發(fā)現(xiàn)(表1),平均回收率為99.71%,RSD=1.14%(n=7)。
2.3.2樣品含量的測(cè)定。按“1.2.3.5”方法操作,測(cè)得布洛芬的峰面積分別為306.01、330.48、335.29,通過(guò)HPLC測(cè)定布洛芬的含量分別為96.9%、101.3%和102.0%。

注:a.甲醇∶磷酸二氫鉀∶磷酸(700∶300∶0.1);b.乙腈:0.01 mol/L磷酸溶液(40∶60);c.乙酸銨緩沖液∶乙腈(40∶60)。Note: a. Methanol∶monopotassium phosphate∶phosphoric acid (700∶300∶0.1); b. Acetonitrile:0.01 mol/L phosphoric acid (40∶60); c. Ammonium acetate buffer∶acetonitrile (40∶60).圖1 不同流動(dòng)相的對(duì)照品溶液HPLC圖Fig. 1 HPLC of control solutions with different mobile phases
2.4紫外分光光度試驗(yàn)
2.4.1線性關(guān)系考察。按照“1.2.4.1”方法操作,測(cè)得5種不同體積的樣品在263nm波長(zhǎng)處吸光值分別為0.151、0.210、0.420、0.542和0.683。以濃度C(mg/L)為橫坐標(biāo)、吸光度A為縱坐標(biāo)進(jìn)行線性回歸,得方程A=1.816 1C+0.017 9(r=0.999 7),說(shuō)明布洛芬在0.07~0.36mg/L內(nèi)吸光度和溶液的濃度呈良好的線性關(guān)系。
2.4.2精密度試驗(yàn)。按“1.2.4.2”方法操作,得色譜峰面積平均值為357.71,RSD為0.576%,表明紫外分光光度計(jì)精密度很好。
2.4.3重復(fù)性試驗(yàn)。按“1.2.4.3”方法操作,測(cè)定7份樣品吸光值,計(jì)算布洛芬含量為0.21%,RSD為1.05%,說(shuō)明該方法重現(xiàn)性良好。
2.2.4樣品含量測(cè)定。按“1.2.4.4”方法操作,測(cè)得3份布洛芬吸收值分別為0.595、0.608、0.602,按回歸方程計(jì)算布洛芬含量分別為103.3%、103.9%和103.2%。

圖2 純甲醇(a)和60%甲醇(b)溶解后的對(duì)照品溶液HPLC圖Fig. 2 HPLC of reference solutions after dissolved by pure methanol (a) and 60% methanol (b)
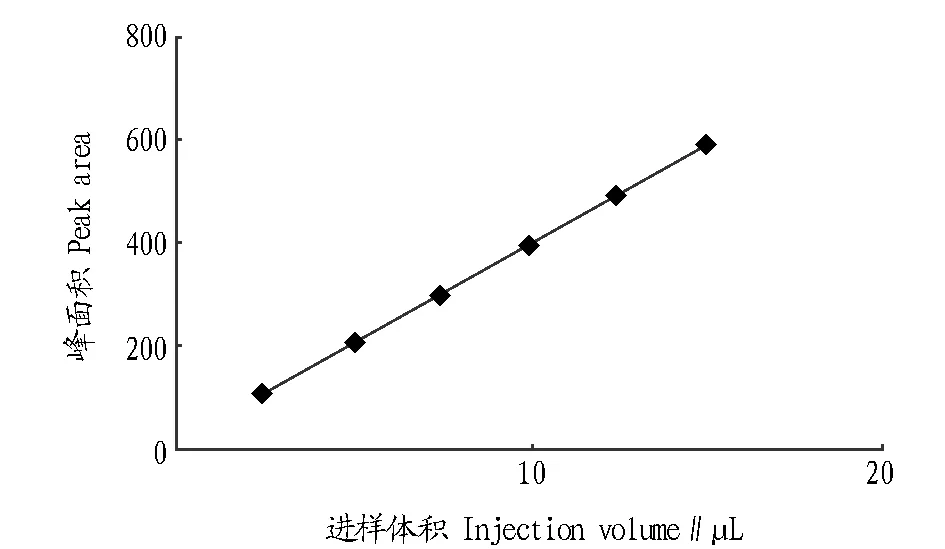
圖3 對(duì)照品溶液標(biāo)準(zhǔn)曲線Fig. 3 Standard curve of reference solution
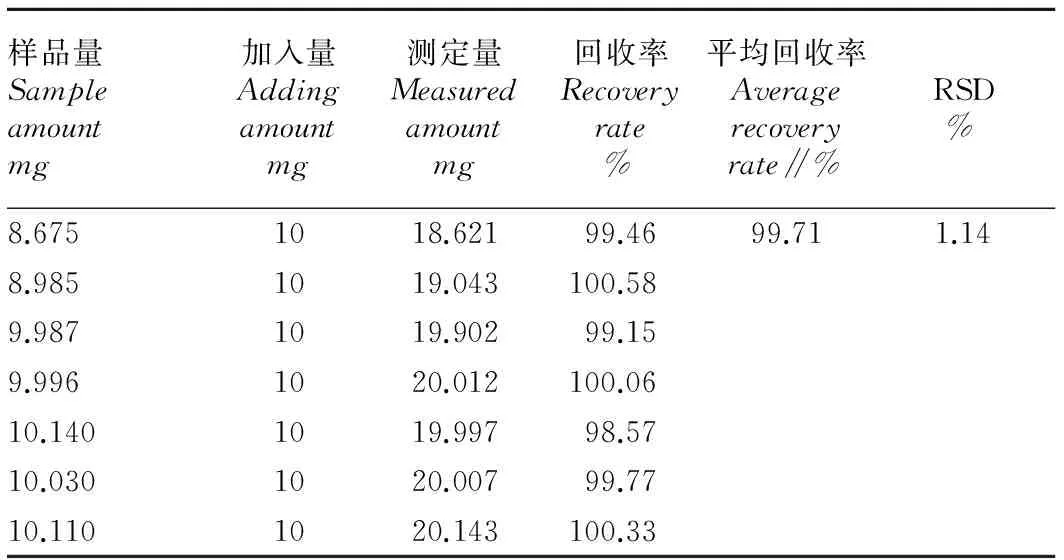
樣品量Sampleamountmg加入量Addingamountmg測(cè)定量Measuredamountmg回收率Recoveryrate%平均回收率Averagerecoveryrate∥%RSD%8.6751018.62199.4699.711.148.9851019.043100.589.9871019.90299.159.9961020.012100.0610.1401019.99798.5710.0301020.00799.7710.1101020.143100.33
3小結(jié)與討論
該試驗(yàn)通過(guò)優(yōu)化HPLC的流動(dòng)相,確定最佳色譜條件測(cè)定布洛芬緩釋片中布洛芬的含量,并與紫外分光光度法比較。結(jié)果發(fā)現(xiàn),使用不同濃度的甲醇溶解對(duì)對(duì)照品主峰的峰形有一定的影響,對(duì)照品選用60%甲醇溶解較好,且以流動(dòng)相為乙酸銨緩沖液∶乙腈(40∶60)的HPLC方法最佳,布洛芬在1.05~6.30μg范圍內(nèi)線性關(guān)系很好,平均回收率為99.71%,RSD=1.14%,重現(xiàn)性好。在紫外分光光度試驗(yàn)中,4-異丁基苯乙酮結(jié)構(gòu)上存在共軛體系并在263nm的吸收遠(yuǎn)遠(yuǎn)強(qiáng)于布洛芬,如用自身對(duì)照法進(jìn)行雜質(zhì)控制是不合適的,需采用雜質(zhì)對(duì)照品法試驗(yàn)。雖然2種方法測(cè)定布洛芬含量相差較小,但從2種方法與其試驗(yàn)過(guò)程可知,紫外分光光度法采用不同濃度的氫氧化鈉溶液處理樣品會(huì)影響測(cè)定結(jié)果,200~400nm波長(zhǎng)下掃描,效果不理想;HPLC法能夠排除有關(guān)輔料物質(zhì)及人為誤差的干擾,專屬性強(qiáng),該方法操作簡(jiǎn)便、重現(xiàn)性好、實(shí)用性強(qiáng),可作為布洛芬緩釋片中布洛芬含量的質(zhì)量控制方法。
參考文獻(xiàn)
[1] 劉忠,宋紅萍,徐雋,等.高效液相色譜法測(cè)定布洛芬注射液的含量及有關(guān)物質(zhì)[J].中國(guó)醫(yī)院藥學(xué)雜志,2009,29(10):856-858.
[2] 張軼突,陳堯,誶志榮,等.布洛芬緩釋膠嚢單劑量與多劑量給藥的人體藥代動(dòng)力學(xué)及生物等效性研究[J].中國(guó)臨床藥理學(xué)與治療學(xué),2014,19(3):297-301.
[3]CHENWW,HUXH,HONGYZ,etal.Ibupro-fennanoparticlespreparedbyaPGSSTM-basedmethod[J].Powdertechnology,2013,245(2):241-250.
[4]ORTEGA-ALVAROA,BERROCOSOE,REY-BREAR,etal.Comparisonoftheantinociceptiveeffectsofibuprofenarginateandibu-profeninratmodelsofinflammatoryandneuropathicpain[J].Lifesciences,2012,90(1/2):13-20.
[5] 雷艷虹,梁淑彩,葉姍.化學(xué)計(jì)量學(xué)法測(cè)定阿司匹林與布洛芬[J].四川理工學(xué)院學(xué)報(bào)(自然科學(xué)版),2008,21(4):65-67.
[6] 國(guó)家藥典委員會(huì).中華人民共和國(guó)藥典:二部[S].北京:化學(xué)工業(yè)出版社,2005: 96.
[7]KHOSHAYANDMR,ABDOLLAHIH,SHARIATPANAHIM,etal.Simultaneousspectrophotometricdeterminationofparac-etamol,ibuprofenandcaffeineinpharmaceuticalsbyche-mometricmethods[J].SpectrochimicaactapartA:Moiecularandbiomolecularspectroscopy,2008,70(3):491-499.
[8] 傅厚暾,周姣.離子色譜法分析布洛芬片劑中的布洛芬含量[J].分析化學(xué),2001(7):46-47.
[9]RAODD,RAOLPV,SAITLSS,etal.Simultaneousdeterminationofibuprofenanddiphen-hydraminecitrateintabletsbyvalidatedLC[J].Chromatographia,2009,69(9):1133-1136.
[10] 尹輝,胡容峰,高宇,等.右旋布洛芬緩釋片的含量測(cè)定及體外釋放特性研究[J].安徽中醫(yī)學(xué)院學(xué)報(bào),2010,29(1):60-63.
[11] 國(guó)家藥典委員會(huì).中華人民共和國(guó)藥典:2010年版一部[S].北京:化學(xué)工業(yè)出版社,2010:120.
[12] 譚博,趙悅輝.紫外分光光度法測(cè)定布洛芬片的含量[J].中國(guó)藥業(yè),2007,16(23):21.
作者簡(jiǎn)介王博(1992- ),男,河南周口人,碩士研究生,研究方向:藥物分析。*通訊作者,講師,碩士,從事海洋活性物質(zhì)篩選研究。
收稿日期2016-04-10
中圖分類號(hào)R 971+.1
文獻(xiàn)標(biāo)識(shí)碼A
文章編號(hào)0517-6611(2016)16-119-03
OptimizationofthedetectionofIbuprofenContentinIbuprofenSustainedReleaseTablet
WANGBo,WUJie-lian*,WUMing-ming
(CollegeofPharmacy,JiangxiScienceandTechnologyNormalUniversity,Nanchang,Jiangxi330013)
Abstract[Objective] To establish the optimal method for the content determination in ibuprofen sustained release tablet. [Method] Ultraviolet spectrophotometry (263 nm detection wavelength) and HPLC method (Agilent C18chromatographic column, 1.0 mL/min flow rate, 263 nm detection wavelength) were used to detect the content of ibuprofen in ibuprofen sustained release tablet. The optimal quality control method was finally established to determine the ibuprofen content in ibuprofen sustained release tablet. [Result] When the mobile phase was ammonium acetate :acetonitrile (40∶60), HPLC method was the optimal. There were good linear relationship when the ibuprofen was within the range of 1.05- 6.3 μg (r = 1.000 0). The average recovery rate was 99.71% with RSD=1.14% and good reproducibility. [Conclusion] The optimal content of ibuprofen sustained release tablet is detected by HPLC method. This method is simple and effective, with good reproducibility and high sensitivity.
Key wordsIbuprofen sustained release tablets; Ultraviolet spectrophotometry; HPLC method; Content determination; Optimization

