雷帕霉素的三氮唑新衍生物FIM-X13對人胃癌細胞株AGS的作用及機制的初步研究
楊丹,陳曉明,李夸良,謝立君,潘福生,黃捷
?
雷帕霉素的三氮唑新衍生物FIM-X13對人胃癌細胞株AGS的作用及機制的初步研究
楊丹,陳曉明,李夸良,謝立君,潘福生,黃捷
【摘要】
目的研究雷帕霉素的三氮唑新衍生物 FIM-X13 對人胃癌細胞株 AGS 的作用,探討其作用機制并分別與雷帕霉素和依維莫司比較。
方法磺酰羅丹明 B 檢測 FIM-X13 對 AGS 增殖的抑制活性;流式細胞術檢測 FIM-X13 對 AGS 細胞凋亡及周期影響;Western blot 分析 AGS 細胞內 mTOR、p70S6K1、S6 和 4EBP1 的磷酸化水平。
結果FIM-X13 能顯著抑制 AGS 細胞的增殖,IC50為(9.32 ± 0.70)μmol/L,抑制能力強于雷帕霉素和依維莫司;FIM-X13 能顯著誘導 AGS 細胞凋亡及阻滯細胞周期于G1期,其誘導 AGS 細胞凋亡和阻滯細胞周期的能力均強于雷帕霉素及依維莫司;FIM-X13 能顯著抑制 AGS 細胞內 mTOR、p70S6K1、S6 和 4EBP1 的磷酸化,抑制能力與雷帕霉素和依維莫司相當。
結論雷帕霉素的三氮唑新衍生物 FIM-X13 對人胃癌細胞株 AGS 的抑制活性強于雷帕霉素和依維莫司。與雷帕霉素和依維莫司一樣,FIM-X13 主要通過抑制 AGS 的mTOR 信號通路抑制細胞增殖、誘導細胞凋亡及阻滯細胞周期于 G1期等發揮抗腫瘤作用。
【關鍵詞】胃腫瘤;哺乳動物雷帕霉素靶蛋白;雷帕霉素三氮唑衍生物
www.cmbp.net.cn中國醫藥生物技術, 2016, 11(3):224-228
作者單位:350122 福州,福建中醫藥大學藥學院(楊丹、黃捷);350007福州,福建省微生物研究所(楊丹、陳曉明、李夸良、謝立君、黃捷);310012 杭州華東醫藥集團新藥研究院有限公司(潘福生)
哺乳動物雷帕霉素靶蛋白(mTOR)是一種保守的絲-蘇氨酸蛋白激酶,直接或間接參與細胞增殖、生長和代謝有關環節的調控,處于復雜的細胞內信號轉導途徑的中心,mTOR 信號轉導途徑過度激活與腫瘤細胞的生長、增殖、代謝和轉移密切相關[1]。mTOR 抑制劑雷帕霉素衍生物依維莫司和替西羅莫司已作為抗癌藥物應用于臨床。
胃癌是常見惡性腫瘤之一,世界范圍內的發病率和死亡率一直居高不下[2]。研究表明,60% ~ 80%胃癌中存在 mTOR 信號通路過度激活[3],激活與mTOR 上游的關鍵蛋白基因如 PIK3R3[4]、PIK3CA[5]和 PTEN[6-7]等突變及與 mTOR 相關的信號通路失調[8]有關。依維莫司治療胃癌的 I/II 期臨床試驗已取得較好效果[9-10]。本文報道雷帕霉素的三氮唑新衍生物 FIM-X13 對胃癌細胞株 AGS的作用,與雷帕霉素和依維莫司進行比較,探討其用于治療胃癌的可能性。
1 材料與方法
1.1材料
人胃癌細胞株 AGS 購自中科院上海細胞庫;FIM-X13(純度 > 95%)由福建省微生物研究所合成,雷帕霉素(純度 > 95%)由福建科瑞藥業有限公司生產,依維莫司(純度 > 95%)購自成都雅途生物醫藥公司,三種化合物用二甲基亞砜(DMSO)配成 1 mmol/L 儲存液,-20℃ 保存;兔抗 mTOR、p-mTOR(Ser2448)、p70S6K1、p-p70S6K1(Thr389)、4EBP1、p-4EBP1(Ser65)、S6、p-S6(Ser235/236)和 GAPDH 抗體購自美國 Cell Signaling Technology公司;HRP 標記的兔抗羊 IgG 二抗購自美國Bioworld Technology 公司;F12 培養基、胎牛血清、消化胰酶和磷酸鹽緩沖液(PBS)購自美國 Gibco公司;NC 膜和 ECL 發光試劑均購自美國 Biorad公司;磺酰羅丹明 B(sulforhodamine B,SRB)購自美國 Sigma 公司,以 1% 乙酸配制成 4% 溶液,4 ℃ 儲存;三氯乙酸(TCA)購自國藥集團股份有限公司;Annexin V-FITC/PI 雙染檢測細胞凋亡試劑盒和細胞周期檢測試劑盒購自南京諾唯贊生物科技有限公司;BCA 蛋白定量試劑盒購自上海碧云天生物技術有限公司;硫酸慶大霉素購自福建匯天生物藥業有限公司。
1.2方法
1.2.1人胃癌細胞株 AGS 的培養AGS 細胞在含 10% 胎牛血清、0.08 U/L 慶大霉素的 F12培養基中,于 37 ℃、5% CO2飽和濕度條件下培養。
1.2.2SRB 蛋白染色法檢測 FIM-X13 對胃癌細胞株 AGS 增殖的影響操作方法參照文獻[11]進行,將對數生長期的 AGS 細胞以 10 000 個/孔接種于 96 孔培養板,培養 24 h 后,加入用培養基稀釋至終濃度分別為 10、15 和 20 μmol/L 的FIM-X13,以相同濃度梯度的雷帕霉素和依維莫司作為陽性對照,不加藥培養基作空白對照。每個濃度設 3 個重復孔。培養 48 h,用預冷體積分數10% 的 TCA 固定細胞,4 ℃ 放置 1 h 后蒸餾水洗滌 5 次,室溫自然干燥。加入由體積分數 1% 冰醋酸配制的 0.4% SRB 溶液,室溫染色 15 min,去上清液,以 1% 醋酸洗滌 5 次,室溫自然干燥。最后加入 10 mmol/L Tris 溶液(pH 10.5),酶標儀540 nm 波長下測定 OD 值。細胞增殖抑制率(%)=(1 - OD實驗組/OD空白對照組)× 100%。并計算各化合物對 AGS 細胞的 IC50。
1.2.3Annexin V-FITC/PI 雙染法檢測 FIM-X13 對 AGS 細胞凋亡的影響將對數生長期的 AGS細胞以 6 × 105個/孔種入 6 孔板并培養 24 h,傾去培養基,加入用培養基稀釋至終濃度分別為 10、15 和 20 μmol/L 的 FIM-X13,另設 15 μmol/L 雷帕霉素和依維莫司作為兩個陽性對照組及不加藥培養基作為空白對照組,繼續培養 48 h 后,采用AnnexinV-FITC/PI 凋亡試劑盒測定細胞凋亡率:不含 EDTA 的胰酶消化細胞后,PBS 洗滌 2 次,用結合緩沖液 500 μl 重懸細胞后加入 5 μl AnnexinV-FITC 和 PI,室溫黑暗條件下反應 5 min后,流式細胞儀檢測細胞凋亡情況。
1.2.4PI 標記檢測 FIM-X13 對 AGS 細胞周期的影響細胞培養和藥物處理同 1.2.3,采用細胞周期檢測試劑盒測定細胞周期。以不含 EDTA 的胰酶消化細胞后 PBS 洗滌 2 次。細胞用 75% 預冷的乙醇 4 ℃ 固定 12 h 后,預冷 PBS 洗滌細胞1 次,然后加入 200 μl 預冷的 PBS 重懸細胞。向細胞懸液中加入 20 μl RNase A 溶液,37 ℃ 水浴30 min,400 目篩網過濾。向濾液中加入 400 μl PI染液,搖勻后,4 ℃ 避光孵育 30 min,流式細胞儀檢測細胞周期。
1.2.5Western blot 檢測 FIM-X13 對 AGS 細胞mTOR 及其下游蛋白磷酸化的影響細胞培養同1.2.3。傾去培養基,加入用培養基稀釋至終濃度分別為 0.01、0.1 和 1 μmol/L 的 FIM-X13,另設0.1 μmol/L 雷帕霉素和依維莫司作為兩個陽性對照組,不加藥培養基作為空白對照組。繼續培養 48 h后,傾去培養基,用 PBS 洗滌細胞 2 次后,用2% SDS 100 μl 裂解細胞并收集細胞裂解液,沸水浴 10 min 后,10 000 r/min 離心 10 min,棄細胞殘渣,收集蛋白。BCA 蛋白試劑盒測定細胞裂解液蛋白含量并將各樣品蛋白含量定量至一致。根據不同待測蛋白質的分子量選擇不同濃度的 SDS-聚丙烯酰胺凝膠電泳分離蛋白,半干式轉膜儀將目標蛋白轉移至 NC 膜,5% 脫脂牛奶封閉空白位點,特異性一抗 4 ℃ 振搖孵育過夜。次日,蛋白條帶在 TBST 中潤洗 3 次,每次 15 min。二抗孵育 1 h后,TBST 潤洗 3 次,每次 15 min。ECL 發色法顯影。以 GAPDH 作為內參蛋白。Image-Pros Plus 6.0 計算 Western blot 條帶灰度值。
1.3統計學處理
2 結果
2.1FIM-X13 抑制 AGS 細胞增殖
FIM-X13 作用 AGS 細胞 48 h 后,AGS 細胞增殖受到抑制,FIM-X13 對 AGS 細胞增殖的抑制活性隨濃度升高而增強,其 IC50為(9.32 ± 0.70)μmol/L,強于雷帕霉素(14.68 ± 1.07)μmol/L 和依維莫司(14.66 ± 1.11)μmol/L,差異具有統計學意義(P < 0.05)(圖1)。
2.2FIM-X13 誘導 AGS 細胞凋亡
與空白對照組相比,FIM-X13 顯著誘導 AGS細胞的凋亡(P < 0.05),誘導能力隨濃度增加而增強。在相同濃度下,FIM-X13 誘導細胞凋亡能力顯著高于雷帕霉素和依維莫司,差異具有統計學意義(P < 0.05)(圖2)。
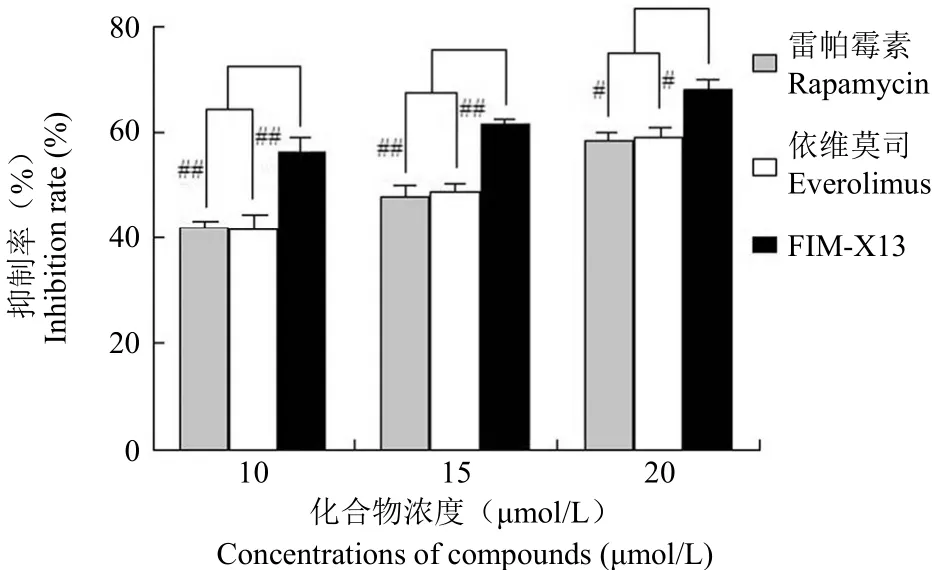
圖1 FIM-X13、雷帕霉素和依維莫司對 AGS 細胞增殖的抑制作用比較(與雷帕霉素或依維莫司相比,#P < 0.05,##P < 0.01)Figure 1 In comparison of FIM-X13 with rapamycin and everolimus on inhibiting cell proliferation in AGS cell line (#P < 0.05,##P < 0.01 vs rapamycin or everolimus)
2.3FIM-X13 阻滯 AGS 細胞周期于 G1期
FIM-X13 能夠阻滯 AGS 細胞周期于 G1期,其 G1期細胞百分比與空白對照組相比,差異具有統計學意義(P < 0.01),隨著 FIM-X13 濃度增大,其阻滯細胞周期的能力增強。在相同濃度下,FIM-X13 阻滯 AGS 細胞周期的能力強于雷帕霉素和依維莫司,差異具有統計學意義(P < 0.05)(圖3)。
2.4FIM-X13 抑制 AGS 細胞 mTOR 及其下游蛋白的磷酸化
Western blot 檢測表明,FIM-X13 顯著抑制mTOR、p70S6K1、S6 和 4EBP1 的磷酸化(P <0.05)并具有濃度梯度效應。與相同濃度的雷帕霉素和依維莫司相比,活性相近(P > 0.05)(圖4)。上述結果表明,與雷帕霉素和依維莫司一樣,FIM-X13 能抑制 mTOR 信號轉導途徑的過度活化,為 mTOR 信號轉導途徑抑制劑。
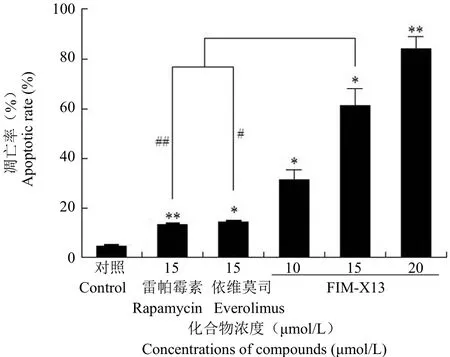
圖2 FIM-X13、雷帕霉素和依維莫司誘導 AGS 細胞凋亡的比較(與空白組相比,*P < 0.05,**P < 0.01;與雷帕霉素或依維莫司相比,#P < 0.05,##P < 0.01)Figure 2 In comparison of FIM-X13 with rapamycin and everolimus on reducing cell apoptosis in AGS cell line (*P <0.05,**P < 0.01 vs control;#P < 0.05,##P < 0.01 vs rapamycin or everolimus)
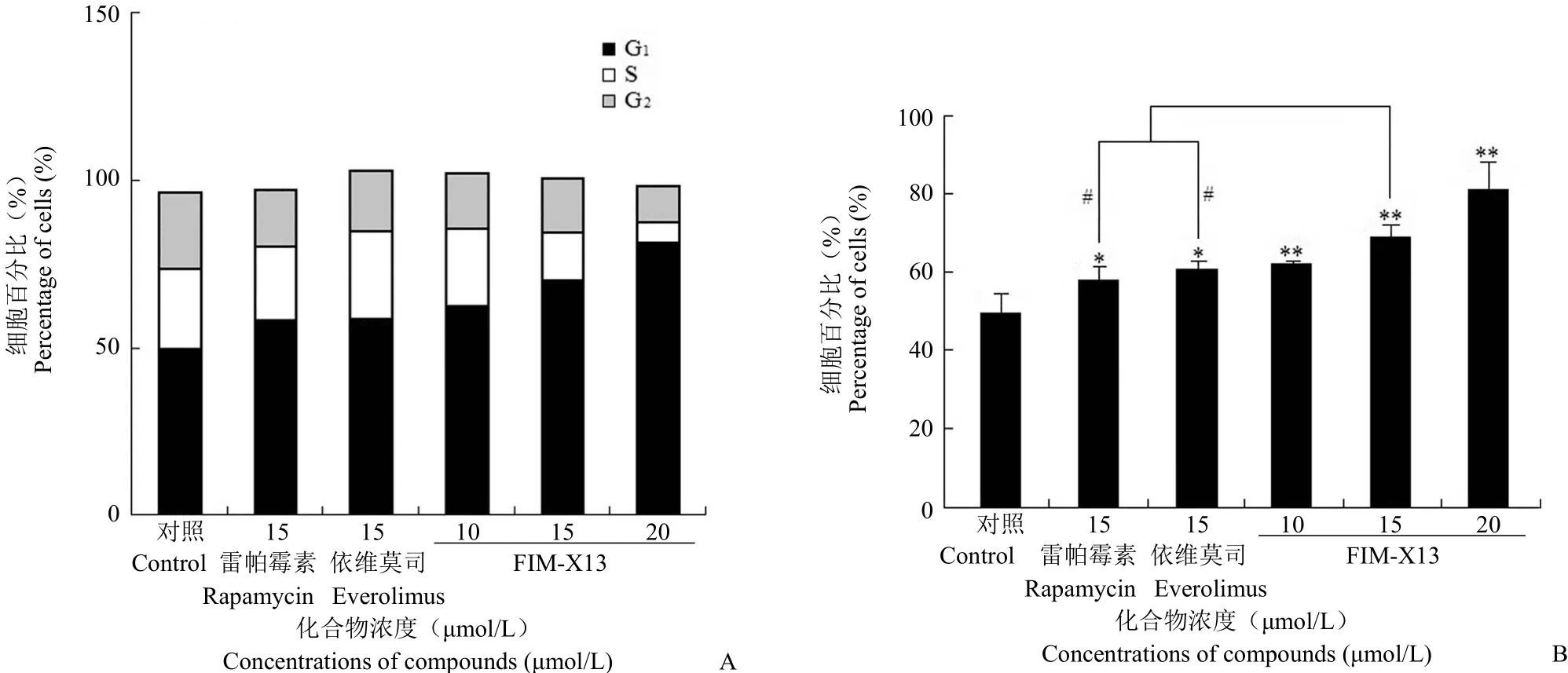
圖3 FIM-X13、雷帕霉素和依維莫司阻滯 AGS 細胞周期作用的比較(A:各細胞周期所占比例分析結果;B:G1期細胞百分比分析結果;與空白組相比,*P < 0.05,**P < 0.01;與雷帕霉素或依維莫司相比,#P < 0.05)Figure 3 In comparison of FIM-X13 with rapamycin and everolimus on cell cycle arresting AGS cell line (A: The comparision of percentage of different cell cycle; B: The analysis of G1percentages;*P < 0.05,**P < 0.01 vs control;#P < 0.05 vs rapamycin or everolimus)
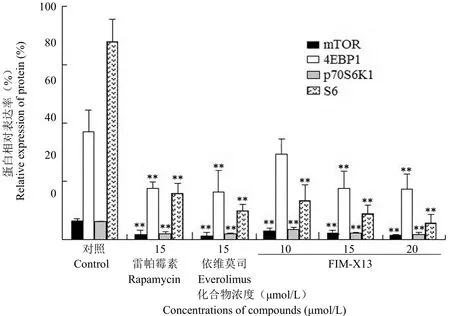
圖4 FIM-X13、雷帕霉素和依維莫司對 AGS 細胞 mTOR 及其下游蛋白磷酸化抑制作用的比較(與空白組相比,**P <0.01)Figure 4 In comparison of FIM-X13 with rapamycin and everolimus on inhibiting the phosphorylation of mTOR and its downstream proteins in AGS cell line (**P < 0.01 vs control)
3 討論
綜上所述,FIM-X13 具有很強的抑制胃癌細胞株 AGS 增殖的作用,抑制能力強于雷帕霉素和依維莫司。與雷帕霉素和依維莫司一樣,FIM-X13 通過抑制 mTOR 信號轉導途徑、誘導 AGS 細胞凋亡、阻斷 AGS 細胞于 G1期等達到抑制 AGS細胞增殖的作用。提示 FIM-X13 作為 mTOR 抑制劑,在治療胃癌方面值得開展進一步體內外藥效研究。
含有三氮唑基團的衍生物具有包括抗腫瘤在內的多種生物學活性,一直是藥物研究的熱點。其原理是三氮唑五元芳香唑環上的 3 個氮原子很容易與生物體內的各種酶和受體以非共價鍵相互作用。三氮唑衍生物的抗癌機制多樣,如 1,2,3-三氮唑衍生物抑制熱休克蛋白合成、抑制組氨酸去乙酰化酶活性、抑制微管聚合作用、抑制蛋白酪氨酸激酶活性等[12],抑制芳香化酶活性的三氮唑衍生物來曲唑、阿那曲唑和伏氯唑已作為治療乳腺癌的藥物應用于臨床。FIM-X13 為 1,2,3-三氮唑 C43-雷帕霉素,其對 AGS 細胞增殖抑制能力強于雷帕霉素和依維莫司,說明 1,2,3-三氮唑駢合雷帕霉素增強了雷帕霉素的抗胃癌活性,其機制是否達到預期的三氮唑和 mTOR 抑制聯合發揮作用還有待進一步探討。本研究為雷帕霉素與三氮唑類化學半合成及雷帕霉素類 mTOR 抑制劑與三氮唑類藥物聯合治療胃癌提供借鑒。此外,從化學結構分析,三氮唑的 3 個氮原子增加了化合物的極性,可能從藥代動力學方面也比母核雷帕霉素有更好的表現。
PI3K/AKT/TSC/mTOR 信號轉導途徑中,PI3K接受來自胰島素或胰島素樣生長因子的信號,通過級聯反應磷酸化 AKT 的蘇氨酸 308 位點激活AKT,后者抑制了 TSC 從而激活 mTORC1[1]。mTORC1 上游任何激酶如 PI3K、AKT、TSC 基因的突變和缺失都促進 mTOR 信號途徑的活化,mTOR 通過對其下游 4EBP1 和 S6K1 的磷酸化激活了與核糖體發生、細胞增殖和代謝相關蛋白的翻譯,促進腫瘤的生長、增殖和轉移[3]。AGS 為PI3K 基因 PIK3CA 突變的胃癌細胞株細胞,PIK3CA 基因的突變使 PI3K 異常表達,造成AGS 細胞的 mTOR 信號途徑過度活化。繼手術、放化療后,針對癌癥發生、發展相關信號途徑關鍵激酶的靶向治療成為晚期腫瘤治療的重要手段,其中的小分子靶向藥物數量有限。因此,可通過其他胃癌株進一步研究,以明確 FIM-X13是否是由PIK3CA 基因突變造成的 mTOR 信號途徑過度激活的胃癌潛在治療藥物。
參考文獻
[1] Porta C, Paglino C, Mosca A. Targeting PI3K/Akt/mTOR signaling in cancer. Front Oncol, 2014, 4:64.
[2] Siegel RL, Miller KD, Jemal A. Cancer statistics, 2015. CA Cancer J Clin, 2015, 65(1):5-29.
[3] Advani SH. Targeting mTOR pathway: a new concept in cancer therapy. Indian J Med Paediatr Oncol, 2010, 31(4):132-136.
[4] Zhou J, Chen GB, Tang YC, et al. Genetic and bioinformatic analyses of the expression and function of PI3K regulatory subunit PIK3R3 in an Asian patient gastric cancer library. BMC Med Genomics, 2012,5:34.
[5] Samuels Y, Wang Z, Bardelli A, et al. High frequency of mutations of the PIK3CA gene in human cancers. Science, 2004, 304(5670):554.
[6] Li M, Sun H, Song L, et al. Immunohistochemical expression of mTOR negatively correlates with PTEN expression in gastric carcinoma. Oncol Lett, 2012, 4(6):1213-1218.
[7] Wen YG, Wang Q, Zhou CZ, et al. Mutation analysis of tumor suppressor gene PTEN in patients with gastric carcinomas and its impact on PI3K/AKT pathway. Oncol Rep, 2010, 24(1):89-95.
[8] Shimobayashi M, Hall MN. Making new contacts: the mTOR network in metabolism and signalling crosstalk. Nat Rev Mol Cell Biol, 2014,15(3):155-162.
[9] Xu B, Wu Y, Shen L, et al. Two-dose-level confirmatory study of the pharmacokinetics and tolerability of everolimus in Chinese patients with advanced solid tumors. J Hematol Oncol, 2011, 4:3.
[10] Doi T, Muro K, Boku N, et al. Multicenter phase II study of everolimus in patients with previously treated metastatic gastric cancer. J Clin Oncol, 2010, 28(11):1904-1910.
[11] Huang J, Yang GX, Yu H, et al. Sirolimus F904 and its derivative FIM-A (AP23573) anticncer activity in vitro. J Fujian Normal Univ (Nat Sci Ed), 2010, 26(5):63-66. (in Chinese)黃捷, 楊國新, 余輝, 等. 西羅莫司F904及其衍生物FIM-A (AP23573)的體外抗癌活性. 福建師范大學學報(自然科學版),2010, 26(5):63-66.
[12] Zhou CH, Wang Y. Recent researches in triazole compounds as medicinal drugs. Curr Med Chem, 2012, 19(2):239-280.
Author Affiliations: Fujian University of Traditional Chinese Medicine, Fuzhou 350122, China (YANG Dan, HUANG Jie); Fujian Institute of Micbiology, Fuzhou 350007, China (YANG Dan, CHEN Xiao-ming, LI Kua-liang, XIE Li-jun, HUANG Jie); Hangzhou HuaDong Medicine Group Pharmaceutical Research Institute Co. Ltd., Hangzhou 310012, China (PAN Fu-sheng)
www.cmbp.net.cnChin Med Biotechnol, 2016, 11(3):224-228
Preliminary study on effect and mechanism of a novel rapamycin containing triazole derivative FIM-X13 on gastric carcinoma AGS cell line
YANG Dan, CHEN Xiao-ming, LI Kua-liang, XIE Li-jun, PAN Fu-sheng, HUANG Jie
【Abstract】
ObjectiveOur purpose is to investigate the inhibitory effect and mechanism of a novel rapamycin containing triazole derivative FIM-X13 on gastric carcinoma as compared with rapamycin or everolimus separately.
MethodsThe proliferation of cancer cells was tested by sulforhodamine B assay. The apoptosis and cell cycle of cancer cells were individually analyzed by flow cytometry. The expressions of mTOR, p70S6K1, S6, 4EBP1 and their phosphorylation level were separately detected by Western blot.
ResultsFIM-X13 inhibited the proliferation of gastric carcinoma AGS cells in a dose-dependent manner with IC50value of (9.32 ± 0.70) μmol/L and the inhibitory effect was even more potent than that of rapamycin and everolimus. It also induced apoptosis and G1phase cell cycle arrested in AGS cells. In addition, FIM-X13 suppressed the phosphorylation level of mTOR and its downstream targets of 4EBP1, p70S6K1 and S6, which was consistent with rapamycin and everolimus.
ConclusionThe novel triazole-containing rapamycin derivate FIM-X13 exerts more potent effect on cell proliferation than rapamycin and everolimus do. Similar to rapamycin and everolimus, FIM-X13 significantly inhibits proliferation of gastric cancer cell, induces cell apoptosis and G1phase cell cycle arrest via blocking mTOR pathway. FIM-X13 may become a promising mTOR inhibitor candidate for the treatment gastric carcinoma.
【Key words】Stomach neoplasms;TOR serine-threonine kinases;Rapamycin triazole containing derivative
DOI:10.3969/j.issn.1673-713X.2016.03.005
基金項目:國家自然科學基金(81502935);福建省屬工藝類科研院所基本科研專項(2015R1009-7)
通信作者:黃捷,Email:xlms2003@163.com
收稿日期:2015-12-21
Corresponding Author:HUANG Jie, Email: xlms2003@163.com

