太湖沉積物鐵形態(tài)分布特征及磷鐵相關性分析
楊文斌,唐 皓,韓 超,丁士明(1.安徽師范大學環(huán)境科學與工程學院,安徽 蕪湖 41003;.中國科學院南京地理與湖泊研究所,湖泊與環(huán)境國家重點實驗室,江蘇 南京 10008)
?
太湖沉積物鐵形態(tài)分布特征及磷鐵相關性分析
楊文斌1*,唐 皓1,2,韓 超2,丁士明2(1.安徽師范大學環(huán)境科學與工程學院,安徽 蕪湖 241003;2.中國科學院南京地理與湖泊研究所,湖泊與環(huán)境國家重點實驗室,江蘇 南京 210008)
摘要:通過對太湖藻型湖區(qū)、草藻過渡型湖區(qū)、草型湖區(qū)柱狀沉積物進行鐵的形態(tài)分級分析沉積物中不同提取態(tài)磷鐵含量,獲得不同形態(tài)鐵的空間分布特征.結果表明:沉積物總鐵含量藻型湖區(qū)31.57mg/g(SD=8.51)>過渡型湖區(qū)30.34mg/g(SD=11.97)>草型湖區(qū)25.25mg/g(SD=4.59),不同湖區(qū)沉積物中鐵形態(tài)的含量依次為可還原(晶型)鐵氧化物Feox2>碳酸鹽鐵Fecarb>易還原(無定形)鐵氧化物Feox1>低活性硅酸鐵Feprs>磁鐵礦Femag>可吸附性Fe(Ⅱ),Fecarb、Feox1、Feox2,3種鐵形態(tài)屬于高活性鐵Fe(III),含量為7.79,6.16,8.18mg/g,分別占總鐵含量的28.56%,21.54%,29.53%,表明高活性鐵(III)是沉積物中最主要的鐵形態(tài);沉積物中各提取態(tài)磷含量大小比較為NH2OH?HCl-P>MgCl2-P>NaAc-P>Na2S2O4-P>濃HCl-P>(NH4)2C2O4-P,含量較高的MgCl2-P(0.067mg/g)、NaAc-P(0.061mg/g)、NH2OH?HCl-P(0.068mg/g),分別占總提取磷的35.28%、31.97%和22.55%,是沉積物鐵分級提取態(tài)磷中最主要的形態(tài).磷-鐵相關性分析表明,二者之間呈顯著的正相關(P<0.05),進一步從鐵形態(tài)分級角度證實鐵是沉積物內源磷釋放的關鍵因子.
關鍵詞:鐵形態(tài)分級;藻型湖區(qū);草藻過渡型湖區(qū);草型湖區(qū);相關性分析;太湖
? 責任作者, 教授, ywb1968@mail.ahnu.edu.cn
磷已被證實是我國大多數(shù)湖泊富營養(yǎng)化的主要限制性因子,對水體營養(yǎng)狀態(tài)和生態(tài)系統(tǒng)結構發(fā)揮著十分關鍵的調控作用[1-3].盡管近些年對外源污染治理力度的加大,但湖泊污染現(xiàn)狀依然嚴峻,究其原因與內源污染的強度增加有關,其中,內源磷污染備受關注.已有研究發(fā)現(xiàn),很多淺水富營養(yǎng)化湖泊都會發(fā)生高強度的內源磷污染,造成水體富營養(yǎng)化治理效果出現(xiàn)滯后的現(xiàn)象[4-5].國內外圍繞沉積物磷內源污染發(fā)生過程及界面交換機制開展了大量研究,經典的內源磷釋放機制是1941年Mortimer[7]提出的鐵-磷耦合機制.該機制認為,沉積物磷的釋放能力受鐵控制,即好氧條件下,FeO(OH)對無機磷有著較強的吸附能力;在厭氧條件下,FeO(OH)被還原溶解,同時釋放所吸附的磷[8].Jensen等[9]在對丹麥100多個湖泊沉積物中Fe和P的調查發(fā)現(xiàn),沉積物中的總鐵含量與總磷含量呈顯著正相關.鐵的還原與有機質氧化降解的耦合作用,是沉積物早期成巖過程中最為重要的生物地球化學反應之一[10].由此可見,沉積物鐵是控制內源磷釋放的關鍵因子之一,在調節(jié)湖泊生態(tài)環(huán)境質量及生物生產力方面扮演重要作用.
鐵在沉積物中是以不同形態(tài)存在的,不同的賦存形態(tài)與環(huán)境的相互作用會直接影響到其在環(huán)境中的生物可利用性、釋放、遷移等特性.我國最早對鐵的研究是19世紀30年代對水稻土中鐵的氧化還原機制及其對層狀粘土礦物的掩蓋作用[11];鄒元春等[12]研究了三江平原典型多級溝渠系統(tǒng)0~60cm沉積物全鐵含量的空間分布特征,結果表明各類型、各等級的沉積物鐵含量具有極顯著差異,整個多級溝渠系統(tǒng)沉積物各層的鐵含量沒有顯著性差異.楊宏偉等[13]應用顆粒物中鐵的連續(xù)浸提技術研究了黃河干流表層沉積物中鐵形態(tài)的分布特征及相關性;王超等[14]考察了典型城市淺水湖泊沉積物不同的磷和鐵形態(tài)分布特征并初步分析二者相關關系,證實沉積物總磷的變化受活潑性鐵形態(tài)影響最大.盡管如此,目前對太湖沉積物鐵或磷形態(tài)的單獨研究較多,且多集中在表層沉積物形態(tài)分布變化,而對太湖沉積物不同湖區(qū)不同鐵形態(tài)的總量測定和空間分布的系統(tǒng)研究,特別是從沉積物鐵的形態(tài)分級提取角度討論沉積物中磷鐵同步變化規(guī)律的研究尚少.本研究選擇太湖3種不同類型的湖區(qū),采用鐵分級方法獲得不同形態(tài)的鐵和磷濃度在3種類型湖區(qū)的空間(水平和垂直)分布特征,并分析不同形態(tài)鐵與相應結合態(tài)磷的相關性,旨在為沉積物中不同鐵形態(tài)的總量測定和空間分布及為磷鐵經典耦合機制提供依據(jù).
1 材料和方法
1.1 研究區(qū)域概況
本文以太湖的藻型湖區(qū)竺山灣附近(31.338°N,120.180°E,標記為1#)、草藻過渡湖區(qū)湖心附近(31.387°N,120.296°E,2#)和草型湖區(qū)胥口灣附近(31.289°N,120.321°E,3#)為研究對象,在每個湖區(qū)分別選取1個采樣點.其中,竺山灣位于太湖北部湖區(qū)屬于富營養(yǎng)化程度較高的藻型湖泊,該湖灣以浮游植物占優(yōu)勢,水體透明度較低,TN、TP和CODMn平均值分別為:6.08, 0.231, 7.40mg/L高于東部湖區(qū)及湖心.東部胥口灣屬于相對健康的草型湖泊,水生植物豐富,水質較好,水體透明度為0.57m屬3個湖區(qū)最高值,另外CODMn、TN和TP的濃度分別為4.99,1.57, 0.054mg/L,該湖區(qū)表層沉積物為砂質,顏色呈烏黑色.湖心區(qū)水質相對較好,水體透明度為0.24m,CODMn為4.99mg/L,TN平均值為2.93mg/L,TP平均值為0.109mg/L,為草藻過渡型湖區(qū)[15].
1.2 樣品采集與處理
于2014年10月采用沉積物柱狀樣品采樣器(φ9cm,中國科學院南京地理與湖泊研究所)采集沉積物柱芯,并立即帶回實驗室,取其上層5cm以0.5cm的厚度進行切片,6~12cm的沉積物以1cm的厚度進行切片,共計17個切片樣品,裝入自封袋放入冷凍干燥機(ALPHA 1-2LD plus ,德國Christ)干燥,干燥后的土樣充分研磨混勻,然后過100目篩,貯存在自封袋中備用,同時同步監(jiān)測水體水質(HORIBA,U-53)并采集上覆水和表層沉積物,帶回實驗室進行相關理化分析.

圖1 太湖采樣點示意Fig.1 Sampling sites in Lake Taihu
1.3 沉積物中鐵的分級提取
對太湖沉積物中鐵形態(tài)采用6級分組法連續(xù)提取,具體方法見表1,該法是在鐵的化學序列提取法[16]上進行改進.具體改進為:(1)添加了一步可吸附性鐵(Adsorbed Fe(II))的提取之后,再對沉積物中剩下的活性鐵進行提取;(2)黃鐵礦鐵(Fepy)主要是由易還原(無定形)鐵氧化物(Feox1)和可還原(晶型)鐵氧化物(Feox2)轉化得到,經過第3、4步的提取后黃鐵礦鐵已經低于檢測限,所以省去這一步的提取;(3)非活性鐵或者無活性鐵(FeU)則直接用總鐵含量減去第2到6步提取的鐵含量既得,無需單獨提取.樣品做3個平行試驗,結果用平均值表示.
本文并未對沉積物中磷進行單獨的分級提取,而是從鐵分級方法提取不同磷形態(tài),按照表1提取方法提取后獲得磷含量總和稱為提取態(tài)總磷TP提取,各結合態(tài)磷用浸提劑-P表示.王振華等[17]在研究東部平原湖區(qū)對沉積物進行磷連續(xù)提取方法測定時,也同時對浸提液中的鐵進行了測定.為考察該分級方法的可靠性,將鐵分級的方法與楊宏偉[18]總結的沉積物中磷的連續(xù)浸提法進行了對比,可以得出在對可吸附性鐵Fe(II)、Fecarb、Feox2、Feprs進行提取的同時,其浸提劑和浸提方法也可以提取出部分的可交換態(tài)Pex、鈣結合態(tài)磷中的Paut、閉蓄態(tài)磷Pobs以及有機磷Porg.

表1 沉積物中鐵的分級和提取方法Table 1 Classification of Fe forms in sediments and extraction methods
1.4 沉積物全量元素及TOC的測定
依據(jù)《土壤農業(yè)化學分析方法》[19]進行了沉積物土壤元素全量分析,并進行適當修正.具體步驟如下:在濾紙上稱取0.200~0.209g偏硼酸鋰,稱取0.05000~0.05019g樣品倒入偏硼酸鋰上,小心重復折疊濾紙以將兩者混勻.將濾紙折疊成一小球,放入坩堝中,將坩堝放進預先已升溫至1000℃的馬弗爐中,加熱15~20min.取出坩堝,稍冷卻后將熔珠倒入預先裝有25mL8%(V/V)硝酸的比色管中,將比色管放入超聲波清洗器中,超聲溶解熔珠.待完全溶解后以去離子水定容,加蓋搖勻,經進口PES水系針頭濾器(0.45μm)過濾,倒入離心管存儲待測.
沉積物TOC含量采用《土壤農化分析(第三版)》[20]中重鉻酸鉀外加熱法進行測定,稱取0.1000g~0.5000g(精確至0.0001g),通過0.149mm篩孔的風干土樣置于硬質試管中,加入0.1g硫酸銀.加入5.00mL 0.8000mol/L重鉻酸鉀標準溶液,再用注射器注入5mL硫酸,小心旋轉搖勻.將盛有土樣的硬質試管插入加熱至185~190℃的油浴鍋內的鐵絲籠架中加熱,控制油浴鍋內溫度在170~180℃,并使溶液保持沸騰5min.取出鐵絲籠架,待硬質試管稍冷后將混合物洗入250mL錐形瓶中,加入3~4滴鄰菲啰啉指示劑,用0.2mol/L硫酸亞鐵銨標準溶液滴定至溶液由橙黃色經藍綠色到棕紅色為終點.再根據(jù)公式計算有機質含量.
采用Optima 2100DV電感耦合等離子體光譜儀(ICP-AES,美國PerkinElmer公司)對鐵分級待測液和全量元素待測液進行測定,得到的3個點位0~12cm深度沉積物中的6種提取態(tài)磷、鐵的含量和總磷、總鐵含量.
1.5 數(shù)據(jù)處理
本文數(shù)據(jù)分析使用SPSS19.0,圖形繪制使用Origin9.0進行處理.
2 結果與討論
2.1 理化性質
表2常規(guī)水質指標數(shù)據(jù)中,采樣的溫度都在16.30~17.35℃,可忽略溫度對水質的影響.DO和ORP是衡量水體氧化還原狀況的指標,天然水體的飽和溶解氧在4~14mg/L范圍內,各采樣點的DO均飽和,處于好氧狀態(tài),其中1號點位于污染較重的竺山灣,DO明顯小于其他點位;一般天然水體的pH值位于6.5~8.5之間,太湖水體的pH位于8.6~9.3之間,偏堿性,這是由于太湖富營養(yǎng)化污染造成,藻類聚集光合作用導致水體的pH值升高[15];總溶解態(tài)固體(TDS)、電導率是間接表示水中溶解性鹽類的含量,溶解的鹽類均以離子狀態(tài)存在,具有一定的導電能力,因此若水體電導率高,說明水中含有溶解性固體多,可間接說明污染物含量高;濁度(NTU)是水中由于含有懸浮及膠體狀態(tài)的雜質而產生的渾濁,濁度跟水深、水流和風速等都有關,在不同的點位差異很大.

表2 研究點位常規(guī)水質參數(shù)、營養(yǎng)鹽指標及沉積物部分理化指標值Table 2 Physic-chemical properties of waters and sediments from the investigated locations
從表2可以看出,在污染較重的1#點,水體中氮磷含量明顯高于其他區(qū)域;而3#點氮磷含量較低,污染較輕,葉綠素含量的分布也呈現(xiàn)同樣的趨勢.沉積物中總磷的變化趨勢和總鐵一樣,竺山灣最高1.00(0.51~1.65)mg/g,湖心其次0.74(0.34~ 1.25)mg/g,草型湖區(qū)含量最低0.45(0.22~ 0.93)mg/g,竺山灣屬于西北部藻型湖區(qū),處于富營養(yǎng)化狀態(tài),水體污染程度明顯高于東部及南部且變化梯度大,這反應了太湖水體的總體污染狀況[21].
2.2 不同湖區(qū)鐵的含量和形態(tài)分布特征
2.2.1 不同湖區(qū)全量總鐵及鐵形態(tài)分級總鐵含量分布特征 將湖泊表層沉積物剖面分級提取所得到的每步鐵含量相加,得到太湖表層沉積物鐵分級TFe含量(TFe分級),濃度范圍為13~47mg/g之間,均值為27.88mg/g.這與Liu等[22]在2012年測得的太湖沉積物金屬Fe含量平均值為35.3mg/g基本一致,其中1#柱狀沉積物TFe分級含量16~41mg/g,均值為30.29mg/g(SD=8.56);2#柱狀沉積物TFe分級濃度范圍在13~47mg/g,均值29.06mg/g(SD=11.97);3#柱狀沉積物TFe分級含量14~31mg/g,均值24.29mg/g(SD=4.58).通過土壤元素全量分析測得的3個采樣點的全量總Fe(TFe)為31.57mg/g(SD=8.51),30.34mg/g(SD= 11.97),25.25mg/g(SD=4.59),TFe分級占全量TFe的比例為95.95%,95.78%,96.21%,太湖3種類型湖區(qū)的沉積物總鐵含量在藻型湖區(qū)富營養(yǎng)化程度最高,過渡型湖區(qū)其次,草型湖區(qū)具有較強的自凈能力,因而3種湖區(qū)沉積物表層磷鐵的累積能力也依次減弱.

圖2 研究點位沉積物剖面中各形態(tài)鐵濃度及全量總鐵濃度Fig.2 Vertical profiles of different iron speices and total iron in the sediments from the investigated locations
2.2.2 不同湖區(qū)沉積物中各形態(tài)鐵含量垂直分布特征 由圖2可知,藻型湖區(qū)、過渡型湖區(qū)可吸附性Fe(II)幾乎均低于檢測限(<0.011mg/L),這是因為太湖水體偏堿性(pH位于8.6~9.3),水體中大部分鐵離子由于形成氫氧化物而沉積在沉積物表面上,自由的可吸附性Fe(II)含量極低.1#剖面TFe分級含量整體趨勢是隨著深度先略微降低后緩慢升高,在2~3cm深度含量最低,之后隨深度緩慢升高,在8cm深度達到最大值.各形態(tài)鐵含量隨深度的變化與TFe分級變化趨勢一致.但每種形態(tài)Fe在不同深度所占百分比有顯著變化,Fecarb占TFe分級百分比逐漸升高,最終占最大比例,Feox1和Feox2占TFe分級的百分比隨著深度而緩慢降低,Femag和Feprs所占比例相對穩(wěn)定.Fecarb的形成條件較為苛刻,只發(fā)生在富鐵、缺硫、且碳酸鹽含量很高的亞氧和無氧沉積環(huán)境中[23],1#沉積物隨著深度的增加,Fecarb比Feox1、Feox2增加的幅度要大,說明該區(qū)域內鐵及碳酸鹽含量下層高于上層,這是因為附近分布著太滆運河沙塘港武進港和直湖港,富營養(yǎng)化區(qū)域水體自凈能力差,河流輸入了大量的污染物導致沉積物表層磷鐵含量不斷累積,經過時間推移表層的營養(yǎng)物質被覆蓋到下層,因此外源污染物的長期輸入造成藻型湖區(qū)表層沉積物鐵含量隨深度增加而增加,從而各形態(tài)鐵尤其是Fecarb含量隨深度增加而增加.
2#剖面TFe分級含量整體趨勢是減小,首先升高至3.5cm深度銳減,4cm處又升到最大值47mg/g,4.5cm處鐵含量再次下降至22mg/g后趨于平緩,各形態(tài)鐵含量均與TFe分級變化一致.Fecarb與Feprs所占TFe分級比例先減小后增大,最終分別占TFe分級的29%和35%, Feox1和Feox2先增大后減小,Femag所占比例相對穩(wěn)定.2#湖心區(qū)受污染程度輕,是沉積物剖面上層鐵含量高于下層的主要原因.沉積物-水界面往下,周圍環(huán)境由好氧到厭氧轉變顯著,出現(xiàn)厭氧情況時,FeO(OH)被還原溶解,導致沉積物Fe3+溶解進而轉化為Fe2+, Fecarb、Feprs占TFe分級比例增減趨勢與Feox1、Feox2相反,因為Feox1和Feox2中的水鐵礦、纖鐵礦、針鐵礦、赤鐵礦等均是以Fe3+形式存在的鐵氧化物,缺氧時其氧化溶解有助于形成以Fe2+形式存在的晶型Fecarb中的菱鐵礦和鐵白云石以及層狀硅酸鹽鐵Feprs,Fe(III)的還原性溶解及再氧化生成自生Fe(III)氧化物是沉積物中Fe循環(huán)的主要路徑.
3#剖面TFe分級含量整體趨勢較平緩,在3cm深度緩慢升高,在5cm深度達到最高值,之后緩慢降低,于10cm深度降到最低值.Fecarb含量變化與
TFe分級一致,除Feox2隨著深度增加含量有著明顯的大幅增加外,其余形態(tài)均隨著深度而減小,且各形態(tài)所占比例的變化趨勢和含量呈一致.3#草型湖區(qū)浮游植物和沉水植物茂盛,生物量較大,對污染物緩沖作用強,水體具有較強的自凈能力,所以沉積物表層磷鐵累積量相對小,沉積物-水界面鐵含量變化不顯著.而晶型鐵氧化物Feox2含量的大幅增加,可能與Feox1中無定型鐵氧化物水鐵礦在草型湖區(qū)純度較高,很容易向更穩(wěn)定的針鐵礦或赤鐵礦轉化有關.
2.2.3 不同湖區(qū)沉積物中各形態(tài)鐵含量分布特征 太湖3種類型湖區(qū)的柱狀沉積物中,各鐵形態(tài)的含量依次為Feox2>Fecarb>Feox1>Feprs>Femag>可吸附性Fe(II),Fecarb、Feox1、Feox23種鐵形態(tài)含量最高,分別占TFe分級的18.25%~39.51%, 12.45%~27.76,26.55%~32.95%,合計占TFe的72.56%~84.91%,其次為Feprs,約占TFe的11.94%~23.98%.太湖表層沉積物中層狀硅酸鹽鐵Feprs的平均含量(4.92mg/g)明顯低于世界陸架沉積物(150μmol/g即8.40mg/g),全球河流顆粒物中的含量(216.17μmol/g即12.11mg/g),以及長江顆粒物中Feprs的含量(307.14μmol/g即17.20mg/g)[24-25],太湖表層沉積物中鐵形態(tài)大部分是以Fecarb、Feox1、Feox2等高活性鐵形式存在,低活性硅酸鹽鐵含量較低.Femag含量很低,占TFe分級的2.34%~3.45%,磁鐵礦是 Fe(II)和 Fe(III)混合價態(tài)的鐵氧化物,在沉積物中的含量普遍較低,主要來自礦物巖碎屑或火山巖碎屑,以及細粒徑的海洋自生磁鐵礦,低含量的Femag說明生物控制的磁鐵礦形成機制在太湖表層沉積物中不占重要地位.海洋沉積物的厭氧環(huán)境中,以自生菱鐵礦(晶型FeCO3)和鐵白云石[Ca(Fe2+,Mg2+, Mn2+)(CO3)2]形態(tài)存在的碳酸鹽鐵(II)Fecarb發(fā)生在富鐵、再懸浮頻繁的河口、三角洲和陸架泥質沉積物中,Fe(III)氧化物的還原主要有2個相互競爭的路徑完成,即微生物(異化)還原和化學(硫化物)還原[26-27],在海洋沉積物的含氧環(huán)境中活性Fe(III)氧化物含量高、有機質含量相對較低的情況下,鐵異化還原是有機質礦化的重要路徑,有利于晶型碳酸鹽鐵(菱鐵礦)的形成.將圖3不同湖區(qū)沉積物有機質剖面與圖2對比,有機質含量與3個湖區(qū)沉積物剖面中Fecarb形態(tài)含量呈一定的負相關性,更進一步證明了太湖湖區(qū)表層沉積物有機質含量對沉積物中碳酸鹽鐵的影響,有機質含量低說明有機質礦化程度高,從而鐵異化還原程度高,有利于晶型Fecarb的形成.湖心區(qū)表層(0~3cm深度)沉積物有機質含量低于藻型湖區(qū),因而其Fecarb含量相對較高;草型湖區(qū)由于水生植物豐富,其死亡后沉降到沉積物表面造成草型湖區(qū)有機質含量反而高于藻型湖區(qū)[26],所以晶型碳酸鹽鐵Fecarb含量草型湖區(qū)>藻型湖區(qū)>湖心.Feox1易還原(無定形)鐵氧化物和Feox2可還原(晶型)鐵氧化物是太湖表層沉積物中所占比例最高的鐵形態(tài),主要成分是高活性鐵(III)氧化物,來源于沉積物中鐵的原生礦物及鐵硅酸鹽礦物風化后再結晶的產物,如赤鐵礦和針鐵礦.其中Feox1平均含量(6.16mg/g)比富含鐵的Mississippi三角洲沉積物含量(145μmol/g即8.12mg/g)[28]低,但Feox2平均含量(8.18mg/g)比Mississippi三角洲沉積物含量(72.7μmol/g即4.07mg/g)高,說明鐵單礦物是太湖沉積物中鐵主要的存在形式,太湖底泥中較高的活性鐵(III)是控制內源磷釋放的關鍵因子,太湖具有較高的釋放風險和生物可用性.

圖3 太湖研究點位沉積物有機質含量垂直剖面Fig.3 Vertical profiles of TOC in the Surface sediments of different regions from the investigated locations of Taihu
2.3 不同提取態(tài)磷形態(tài)分布特征
藻型湖區(qū)竺山灣柱狀沉積物中占TP提取含量較高的是MgCl2-P、NaAc-P、NH2OH·HCl-P,分別占總提取磷的35.28%、31.97%和22.55%,而湖心區(qū)和草型湖區(qū)除這3種磷形態(tài),Na2S2O4-P也占了較高的比例,湖心區(qū)和草型湖區(qū)4種形態(tài)磷分別占TP提取的17.09%,18.61%,47.66%, 13.41%和25.33%,20.79%,28.41%,19.10%,綜上太湖3個湖區(qū)沉積物中各結合態(tài)磷含量占TP提取的百分比平均值大小為NH2OH·HCl-P(32.87%)> MgCl2-P(25.90%)>NaAc-P(23.79%)>Na2S2O4-P(13.31%)>濃HCl-P(3.43%)>(NH4)2C2O4-P(0.69%),雖然3個湖區(qū)表層沉積物中吸附性Fe(Ⅱ)占總鐵的比例極低,但其分級提取的磷含量卻很高,這可能由于氯化鎂不僅能提取吸附性Fe(Ⅱ),還能提取其他交換態(tài)吸附性金屬離子,其結合態(tài)的磷含量較高因而提高了這一部分提取態(tài)磷所占比例.根據(jù)楊宏偉等[18]總結的沉積物中磷的連續(xù)浸提法與鐵分級提取方法對比得出,提取得到的MgCl2-P、NaAc-P、Na2S2O4-P、濃HCl-P中包括了部分的可由磷分級方法提出的可交換態(tài)Pex、鈣結合態(tài)磷中的Paut、閉蓄態(tài)磷Pobs以及有機磷Porg,并且提取態(tài)磷含量MgCl2- P(25.90%)> NaAc-P(23.79%)>Na2S2O4-P(13.31%)與馬旭陽等[29]通過磷分級方法得到的PCa(81.96%~ 97.74%)>Pex(0.36%~7.41%)>Pobs(0.00%~ 0.92%)相一致;此外通過表2可知,TP提取同總鐵總磷有著一樣的變化趨勢,3個點TP提取占TP的百分比分別是43.06%,22.75%,20.20%,這與張路等[30]得到的位于太湖重污染湖區(qū)Fe-P約占測定總磷含量的50%,其他樣點的Fe-P相對含量均小于25%的結論相一致;而沉積物中Pex、PAl、PFe化學性質活潑,易從沉積物中溶解釋放而被生物利用,一般將三者之和稱為活性磷Bio-P[14],因此通過鐵分級方法提取的磷形態(tài)主要是活性磷中的部分Pex和PFe,其次為部分無機磷(PCa和Pobs)和有機磷Porg,而對水體磷負荷影響最大最容易釋放的就是活性磷Bio-P,尤其是在太湖這種Pca不易釋放的堿性水體中,高含量Bio-P的釋放導致了嚴重的水體富營養(yǎng)化現(xiàn)象.
從鐵形態(tài)分級提取得到的磷鐵含量垂直剖面(圖4)可以看出,隨著剖面深度的增加,3個采樣點磷形態(tài)變化和相對的鐵形態(tài)變化類似,1#剖面Fe分級提取的磷鐵含量均隨著剖面深度的增加而增加,且在剖面-3.5~-4.5cm處達到最小值,之后逐漸升高,在-8~-10cm處達到最大值;2#剖面磷鐵含量隨著沉積物剖面深度整體降低,且在-3cm處突然降低于-3.5cm處達到一個極小值,-4cm處升到極大值,之后再降低之后平穩(wěn);3#剖面磷鐵含量整體呈下降趨勢,除了第4步氧化還原鐵Feox2和Na2S2O4-P含量先升高后降低之后保持穩(wěn)定外,其余4步的磷鐵含量均在-2~3cm處先降低到極小值后,在-3~4cm處升到極大值,之后含量再次降低并保持平穩(wěn).由此可見,鐵形態(tài)分級提取得到的磷鐵具有極高的同步性,這是由于在提取不同形態(tài)鐵的同時,影響了與這一形態(tài)鐵相結合的磷形態(tài),或者是當水動力條件和理化因子發(fā)生改變時,導致鐵會以活性鐵形式從沉積物中釋放出Fe3+、Fe2+,與水體中的磷酸根陰離子發(fā)生絡合或者吸附反應,從而影響控制與之相關的磷形態(tài),采用鐵分級方法提取出的磷是與鐵形態(tài)最相關的磷形態(tài),因此二者的變化規(guī)律具有很好的同步性.王超等[19]采用磷、鐵分級方法也獲得沉積物中交換態(tài)磷Ex-P、鋁磷Al-P與可交換態(tài)鐵F1、無定形的鐵錳氧化物和水化氧化物結合態(tài)之間同步變化規(guī)律.馬旭陽[29]對黃河沉積物中鐵與磷的形態(tài)分布及相關分析中也發(fā)現(xiàn)過,黃河沉積物中Fe-6(殘渣態(tài)Fe)與Paut、PDe之間呈極顯著正相關(P<0.01),相關系數(shù)為0.558,0.618.不同磷、鐵形態(tài)之間的同步變化說明沉積物中鐵對磷的影響,為驗證磷鐵經典耦合機制提供了依據(jù).

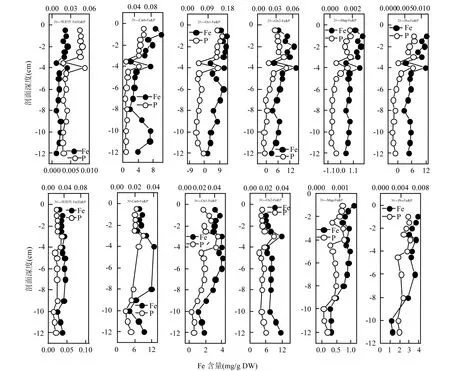
圖4 太湖研究點位沉積物Fe分級形態(tài)提取磷鐵含量垂直剖面Fig.4 Vertical profiles of Fe and P of sequential extraction for iron in the sediments from the investigated locations of Taihu
2.4 沉積物中磷與鐵形態(tài)的相關性
2.4.1 w(TFe)/w(TP)評價太湖不同湖區(qū)沉積物中磷的釋放風險 Jensen等[31]表明,w(∑Fe)/ w(∑P)是判斷沉積物中磷釋放潛力的指標,若沉積物中w(∑Fe)/w(∑P)大于15或20,則鐵控制磷釋放,磷釋放受到其抑制.太湖藻型、過渡型、草型湖區(qū)沉積物中w(∑Fe)/w(∑P)分別為33.27、43.23、55.08,說明太湖3種典型湖區(qū)沉積物中磷的釋放主要受鐵控制,但此外也會受到周邊環(huán)境、工農業(yè)生產水平等因素影響.
2.4.2 沉積物中不同形態(tài)鐵和磷之間的相關性分析 在對太湖不同湖區(qū)沉積物進行鐵的不同形態(tài)分級分析時,同時分析了不同浸提液提取的磷鐵含量及其相關性,從表3可以看出,太湖不同湖區(qū)沉積物磷鐵關系密切,鐵對磷的影響較大.除草型湖區(qū)對污染物緩沖作用強而導致Feox2大幅增加,因而與其他提取態(tài)磷鐵含量呈負相關外,其余不同湖區(qū)不同形態(tài)鐵之間相關性比較顯著,不同提取態(tài)磷含量也多呈正相關,并且磷鐵含量的相關系數(shù)都較高,第1步至第6步提取的分別是可吸附性Fe(Ⅱ),Fecarb,Feox1,Feox2,Femag,Feprs及同步提取的MgCl2-P,NaAc-P,NH2OH·HCl-P, Na2S2O4-P, (NH4)2C2O4-P,濃HCl-P磷含量隨沉積物剖面深度的變化都屬于顯著相關和極顯著相關(P>0.05,不顯著相關;P<0.05,顯著相關;P<0.01極顯著相關),其中1#剖面Fecarb及NaAc-P相關系數(shù)達到0.897(P<0.001),2#湖心區(qū)連二亞硫酸鈉和濃HCl提取的Feox2、Feprs及磷含量相關系數(shù)達到0.898和0.913(P<0.001),3#剖面Feox1和鹽酸羥氨-P相關系數(shù)為0.830(P<0.001).

表3 研究點位表層沉積物Fe分級形態(tài)提取磷鐵相關性Table 3 The relationships between different Fe and P fractions in the surface sediments from the investigated locations
太湖3個湖區(qū)沉積物中可吸附性Fe(Ⅱ)與MgCl2-P之間呈顯著正相關關系,相關系數(shù)分別為0.741(P<0.01)、0.919(P<0.01)和0.562(P<0.05),說明沉積物中部分由MgCl2所提取出的部分Pex的釋放受可吸附性Fe(II)的限制.Pex是非常活潑的形態(tài),當水動力條件和理化因子發(fā)生改變時釋放出PO43-進入水體,而以被吸附形式存在的可吸附性Fe(II)也會解吸進入水體,與其他離子進行反應.沉積物磷循環(huán)與鐵循環(huán)密切相關,Fe2+會與PO43-產生FePO4沉淀或吸附在FeO(OH)表面, 使Pex含量降低,但是在太湖這種堿性環(huán)境中,OH-與PO43-競爭表面吸附點位,導致部分Pex釋放,所以沉積物中可吸附性Fe(II)與MgCl2-P之間存在顯著正相關關系.
太湖不同湖區(qū)沉積物中Feprs與濃HCl-P呈顯著正相關關系,相關系數(shù)為0.717(P<0.01), 0.913(P<0.01),0.713(P<0.05).這部分提取的Feprs是除Femag和Fecarb以外的表硅酸鹽礦物,屬于低活性硅酸鐵,濃HCl灼燒能提取出部分有機磷Porg,Porg在礦化過程中能夠形成有機體膠膜,覆蓋在粘粒礦物、氧化鐵(或氫氧化鐵)以及碳酸鈣等礦物表面,從而影響鐵元素的釋放,因此二者呈顯著正相關關系.
不同湖區(qū)沉積物中Fecarb及NaAc-P,Feox1與NH2OH·HCl-P,Feox2與Na2S2O4-P均呈現(xiàn)顯著相關(P<0.01),高活性鐵(III)氧化物Feox1、Feox2和碳酸鹽鐵(Ⅱ)是占鐵分級總鐵Fe分級中比例最大的三種形態(tài)鐵,碳酸鹽結合態(tài)鐵對環(huán)境變化比較敏感,特別是當水體的酸堿條件發(fā)生改變時, 隨著碳酸鹽的分解,鐵會以活性鐵形式從沉積物中釋放出來, 進而與磷酸根陰離子發(fā)生絡合或吸附反應,而同步提取出的磷形態(tài)也是除MgCl2-P外3種含量最高的提取態(tài)磷,同時也是對水體磷負荷影響最大最容易釋放的就是活性磷Bio-P及Fe-P,說明太湖底泥中高活性鐵(III)是控制磷釋放的關鍵因子,高活性形態(tài)的鐵導致活性磷的釋放,水體內源磷負荷加重,太湖具有較高的釋放風險和生物可用性.
3 結論
3.1 太湖沉積物樣品中TFe分級含量藻型湖區(qū)30.29mg/g>過渡型湖區(qū)29.06mg/g>草型湖區(qū)24.29mg/g,各形態(tài)鐵以高活性鐵(III)氧化物Feox1、Feox2和碳酸鹽鐵(II)Fecarb所占比例最大,可還原(晶型)鐵氧化物Feox2是沉積物中鐵的主要存在形式;有機質含量與3個湖區(qū)沉積物剖面中Fecarb形態(tài)含量呈一定的負相關性,這證明了太湖湖區(qū)表層沉積物有機質含量對沉積物中碳酸鹽鐵的影響.
3.2 太湖不同湖區(qū)沉積物中各結合態(tài)磷以NH2OH·HCl-P所占比例最大,氯化鎂可能提取了其他交換態(tài)吸附性金屬離子結合的磷而提高了MgCl2-P所占比例,其余提取態(tài)磷所占比例同提取態(tài)鐵一致.通過鐵分級方法提取的磷形態(tài)主要是活性磷中的部分Pex和PFe,其次為部分無機磷(PCa和Pobs)和有機磷Porg,最易釋放的活性磷Bio-P導致了水體內源磷負荷加重.
3.3 通過判斷沉積物中磷釋放潛力的指標w(∑Fe)/w(∑P)得出太湖3種典型湖區(qū)沉積物中磷的釋放主要受鐵控制;3種不同湖區(qū)Fe形態(tài)分級得到的磷鐵呈現(xiàn)顯著正相關性(P<0.05),占Fe分級中比例最大的高活性鐵(III),控制著對水體磷負荷影響最大最容易釋放的活性磷Bio-P及Fe-P,說明太湖沉積物中鐵是控制磷釋放的關鍵因子,高含量高活性的磷鐵證明太湖具有較高的釋放風險和生物可用性.
參考文獻:
[1] 高 麗,楊 浩,周健民.湖泊沉積物中磷釋放的研究進展 [J].土壤, 2004,36(1):12-15.
[2] Downing J A, Cauley Mc E. The nitrogen: phosphorous relationship in lakes [J]. Limnology and Oceanography, 1992, 37(5):36-945.
[3] Jin L V, Wu H J, Chen M Q. Effects of nitrogen and phosphorus on phytoplankton composition and biomass in 15subtropical, urban shallow lakes in Wuhan, China [J]. Limnologica Ecology and Management of Inland Waters, 2011,41(1):48-56.
[4] Christophoros C, Fytianos K. Conditions affecting the release of phosphorus from surface lake sediments [J]. Journal of Environmental Quality, 2006,35(5):1181–1192.
[5] Bostrom B, Andersen J M, Fleischer S, et al. Exchange of phosphorus across the sediment-water interface [J]. Hydrobiologia, 1988,170(3):229-244.
[6] EINSELE W. Uber dieBeziehungen des EisenkreislaufszumPhosphatkreislaufim Eutrophen See [J]. Arch. Hydrobiol., 1936, 29:664-686.
[7] Mortimer C. The exchange of dissolved substances between mud and water in lakes [J]. J. Ecol., 1941,29:280-329.
[8] Rozan T F, Taillefert M, Trouwborst R E, et al. Iron-sulfurphosphorus cycling in the sediments of a shallow coastal bay: Implications for sediment nutrient release and benthic macroalgal blooms [J]. Limnology and Oceanography, 2002,47(5):1346-1354.
[9] Jensen H S, Kristensen P, Jeppesen E, et al. Iron: phosphorus ratio in surface sediment as an indicator of phosphate release from aerobic sediments in shallow lakes [J]. Hydrobiologia, 1992, 235(1):731-743.
[10] Lovely D R. Dissimilatory Fe (Ⅲ) and M n (Ⅳ) reduction [J]. Microbiol. Rev., 1991,55:259-287.
[11] 熊 毅,陳家坊,馬毅杰,等.土壤膠體(第二冊) [M]. 北京:科學出版社, 1985:245-268.
[12] 鄒元春,呂憲國,等.三江平原多級溝渠系統(tǒng)沉積物中鐵的分布特征 [J]. 環(huán)境科學, 2009,30(3):889-893.
[13] 楊宏偉,吳雅麗,等.黃河干流表層沉積物鐵形態(tài)的分布特征及相關性分析 [J]. 中國環(huán)境科學, 2015,35(12):3663-3669.
[14] 王 超,鄒麗敏,王沛芳,等.典型城市淺水湖泊沉積物中磷與鐵的形態(tài)分布及相關關系 [J]. 環(huán)境科學, 2008,29(12):3400-3404.
[15] 朱廣偉.太湖水質的時空分異特征及其與水華的關系 [J]. 長江流域資源與環(huán)境, 2009,18(5):439-445.
[16] S. W. Poulton, D. E. Canfield . Development of a sequential extraction procedure for iron:implications for iron partitioning in continentally derived particulates [J]. Chemical Geologym, 2005, 214:209–221.
[17] 王振華.湖泊沉積物鐵鋁對磷賦存形態(tài)及其轉化的影響 [D].哈爾濱:東北農業(yè)大學, 2012.
[18] 楊宏偉,郭博書,李經緯.內蒙古沙漠與沙塵粒子中磷形態(tài)分布特征及其環(huán)境意義 [J]. 環(huán)境化學, 2012,31(7):990- 997.
[19] 魯如坤.土壤農業(yè)化學分析方法 [M]. 南京:河海大學出版社, 2000.
[20] 鮑士旦.土壤農化分析 [M]. 北京:中國農業(yè)出版社, 2005.
[21] 袁和忠,沈 吉,等.太湖水體及表層沉積物磷空間分布特征及差異性分析 [J]. 環(huán)境科學, 2010,31(4):954-959.
[22] Enfeng Liu. Gavin F. Comprehensive evaluation of heavy metal contamination in surface and core sediments of Taihu Lake, the third largest freshwater lake in China [J]. Environ. Earth. Sci., 2012,67:39–51.
[23] Aller R C, Heilburun C, Panzeca C, et al. Coupling between sedimentary dynamics,early diagenetic processes, and biogeochemical cycling in the Amazon-Guianas mobile mudbelt: coastal French Guiana [J]. Marine Geology, 2004,208:331-360.
[24] Raiswell R, Canfield D E, Sources of iron for pyrite formation in marine sediments [J]. American Journal of Science, 1998,298: 219-245.
[25] Poulton S W, Raiswell R. The low-temperature geochemical cycle of iron:from continental fluxes to marine sediment deposition [J]. American Journal Science, 2002,302:774-805.
[26] Thamdrup B. Bacterial manganese and iron reduction in aquatic sediments [J]. Advances in Microbiology and Ecology, 2000,16: 41–84.
[27] Lovley D R, Holmes D E, Nevin K P. Dissimilatory Fe(III) and Mn(IV) reduction [J]. Advances in Microbial Physiology, 2004,49: 219-286.
[28] Canfield D E. Reactive iron in marine sediments. Geochimicaet Cosmochimica Acta, 1989, 53:619-632.Thamdrup B. Bacterial manganese and iron reduction in aquatic sediments [J]. Advances in Microbiology and Ecology, 2000,16:41–84.
[29] 馬旭陽.黃河水體沉積物中鐵與磷的形態(tài)分布及相關分析 [D].呼和浩特:內蒙古師范大學, 2015.
[30] 張 路,范成新,等.太湖及其主要入湖河流沉積磷形態(tài)分布研究 [J]. 地球化學, 2014,33(4):423-432.
[31] Jensen H S, Kristensen P, Jeppesen E, et al. Iron: Phosphorus ratio in surface sediment as an indicator of phosphate release from aerobic sediments in shallow lakes [J]. Hydrobiologia, 1992,235/ 236:731–743.
Distribution of iron forms and their correlations analysis with phosphorus forms in the sedimentary profiles of Taihu Lake.
YANG Wen-bin1*, TANG Hao1,2, HAN Chao2, DING Shi-ming2(1.College of Environmental Science and Engineering, Anhui Normal University, Wuhu 241003, China;2.State Key Laboratory of Lake Science and Environment, Nanjing Institute of Geography and Limnology, Chinese Academy of Sciences, Nanjing 210008, China). China Environmental Science, 2016,36(4):1145~1156
Abstract:Occureneces and distributions of iron forms in the sediment cores from three typically zones of Lake Taihu, i.e. phytoplankton dominated zone, macrophyte dominated zone, and phytoplankton-macrophyte transition zone, were investigated using the sequential extraction procedure. Generally, the total iron contents decreased in the order: phytoplankton dominated zone (31.57±8.51mg/g)> phytoplankton- macrophyte transition zone (30.34± 11.97mg/g)> macrophyte dominated zone (25.25±4.59mg/g), while the contents of different iron forms in the interest sites followed the variations: reducible oxides Feox2>carbonate associated Fe Fecarb>easilyreducible oxidesFeox1>poorly reactive sheet silicate FeFeprs>magnetite Femag>Absorbed Fe(Ⅱ), Fecarb、Feox1、Feox2weremeasured to be7.79mg/g, 6.16mg/g, 8.18mg/g, accounting for 28.56%, 21.54%, 29.53% of total iron respectively, suggesting those highly reactive iron Fe(III) were the dominated iron forms. The concents of different extracted phosphorus in sediment decreased in the order: NH2OH·HCl-P>MgCl2-P>NaAc-P>Na2S2O4-P>Concentrated HCl-P>(NH4)2C2O4-P. Three dominated phosphorus fractions including MgCl2-P、NaAc-P、NH2OH?HCl-Pwere measured to be 0.067mg/g, 0.061mg/g, 0.068mg/g, accounting for 35.28%、31.97% and 22.55% of the total extracted phosphorus.Significantly positive relationships were observed between the extracted phosphorus and iron fractions using the sequential extraction (P<0.05), further confirming the concomitant release of phosphorus from reduction dissolution ofFe (oxyhydr) oxides in sediments.
Key words:sequential extraction for iron;phytoplankton dominated zone;macrophyte dominated zone;phytoplanktonmacrophyte transition zone;correlativity;Taihu Lake
作者簡介:楊文斌(1968-),男,安徽長豐人,教授,博士,主要從事水環(huán)境生態(tài)修復研究.發(fā)表論文20余篇.
基金項目:安徽省自然科學基金項目(1208085MD60);國家自然科學基金項目(31070338)
收稿日期:2015-09-10
中圖分類號:X171
文獻標識碼:A
文章編號:1000-6923(2016)04-1145-12

