異丁烷-丁烯固體酸烷基化反應動力學研究進展
劉曉宇,周祥,郭錦標,王鑫磊,付翁(中國石油化工股份有限公司石油化工科學研究院,北京100083)
?
異丁烷-丁烯固體酸烷基化反應動力學研究進展
劉曉宇,周祥,郭錦標,王鑫磊,付翁
(中國石油化工股份有限公司石油化工科學研究院,北京100083)
摘要:探究了固體酸烷基化反應機理和轉化規律,對其進行動力學研究具有重要的理論和現實意義。概述了固體酸烷基化反應體系具有代表性的動力學研究成果,總結了不同尺度動力學模型的建立規則和對改善催化劑失活所提供的建議,指出建立固體酸烷基化分子水平機理層面動力學模型,對本征動力學性質進行描述,反映動力學參數與原料性質、操作變量、催化劑之間存在的內在聯系,可以更好地為新型催化劑研發、反應器設計和工藝流程優化提供理論支持。
關鍵詞:烷基化;固體酸;動力學;催化劑失活;機理層面動力學模型
第一作者:劉曉宇(1984—),女,博士研究生,主要從事烷基化反應動力學研究工作。聯系人:郭錦標,教授級高級工程師。E-mail guojinbiao.ripp@sinopec.com。
面對日益嚴重的環境污染問題,發展經濟型清潔汽油燃料已是當務之急。目前我國汽油的主要成分是催化汽油和重整汽油,此外還需添加MTBE等高辛烷值組分。隨著新汽油使用標準的頒發,對汽油中芳烴、烯烴、硫含量等指標的限制更為嚴格,亟需開發清潔的高品質汽油調合組分,要求其具有高辛烷值,又要控制對芳烴、烯烴、硫等的引入,滿足環保要求。利用催化裂化產物裂化氣中的異丁烷與丁烯生產的烷基化汽油,其主要成分為異辛烷,具有辛烷值高(RON95~98)、無芳烴、硫,Reid蒸汽壓低等優點,是十分理想的汽油調合組分。
傳統的烷基化汽油生產工藝使用的是液體酸催化劑[1],如氫氟酸、硫酸等,但是液體酸催化劑存在高酸耗、設備腐蝕、廢硫酸處理困難和HF腐蝕性揮發等環境污染和安全問題。因此,國內外著力開發既可滿足安全和環保要求,又易于再生的固體酸催化劑及生產工藝。目前已開展研究的固體酸催化劑主要有分子篩、雜多酸、固體超強酸[2-4]等,但由于都存在快速失活和選擇性差的問題,難以實現工業化。因此更多研究關注其反應動力學,通過對反應機理進行探索,描述反應物的轉化規律,可對反應器設計、工藝流程優化、新型催化材料開發提供理論支持。
1 烷基化反應機理
烷基化反應機理研究在文獻中多見報道[5],遵循正碳離子反應機理,為B酸催化體系。反應中間體為正碳離子,不同于液體酸催化體系,固體酸催化體系的反應中間體為吸附態正碳離子。CORMA 等[6]利用ONIOM方法,證明在B酸中心上烯烴發生質子化反應,通過類似正碳離子結構的過渡態,然后與分子篩表面上的O原子結成烷氧鍵,生成相對穩定的中間體。JANIK等[7]則以雜多酸為例,應用DFT分子模擬技術,確定反應中間體正碳離子以烷氧鍵形式吸附在催化劑表面,并計算了上述反應的能壘,如圖1所示。由此可以認為,固體酸烷基化反應中間體是與催化劑表面生成烷氧鍵的吸附態正碳離子。

圖1 固體酸催化體系中吸附態正碳離子存在形式
固體酸反應體系中包括8種基元反應類型,分別為質子化反應/去質子化反應、PCP異構反應、分子內氫/甲基轉移反應、聚合反應、β-斷裂反應、分子間氫轉移反應(hydride transfer)。實驗證明,在非高溫反應條件下,烷烴不能發生脫氫和脫甲基反應,生成正碳離子[8]。
(1)質子化反應 該反應是烷基化反應的始發反應,按照Markovnikov’s規則,由烯烴雙鍵與催化劑活性中心的氫質子發生反應,經過過渡態,生成吸附態的正碳離子中間體,反應快速達到平衡。隨著催化劑酸強度增加,可以降低反應活化能,加速反應進行[9],如式(1)。

(2)去質子化反應 該反應是質子化反應的逆反應,吸附態的正碳離子發生脫附反應,生成烯烴,還原催化劑活性中心,比質子化反應具有更高的能壘,如式(2)。

(3)分子內氫轉移和分子內甲基轉移反應 這兩類基元反應是不產生支鏈變化的異構化反應,發生在帶有正電荷或甲基取代基的碳原子和比鄰碳原子之間,如式(3)、式(4)。
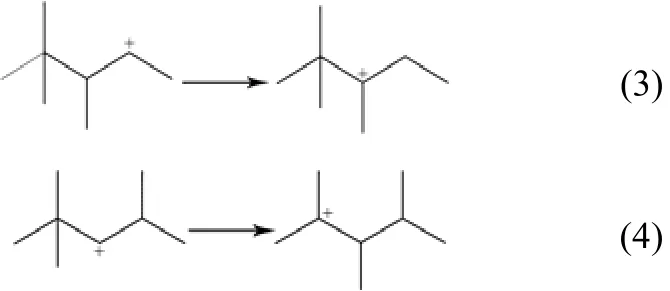
(4)PCP異構化反應 吸附態正碳離子按照Brouwer’s反應規則發生PCP異構,產生支鏈變化。BORONAT等[10]分別討論直鏈C4+和直鏈C5+發生PCP反應的機理路徑,發現直鏈C4+通過甲基環丙烷伯正碳離子過渡態,生成叔丁基正碳離子。而直鏈C5+則不同于直鏈C4+,無法經過PCP異構直接生成叔正碳離子。而是先由經過PCP異構生成仲正碳離子,而后發生分子內氫轉移反應,生成叔正碳離子,如式(5)、式(6)。
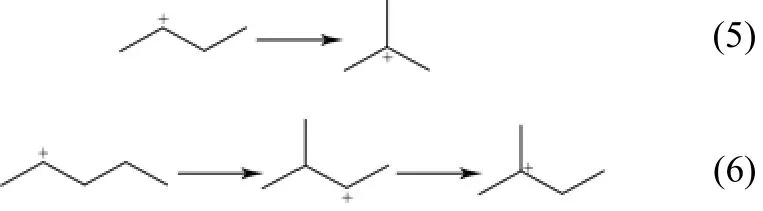
(5)聚合反應 該反應發生在正碳離子和烯烴之間,吸附態正碳離子的正電荷進攻烯烴雙鍵,帶有正電荷的碳原子與具有較少取代基的雙鍵碳原子之間生成新的σ鍵,如式(7)。
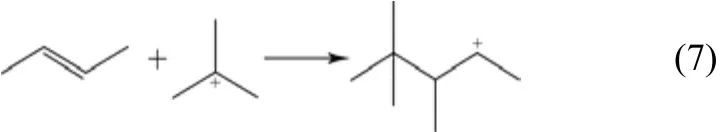
(6)β-斷裂反應 該反應是帶有正電荷的碳原子的α位和β位之間發生斷鍵,相對應生成小分子的烯烴和正碳離子。大分子正碳離子更易發生β-斷裂反應,隨著催化劑酸強度越大[10],越有利于β-斷裂反應的發生,正碳離子碳鏈越長,越易于發生β-斷裂反應,如式(8)。

(7)分子間氫轉移反應 該反應發生在B酸中心上[11],由正碳離子攻擊異丁烷的C—H鍵,正碳離子生成相應的烷烴,異丁烷生成叔丁基正碳離子。此反應為決定催化劑失活快慢的關鍵步驟,如式(9)。
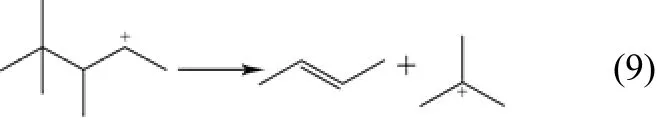
根據生成目標產物和副產物的反應路徑,可將烷基化反應體系劃分為主反應體系和副反應體系。在主反應體系中,首先由丁烯(C4=)接受B酸中心提供的氫質子,生成吸附態正碳離子(CR+)后與C4=發生聚合反應生成C8+,再與異丁烷(C40)發生分子間氫轉移反應,對應生成tri-C4+和目標產物iC80。在副反應體系中,C8+可以繼續與C4=發生聚合反應,生成C12+等大分子的不飽和高聚物,不易發生去質子化反應和分子間氫轉移反應,導致催化劑失活。CR+還可以發生β-斷裂反應,生成C3+~C9+和C3=~C9=。體系中所有CR+都可以發生分子內氫/甲基轉移和PCP異構反應,并與C40發生分子間氫轉移反應,所以烷基化反應體系中物種分布主要包括:C30~C90,C3=~C9=,C3+~C12+,見圖2。
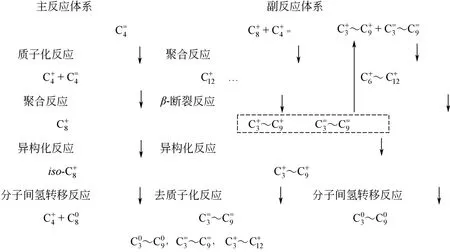
圖2 烷基化反應體系物質分布
烷基化反應產物中最理想組分為三甲基戊烷(TMP),主要是由tri-C4+與丁烯聚合生成,而sec-C4+與丁烯聚合對應生成DMH(二甲基己烷),由此可見,反應中間體正碳離子的結構與目標產物分布密切相關。
引起催化劑失活的原因[12]是反應過程中生成C12+等大分子的不飽和高聚物,覆蓋在催化劑活性中心上或堵塞催化劑孔道,并隨著催化劑的失活,產物選擇性發生變化,產物中TMP和DMH收率下降,C5~C10組分增多。
2 烷基化動力學
研究反應動力學的目的是明確化學反應速率,一是可以通過擬合反應速率與反應條件(溫度、壓力和組分濃度等)之間的關系,從宏觀角度建立關聯模型;二是實現對反應機理的驗證,對本征動力學性質進行描述,從微觀角度建立分子水平動力學模型,可以分為路徑層面和機理層面兩個層次。對于固體酸烷基化反應體系,諸多研究工作分別從宏觀和微觀研究反應物的轉化規律進行動力學研究,建立不同尺度的動力學模型。
早期,SIMPSON等[13]從探求液-固相反應失活路徑的角度,對烷基化體系進行動力學分析,建立了與反應條件關聯的烯烴轉化速率模型。針對主要反應:丁烯與C4+發生聚合反應(速率常數k1)、C8+發生分子間氫轉移反應(速率常數k2)和丁烯與C8+發生聚合反應(速率常數k3),進行了討論。通過實驗數據,計算出烯烴與C4+聚合反應速率常數k1大于其與C8+聚合反應的速率常數k3,而k3又遠遠大于異丁烷與C8+發生分子間氫轉移的反應速率常數k2。得出結論:由于k1>k3>k2,導致生成C12+的速率大于生成異辛烷的速率,從而引起催化劑的失活。而引起k2過小的原因是分子間氫轉移反應受空間位阻影響。此外在液相反應條件下,對于超穩Y型分子篩催化劑而言,引起失活的原因還有嚴重的內擴散限制,并應用脈沖實驗對此進行了驗證,當反應物以氣態參與反應,消弱內擴散影響時,可減緩失活。因此設定丁烯聚合和分子間氫轉移反應為一級反應,并引入擴散系數,在不考慮催化劑失活的情況下,認為反應體系中各烴類轉化近似平衡,所以將C4=的轉化率與k1、k2進行關聯,回歸出烯烴轉化率與反應條件之間的數學關系。然后以催化劑活性中心被不易脫附的高聚物(C12+)覆蓋視為催化劑失活,將催化劑失活速率和異丁烷與C8+發生分子間氫轉移的反應速率常數k3進行關聯,以此建立的失活動力學模型。該研究從動力學的角度對固體酸失活路徑進行了闡述,因此反應條件優化和反應器設計以及分子篩改性應側重解決分子間氫轉移反應的空間位阻和內擴散影響。TAYLOR等[14]進一步將反應時間作為衡量因素,建立了考慮反應時間的失活動力學模型,將總包反應IB(異丁烷)+2B(丁烯)—→Products設定為一級反應,根據阿倫尼烏斯公式求取反應速率常數。引入失活速率常數kd(kd與反應時間定量相關),以校正實際反應速率常數kw。然后將反應速率與烯烴轉化率、烯烴流率和催化劑用量進行關聯,求得kd和kw,進而可知對應的活化能和指前因子。該模型可用來估算不同溫度下隨時間變化的丁烯轉化率和有效反應時間。
上述對固體酸體系的動力學研究都是在實驗數據的基礎上,以烯烴轉化率為研究對象,回歸其與反應時間、反應條件的定量關系的關聯模型,并不能從反應本質出發,討論催化劑對反應速率和方向的影響,從預測產物組成和分布的角度反映催化性能。因而NAYAK等[11]嘗試將反應體系進行細致的劃分,研究不同反應之間的關系,進行產物的預測。對體系中6個反應路徑進行討論,建立分子水平路徑層面動力學模型,在SIMPSON等研究的基礎上,對內擴散限制影響進行動力學研究。NAYAK認為體系為B酸催化,將活性中心濃度設定為B酸濃度,將生成C12+的B酸中心視為失活。應用所建模型分析可知,減小分子間氫轉移反應受內擴散限制影響,可減緩催化劑失活。進而得出結論:催化劑上B酸中心以“蛋殼”(在催化劑外表面成薄層分布)形式分布可對抑制催化劑失活有積極作用,并且隨著硅鋁比的下降,B酸中心增加,可以增加產物中TMP的含量。增加進料烷烯比,同樣可以改善催化劑失活。該模型對C8產物的預測結果與實驗結果相比較,偏差在5%范圍內,但該路徑層面動力學模型對產物組成和收率不能實現分子水平的預測,且動力學參數依賴實驗數據回歸,外推性差。
SANCHEZ-CASTILLO等[15]以預測產物分子水平為目的,在機理層面對氣-固相烷基化體系進行研究,建立適用于523~773K溫度范圍的動力學模型。認為體系中包含7種基元反應,分別為烯烴質子化、正碳離子去質子化、異構化、分子間氫轉移、聚合、β-斷裂、異丁烷脫氫/脫甲基反應(高溫下發生)。該動力學模型將反應中間體設定為吸附態正碳離子,建立求取吸附焓的經驗公式以此計算取吸附態正碳離子生成焓,其中取值為?90kJ/mol;Ha作為回歸參數。根據反應機理,構建的反應網絡包括277個分子和中間體,370個基元反應,共劃分為4個反應族。根據反應族概念和熱力學限制將動力學參數化簡為12個,并利用分子模擬計算和實驗數據回歸的方法分別計算活化能。對于質子化反應,設定所有反應的活化能為固定值,利用分子模擬技術計算活化能為50kJ/mol;對聚合/裂化反應,根據正碳離子在反應過程中結構的變化,將活化能劃分為3種,回歸得到Ett=102.2kJ/mol、Est=Ess= 115.1kJ/mol;對于異構化反應,利用分子模擬技術計算活化能,其中無支鏈數變化異構化反應活化能為80kJ/mol,有支鏈數變化異構化反應活化能為110kJ/mol;對于分子間氫轉移反應族,根據發生反應的正碳離子碳數分別回歸活化能EC3=64.3kJ/mol、EC4=76.5kJ/mol、EC≥5=62.2kJ/mol。將計算得出的參數應用于模型,預測產物組成與實驗數據趨勢吻合。然后通過考察各基元反應對產物收率影響,進行靈敏度分析,將反應網絡化簡為31個反應,構建了涵蓋主要動力學信息的反應網絡。該模型對固體酸烷基化反應體系實現了機理層面的定性研究,但模型定量研究上存在偏差,沒有細致討論各基元反應反應速率的差異,體現催化劑對不同類型基元反應的催化活性。
MARTINIS等[8,16]建立的考慮催化劑失活的單事件機理層面動力學模型,對烷基化體系進行更為細致的定性研究,并著重在定量的角度,將動力學參數與催化劑性質相關聯,考慮催化活性對反應速率的影響。該模型根據體系中基元反應類型共劃分為7個反應族:烯烴質子化、正碳離子去質子化、分子內氫轉移、分子內甲基轉移、分子間氫轉移、聚合、β-斷裂。根據反應機理,制定反應規則,利用計算機軟件生成包含3130個基元反應的反應網絡。利用單事件概念、Evans-Polanyi關系式和熱力學約束將3130個動力學參數化簡為11個。并根據線性自由能關系,利用熱力學參數計算動力學參數。因此,活化能轉化為參數E0,α和反應焓變的函數,結合實驗數據對參數E0、α進行回歸。并通過引入穩定能,建立了計算吸附態正碳離子生成焓的新方法,將動力學參數與催化劑性質相關聯。將碳數大于8的正碳離子視為積炭前體,失活函數通過活性中心被不可逆吸附正碳離子的覆蓋率來表示,并在反應速率方程中引入失活系數,以此校正為實際反應速率。利用實驗數據對于模型預測結果進行驗證,預測結果與實驗數據較好吻合。通過對各反應族活化能的計算發現,分子間氫轉移活化能較大,這是造成C8+易與烯烴發生聚合反應,不易與異丁烷發生分子間氫轉移反應的原因,從而引起催化劑失活,所以催化劑設計應關注具有高密度的中強酸活性中心的介孔分子篩催化劑,以改善催化劑失活。
3 結語
對于固體酸烷基化體系的動力學研究,從SIMPSON等和TAYLOR等所建立的關聯模型可以看出分子篩催化劑改性應側重解決分子間氫轉移反應的空間位阻和內擴散影響。而NAYAK等所建立的路徑層面動力學模型,通過對B酸催化機理驗證和內擴散影響考慮,提出了對分子篩催化劑構型的改性優化和反應器設計的建設性意見,認為B酸中心以“蛋殼”(在催化劑外表面成薄層分布)形式分布可對抑制催化劑失活有積極作用,并且隨著硅鋁比的下降,B酸中心增加,可以增加產物中TMP的含量。SANCHEZ-CASTILLO等和MARTINIS等建立了分子水平機理層面動力學模型,更深入對本征動力學的研究,對反應網絡中基元反應反應速率進行理論計算,將動力學參數與催化劑酸中心濃度和酸強度相關聯,認為新型固體酸烷基化催化劑研發應關注具有高密度的中強酸活性中心的介孔分子篩催化劑,可以有效降低分子間氫轉移反應活化能,改善催化劑失活。
隨著研究固體酸烷基化反應體系的關注點越來越轉向反應組分發生表面反應的轉化規律,因此對固體酸烷基化反應體系進行分子水平機理層面動力學研究可以更好地對本征動力學性質進行描述,將動力學參數與催化劑性質相關聯,以體現催化劑活性差異,反映出其與原料性質、操作變量、催化劑之間存在的內在聯系,為新型固體酸催化劑研發提供定性和定量的理論支持。然而,機理層面動力學模型規模較大,存在參數計算、優化和模型求解困難等問題,部分參數仍依賴實驗數據回歸。因此控制模型規模合理而又不損失動力學信息和建立本征動力學參數的計算方法,是有待解決的重要問題。并且隨著分析技術的發展,完善對積炭的定性分析,進一步明確失活機理,對固體酸烷基化體系的動力學研究將更為全面,在此基礎上建立分子水平機理層面動力學模型將作為該領域的發展方向,可以更好地為新型催化劑研發、反應器設計和工藝流程優化提供理論支持。
參考文獻
[1]WEITKAMP J,TAA Y. Isobutane/butene alkylation on solid catalysts where do we stand[J]. Catalysis Today,1999,49:193-199.
[2]CORMA A,MARTINEZ A. Chemistry,catalysts and process for isoparaffin-olefin alkylation:actual situation and future trends[J]. Catal. Rev.:Sci. Eng.,1993,35(4):83-570.
[3]何奕工,舒興田. 超臨界流體狀態下的異構烷烴與烯烴烷基化反應[J]. 催化學報,1999,40(3):403-408.
[4]CORMA A,JUAN-RAJADELL M I,LOPEZ-NIETO J M,et al. A comparative study of O42?/ZrO2and zeolite beta as catalysts for the isomerization of n-butane and the alkylation of isobutane with 2-butene[J]. Applied Catalysis A,1994,111(2):175-189.
[5]FELLER A,ZUAZO I,GUZMAN A. Common mechanistic aspects of liquid and solid acid catalyzed alkylation of isobutane with n-butene[J]. Journal of Catalysis,2003,216:313-323.
[6]BORONAT M,VIRUELA P M,CORMA A. Reaction intermediates in acid catalysis by zeolites:prediction of the relative tendency to form alkoxides or carbocations as a function of hydrocarbon nature and active site structure[J]. J. Am. Chem. Soc.,2004,126:3300-3309.
[7]JANIK M J,DAVIS R J,NEUROCK M. A density functional theory study of the alkylation of isobutane with butene over phosphotungstic acid[J]. Journal of Catalysis,2006,224:65-77.
[8]MARTINIS J M,FROMENT G F. Alkylation on solid acids.Part 1.Experimental investigation of catalyst deactivation[J]. Ind. Eng. Chem. Res.,2006,45:940-953.
[9]FANG H,ZHENG A,LI S,et al. New insights into the effects of acid strength on the solid acid catalyzed reaction:theoretical calculation study of olefinic hydrocarbon protonation reaction[J]. J. Phys. Chem. C,2010,114(22):10254-10264.
[10]BORONAT M,VIRUELA P,CORMA A. Theoretical study of the mechanism of branching,rearrangement of carbenium ions[J]. Applied Catalysis A:General,1996,146:207-223.
[11]NAYAK S V,RAMACHANDRAN P A,DUDUKOVIC M P. Modeling of key reaction pathways:zeolite catalyzed alkylation processes[J]. Chemical Engineering Science,2010,65:335-342.
[12]BARTHOLOMEW C H. Mechanisms of catalyst deactivation[J]. Applied Catalysis A:General,2001,212:17-60.
[13]SIMPSON M F,WEI J,SUNDARESAN S. Kinetic analysis of isobutane/butene alkylation over ultrastable H-Y zeolite[J]. Ind. Eng. Chem. Res.,1996,35:3861-3873.
[14]TAYLOR R J,SHERWOOD JR D E. Effects of process parameters on isobutane/2-butene alkylation using a solid acid catalyst[J]. Applied Catalysis A:General,1997,155:195-215.
[15]SANCHEZ-CASTILLO M A,AGARWAL N,MILLERET C,et al. Reaction kinetics study and analysis of reaction schemes for isobutane conversion over USY zeolite[J]. Journal of Catalysis,2002,205:67-85.
[16]MARTINIS J M,FROMENT G F. Alkylation on solid acids. Part 2.Single-event kinetic modeling[J]. Ind. Eng. Chem. Res.,2006,45:954-967.
研究開發
Advances in the research development of isobutane/butene solid acid-catalyzed alkylation kinetics
LIU Xiaoyu,ZHOU Xiang,GUO Jinbiao,WANG Xinlei,FU Weng
(Research Institute of Petroleum Processing,SINOPEC,Beijing 100083,China)
Abstract:Kinetic analysis for understanding the reaction mechanism and hydrocarbon transformations rules has both theoretical and practical significance. The typical development and main research methods at different scales for alkylation kinetics are reviewed in this paper. Recommendations for improving the catalyst are made. The molecular-based kinetic modeling could provide detailed and explicit descriptions of the intrinsic kinetic properties,which reflect the relationship between the kinetic parameters and the feedstock,reaction conditions and catalyst. Mechanistic kinetic modeling could show important theoretical support for the optimization of reactor configuration,technological process and catalysts research.
Key words:alkylation; solid acid; kinetics; catalyst deactivation; mechanistic kinetic modeling
中圖分類號:TE 624.4
文獻標志碼:A
文章編號:1000–6613(2016)04–1007–05
DOI:10.16085/j.issn.1000-6613.2016.04.006
收稿日期:2015-08-12;修改稿日期:2015-11-01。

