十六烷基三甲基溴化銨修飾P型沸石吸附水中直鏈烷基苯磺酸鈉的研究
譚文淵, 徐 曼, 曾 英
(1. 成都理工大學材料與化學化工學院, 成都 610059;
2. 四川理工學院分析測試中心, 自貢 643000)
?
十六烷基三甲基溴化銨修飾P型沸石吸附水中直鏈烷基苯磺酸鈉的研究
譚文淵1,2, 徐曼2, 曾英1
(1. 成都理工大學材料與化學化工學院, 成都 610059;
2. 四川理工學院分析測試中心, 自貢 643000)
摘要通過使用堿液對天然斜發沸石(Z)進行處理制得P型沸石(PZ), 再用十六烷基三甲基溴化銨(CTMAB)對Z和PZ進行修飾, 制得有機改性沸石ZC和PZC, 對比考察了ZC和PZC對直鏈烷基苯磺酸鈉(LAS)的吸附性能. 實驗結果表明, 制得的PZ硅/鋁比為2, 比Z(4.85)降低58.8%; PZ的零凈電荷點、比表面積、孔徑和孔容均高于Z; 吸附平衡時間為4 h. 當pH=2時, ZC和PZC對LAS吸附量達到最高, 吸附數據符合Langmuir準二級動力學方程和Langmuir等溫吸附方程, 飽和吸附量(qm)分別為12.658和27.100 mg/g, 吸附過程主要為單分子層的化學吸附, PZC的吸附速率常數大于ZC, 具有更好的動力學性能.
關鍵詞P型沸石; 十六烷基三甲基溴化銨; 直鏈烷基苯磺酸鈉; 吸附
直鏈烷基苯磺酸鈉(LAS)是一種重要的陰離子表面活性劑, 每年我國消耗的LAS總量超過100萬噸. 大量的LAS進入水體會在環境和生物體內累積并對動植物產生毒害作用[1~3]. LAS已成為我國地表水體標志性有機污染物之一, 許多環境工作者一直致力于LAS廢水的處理研究[4~13]. 宋揚等[14]在優化的實驗條件下采用Fenton氧化-好氧接觸工藝將含高濃度硫酸鹽的LAS廢水中的LAS濃度由490 mg/L降至23 mg/L. 廢水中LAS的處理方法較多, 采用吸附法處理LAS廢水具有操作簡單的特點[15], 但需要進一步開發高效、環境友好、價廉易得的吸附劑[16,17].
我國天然沸石種類多, 資源豐富, 價格低廉, 具有多種特殊理化性能, 在水處理及催化領域已有廣泛應用[18~23]. 但天然沸石孔道容易被細碎顆粒堵塞, 造成孔道相互連通的程度較差; 且沸石表面鋁氧結構帶負電荷且具有極強的親水性, 導致天然沸石吸附有機物及陰離子污染物的性能極差. 因此, 為了滿足沸石對污染物的處理要求, 常常需要對其進行改性處理, 處理方法主要是內部改性[24~26]和外部改性[27,28]. 內部改性是為了改變沸石的內部結構、孔徑, 使污染物進入沸石孔道內部從而得以去除, 主要用于小分子污染物的去除; 外部改性是對沸石外表面的改性, 通過離子置換以增大污染物質在不同相的分配系數來使沸石具有去除污染物的能力, 通常是用于有機污染物尤其是大分子有機污染物的去除[29].
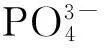
本文對天然斜發沸石進行內部和外部兩步改性處理: 先用堿液對沸石進行處理, 制得P型沸石, 降低硅鋁比, 增加離子交換能力; 再用CTMAB對P型沸石進行表面有機改性, 在沸石表面形成疏水層; 然后研究兩步改性后的沸石對溶液中LAS的吸附性能, 探討了降低硅鋁比對沸石吸附LAS性能的影響.
1實驗部分
1.1試劑與儀器
直鏈烷基苯磺酸鈉(天津博迪化工股份有限公司); 十六烷基三甲基溴化銨(成都市科龍化工試劑廠); 濃鹽酸(HCl, 質量分數36.46%, 鄭州鑫誠化工有限公司); 氫氧化鈉(NaOH, 成都市恒億化工產品有限公司); 濃硝酸(HNO3, 質量分數65%—68%, 成都市科龍化工試劑廠). 以上試劑均為分析純. 天然斜發沸石(2~4 mm, 北票鑫鑫沸石廠).
美國PE公司LAMDA35型紫外-可見雙光束全波段掃描分光光度計; 捷克TESCAN公司VEGA3Easyrobe型掃描電子顯微鏡及布魯克X射線電子能譜儀(SEM-EDS); 德國布魯克AXE公司D2 PHASER型X射線衍射(XRD), CuKα射線源, 管電壓30 kV, 管電流10 mA, 掃描角度(2θ)為7°~35°, 步長0.02°, 每步掃描時間0.2 s; 北京彼奧德電子有限責任公司SSA-4300型孔徑及比表面測定儀; 美國PE公司Frontier Near/Mid-IR Std型傅里葉變換紅外光譜儀(FTIR), 將沸石與溴化鉀(質量比為1∶10)混合研磨后壓片; 德國Elementar公司Vario EL cube型元素分析儀; 奧豪斯(上海)公司STARTER 2100型酸度計.
1.2有機改性沸石的制備
1.2.1天然沸石的預處理 將天然斜發沸石(Z)用粉碎機粉碎后篩選出60~80目的樣品, 用去離子水多次洗滌后在電熱鼓風干燥箱(105 ℃)中干燥2 h, 放入干燥器中備用.
1.2.2P型沸石的制備參照文獻[32]方法, 將30 g預處理后的沸石放入250 mL圓底燒瓶中, 向燒瓶中加入100 mL 5 mol/L的氫氧化鈉溶液, 在(95±5) ℃回流加熱70 h, 加少量酸中和后, 用去離子水洗至中性, 于電熱鼓風干燥箱(105 ℃)中干燥2 h, 放入干燥器中備用. 所得樣品記為PZ.
1.2.3CTMAB改性沸石的制備參照文獻[33]方法, 將經過預處理的天然沸石和水熱反應后的P型沸石各10 g加入到2個錐形瓶中, 再依次加入150 mL CTMAB(1 g/L)溶液, 混合后放入電熱恒溫振蕩槽振蕩24 h, 控制溫度為30 ℃, 轉速為120 r/min. 用去離子水清洗CTMAB修飾后的沸石2~3次, 放入電熱鼓風干燥箱干燥, 即制得樣品ZC和PZC.
1.3沸石零凈電荷點(PZNC)的測試
沸石的PZNC通過質量滴定(Mass titration)法測定[34,35]: 取25 mL濃度為0.001 mol/L的NaNO3溶液于6個25 mL比色管中, 用HNO3或NaOH溶液調節初始pH值分別為2, 4, 6, 8, 10, 12后, 分別加入一定量的沸石, 使沸石固體濃度(cs)為5 g/L, 在恒溫(25±0.2) ℃下振蕩24 h, 測定懸浮液的平衡pH值. 再改變沸石固體濃度分別為10, 50, 100, 150和200 g/L, 重復上述操作, 將平衡pH值對cs作圖得到質量滴定曲線, 即可得到沸石的PZNC值.
1.4pH值對吸附量的影響
采用HCl和NaOH調節體系pH值, 配制濃度為30 mg/L、pH值分別為2, 4, 6, 8, 10, 12的LAS溶液, 分別取每種pH值溶液各200 mL, 加入0.2 g有機改性后的沸石ZC和PZC, 放入電熱恒溫振蕩水槽中, 調節溫度為20 ℃, 轉速為120 r/min, 4 h后采用紫外-可見分光光度法測定溶液中LAS的濃度, 得到pH值對吸附量的影響曲線. 按下式計算沸石對LAS的吸附量qt(mg/g).
(1)
式中: c0(mg/L)為LAS的初始濃度; ct(mg/L)為吸附LAS后t時刻的濃度; V(L)為加入LAS溶液的體積; m(g)為沸石質量.
1.5溫度對吸附量的影響
稱取ZC和PZC各0.2g依次加入到200mL30mg/LLAS(最佳吸附的pH值下)溶液中, 將溶液放入電熱恒溫振蕩槽內, 分別設置溫度為20, 30, 40和50 ℃, 轉速為120r/min, 吸附4h后采用紫外-可見分光光度法測定溶液中LAS濃度. 按式(1)計算沸石對LAS的吸附量.
1.6時間對吸附量的影響
稱取ZC和PZC各0.2g依次加入到200mL30mg/LLAS(最佳吸附的pH值下)的溶液中, 將溶液放入電熱恒溫振蕩槽內, 設置最佳吸附溫度, 轉速為120r/min, 吸附不同時間后采用紫外-可見分光光度法測定溶液中LAS濃度. 按式(1)計算沸石對LAS的吸附量.
1.7吸附動力學參數的確定
根據1.6節中所得實驗數據, 用Langmuir準一級動力學模型和準二級動力學模型進行擬合并求得吸附速率常數:
(2)
(3)
式中: qe(mg/g)為平衡吸附量; k1(min-1)為準一級反應吸附平衡速率常數; k2[g/(mg·min-1)]為準二級反應吸附平衡速率常數.
1.8吸附等溫線的確定
配制一系列濃度為10, 20, 30, 40, 50, 60, 70, 80, 90和100mg/L的LAS溶液(最佳吸附的pH值下)各200mL, 分別向每組加入ZC和PZC各0.2g, 將混合后的溶液放入到電熱恒溫振蕩水槽中, 控制轉速為120r/min, 調節溫度為最佳吸附溫度, 振蕩至平衡后, 采用紫外-可見分光光度法測定溶液中LAS濃度. 用Langmuir和Freundlich吸附等溫式對吸附結果進行處理得到吸附等溫線.Langmuir和Freundlich吸附等溫式如下:
(4)
(5)
式中:Ce(mg/L)為吸附平衡時LAS的質量濃度;qm(mg/g)為飽和吸附容量;KL(L/mg)表示LAS與吸附劑之間作用力的大小;KF和n為待定系數.
2結果與討論
2.1沸石的表征
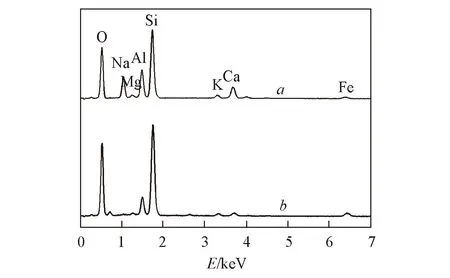
Fig.1 EDS of PZ(a) and Z(b)
對原沸石和在1.2節中制得的P型沸石進行EDS分析(圖1), 結果表明, 原沸石中硅與鋁的摩爾分數分別為19.70%和4.06%, P型沸石中硅與鋁的摩爾分數分別為13.72%和6.84%. 可以看出, 經過堿液處理后, 沸石中的部分硅溶解, 使得硅鋁比變為2, 相對于原沸石硅鋁比(4.85)降低58.8%. 相關沸石的SEM形貌分析結果見圖2. 由圖2可見, 原沸石聚結成塊, 且細碎顆粒較多; 而P型沸石表面分布著較規則的顆粒. Kazemian等[36]認為是在堿液處理過程中溶解了無定形凝膠雜質和小沸石晶體, 純化大晶體所致; 經過CTMAB修飾后, 原沸石和P型沸石均可看見覆蓋著一層灰色物質, 推測為CTMAB.

Fig.2 SEM images of Z(A), ZC(B), PZ(C) and PZC(D)
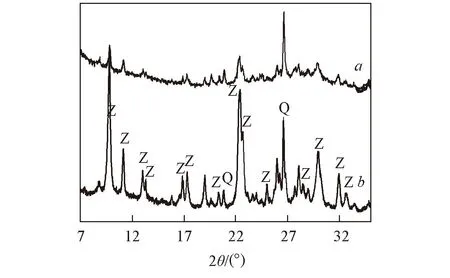
Fig.3 XRD patterns of PZ(a) and Z(b) Z: Zeolite; Q: Quartz.
沸石改性前后的XRD測試結果見圖3. 對比沸石經堿液處理后的XRD譜與天然斜發沸石的標準衍射譜(JCPDS39-1383)發現, 經堿液處理后的沸石仍在2θ=9.88°, 11.21°, 13.05°, 17.38°, 19.09°, 22.36°, 22.52°和26.04°處出現了特征衍射峰, 說明沸石的骨架結構并未發生改變. 同時在該沸石樣品中可發現有少量共生石英礦物.
沸石的質量滴定曲線見圖4. 可以看出, P型沸石的PZNC值比原沸石增大, 可以推測沸石經過堿液處理后硅鋁比降低, 鋁氧四面體在沸石晶體中所占比例增加, 沸石的結構負電荷增多. 沸石改性前后的比表面積和孔徑測試結果見表1. 沸石在內部改性后比表面積、總孔容積和孔徑增加; 在進行外表面改性后, 比較面積和總孔容積減小. 這是由于沸石經堿液處理后, 溶解了部分硅和其中的無定形凝膠雜質, 沸石變得疏松; 而在表面改性后CTMAB附著在沸石表面堵塞了一些孔道所致.
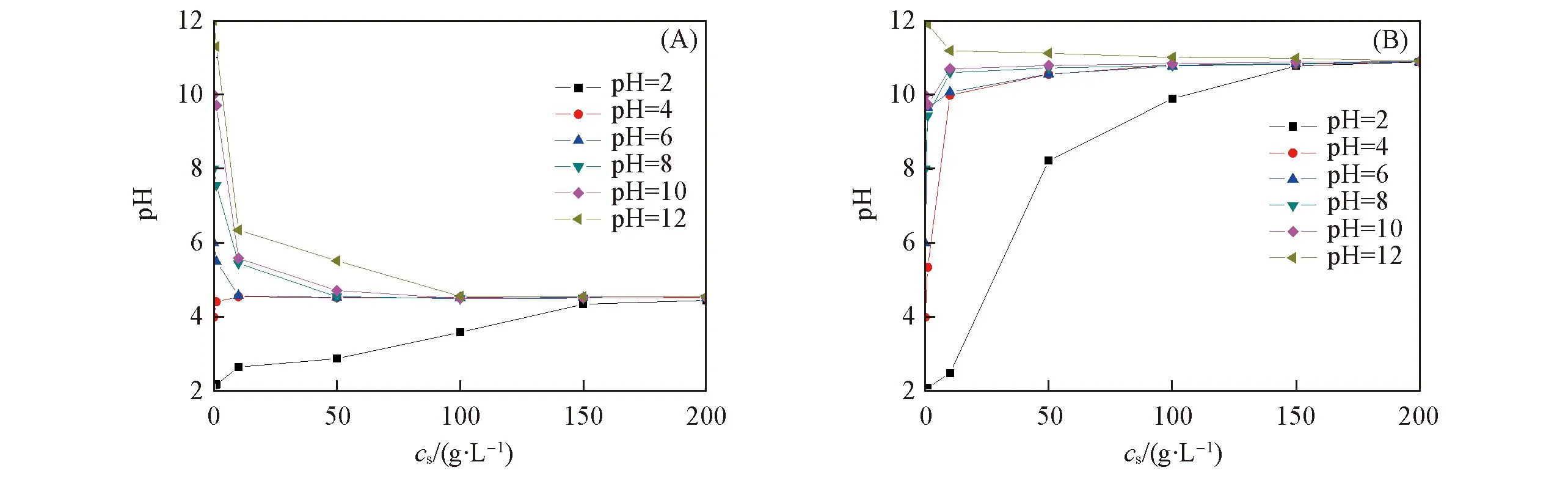
Fig.4 Mass titration curves of Z(A) and PZ(B)

ZeoliteSBET/(m2·g-1)Totalporevolumeofadsorption(BJH)/(cm3·g-1)Mostprobableporesize(BJH)/nmZ12.7940.07041.86ZC9.1810.07001.94PZ42.0530.21473.78PZC30.1350.18271.92

Fig.5 IR spectra of CTMAB(a), ZC(b), PZC(c) and Z(d)
沸石的IR測試結果見圖5. 對比有機改性前后樣品的紅外吸收峰位置可以看出, 有機改性沸石具有與天然沸石相似的骨架, 但在2920及2850 cm-1處出現了CTMAB的—CH2和—CH3對稱和反對稱伸縮振動強吸收峰, 而天然沸石在相同位置無明顯峰出現, 說明沸石經改性處理后表面已經負載了CTMAB.
ZC和PZC沸石表面的C, H, N元素主要來源于CTMAB, 因此測定沸石表面C, H, N元素的含量能夠得出沸石表面CTMAB的含量. 表2列出了ZC和PZC兩種沸石表面C, H, N的含量及對應CTMAB的含量. PZC表面CTMAB的含量為24.73 mg/g, 是ZC的2倍. 這主要是由于PZ的硅鋁比低于Z, 離子交換容量更大[37,38], CTMAB中的R4-N+離子更易與PZ發生離子交換作用.

Table 2 Results of C, H, N measurement and CTMAB loading
2.2pH值、溫度和時間對吸附量的影響
圖6示出了pH值對吸附效果的影響. 由圖6可以看出, 改性沸石的吸附效果隨pH值的增高逐漸降低, 低pH值有利于沸石對LAS的吸附. pH=2時, 吸附效果最好, 故選擇在pH=2下, 測定不同溫度改性沸石吸附LAS的影響. 不同溫度下, 改性沸石對LAS吸附影響見圖7. 由圖7可以看出, 隨著溫度的升高, 吸附量逐漸減小, 這可能是隨著溫度升高, 分子運動加劇, 使得LAS難以被吸附; 在pH=2, 溫度為20 ℃下, 測定不同時間改性沸石對LAS的吸附情況, 結果見圖8. 可以看出在吸附4 h吸附量后趨于平衡.
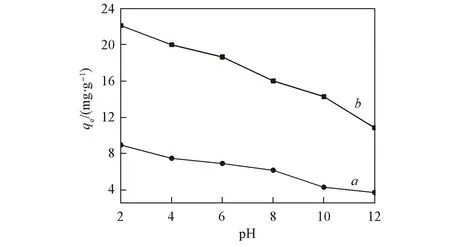
Fig.6 Effect of pH on LAS adsorption onto ZC(a) and PZC(b)
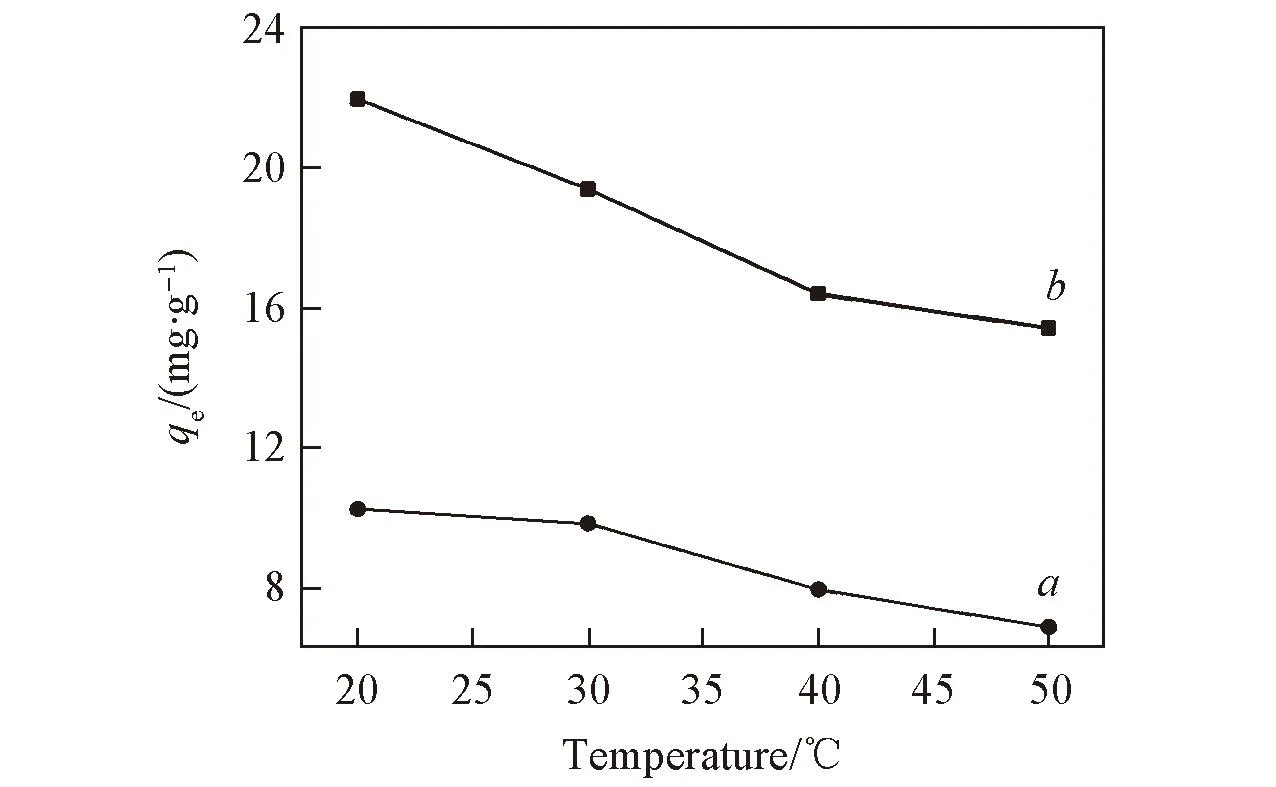
Fig.7 Effect of temperature on LAS adsorption onto ZC(a) and PZC(b)
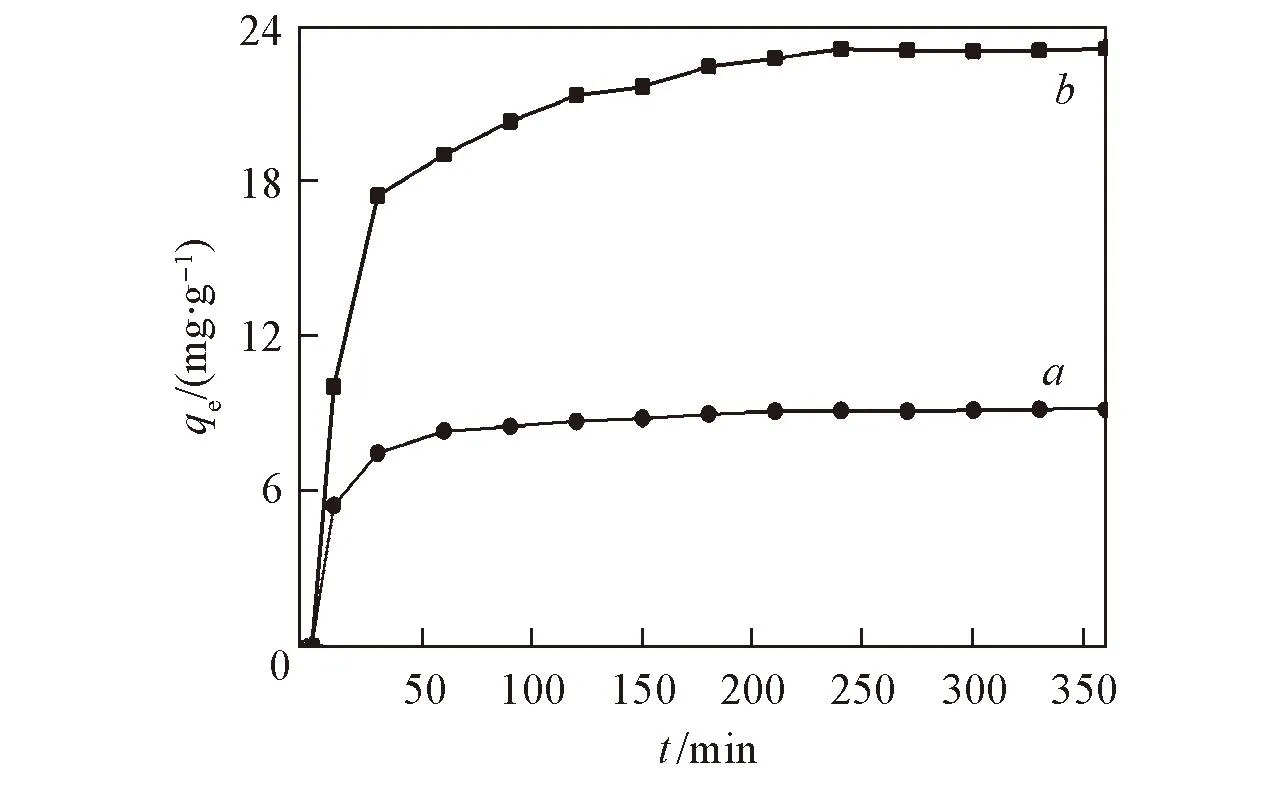
Fig.8 Effect of time on LAS adsorption onto ZC(a) and PZC(b)
2.3吸附動力學參數的確定
將CTMAB修飾改性后沸石吸附LAS的數據分別代入式(2)和式(3)進行擬合, 得到Langmuir準一級和準二級曲線(圖9), 速率常數及相關系數見表3. 可以看出, 準二級動力學模型的相關系數(R2)均為0.999, 描述擬合精度的吸附誤差Δq均≤0.037, 說明有機改性沸石對LAS的吸附過程更符合Langmuir準二級動力學模型, 以化學吸附為主.
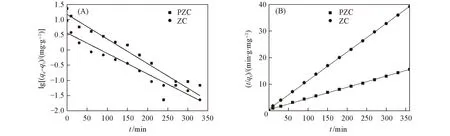
Fig.9 Kinetic model fitting of Langmuir pseudo-first order(A) and pseudo-second order(B)
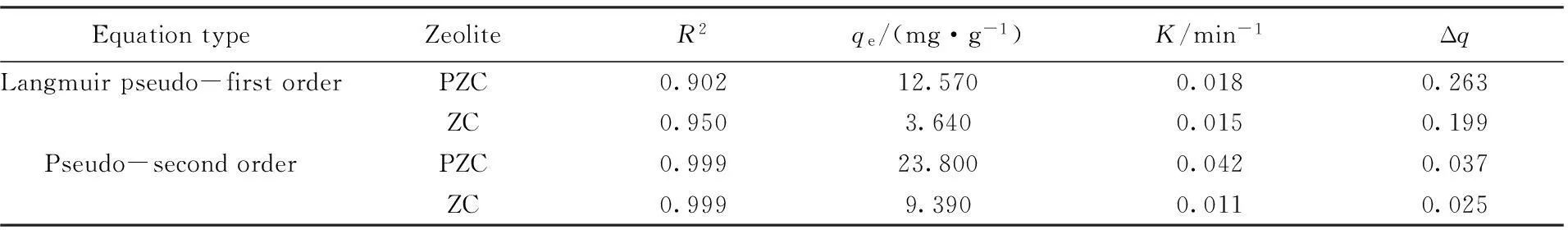
EquationtypeZeoliteR2qe/(mg·g-1)K/min-1ΔqLangmuirpseudo-firstorderPZC0.90212.5700.0180.263ZC0.9503.6400.0150.199Pseudo-secondorderPZC0.99923.8000.0420.037ZC0.9999.3900.0110.025
2.4吸附等溫線的確定
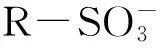
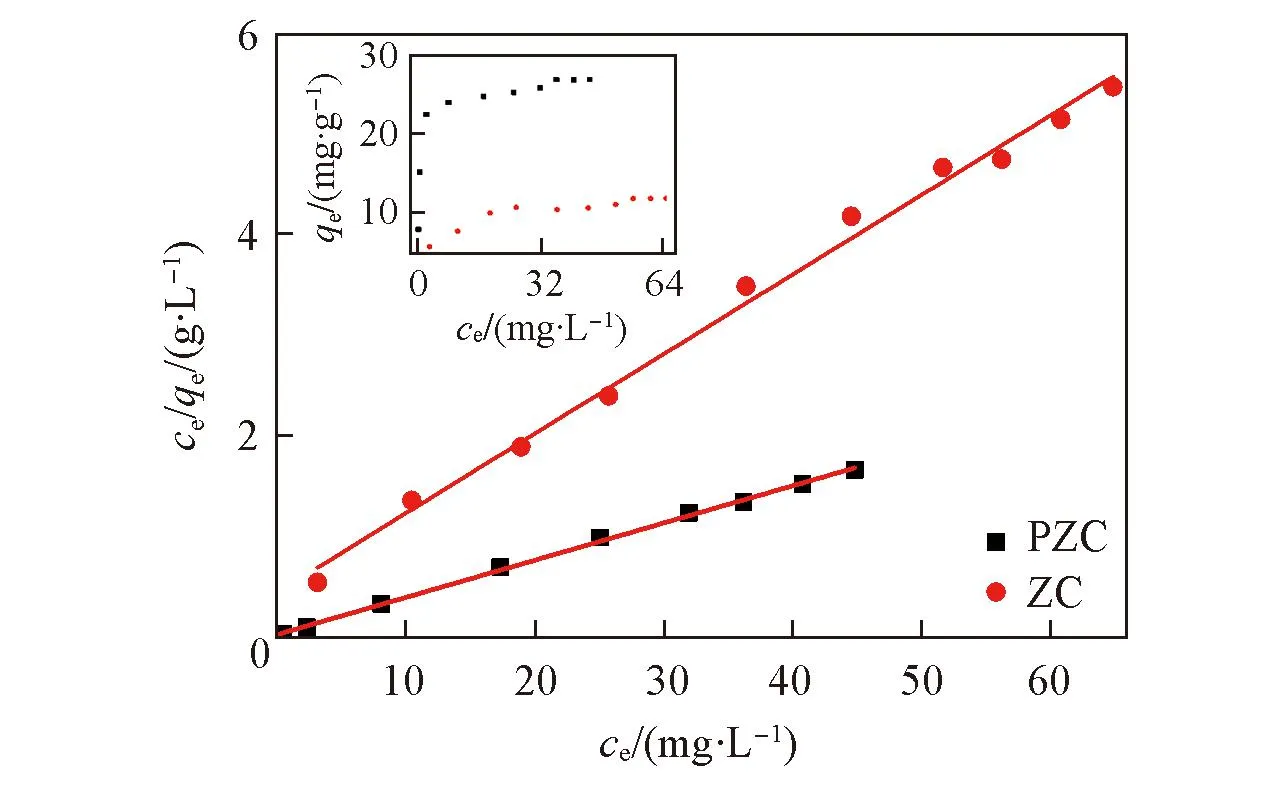
Fig.10 LAS adsorption isotherms of Langmuir equation The inset shows the varies of the adsorption capacity with the concentration at equilibrium.
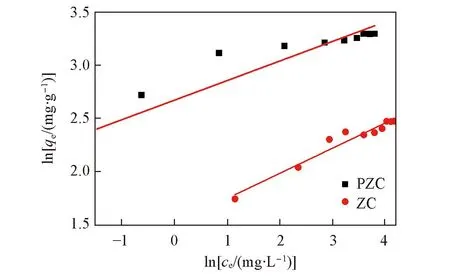
Fig.11 Adsorption isotherms of Freundlich equation

ZeoliteLangmuirequationFreundlichequationqmKLR2KFnrPZC27.1001.1570.98914.4405.4640.950ZC12.6580.1770.9944.5474.2540.818
3結論
以天然斜發沸石為基體, 通過5 mol/L NaOH堿液處理得到P型沸石, 在CTMAB修飾后對其進行了表征, 并研究其對LAS的吸附性能. 實驗結果表明, 制得的P型沸石硅鋁比為2, 比原沸石(4.85)降低58.8%; P型沸石的零凈電荷點、比表面積、孔徑和孔容均高于原沸石; 吸附平衡時間為4 h, pH=2時, 達到最佳吸附量; P型沸石和原沸石對LAS吸附均符合Langmuir準二級動力學方程和Langmuir等溫吸附方程, 飽和吸附量qm分別為27.100和12.658 mg/g, 說明吸附過程主要為單分子層的化學吸附; P型沸石具有更好的動力學性能, 其吸附速率常數大于原沸石. 該類改性沸石在處理LAS廢水中將具有重要的應用前景.
參考文獻
[1]Hodges G., Roberts D. W., Marshall S. J., Dearden J. C.,Chemosphere, 2006, 63(9), 1443—1450
[2]Hampel M., Moreno-Garrido I., González-Mazo E., Blasco J.,Ecotoxicol.Environ.Saf., 2009, 72(4), 1303—1308
[3]Rico-Rico A., Temara A., Hermens J. L.,Environ.Pollut., 2009, 157(2), 575—581
[4]Oliver-Rodríguez B., Zafra-Gómez A., Reis M. S., Duarte B. P. M.,Chemosphere, 2015, 131, 1—8
[5]Gong J. S., Wang Y., Zhang D. D., Li H., Zhang X. M., Zhang R. X.,Chem.Res.ChineseUniversities, 2015, 31(1), 91—97
[6]Shah A. A., Nawaz A., Kanwal L.,Int.Biodeterior.Biodegrad., 2015, 98, 35—42
[7]Anachkov S. E., Tcholakova S., Dimitrova D. T., Denkov N. D.,ColloidsSurf.,A:Physicochem.Eng.Asp., 2015, 466, 18—27
[8]García-Luque E., González-Maz E., Forja J. M.,Gómez-ParraA.,CoastalandShelfScience, 2009, 81(3), 353—358
[9]Terechova E. L., Zhang G. Q., Chen J., Sosnina N. A., Yang F. L.,J.Environ.Chem.Eng., 2014, 2(4), 2111—2119
[10]Delforno T. P., Moura A. G. L., Okada D. Y., Sakamoto I. K., Varesche M. B. A.,Bioresour.Technol., 2015, 192, 37—45
[11]Hernández-Soriano M. C., Mingorance M. D., Pea A.,J.Environ.Monit., 2012, 95, S223—S227
[12]García M. T., Campos E., Ribosa I., Latorre A., Sánchez-Leal J.,Chemosphere, 2005, 60(11), 1636—1643
[13]Dehghani M. H., Najafpoor A. A., Azam K.,Desalination, 2010, 250, 82—86
[14]Song Y., Wang X. J., Mai J. S.,ChinaSurfactantDetergent&Cosmeitcs, 2008, 38(1), 12—15(宋揚, 汪曉軍, 麥均生. 日用化學工業, 2008, 38(1), 12—15)
[15]Bi Y. J.,PreparationofZn/AlHydrotaicite-likedCompoundandtheResearchonCapabilityofAdsorptionRemovalofAnionicSurfactantsfromAqueousSolution, Shandong University, Jinan, 2007(畢研俊. Zn/Al類水滑石制備及其吸附去除水中陰離子表面活性劑性能研究, 濟南: 山東大學, 2007)
[16]Garcia M. T., Compos E., Dalmau M.,Chempsphere, 2002, 49(3), 279—286
[17]Wang L., Zhang C., Zhong M. J., Qian P.,Chem.J.ChineseUniversities, 2015, 36(7), 1358—1366(汪靚, 張超, 鐘明靜, 錢萍. 高等學校化學學報, 2015, 36(7), 1358—1366)
[18]Hosseinpou M., Charkhi A., Ahmadi S. J.,JournalofSupercriticalFluids, 2015, 102, 40—49
[19]Hou T. Y., Jiang Y. S., Li F. F., Sun S. M.,Chem.J.ChineseUniversities, 2006, 27(1), 100—103(侯天意, 蔣引珊, 李芳菲, 孫申美. 高等學校化學學報, 2006, 27(1), 100—103)
[20]Zhang L. L., Liu S. Y., Li Z. J., Yao J., Wang G. Y.,Chem.J.ChineseUniversities, 2014, 35(4), 812—817(張麗雷, 劉紹英, 李子健, 姚潔, 王公應. 高等學校化學學報, 2014, 35(4), 812—817)
[21]Courtney T. D., Chang C. C., Gorte R. J., Lobo Raul F., Wei F.,MicroporousMesoporousMater., 2015, 210, 69—76
[22]Liao Z. L., Chen H., Zhu B. R., Li H. Z.,Chemosphere, 2015, 134, 127—132
[23]Benaliouche F., Hidous N., Guerza M., Zouad Y., Boucheffa Y.,MicroporousMesoporousMater., 2015, 209, 184—188
[24]Camino G. A., Aida G. A., Elena S., Antonio A. R., Javier G. M., Rafael L.,J.Mol.Catal.A:Chem., 2015, 406, 40—45
[25]Nikolay K., Clement A., Gerard J. B., Venkata G. P., Sripathi, Emiel J . M.,J.Membr.Sci., 2015, 484, 140—145
[26]Thiago F. C., Heloise O. P., Peter H., Dilson C.,MicroporousMesoporousMater., 2015, 202, 198—207
[27]Arezou N., Alireza N. E.,J.Ind.Eng.Chem., 2015, 2567, 1—7
[28]Maedeh B., Alireza N. E.,ColloidsSurf.,A:PhysicochemicalandEngineeringAspects, 2015, 479, 35—45
[29]Li X. H., Zhu K.,WaterPurificationTechnology, 2008, 27(3), 5—8, 24(李效紅, 朱琨. 凈水技術, 2008, 27(3), 5—8, 24)
[30]Anaraki A. M., Ejhieh A. N.,J.ColloidInterfaceSci., 2015, 440, 272—281
[31]Xiao J. Q., Wei Z. Y.,SP&BMHRelatedEngineering, 2007, 5, 19—22(肖舉強, 魏朝燕. 硫磷設計與粉體工程, 2007, 5, 19—22)
[32]Zhang Z. H., Dou T., Zhang Z. Y.,IndustrialCatalysis, 2004, 12(10), 49—53(張志華, 竇濤, 張瑛. 工業催化, 2004, 12(10), 49—53)
[33]Silvio R. T., Rubio J.,Miner.Eng., 2010, 23, 771—779
[34]Xu J., Hou W. G., Zhou W. Z., Tai P. D.,ActaChim.Sinica, 2007, 65(13), 1191—1196(徐潔, 侯萬國, 周維芝, 臺培東. 化學學報, 2007, 65(13), 1191—1196)
[35]Li L. F., Hou W. G., Dai X. N., Liu C. X.,ActaChim.Sinica, 2004, 62(4), 429—432(李麗芳, 侯萬國, 戴肖南, 劉春霞. 化學學報, 2004, 62(4), 429—432)
[36]Kazemian H., Modanls H.,J.Radioanal.Nucl.Chem., 2003, 258, 551—560
[37]Xie J., Wang Z., Wu D. Y.,EnvironmentalScience, 2012, 33(12), 4361—4367(謝杰, 王哲, 吳德意. 環境科學, 2012, 33(12), 4361—4367)
[38]Wan D. J., Yuan H. J., Qu D.,ChineseJournalofEnvironmentalEngineering, 2011, 5(12), 2681—2685(萬東錦, 袁海靜, 曲丹. 環境工程學報, 2011, 5(12), 2681—2685)
Study on the Adsorption Ability to Linear Alkylbenzene Sulfonate of
Zeolite P Modified by Cetrimonium Bromide in Waste Water?
TAN Wenyuan1,2*, XU Man2, ZENG Ying1
(1.CollegeofMaterialsandChemistry&ChemicalEngineering,ChengduUniversityof
Technology,Chengdu610059,China;
2.AnalysisandTestingCenter,SichuanUniversityofScience&Engineering,Zigong643000,China)
AbstractZeolite P(PZ) was prepared by the natural clinoptilolite(Z) that was treated with lye, and then Z and PZ were modified by cationic surfactant cetrimonium bromide(CTMAB) to prepare ZC and PZC. The adsorption abilities of ZC and PZC to linear alkylbenzene sulfonate(LAS) were studied. The results indicated that the Si/Al ratio of PZ was 2, 58.8% lower than that of Z(4.85); the point of zero net charge(PZNC), specific surface area, pore radius and pore volume of PZ were higher than those of Z; the adsorption equilibrium was reached after 4 h. ZC and PZC had a maximum adsorption capacity for LAS at pH=2. The adsorption process was well fitted with pseudo-second order kinetic equation and Langmuir isothermal adsorption model. The amount of saturated adsorption of ZC and PZC are 12.658 and 27.100 mg/g, respectivey, showing that the adsorption process is described primarily for the monolayer and chemical adsorption, the adsorption of LAS on PZC is better than that on ZC in view of point of capacities and velocities.
KeywordsZeolite P; Cetrimonium bromide(CTMAB); Linear alkylbenzene sulfonate(LAS); Adsorption
(Ed.: F, K, M)
? Supported by the Mineral Resources Chemistry Key Laboratory Foundation of Sichuan Higher Education Institutions, China(No.KCZ201111).
doi:10.7503/cjcu20150579
基金項目:礦產資源化學四川省高校重點實驗室項目(批準號: KCZ201111)資助.
收稿日期:2015-08-20. 網絡出版日期: 2015-12-20.
中圖分類號O647.32
文獻標志碼A
聯系人簡介: 譚文淵, 男, 高級實驗師, 主要從事污水處理及儀器分析研究. E-mail: tanwenyuan@suse.edu.cn

