紅絲線藥材的HPLC指紋圖譜研究Δ
曹慶璽,鄧潔媚,姬生國,王 東(廣東藥科大學中藥學院,廣州 510006)
紅絲線藥材的HPLC指紋圖譜研究Δ
曹慶璽*,鄧潔媚,姬生國,王 東#(廣東藥科大學中藥學院,廣州 510006)
目的:建立紅絲線藥材的高效液相色譜(HPLC)指紋圖譜。方法:采用HPLC法。色譜柱為ODS-C18,流動相為甲醇-水(梯度洗脫),流速為1.0 ml/min,檢測波長為370 nm,柱溫為30Ⅱ,進樣量為20 μl。以2號色譜峰為參照峰,測定11批樣品的HPLC圖譜,采用《中藥色譜指紋圖譜相似度評價系統》(2004 A版)進行共有峰指認和相似度評價。結果:11批藥材樣品HPLC圖譜有10個共有峰,相似度均≥0.965。經驗證,11批樣品HPLC圖譜與對照圖譜具有較好的一致性。結論:該試驗所建立的HPLC指紋圖譜專屬性強、結果穩定,可作為紅絲線藥材質量評價的主要依據之一。
紅絲線;指紋圖譜;高效液相色譜法;質量評價
紅絲線Lycianthes biflora,又名山藍、紅藍、觀音草,來源于爵床科紅絲線草屬植物紅絲線Peristrophe roxburghiana(Schult.)Brem.的全草,主產于云南、四川南部、廣西、廣東、江西、福建、臺灣等地。作為一種民間草藥,其常用于止咳祛痰和治咯血、跌打損傷等癥。《常用中草藥手冊》載:“淡涼,散瘀、止血,治跌打淤腫、急性扭挫傷、內傷咳血”[1]。《全國中草藥匯編》載:“甘、淡、涼。清肺止咳,散瘀止血。治肺結核咯血、肺炎、糖尿病、跌打損傷腫痛”[2]。研究表明,紅絲線含有可食用的、無毒的天然色素[3-4],還具有多種活性成分[5],如生物堿[6]、萜類化合物[7]、有機酸[8]、黃酮類化合物[9]、揮發油[10]、脂肪族化合物及微量元素等[11];紅絲線提取物具有降壓[12]、保肝護肝[13]、鎮咳止咳[14]、抗氧化[15]等藥理作用。但目前市售紅絲線藥材質量參差不齊,甚有摻假,嚴重影響了用藥的安全性和有效性。本課題組擬通過對紅絲線藥材的高效液相色譜(HPLC)指紋圖譜進行研究,為其質量評價提供依據。
1 材料
1.1 儀器
LC-20AT型HPLC儀(包括SPD-20A二極管陣列檢測器)、BP211B型電子天平(日本Shimadzu公司);HH-4型恒溫水浴鍋(江蘇省金壇市宏華儀器廠);KQ-500DE型數控超聲波清洗器(昆山市超聲儀器有限公司,功率:500 W,頻率:40 kHz);RE-2000B型旋轉蒸發儀(上海亞榮生化儀器廠)。
1.2 試劑
甲醇為色譜純,乙醇為分析純,水為重蒸水。
1.3 藥材
11批樣品(見表1)經廣東藥學院中藥學院姬生國教授鑒定為真品。樣品經低溫干燥后粉碎過60目篩,保存于密封袋內,置于干燥器中,備用。
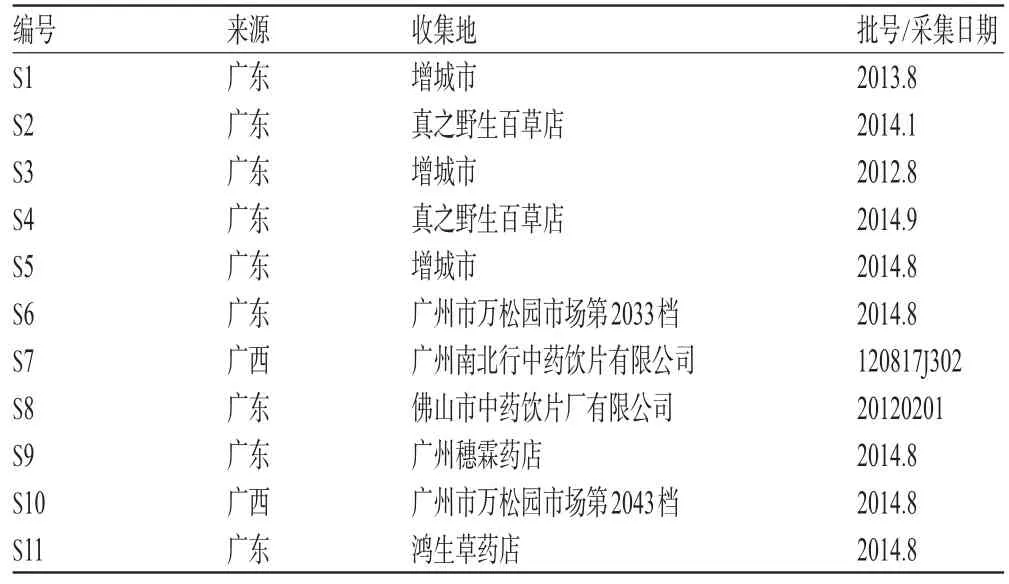
表1 紅絲線藥材來源Tab 1 Source of L.biflora
2 方法與結果
2.1 色譜條件
色譜柱:ODS-C18(250 mm×4.6 mm,5 μm);流動相:甲醇(A)-水(B),梯度洗脫(0~60 min,20%→90%A);流速:1.0 ml/min;檢測波長:370 nm;柱溫:30Ⅱ;進樣量:20 μl。
2.2 供試品溶液的制備
精密稱取樣品粉末1 g,置于錐形瓶中,加75%乙醇20 ml,超聲處理60 min,冷卻至室溫,減壓抽濾,濾液以旋轉蒸發儀蒸干,以5 ml 80%甲醇溶解,經0.45 μm微孔濾膜濾過,即得。
2.3 方法學考察
2.3.1 精密度試驗 取“2.2”項下供試品溶液適量,按“2.1”項下色譜條件連續進樣測定6次,以2號峰的保留時間和峰面積為參照,記錄各共有峰相對保留時間和相對峰面積。結果,各共有峰相對保留時間和相對峰面積的RSD均<3%(n=6),表明方法精密度良好。
2.3.2 穩定性試驗 取“2.2”項下供試品溶液(批號:120817J3 02)適量,分別于室溫下放置0、2、4、6、8 h時按“2.1”項下色譜條件進樣測定,以2號峰的保留時間和峰面積為參照,記錄各共有峰相對保留時間和相對峰面積。結果,各共有峰相對保留時間和相對峰面積的RSD均<3%(n=5),表明供試品溶液在室溫放置8 h內基本穩定。
2.3.3 重復性試驗 精密稱取同一批樣品(批號:120817J302)適量,按“2.2”項下方法制備供試品溶液,共6份,再按“2.1”項下色譜條件進樣測定,以2號峰的保留時間和峰面積為參照,記錄各共有峰相對保留時間和相對峰面積。結果,各共有峰相對保留時間和相對峰面積的RSD均<3%(n=6),表明本方法重復性良好。
2.4 指紋圖譜的建立與對照圖譜的生成
2.4.1 指紋圖譜的建立 取11批樣品適量,按“2.2”項下方法制備供試品溶液,再按“2.1”項下色譜條件進樣測定,得特征指紋圖譜,詳見圖1。
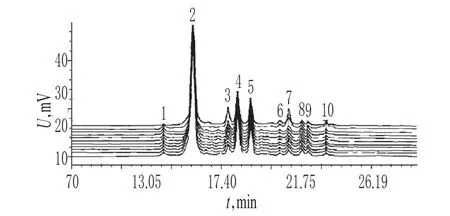
圖1 11批樣品高效液相色譜指紋圖譜Fig 1 HPLC chromatograms fingerprint of 11 batches of samples
2.4.2 對照圖譜的生成 采用國家藥典委員會發布的《中藥色譜指紋圖譜相似度評價系統》(2004 A版)對11批樣品HPLC圖譜進行圖譜擬合,生成對照圖譜,詳見圖2。結果表明,11批樣品HPLC圖譜共有特征峰10個,其中2號色譜峰的峰形好、分離度高、含量高,因此選擇作為參照峰。
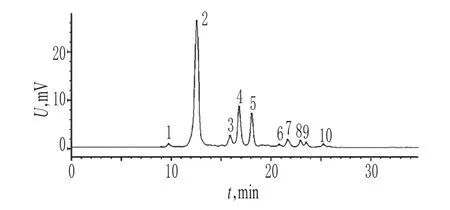
圖2 11批樣品高效液相色譜對照圖譜Fig 2 HPLC chromatograms control of 11 batches of samples
2.5 相似度分析
采用《中藥色譜指紋圖譜相似度評價系統》(2004 A版)對11批樣品HPLC圖譜進行相似度分析,結果見表2。表2顯示,11批樣品HPLC圖譜雖然共有峰面積存在一定的差異,但整體特征相似,其相似度均≥0.965,說明11批樣品HPLC圖譜與對照圖譜具有較好的一致性;不同批次藥材雖有差異但仍具有較好的相關性。
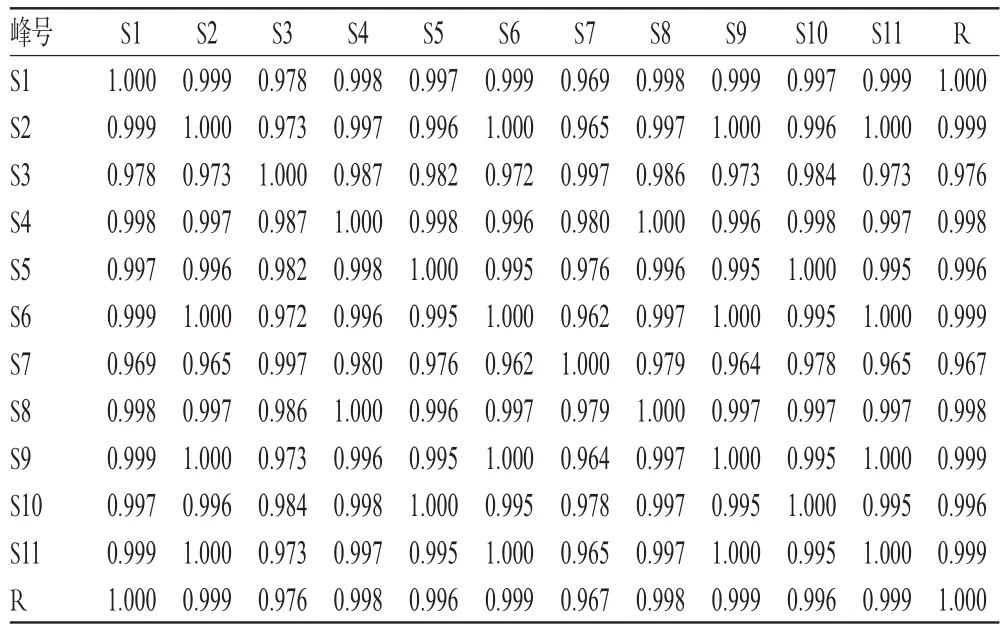
表2 11批樣品的相似度評價結果Tab 2 Similarity evaluation results of 11 batches of samples
2.6 變質樣品的檢測
取樣品適量,按“2.2”項下方法制備供試品溶液,共6份,再按“2.1”項下色譜條件進樣測定,記錄色譜并與對照圖譜進行疊加對比,詳見圖3。圖3表明,兩者圖譜差異明顯,變質的藥材樣品HPLC圖譜與對照圖譜的相似度僅為0.609,遠小于規定的0.90。
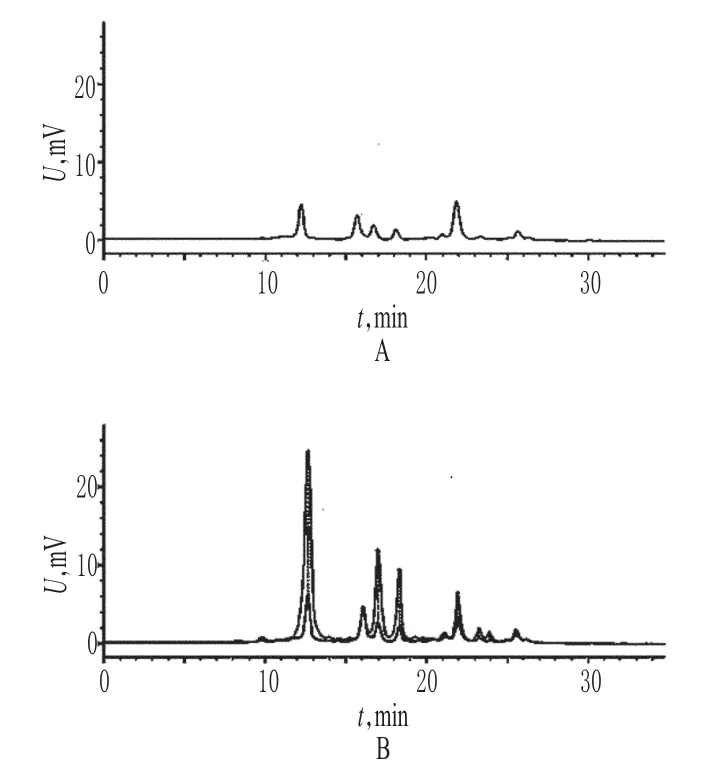
圖3 變質樣品與正品的高效液相色譜圖A.變質樣品;B.變質樣品與正品疊加圖譜Fig 3 HPLC chromatograms of degenerate sample and genuine sampleA.degenerate sample;B.superposed of degenerate sample and genuine sample
3 討論
試驗初期,筆者以蒸餾水,60%、100%甲醇和30%、50%、70%、75%、95%乙醇這8種溶劑作為提取溶劑進行比較,結果顯示,以75%乙醇作為提取溶劑,所得供試品溶液出峰數相對較多。故最終選取75%乙醇作為提取溶劑。
以甲醇-水、乙腈-水作為流動相進行比較,發現乙腈-水系統洗脫的共有峰分離度不高,幾個共有峰融合為一個峰,故選用分離度相對較好的甲醇-水為流動相進行試驗;并選取了能使基線穩定、各峰均能有所體現的370 nm作為檢測波長。
本試驗所構建的紅絲線藥材HPLC指紋圖譜有10個共有色譜峰,相似度均≥0.965,說明該指紋圖譜可以代表紅絲線藥材的鑒別特征;通過與變質樣品的HPLC圖譜比較,可以很直觀地看出變質樣品的各色譜峰與對照圖譜相似度差別很大,而這也可以作為變質藥材品質評價的指標。綜上所述,本試驗所建立的HPLC指紋圖譜專屬性強、結果穩定,可作為紅絲線藥材質量評價的主要依據之一。
[1] 廣州部隊后勤衛生部.常用中草藥手冊[M].北京:人民衛生出版社,1969:852-853.
[2] 謝宗萬.全國中草藥匯編[M].北京:人民衛生出版社,1996:266.
[3] 姚小青,劉曉明,楊朝竣,等.山藍中紅絲線素的分離純化研究與含量測定[J].中國藥學雜志,2012,47(19):1 535.
[4] 謝運昌.紅絲線色素的提取和應用研究[J].廣西輕工業,1993(3):29.
[5] 劉同方,于華忠,劉建蘭,等.紅絲線化學成分及藥理活性研究進展[J].廣東農業科學,2013(19):116.
[6] 暴惠賓.紅絲線化學成分研究[D].南寧:廣西大學,2009.
[7] 陳伯財,鐘銳,姬生國.十萼茄的生藥學研究[J].廣東藥學院學報,2009,25(3):259.
[8] 徐玉琳,張尚榮,張少歡,等.HPLC法測定紅絲線草中紅絲線素含量[J].中藥材,2008,31(8):1 180.
[9] 蔣紅芝,陸春何.分光光度法測定紅藍草中總黃酮的含量[J].廣西輕工業,2009(9):18.
[10] 郭夫江,李援朝.麻栗坡紅絲線中的酚類和酰胺類成分[J].中國中藥雜志,2011,36(18):2 507.
[11] 謝運昌,程菊英,蔣躍華,等.紅絲線色素中的微量元素[J].廣西輕工業,1994(3):24.
[12] 徐玉琳,李英,林秋曉,等.紅絲線草醇提取物的降壓作用研究[J].今日藥學,2011,21(2):77.
[13] 秦樹森,劉笑甫,張可鋒.紅絲線多糖對大鼠急性肝損傷的保護作用[J].華西藥學雜志,2010,25(5):559.
[14] 林志云,利紅宇.紅絲線的鎮咳祛痰和免疫藥效研究[J].廣東藥學,2004,14(1):37.
[15] 楊朝竣,劉曉明,晉興華,等.山藍中的色素成分鑒定及體外抗氧化活性研究[J].食品工業科技,2012,33(18):156.
Study on HPLC Fingerprint of Lycianthes biflora
CAO Qingxi,DENG Jiemei,JI Shengguo,WANG Dong(School of Traditional Chinese Medicine,Guangdong Pharmaceutical University,Guangzhou 510006,China)
OBJECTIVE:To establish the HPLC fingerprints of Lycianthes biflora.METHODS:HPLC was performed on the column of Dima ODS-C18with mobile phase of methanol-water(gradient elution)at a flow rate of 1.0 ml/min,the detection wavelength was 370 nm,column temperature was 30Ⅱ,and injection volume was 20 μl.Using chromatographic peak 2,the HPLC chromatograms of 11 batches were determined,and common peak identification and similarity evaluation were conducted by using Fingerprint Similarity Evaluation System of Traditional Chinese Medicine(version A in 2004).RESULTS:There were 10 common peaks in the HPLC chromatograms of 11 batches,the similarity was no lower than 0.965.According to the verification,the HPLC chromatograms of 11 batches and reference patterns had a good consistency.CONCLUSIONS:The established fingerprint is specific,stable,and can be used for one of the main basis of quality evaluation of L.biflora.
Lycianthes biflora;Fingerprint;HPLC;Quality evaluation
R284.1
A
1001-0408(2016)36-5130-03
2015-12-31
2016-02-28)
(編輯:張 靜)
廣東省科技計劃項目(No.2009B030801044)
*碩士研究生。研究方向:中藥質量控制。E-mail:caoqingxi_ 0223@163.com
#通信作者:副教授,碩士。研究方向:中藥質量分析。電話:020-39352181。E-mail:jsgwdxy@126.com
DOI10.6039/j.issn.1001-0408.2016.36.28

