微藻水熱液化生物油物理性質與測量方法綜述
張冀翔,王東,魏耀東(中國石油大學(北京)化學工程學院,北京 102249)
?
微藻水熱液化生物油物理性質與測量方法綜述
張冀翔,王東,魏耀東
(中國石油大學(北京)化學工程學院,北京 102249)
摘要:微藻水熱液化生物油由于性質較差,不能直接作為車載燃料使用,而作為原料油與現代石油煉制工藝相結合是一種新的應用途徑。本文綜述了微藻水熱液化生物油的物理性質,包括密度、黏度、酸性、熱值與元素組成、沸程、平均分子量等信息,介紹了常用的測量方法與手段。簡要回顧了微藻水熱液化生物油的精制研究,分析比較了不同精制方法及其效果。重點指出微藻水熱液化生物油與重質原油和常減壓渣油等劣質原料油相比,具有密度和黏度相近、酸值較高、氮氧元素含量較高、熱值較低、重質組分和大分子含量較高等特點,加氫精制能夠有效提升微藻水熱液化生物油性質,但受反應器結焦、催化劑成本和氫氣消耗等因素制約,至今未有突破性成果。
關鍵詞:生物燃料;水熱;液化;微藻;物理性質
第一作者及聯系人:張冀翔(1986—),男,博士,講師,從事生物質燃料研究。E-mail zhjx916@163.com。
生物質是唯一可以用于大規模制取液體燃料的含碳可再生能源。面對過度使用化石燃料帶來的氣候變化和環境污染等問題,由于生物質能的零碳排放特性,研究以生物質為原料生產液體運輸燃料具有重大意義。以液體燃料為目標產物的生物質轉化技術,包括生物化學轉化和熱化學轉化兩種途徑,其中熱化學轉化又有快速熱裂解、間接液化(氣化-合成)和水熱液化等不同工藝。水熱液化,是指生物質在中等溫度(200~375℃)和水熱條件下反應,生成一種油狀產物(生物油),同時得到氣體、水相成分和固體殘渣等其他副產物的過程。水熱液化工藝不需要對原料進行干燥,降低了過程能耗,特別適合處理含水量較高的生物質原料。
進入21世紀后,伴隨著第三代生物質燃料——微藻基生物燃料的研究熱潮,水熱液化工藝研究進入新的階段。相比傳統農林生物質,微藻具有單位時間內單位面積生物質產量高、不占用農業耕地等優勢,是理想的生物質原料來源。一方面,研究者將水熱液化工藝與微藻應用相結合,如處理含油微藻萃取后的藻渣[1-2],或將用于污水處理的微藻進行能源化利用,或與微藻在電廠煙氣固碳方向的應用相結合等[3];另一方面,研究者開始關注生物油油品的改性,如利用加氫金屬催化劑對水熱液化工藝進行優化[4],或對制備得到的生物油進行精制等[5]。面對新的發展機遇,研究者也不斷對水熱液化工藝進行總結。國際上,TOOR等[6]總結了水熱條件下生物大分子的轉化機理,AMIN等[7]整理了不同工藝參數對水熱液化工藝的影響,SAVAGE等[8]對催化劑作用下水生植物的水熱反應進行了總結,SKERGET等[9]對農業和食品加工業廢棄物水熱反應的基本原理和研究進展進行了概括,XIU等[10]對生物油的性質及提質改性方法進行了綜述。在國內,黃付彬等[11]對藻類直接液化制取液體燃料的研究現狀和發展趨勢進行了評述,王敏麗等[12]總結了纖維素、木質素、藻類等多種有機質的水熱液化過程,并對液化機理進行了闡述。此外,還有一些關于生物質熱化學轉化的綜述[3,13-15],也對水熱液化工藝進行了論述。
然而以上綜述中針對水熱液化生物油油品分析的篇幅較少,為填補上述空白,本文將主要對微藻水熱液化生物油(以下簡稱微藻生物油)的物理性質進行綜述,包括密度、黏度、酸性、熱值與元素組成、沸程、平均分子量等信息,比較分析其與重質原油和常減壓渣油等劣質原料油之間的差異,并簡要介紹常用的測量方法。
1 微藻生物油的物理性質
微藻水熱液化反應結束后,液相產物通常會在重力作用下分層,形成漂浮在水相產物上的油狀產物[2,16],研究者一般先將產物經溶劑(正己烷、二氯甲烷等)萃取,再把溶劑蒸發脫除得到生物油。通常,微藻生物油是一種黑色、不透明、瀝青狀物質。
1.1密度
生物油的密度在生產和儲運過程中有著重要意義。生物油密度的測量方法(GB/T 2013)有密度計法(GB/T 1884)、比重瓶法(GB/T 13377)和U形振動管法(SH/T 0604)等。標準密度計法和比重瓶法的生物油用量較大,對于實驗室小型水熱液化裝置,可采用U形振動管法。
由水熱液化產物的分層現象可以推測,微藻生物油的密度比水略小。研究結果顯示,微藻生物油密度約為0.940~0.970g/cm3,大于內燃機燃料油,與劣質原料油相當(0.930~1.000g/cm3)。ROUSSIS 等[17]對微藻Nannochloropsis進行水熱液化,反應溫度260℃,生物油密度為0.9612g/cm3(22.8℃)。ZHU等[2]對微藻N. salina在約350℃條件下進行水熱液化,得到生物油密度為0.943g/cm3(40℃)。ELLIOTT等[18]研究了4種不同來源的微藻Nannochloropsis sp.,水熱液化溫度約350℃,生物油密度為0.943~0.960g/cm3(40℃)。可見不同原料、不同水熱液化溫度條件下,微藻生物油的密度差別不大。AMIN等[7]推薦300℃作為木質纖維素類生物質水熱液化溫度,最新的文獻綜述[19]顯示,多數微藻水熱液化研究者選擇將反應溫度升高到350℃(見表1)。
1.2黏度
黏度是評定油品流動性的指標,不僅與油品的輸送性能密切相關,也是煉油工藝計算的重要參數,還直接影響燃料油的霧化性能。生物油黏度的實驗室測量方法主要是毛細管黏度計法(GB/T 265) ,也可以利用各種自動黏度儀(ASTM D1200 D2983 D7042等)。自動黏度儀可以自動完成整個測量循環,測量精度高,測量范圍寬,實驗室有條件可以采用自動黏度儀進行測量。
微藻生物油黏度約為100~400cP(40℃,1cP=1mPa?s),與孤島原油(333.7 cP,50℃[20])等重質原油接近,高于木質纖維素類生物質快速熱裂解生物油(40~100cP 50℃[14])。DAS等[21]對微藻S. platensis進行水熱液化,得到生物油黏度為189.8cP(40℃),高于同種原料熱裂解生物油79.2cP (40℃)。ELLIOTT等[18]對4種微藻Nannochloropsis sp.的水熱液化研究顯示,制得的生物油黏度為109~338cP(40℃),且原料油脂含量對生物油黏度沒有顯著影響。MINOWA等[22]對微藻Dunaliella tertiolecta分別在250℃、300℃、340 ℃ 3個不同溫度下進行水熱液化,發現所得生物油的黏度隨反應溫度的升高明顯降低。YUAN等[23]利用甲醇、乙醇和二烷等溶劑對微藻Spirulina進行水熱液化,發現液化溶劑對生物油黏度和密度有很大影響。由于水在處理微藻等含水量較高的生物質原料時具有獨特優勢,因此本文不再討論其他溶劑條件的情況。
1.3酸性
微藻生物油呈一定酸性,給其儲存、運輸和加工等環節帶來腐蝕問題。與原油類似,生物油酸性常用總酸值(total acid number,TAN mgKOH/g) 來表示,主要的測量方法有滴定法(GB/T 264)、電位滴定法(GB/T 7304)、顏色指示劑法(GB/T 4945)、半微量顏色指示劑法(SH/T 0163)等。其中滴定法、顏色指示劑法和半微量顏色指示劑法是根據顏色的變化判斷終點,方法簡單,不需要其他特殊設備,但對深色油品的終點難以判斷,而電位滴定法是根據電極電位的變化判斷終點,不受溶液顏色的限制,更適合微藻生物油總酸值的測量。
總酸值較高的環烷基原油,如單家寺原油,其總酸值為7.4 mgKOH/g[20],微藻生物油總酸值則遠高于此,達到50 mgKOH/g以上。DUAN等[5,24]對微藻Nannochloropsis sp.和C. pyrenoidosa進行水熱液化,得到生物油總酸值分別為256mgKOH/g和 133.2mgKOH/g;ELLIOTT等[18]對4種微藻Nannochloropsis sp.的水熱液化研究顯示,生物油總酸值為59~74mgKOH/g。微藻生物油的酸性,主要來自水熱液化反應中生成的酸性含氧化合物,因此在不同原料和不同工藝條件下會有一定差別。
1.4元素組成與熱值
熱值是燃料質量的一項重要指標,生物油熱值越高,其能量密度越大,相對運輸成本就越低。生物油熱值可以通過氧彈量熱儀直接測量,但更多研究者選擇利用元素組成由計算公式得出。針對氮、硫元素和灰分含量的不同,常用的計算公式有Dulong公式HHV(MJ/kg) = 0.3382C + 1.4428 (H?O/8)、Boie公式HHV(MJ/kg) = 0.3516C + 1.16225H - 0.1109O + 0.0628N + 0.10465S、Channiwala和Parikh公式HHV(MJ/kg) = 0.3491C + 1.1783H + 0.1005S - 0.1034O - 0.0151N -0.0211Ash等,FASSINOU等[25]對計算公式進行了總結。元素組成,不僅是微藻生物油熱值計算的依據,也是分析其復雜混合物體系化學組成和結構的入手點。研究者一般利用元素分析儀,分析生物油中碳、氫、氮、硫和氧元素含量。
由于不同種類微藻元素及化學組成存在差異,其水熱液化生物油元素組成也有所不同。表1對微藻生物油的元素組成及熱值進行了總結,其大致范圍是碳70%~80%、氫8%~10%、氮4%~8%、硫<1%、氧8%~15%、熱值32~38 MJ/kg。與重質原油或常減壓渣油相比,微藻生物油的特點是:H/C比較低,氮、氧含量較高,硫含量較低。這意味著微藻生物油中含有較多的芳香基和不飽和鍵,且存在大量非烴化合物,如含氮、含氧化合物等,熱值相對較低,但更加清潔。由表1可知,生物油中氮、氧含量遠低于原料,說明水熱液化過程中有脫氮、脫氧反應發生。TOOR等[26]研究顯示,隨著反應溫度升高到350℃,生物油中氮、硫、氧含量顯著降低,生物油熱值升高。
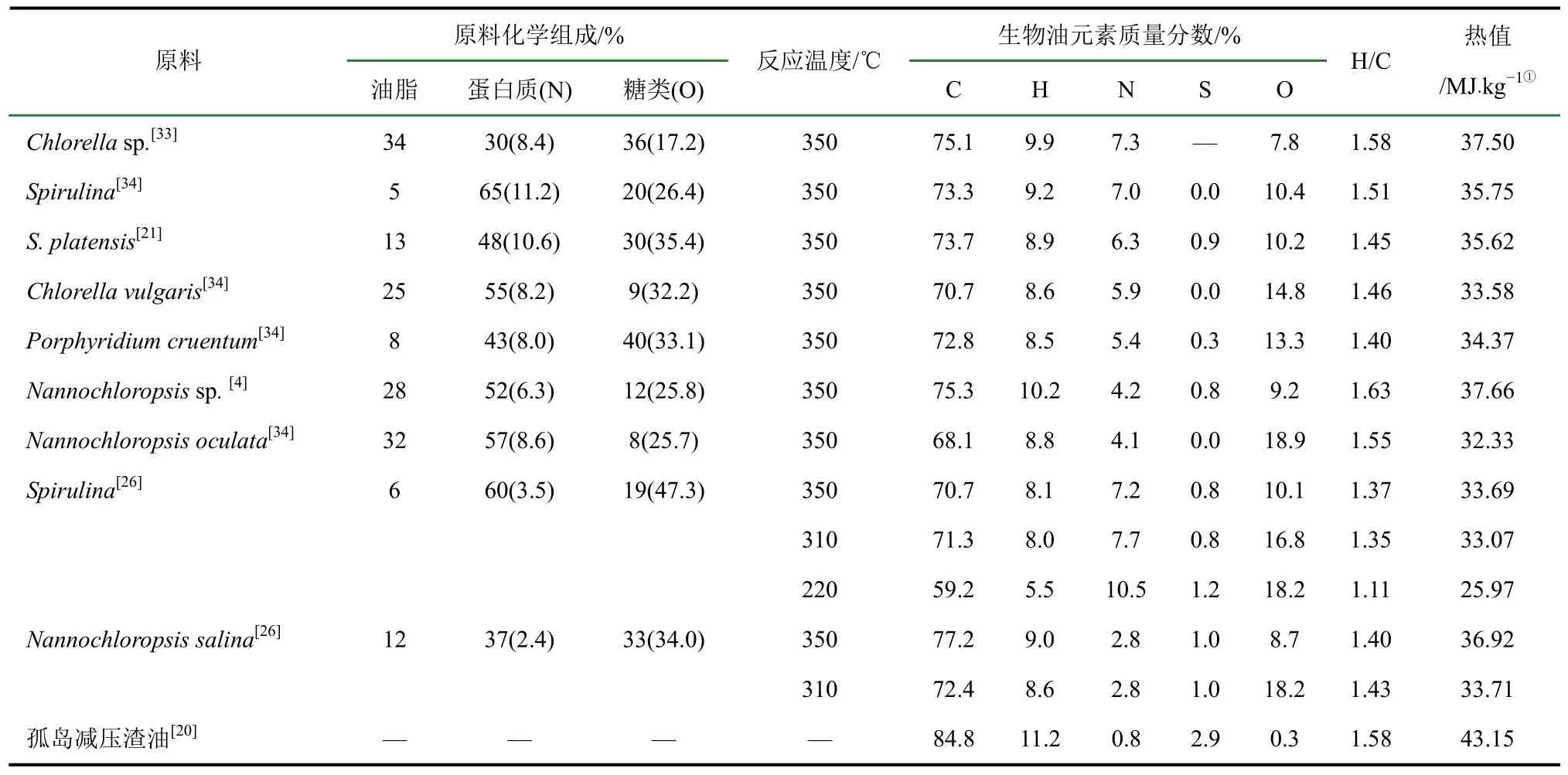
表1 微藻生物油的元素組成與熱值
1.5沸程分布
由元素組成分析可知,微藻生物油與重質原油相比,烷烴特別是直鏈烷烴含量低,芳香基、不飽和鍵以及雜原子化合物含量高,因此其沸程分布也有所不同。生物油沸程分析主要是利用高溫氣相色譜(汽化溫度>400℃)法進行模擬蒸餾(ASTM D2887,D7169)。ROSS等[27]提出利用熱重法分析生物油沸程,但熱重法受加熱速率影響,當缺少高溫氣相色譜實驗條件時,該方法可作為補充。
微藻生物油與重質原油相比,低沸點組分含量較低,高沸點組分含量較高。VARDON等[28]分析了微藻Spirulina、Scenedesmus生物油的沸程分布,并與Illinois頁巖油進行了對比,微藻生物油沸程400℃以上約占46%~55%,其中約20%屬于減壓渣油(>538℃),而與輕質油品相關的低沸點(100~200℃) 組分含量不足5%,明顯低于Illinois頁巖油。ROSIS等[17]報道了相似的研究結果,微藻Nannochloropsis生物油沸程主要分布在332~549℃,約占64%,沸程254℃以下少于5%。EBOIBI 等[29]對微藻Spirulina sp.、Tetraselmis sp.生物油的實驗數據也驗證了微藻生物油沸程分布的一般特點。
1.6平均分子量
微藻生物油是一種復雜混合物體系,分子量范圍很廣,平均分子量可以通過尺寸排阻色譜法(size exclusion chromatography,SEC)測量,它是根據試樣分子的尺寸和分子量不同來實現分離的。測量時生物油通常溶解在有機流動相中,因此該方法也被稱為凝膠滲透色譜法(gel permeation chromatography,GPC)。
生物油中含有大量重質分子,VARDON等[30]報道微藻Spirulina生物油的重均相對分子質量Mw和數均相對分子質量Mn分別為1870和890,其相對分子質量范圍一直延續到10000以上。VARDON 等[28]還對微藻Spirulina、Scenedesmus生物油和Illinois頁巖油進行了分析對比,兩種生物油的平均相對分子質量Mw/Mn分別為1860/700和3260/1330,遠高于頁巖油的670/270。ALBA等[31]報道了類似的結果,反應溫度250℃,微藻Desmodesmus sp.生物油中含有大量重質分子(2000~10000),并有3個明顯的分布峰(400~500,900~1000,1000~1100);當反應溫度升高到375℃時,重質分子含量降低,輕質分子含量增加。BARREIRO等[32]測量了8種不同微藻生物油的相對分子質量分布,在上述相同范圍內出現分布峰,隨著反應溫度的升高,峰逐漸寬化并向輕質分子一端移動。
2 微藻生物油的精制
除反應條件苛刻、設備投資成本較高外,生物油的劣質性進一步限制了其作為化石燃料替代品的應用范圍。微藻生物油存在黏度大、酸值高、氮氧元素含量高、熱值低等缺點,其性質與汽柴油相距甚遠,不能直接作為內燃機燃料使用,因此研究者嘗試了多種方法對微藻生物油進行加工精制。
2.1催化加氫液化
催化加氫液化是指在水熱液化過程中,加入催化劑或氫氣氣氛,以提升生物油性質。催化加氫液化催化劑主要有均相酸堿催化劑和異相金屬催化劑。
2.1.1均相酸堿催化劑
均相本酸堿催化劑主要是通過強酸或強堿性化合物,增加反應環境中H+或OH?濃度,促進生物質大分子分解和生物油生成[35]。其中研究較多的是Na2CO3,文獻普遍認為Na2CO3可以增加液化反應轉化率和生物油產率,并輕微提高生物油熱值[22,36-38]。對于其他性質如黏度,則是溫度的影響仍然起主導作用,催化劑在不同溫度下對生物油黏度的影響并不一致。MINOWA等[22]以Na2CO3為催化劑,考察了微藻Dunaliella tertiolecta在不同溫度下的液化行為,結果表明反應溫度為300℃時,加入5%的Na2CO3可以明顯降低生物油的黏度(14000cP降至5000cP),但在250℃和340℃條件下,加入催化劑使得生物油黏度有不同程度增加。JENA等[35]在相同的催化劑用量下進行了微藻Spirulina platensis的水熱液化研究,結果顯示反應溫度為350℃時,加入Na2CO3使得生物油黏度增大(52.10cP升至74.60cP)。此外,ROSS等[27]對比了堿性催化劑(Na2CO3、KOH)和有機酸性催化劑(CH3COOH、HCOOH)對水熱液化的影響,研究發現使用有機酸性催化劑生物油具有較低的沸點和較好的流動性。
2.1.2異相金屬催化劑
異相金屬催化劑主要是負載型貴金屬或過渡金屬催化劑,通過在反應過程中引入氫氣氣氛,促進加氫反應進行。由于加氫脫氧、加氫脫氮等各類加氫反應存在,生物油元素組成和熱值均能得到改善。DUAN等[4]進行了微藻Nannochloropsis sp.的催化加氫液化研究,結果顯示,在水熱液化過程中加入Pt/C等催化劑后,生物油H/C和O/C分別由1.68 和0.092改善至1.74和0.082,黏度也明顯降低。BILLER等[39]考察了Co-Mo/Al2O3、Ni/Al2O3和Pt/Al2O3對微藻Chlorella vulgaris和Nannochloropsis occulta水熱液化的影響,3種催化劑都具有一定脫氧能力,其中Co-Mo/Al2O3和Pt/Al2O3可以脫除碳水化合物和蛋白質中的氧,而Ni/Al2O3可以脫除脂類中的氧,與不加催化劑相比,生物油中氧含量普遍降低了2%~10%。XU等[40]考察了Ce/HZSM-5對微藻Chlorella pyrenoidosa水熱液化的影響,結果顯示Ce/HZSM-5具有明顯的脫氮效果,微藻生物油氮含量由7.44%降至0.24%。
2.2催化加氫精制
與催化加氫液化不同,催化加氫精制是在水熱液化反應結束后,針對制得的生物油進行精制,常用催化劑包括石油化工加氫催化劑和貴金屬催化劑。DUAN等[5,33]研究發現微藻生物油催化加氫精制效果明顯,在Pt/C和高壓氫氣條件下,生物油O/C和N/C分別由0.063和0.054降至0.041和0.023,酸值由256 mgKOH/g降至25.3 mgKOH/g,熱值提高到43.0 MJ/kg,此外Ru/C和Raney-Ni也有較好的提質效果。ELLIOTT等[18]利用連續流兩段式加氫裝置對微藻生物油進行了催化加氫精制研究,實驗裝置如圖1所示[41]。生物油和氫氣從頂部進入固定床催化反應器,以滴流的形式向下穿過床層,離開反應器后,產物被冷卻并被雙缸采樣系統收集。區域一低溫加氫段使用Ru/C催化劑,區域二高溫加氫段使用硫化Co-Mo催化劑,通過兩段式加氫處理,生物油密度降低到汽柴油水平(0.77~0.80g/mL),黏度降低至3.6cP(40℃)以下,酸值降低至0.2mgKOH/g以下,氮氧元素含量分別降低至0.25%和1.8%以下。
2.3熱加工精制
由于催化加氫精制存在催化劑成本高和氫氣消耗大等問題,ROUSSIS等[17]提出一種無需催化劑和高壓氫氣的生物油熱處理方法,降低了精制成本。微藻生物油在不同溫度(350℃、400℃、450℃)和氮氣氣氛下熱處理60min后,密度由0.9612g/mL降至0.8780g/mL(22.8℃),氧元素含量由5.7%降至0.2%,熱值提高到45 MJ/kg,金屬元素含量也有所降低。通過模擬蒸餾發現,生物油中高沸點組分減少,低沸點組分增加,改善了生物油的沸程分布。另外,熱處理還減少了生物油中的酸性組分,降低了總酸值。熱加工精制產率與催化加氫精制相當,約為80%~86%,而反應壓力大大降低,僅為4.2 MPa,是一種極具應用潛力的微藻生物油精制工藝。
微藻生物油的精制工藝主要有催化加氫液化、催化加氫精制和熱加工精制,催化劑包括均相酸堿催化劑和異相金屬催化劑。通常認為,催化加氫精制效果最佳,催化加氫液化和熱加工精制則次之。催化加氫液化反應結束后,異相催化劑與固體殘渣混合難以分離,且催化劑容易失活,不利于連續生產;均相催化劑成本較低,對微藻生物油的品質提升也有限。催化加氫精制多采用固定床反應器,方便催化劑再生,由于受反應器結焦、催化劑成本和氫氣消耗等因素的限制,微藻生物油精煉制備車載動力燃料的研究至今未報道取得突破性進展。
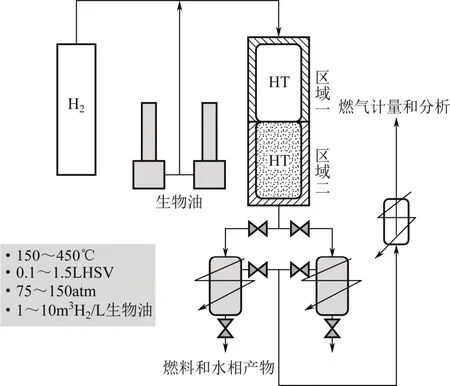
圖1 微藻生物油連續流兩段式加氫裝置[41](1atm=1.013×105Pa)
3 結 語
微藻生物油近些年獲得了很大關注,一些課題組已經展開其連續流生產工藝的研究,以便于未來的工業化放大。但要實現微藻生物油的商業推廣,不僅需要成熟的技術工藝,還需要合適的應用途徑來解決生產成本和經濟性等問題。通過總結與分析可以得出,微藻生物油硫含量較低,其密度、黏度與重質原油和常減壓渣油等劣質原料油性質相近,作為現代石油煉制工業原料油替代品有很大發展潛力。然而微藻生物油氮、氧元素含量較高,不僅降低了熱值,還導致了較高的酸性和腐蝕性;沸程分布和平均相對分子質量也顯示,其重質分子含量較高。催化加氫等工藝可以改善微藻生物油的物理性質,為了開發和優化生產、精制工藝,還需要對微藻生物油的化學組成和性質進行進一步研究。
參考文獻
[1] CHENG J,HUANG R,YU T,et al. Biodiesel production from lipids in wet microalgae with microwave irradiation and bio-crude production from algal residue through hydrothermal liquefaction[J]. Bioresource Technology,2014,151:415-418.
[2] ZHU Y H. ALBRECHT K O,ELLIOTT D C,et al. Development of hydrothermal liquefaction and upgrading technologies for lipid-extracted algae conversion to liquid fuels[J]. Algal Research,2013,2(4):455-464.
[3] RENNAN L,OWENDE P. Biofuels from microalgae:a review of technologies for production,processing,and extractions of biofuels and co-products[J]. Renewable & Sustainable Energy Reviews,2010,14(2):557-577.
[4] DUAN P G,SAVAGE P E. Hydrothermal liquefaction of a microalga with heterogeneous catalysts[J]. Industrial & Engineering Chemistry Research,2011,50(1):52-61.
[5] DUAN P G,SAVAGE P E. Upgrading of crude algal bio-oil in supercritical water[J]. Bioresource Technology,2011,102(2):1899-1906.
[6] TOOR S S,ROSENDAHL L,RUDOLF A. Hydrothermal liquefaction of biomass:a review of subcritical water technologies[J]. Energy,2011,36(5):2328-2342.
[7] AKHTAR J,AMIN N A S. A review on process conditions for optimum bio-oil yield in hydrothermal liquefaction of biomass[J]. Renewable & Sustainable Energy Reviews,2011,15(3):1615-1624.
[8] YEH T M,DICKINSON J G,FRANCK A,et al. Hydrothermal catalytic production of fuels and chemicals from aquatic biomass[J]. Journal of Chemical Technology and Biotechnology,2013,88(1):13-24.
[9] PAVLOVIC I,KNEZ Z,SKERGET M. Hydrothermal reactions of agricultural and food processing wastes in sub- and supercritical water:a review of fundamentals,mechanisms,and state of research[J]. Journal of Agricultural and Food Chemistry,2013,61(34):8003-8025.
[10] XIU S N,SHAHBAZI A. Bio-oil production and upgrading research:a review[J]. Renewable & Sustainable Energy Reviews,2012,16(7):4406-4414.
[11] 黃付彬,馮麗娟,楊文超,等. 藻類直接液化制取液體燃料研究進展[J]. 化工進展,2012(10):2197-2201,2212.
[12] 王敏麗,陳會會,關清卿,等. 有機質亞/超臨界水液化研究進展[J]. 化工進展,2014,33(2):337-345.
[13] PETERSON A A,VOGEL F,LACHANCE R P,et al. Thermochemical biofuel production in hydrothermal media:a review of sub- and supercritical water technologies[J]. Energy & Environmental Science,2008,1(1):32-65.
[14] HUBER G W,IBORRA S,CORMA A. Synthesis of transportation fuels from biomass:chemistry,catalysts,and engineering[J]. Chemical Reviews,2006,106(9):4044-4098.
[15] TRAN N H,BARTLETT J R,KANNANGARA G S K,et al. Catalytic upgrading of biorefinery oil from micro-algae[J]. Fuel,2010,89(2):265-274.
[16] YU G,ZHANG Y H,SCHIDEMAN L,et al. Distributions of carbon and nitrogen in the products from hydrothermal liquefaction of low-lipid microalgae[J]. Energy & Environmental Science,2011,4 (11):4587-4595.
[17] ROUSSIS S G,CRANFORD R,SYTKOVETSKIY N. Thermal treatment of crude algae oils prepared under hydrothermal extraction conditions[J]. Energy & Fuels,2012,26(8):5294-5299.
[18] ELLIOTT D C,HART T R,SCHMIDT A J,et al. Process development for hydrothermal liquefaction of algae feedstocks in a continuous-flow reactor[J]. Algal Research-Biomass Biofuels and Bioproducts,2013,2(4):445-454.
[19] CHOW M C,JACKSON W R,CHAFFEE A L,et al. Thermal treatment of algae for production of biofuel[J]. Energy & Fuels,2013,27(4):1926-1950.
[20] 徐春明,楊朝合. 石油煉制工程[M]. 北京:石油工業出版社,2009:5-45.
[21] JENA U,DAS K C. Comparative evaluation of thermochemical liquefaction and pyrolysis for bio-oil production from microalgae[J]. Energy & Fuels,2011,25(11):5472-5482.
[22] MINOWA T,YOKOYAMA S Y,Kishimoto M,et al. Oil production from algal cells of Dunaliella tertiolecta by direct thermochemical liquefaction[J]. Fuel,1995,74(12):1735-1738.
[23] YUAN X Z,WANG J Y,ZENG G M,et al. Comparative studies of thermochemical liquefaction characteristics of microalgae using different organic solvents[J]. Energy,2011,36(11):6406-6412.
[24] BAI X J,DUAN P G,XU Y P,et al. Hydrothermal catalytic processing of pretreated algal oil:a catalyst screening study[J]. Fuel,2014,120:141-149.
[25] FASSINOU W F,VAN DE STEENE L,TOURE S,et al. What correlation is appropriate to evaluate biodiesels and vegetable oils higher heating value (HHV)?[J]. Fuel,2011,90(11):3398-3403.
[26] TOOR S S,REDDY H,DENG S G,et al. Hydrothermal liquefaction of Spirulina and Nannochloropsis salina under subcritical and supercritical water conditions[J]. Bioresource Technology,2013,131:413-419.
[27] ROSS A B,BILLER P,KUBACKI M L,et al. Hydrothermal processing of microalgae using alkali and organic acids[J]. Fuel,2010,89(9):2234-2243.
[28] VARDON D R,SHARMA B K,BLAZINA G V,et al. Thermochemical conversion of raw and defatted algal biomass via hydrothermal liquefaction and slow pyrolysis[J]. Bioresource Technology,2012,109:178-187.
[29] EBOIBI B E O,LEWIS D M,ASHMAN P J,et al. Hydrothermal liquefaction of microalgae for biocrude production:improving the biocrude properties with vacuum distillation[J]. Bioresource Technology,2014,174:212-221.
[30] VARDON D R,SHARMA B K,SCOTT J,et al. Chemical properties of biocrude oil from the hydrothermal liquefaction of Spirulina algae,swine manure,and digested anaerobic sludge[J]. Bioresource Technology,2011,102(17):8295-8303.
[31] ALBA L G,TORRI C,SAMORI C,et al. Hydrothermal treatment (HTT) of microalgae:evaluation of the process as conversion method in an algae biorefinery concept[J]. Energy & Fuels,2012,26(1):642-657.
[32] BARREIRO D L,ZAMALLOA C,BOON N,et al. Influence of strain-specific parameters on hydrothermal liquefaction of microalgae[J]. Bioresource Technology,2013,146:463-471.
[33] DUAN P G,BAI X J,XU Y P,et al. Catalytic upgrading of crude algal oil using platinum/gamma alumina in supercritical water[J]. Fuel,2013,109:225-233.
[34] BILLER P,ROSS A B. Potential yields and properties of oil from the hydrothermal liquefaction of microalgae with different biochemical content[J]. Bioresource Technology,2011,102(1):215-225.
[35] JENA U,DAS K C,KASTNER J R. Comparison of the effects of Na2CO3,Ca3(PO4)2,and NiO catalysts on the thermochemical liquefaction of microalga Spirulina platensis[J]. Applied Energy,2012,98:368-375.
[36] ZOU S P,WU Y L,YANG M D,et al. Production and characterization of bio-oil from hydrothermal liquefaction of microalgae Dunaliella tertiolecta cake[J]. Energy,2010,35(12):5406-5411.
[37] YANG Y F,FENG C P,INAMORI Y,et al. Analysis of energy conversion characteristics in liquefaction of algae[J]. Resources Conservation and Recycling,2004,43(1):21-33.
[38] ZHOU D,ZHANG L A,ZHANG S C,et al. Hydrothermal liquefaction of macroalgae enteromorpha prolifera to bio-oil[J]. Energy & Fuels,2010,24:4054-4061.
[39] BILLER P,RILEY R,ROSS A B. Catalytic hydrothermal processing of microalgae:decomposition and upgrading of lipids[J]. Bioresource Technology,2011,102(7):4841-4848.
[40] XU Y F,ZHENG X J,YU H Q,et al. Hydrothermal liquefaction of Chlorella pyrenoidosa for bio-oil production over Ce/HZSM-5[J]. Bioresource Technology,2014,156:1-5.
[41] ELLIOTT D C,HART T R,NEUENSCHWANDER G G,et al. Catalytic hydroprocessing of fast pyrolysis bio-oil from pine sawdust[J]. Energy & Fuels,2012,26(6):3891-3896.
·技術信息·
Physical properties and their measuring methods of hydrothermal liquefaction bio-crude from microalgae:a review
ZHANG Jixiang,WANG Dong,WEI Yaodong
(School of Chemical Engineering,China University of Petroleum (Beijing),Beijing 102249,China)
Abstract:Hydrothermal liquefaction (HTL) bio-crude from microalgae cannot be directly used as transportation fuels,but can find new applications when integrated with modern petroleum processing techniques. The physical properties of HTL bio-crude from microalgae,including density,viscosity,acidity,elemental composition,heating value,boiling range distribution and average molecular weight,were summarized and compared to heavy crude oil and residue oil. The measuring methods were also briefly introduced. Upgrading of HTL bio-crude from microalgae was reviewed based on comparing various upgrading methods and performances. It is important to point out that compared with heavy crude oil and residue oil,HTL bio-crude from microalgae has similar density and viscosity,higher acidity,lower heating value,higher content of oxygen and nitrogen and high boiling point components and larger average molecular weight. Hydrotreating of HTL bio-crude from microalgae can significantly improve its quality. However,it was constrained by coking of the reactor,high catalysts cost and hydrogen consumption.
Key words:biofuel; hydrothermal; liquefaction; microalgae; physical property
基金項目:國家自然科學基金(21406265)及中國石油大學(北京)科研基金(2462013YJRC022)項目。
收稿日期:2015-05-04;修改稿日期:2015-05-29。
DOI:10.16085/j.issn.1000-6613.2016.01.013
中圖分類號:TK 6
文獻標志碼:A
文章編號:1000–6613(2016)01–0098–07

