芬嗎通在氯米酚促排卵周期子宮內膜薄患者中的應用
王海燕,孫林,王磊,李北氫,邵小光
(大連市婦女兒童醫療中心生殖醫學中心,大連 116000)
多囊卵巢綜合征(PCOS)是一種常見的婦科內分泌紊亂性疾病。促排卵成為其治療的首選方法。枸櫞酸氯米酚(CC)作為多囊卵巢促排卵的一線藥物,在臨床中廣泛應用。價格低廉,促排卵率高,但其抗雌激素作用使得子宮內膜變薄、宮頸粘液粘稠,從而影響妊娠成功率。本文旨在研究補佳樂及芬嗎通對子宮內膜的影響,選擇更有利于妊娠的雌激素應用于臨床。
資料與方法
一、研究對象
選擇2013年1月至2014年2月在本醫療中心就診的PCOS患者共56例,均行CC 促排卵治療。納入標準:診斷標準采用2003年鹿特丹會議修正的PCOS診斷標準(3項符合兩項):(1)排卵稀發或無排卵;(2)高雄激素血癥的臨床和(或)生化特征;(3)多囊卵巢,以及排除其他原因(先天性腎上腺皮質增生,分泌雄激素的腫瘤和庫欣綜合征)。符合PCOS診斷,基礎內分泌調整至正常,輸卵管造影顯示至少一側輸卵管通暢,常規監測自然周期卵泡及內膜情況,提示無排卵且子宮內膜無異常回聲,男方精液正常,無其他內科合并癥。促排卵前均口服達英-35(先靈,德國)。應用CC促排時,監測卵泡大小達≥14mm 時觀察內膜厚度,選擇內膜厚度≤5 mm 的病例。排除標準:子宮卵巢腫瘤、乳腺結節、宮腔粘連、子宮內膜息肉、內膜異常增生、宮頸病變等病變。
二、研究方法
1.促排卵方法:對于符合入選標準的患者于月經第3天口服CC(法地蘭,塞浦路斯)50mg,每日1次,共5d。陰式B 超儀(深圳邁瑞)監測卵泡大小達≥14mm 時觀察內膜厚度,若內膜厚度<5mm,加用雌二醇。按加用的雌二醇藥物不同隨機分為2組:補佳樂組(n=28)和芬嗎通組(n=28)。前者給予戊酸雌二醇(補佳樂,先靈制藥,德國)2mg/d,后者給予17-β雌二醇(芬嗎通粉色片,蘇威制藥,荷蘭)2 mg/d,兩組同時應用人絕經促性腺激素(HMG,珠海麗珠)肌肉注射,待卵泡發育至直徑≥18mm 時給予人絨毛膜促性腺激素(HCG,寧波人健)10 000U 肌肉注射,指導同房,排卵后補佳樂組繼續應用補佳樂并加用地屈孕酮(達芙通,蘇威制藥,荷蘭)行黃體支持,芬嗎通組應用黃色片(17-β雌二醇2mg+地屈孕酮10mg)共14d,之后化驗是否妊娠。陰道超聲均由主治醫生本人操作,超聲固定為同一臺,排除人為因素引起的誤差。
2.觀察指標:觀察兩組基礎E2水平、卵泡直徑≥14mm時子宮內膜厚度、HCG 日子宮內膜厚度及子宮內膜A 型形態率、HCG 日E2水平、卵泡平均直徑。根據HCG日子宮內膜厚度<6mm,6~8mm,>8mm分組,分別統計HCG 日兩組患者所占的例數。患者均在早7~8時抽血,采用DX1800全自動化學免疫發光儀(BECKMAN COULTER,美國)進行激素測定。按Gonen等[1]評價子宮內膜超聲形態的標準分為A、B、C型。A 型:呈三線型,外層和中央為強回聲線,外層與宮腔中線之間為低回聲區或暗區;B型:為均一的中等強度回聲,宮腔強回聲中線斷續不清;C型:為均質強回聲,無宮腔中線回聲。A,B和C三型分別多見于月經周期中的增生晚期、黃體早期和黃體晚期。統計A 型內膜所占的比例。
三、統計學分析
采用SPSS 13.0軟件進行統計學分析。計數資料采用χ2檢驗,計量資料采用方差分析。P<0.05為差異有統計學意義。
結 果
一、一般情況
補佳樂組患者平均年齡(32.3±2.5)歲,不孕年限平均(4.4±3.0)年。芬嗎通組患者平均年齡(31.3±3.3)歲,不孕年限平均(4.1±2.9)年。兩組比較差異無統計學意義(P>0.05)。兩組患者符合PCOS診斷標準,促排卵前均經過達英-35預處理。
二、兩組患者各項指標比較
補佳樂組和芬嗎通組相比,兩組基礎E2無明顯差異,HCG 日芬嗎通組E2水平明顯高于補佳樂組,差異有統計學意義(P<0.05)。卵泡直徑≥14mm應用雌激素之前,兩組內膜厚度相比較,差異無統計學意義(P>0.05)。應用雌激素后,芬嗎通組的內膜厚度[(7.49±1.16)mm]略高于補佳樂組[(6.52±1.05)mm],但差異無統計學意義(P>0.05)。兩組的最大卵泡直徑及妊娠率相比較,差異無統計學意義(P>0.05)。內膜形態A 型內膜發生率兩組比較,差異無統計學意義(P>0.05)(表1)。
三、HCG 日兩組患者不同子宮內膜厚度比率的比較
芬嗎通組內膜>8 mm 的例數多于補佳樂組,差異有統計學意義(P<0.05)。補佳樂組內膜多集中在6~8mm(表2)。
表1 兩組患者各項指標比較[(±s),n(%)]

表1 兩組患者各項指標比較[(±s),n(%)]
注:與補佳樂組相比,*P<0.05
?
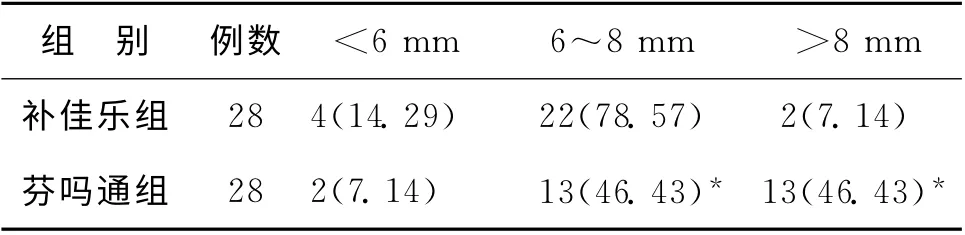
表2 兩組HCG 日不同子宮內膜厚度比率的比較[n(%)]
討 論
CC作為廣泛應用的口服藥,方法簡單,價格便宜,CC的化學結構式與雌激素相似,足以使下丘腦的雌激素受體與之結合而下丘腦受體被占據不能識別內生的雌激素,下丘腦因而發信號給垂體使其刺激卵巢卵泡。CC 同時也有抗雌激素的作用,與子宮頸管的雌激素受體結合,使之變為粘稠,精子不易穿入,也會降低子宮內膜甾體激素受體,影響子宮內膜發育,不利胚胎的著床。子宮內膜發育不良,是臨床上從內膜形態和厚度等方面觀察到的異常,同時也因子宮內膜不能充分的增殖與分泌,致使結構、生化物質分泌等方面異常而不能形成有利的胚胎著床的微環境,從而導致子宮內膜的容受性降低[2]。臨床上常添加雌激素改善這種不利影響,常用的雌激素有補佳樂,為天然雌二醇的戊酸鹽,與人體內自身的雌激素結構相同,原料是谷固醇和膽固醇,主要來源于大豆。Chonchicha等[3]的研究表明在CC 促排卵周期的月經第10~14天,每天添加6mg的戊酸雌二醇能夠抑制內膜變薄,且不干擾卵泡發生和排卵。國內多數研究應用的起始時間在月經周期的5~8d,劑量1~2mg不等[4-6]。
芬嗎通(雌二醇片/雌二醇地屈孕酮片)是17β雌二醇和地屈孕酮的復合制劑,活性組份雌二醇為微粒化雌二醇,具有與體內內源性雌激素相同的化學結構和生物學特性,因此歸為人體雌激素,來源于野生的山藥和大豆。相對于17β-雌二醇,戊酸雌二醇需要經過肝臟的去戊酸,因此17β-雌二醇的肝臟負擔小[7]。芬嗎通其紅色片每粒含17β 雌二醇2mg,黃色片每粒含17β雌二醇2 mg和地屈孕酮10mg。眾多研究表明芬嗎通應用于更年期性激素補充療法方案不增加乳腺癌的風險[8],可改善機體糖代謝、脂代謝、并能降低心血管病和糖尿病風險[9],可有效降低骨質流失,增加骨密度[10]。研究表明芬嗎通應用于輔助生殖技術時,對改善子宮內膜發育不良患者有良好的效果[11]。
很多研究表明增生晚期超聲示三線型圖象并內膜厚度7~14mm,胚胎植入成功率較高[12]。本文界定內膜小于5mm,優勢卵泡已經形成時,盡快補充雌激素,以期待內膜生長并利于受孕。本文嘗試把芬嗎通應用于CC 促排卵周期內膜薄的患者,和同期應用補佳樂比較,分析兩種雌激素藥物的差異。在CC促排卵早期應用芬嗎通可以使卵泡發育緩慢或停滯,分析可能與芬嗎通可使血中雌激素升高較多,而負反饋抑制下丘腦分泌卵泡刺激素有關。晚卵泡期應用時由于優勢卵泡已經形成,雌激素對其影響較小,對卵泡生長速度影響不大。因此本文選擇病例均為晚卵泡期的患者即卵泡直徑≥14 mm,比較了晚卵泡期應用補佳樂2 mg/d 或芬嗎通2mg/d,同時均加用HMG 促排,兩組內膜生長狀況,結果表明芬嗎通組的內膜厚度較補佳樂組高,可能與血中雌激素的增加高有關。自然周期時,子宮內膜在增殖晚期厚度可達8~14 mm,對于子宮內膜發育不良導致的薄型子宮內膜目前尚無統一的判定標準。有學者認為,超排卵周期血清HCG 日內膜厚度<8 mm 時患者的種植率和妊娠率明顯降低[13],當子宮內膜厚度<7 mm 時,妊娠率幾乎為0%[14]。因此改善內膜厚度和形態,或許可提高妊娠率。本文中芬嗎通組的子宮內膜>8mm 的患者的比率增加,但妊娠率沒有差異,需要增加樣本量進一步分析。兩組均無嚴重不良反應。
本文研究表明晚卵泡期內膜薄選擇應用芬嗎通,可以顯著增厚內膜,達到理想結果。但由于本文研究周期數較少,難以更科學評價兩者之間的差別。兩組的用藥劑量更應該細化,以期待得到更科學的結論。今后,尚需更好地探索芬嗎通的個體化應用,達到應用最小的劑量可有理想的結果。
[1] Gonen Y,Casper RF.Prediction of implantation by the sonographic apprearance of the endometrium during controlled ovarian stimulation for in vitro fertilization(IVF)[J].J In Vitro Fert Embryo Transf,1990,7:146-152.
[2] 朱鵬云,林研,劉蕓.激素替代方案應用于子宮內膜生長不良患者凍胚移植內膜準備[J].中華臨床醫師雜志(電子版),2012,6:3289-3292.
[3] Satirapod C,Wingprawat S,Jultanmas R,et al.Effect of estrodiol valerate on endometrium thickness duing clomiphene citrate-stimulated ovulation[J].J Obstet Gynaecol Res,2014,40:96-101.
[4] 楊海虹,高寶輝,金慧佩.小劑量雌激素對誘導排卵增殖期子宮內膜的影響[J].中國婦幼保健,2005,20:1447-1449.
[5] 韓玉芬,敬文娜,張巧平,等.幾種藥物對誘導排卵周期中子宮內膜發育的影響[J].中國計劃生育學雜志,2006,14:424-426.
[6] 李春洋,黃朝霞,程靜,等.不同雌激素對克羅米芬促排卵周期子宮內膜、子宮動脈血流及臨床妊娠率的影響[J].中國婦幼保健,2007,22,5195-5196.
[7] Mashchak CA,Lobo RA,Dozono-Takano R,et al.Comparison of pharmacodynamic properties of various estrogen formulations[J].Am J Obstet Gynecol,1982,144:511-518.
[8] Scheen AJ,Gaspard U.Medication of the month.Femoston Low(0.5 mg estradiol plus 2.5 mg dydrogesterone)for menopausal hormonal replacement therapy[J].Rev Med Liege,2011,66:209-214.
[9] Kirichenko AA,Novichkova IuN.Effect of the treatment with femoston on the cardiovascular system in postmenopausal women[J].Ter Arkh,2001,73:38-40.
[10] Ettinger B,Genant HK,Steiger P,et al.Low-dosage micronized 17beta-estradiol prevents bone loss in postmenopausal women[J].Am J Obstet Gynecol,1992,166:479-488.
[11] 孫林,王磊,柯雪,等.芬嗎通在凍融周期子宮內膜發育不良患者中的應用[J].生殖醫學雜志,2014,23:42-47.
[12] Okohue JE,Onuh SO,Ebeigbe P,et al.The effect of endometrial thickness on in vitro fertilization(IVF)-embryo transfer/intracytoplasmic sperm injection(ICSI)outcome[J].Afr J Reprod Health,2009,13:113-121.
[13] Richter KS,Bugge KR,Bromer JG,et al.Relationship between endometrial thickness and embryo implantation,based on 1,294cycles of in vitro fertilization with transfer of two blastocyst-stage embryos[J].Fertil Steril,2007,87:53-59.
[14] McWilliams GD,Frattarelli JL.Changes in measured endometrial thickness predict in vitro fertilization success[J].Fertil Steril,2007,88:74-81.

