從溶解氧(DO)變化判別污泥活性受銅離子抑制的影響因素
趙文玉,王慶,陸燕勤*,王哲,李東慧
1.桂林理工大學環境科學與工程學院,廣西桂林541004
2.桂林理工大學廣西礦冶與環境科學研究中心,廣西桂林541004
從溶解氧(DO)變化判別污泥活性受銅離子抑制的影響因素
趙文玉1,2,王慶1,陸燕勤1,2*,王哲1,李東慧1
1.桂林理工大學環境科學與工程學院,廣西桂林541004
2.桂林理工大學廣西礦冶與環境科學研究中心,廣西桂林541004
以溶解氧(DO)變化值為評價指標,研究Cu2+對活性污泥微生物毒性的影響因素(MLSS、HRT、pH、溫度及COD負荷),以期為重金屬廢水處理及污水廠進水沖擊預防提供參考和依據。結果表明:提高MLSS能夠顯著提高微生物對Cu2+沖擊的抵抗作用。當系統遭受8 mg/L Cu2+沖擊時,MLSS從500 mg/L增大至3000 mg/L時,DO突變從0.65 mg/L減小至0.13 mg/L,抑制性減少了80%;增加HRT,Cu2+對系統的沖擊作用增大。當HRT從0.5 min增加到3 min時,反應器DO從0.42 mg/L增至0.76 mg/L,沖擊作用增加80.9%;弱酸性條件與Cu2+毒性呈協同效應,弱堿性條件Cu2+可能產生Cu(OH)2沉淀而使其毒性降低。一定范圍升高溫度Cu2+毒性效應增強,當溫度為36.6℃時Cu2+的毒性作用最大;一定范圍內增加COD,有利于系統對Cu2+毒性的抵抗作用,當COD大于537 mg/L時,溶解氧變化程度逐漸降低,抵抗作用逐漸增強。
DO變化值;重金屬Cu;生物抑制性;影響因素
城市污水中,重金屬污染日趨嚴重,以Cu較為常見,其主要來源于采礦、印刷、電鍍等行業的廢水,給城市污水廠生化處理帶來很大困難[1,2]。重金屬主要通過抑制微生物的呼吸作用,與酶的活性或非活性中心結合而使其失去活性,阻礙活性污泥微生物正常的生理代謝功能,致使污水處理系統微生物種群結構發生改變[3],從而影響污水處理效果和水廠的正常運營與管理。
雖然重金屬對微生物的毒性作用機理沒有完全界定,但相關文獻指出重金屬對微生物的毒性作用主要取決于其濃度和種類[4],而Cu等重金屬在各種條件影響下的毒性效應研究同樣重要[6]。反應動力學方面,Pai等[5]通過研究Cu和Cd對異氧生物增長速率和自身氧化速率常數的影響,建立了一種有效的新型抑制率模擬模型,Pamukoglu等[6-8]研究了HRT和SRT等調控參數對Cu離子毒性效應的影響,發現較長HRT時,動力學修正常數對系統性能具有良好的預測能力,增加SRT對COD的去除有利。
在國內關于Cu離子在各種條件影響下對微生物的毒性效應的系統性研究較少,本文以微生物耗氧速率(OUR)為原理,DO變化為指標的測試方法,通過模擬實驗研究分析MLSS,HRT、COD負荷,pH,溫度對Cu離子毒性效應的影響。確定各種影響因素對微生物重金屬中毒的影響程度,以期為污水處理廠的穩定高效運營提供理論支持。
1 材料和方法
1.1 活性污泥重金屬中毒預警裝置
活性污泥重金屬中毒預警裝置如圖1所示,活性污泥取自宜興市某污水處理廠生化池,污水取自該污水處理廠進水,配制一定濃度含有Cu離子的重金屬模擬污水。活性污泥重金屬中毒預警裝置包括反應器、進水、進泥設備等,反應器由有機玻璃制成,有效容積700 mL,底部設有微量曝氣、攪拌器,使反應器中,泥、水、氣三相均勻混合,設溶氧儀對反應器混合液DO進行連續監測。
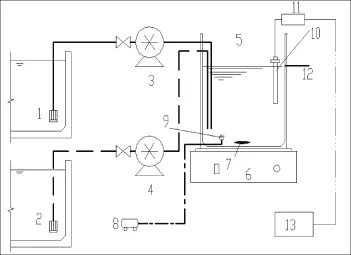
圖1 活性污泥重金屬中毒預警裝置示意圖Fig.1 Schematic diagram of activated sludge poisoning by heavy metals equipment
1.2 試驗方法
首先取自宜興市某污水處理廠污水、污泥,通過蠕動泵按一定比例定量進入反應器,調節微量曝氣閥使混合液DO在2.5±0.3 mg/L范圍內,維持以上條件形成相對穩定的溶解氧值(DO1),通過調節蠕動泵的流量,控制反應器內的污泥濃度(MLSS)和水力停留時間(HRT)然后在污水中定量投加Cu。連續監測DO變化,待DO上升到最高值(DO2)記錄此值。
重金屬Cu由分析純試劑CuSO4·5H2O配置而成,DO連續監測,取樣間隔時間為15 s。當進水含有重金屬Cu時,混合液中微生物的呼吸作用受到抑制,反應器中處于平穩狀態的溶解氧值由基準值(DO1)上升到最高值(DO2),則DO變化值=(DO2-DO1)mg/L,抑制率=(DO2-DO1)/DO1*100%。
2 結果與討論
2.1 MLSS對反應器DO變化的影響
配制廢水Cu離子的濃度均為8 mg/L(以混合液計),調節進水量、進泥量,控制預警反應器中混合液停留時間(HRT)為1 min,實驗時反應器混合液溫度為23.2℃,使用的污泥濃度為4576 mg/L,按照梯度調節泥水比例(1:7、1:3、1:1.6、1:1、1:0.6、1:0.3),得到混合液MLSS依次為為572、1144、1760、2288、2860、3520 mg/L,廢水中加入Cu離子后,預警反應器中DO變化值和抑制率的的變化情況如圖2所示。
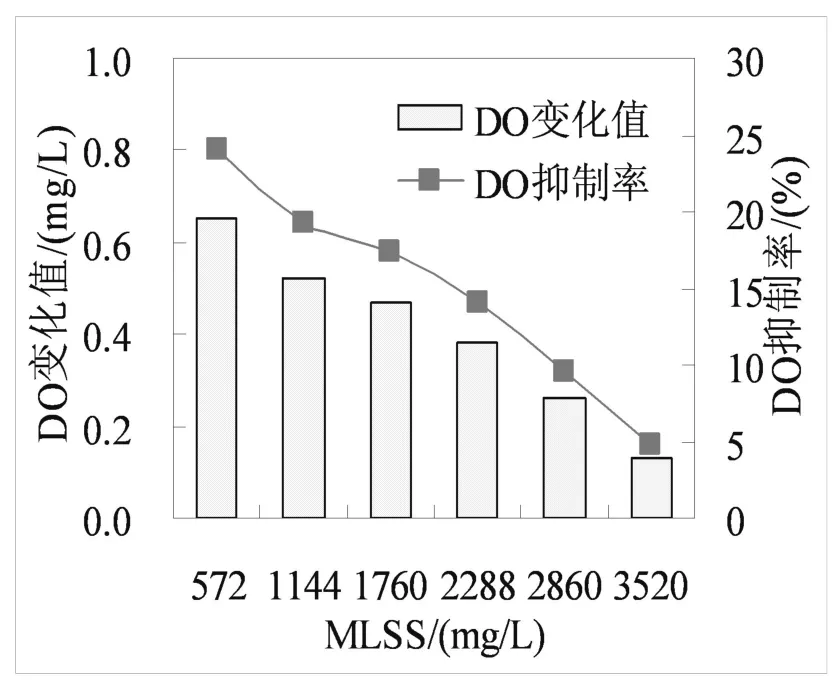
圖2 不同MLSS濃度對預警反應器DO的影響Fig.2 The effect of different MLSS on DO in warning reactor
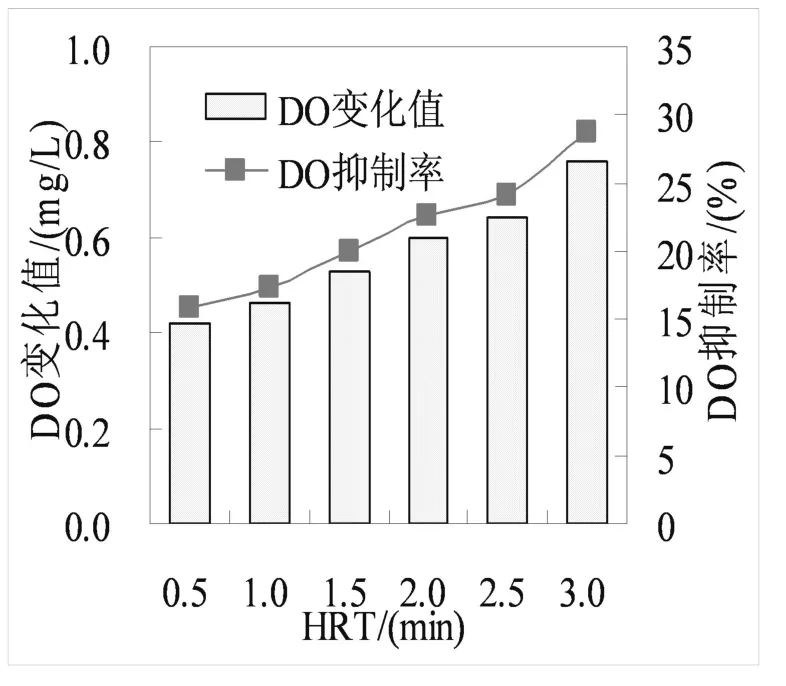
圖3 不同HRT對預警反應器DO的影響Fig.3 The effect of different HRT on DO in warning reactor
由圖2可知,隨著MLSS濃度升高,同一濃度的Cu對預警反應器造成的沖擊逐漸減弱。當MLSS為572 mg/L時,8 mg/L的Cu對活性污泥微生物產生抑制作用,系統產生DO變化為0.65 mg/L,MLSS分別為1144、1760、2288、2860 mg/L時,系統被抑制產生的DO變化分別為0.52、0.47、0.38、0.26 mg/L,當MLSS為3520 mg/L時,系統的抵抗能力達到最大,DO變化值僅為0.13 mg/L,可知當MLSS從572 mg/L增大至3520 mg/L時,DO變化值從0.65 mg/L下降至0.13 mg/L,系統對Cu沖擊的抵抗能力增強80%。所以,實驗結果說明一定程度增加MLSS能夠增強活性污泥系統對重金屬沖擊的抵抗能力,減小MLSS可以起到放大重金屬對活性污泥微生物的毒性作用。
2.2 HRT對反應器DO變化的影響
實驗使用的污泥濃度為4576 mg/L,反應器混合液溫度為23.4℃,控制預警反應器的條件,使MLSS濃度為1144 mg/L,HRT分別為0.5 min、1 min、1.5 min、2 min、2.5 min、3 min,研究不同HRT條件下,8 mg/L Cu對活性污泥的生物抑制性。不同HRT條件下,DO變化值和抑制率的變化情況如圖3。
從圖3可以看出,不同的HRT條件下,受到相同濃度Cu沖擊時,系統的受抑制情況不同。當HRT從0.5 min增至3 min時,系統的DO變化值逐漸增加,受抑制程度逐漸增強。當HRT為0.5 min時,系統受到抑制產生的DO變化值為0.42 mg/L,HRT分別為1、1.5、2、2.5 min時,系統產生的DO變化值分別為0.46、0.53、0.6、0.63 mg/L,當HRT為3 min時,抑制程度達到最大,DO變化值為0.76 mg/L,HRT從0.5 min增至3 min時,DO變化值增加了80.9%。當HRT增加時,Cu離子與微生物的接觸時間增加,使得微生物被抑制的程度增強。所以,從實驗結果可以看出,一定范圍內增加HRT會增加重金屬對系統的抑制作用,同時可以為預警反應器條件的優化提供參考。
2.3 pH對反應器DO變化產生的影響
實驗使用的污泥濃度為4760 mg/L,反應器中混合液的溫度為22.3℃,控制系統的反應條件,使反應器污泥濃度為1190 mg/L,HRT為2 min。調節進水pH(為酸性),最小值調至2.96,梯度約為1個pH單位;調節進水pH(為堿性),最大調至11.3,調節梯度約為0.5個pH單位。圖4和圖5為10 mg/L Cu分別在酸性和堿性條件下對系統進行沖擊,DO變化值和抑制率的情況。
由圖4可見,系統在此條件下運行時,Cu對系統產生的抑制作用隨著pH的減小逐漸增大。原水pH為7.95,當10 mg/LCu對系統沖擊時,DO變化值為0.86 mg/L,當按照梯度調節進水pH分別為6.9、5.95、4.85、3.93時,系統均產生不同程度的抑制作用,DO變化值分別為0.91、1.01、1.03 mg/L,當進水pH為2.96時Cu對系統產生的抑制作用最大,DO變化值達到1.11 mg/L。綜上所述,當進水pH為酸性時,能夠增加Cu離子對活性污泥微生物的毒性,表現出毒性協同作用。
系統運行條件保持一致,堿性條件下Cu對系統的沖擊情況與酸性條件時有所區別,堿性條件下系統的DO變化情況見圖5。
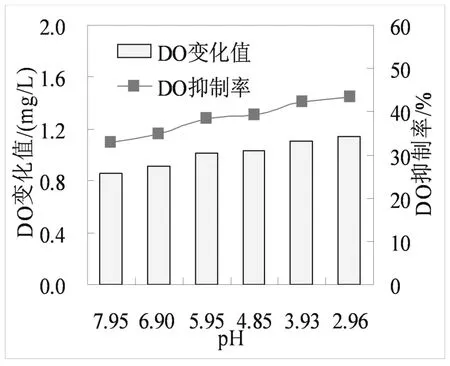
圖4 不同pH(酸性)對預警反應器DO的影響Fig.4 The effect of different pH(acid)on DO in warning reactor
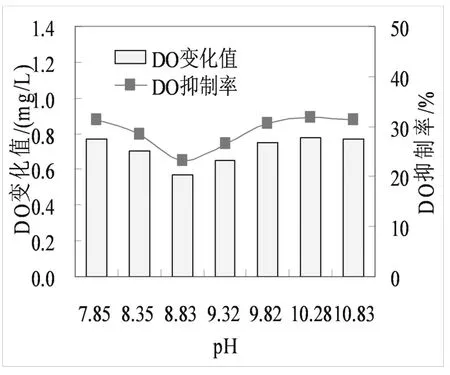
圖5 不同pH(堿性)對預警反應器DO的影響Fig.5 The effect of different pH(alkaline)on DO in warning reactor
由圖5可以看出,進水在堿性條件下時,Cu對系統產生沖擊作用,隨著pH的增加沖擊作用變化不明顯。進水pH在7.85~10.83之間時,DO變化值在0.57~0.78 mg/L之間變化。當進水pH為8.83時,DO變化值最小為0.57 mg/L,說明在弱堿性條件下,Cu對活性污泥微生物的毒性效應減弱,這是由于Cu離子與堿性條件的OH-結合形成Cu(OH)2沉淀,從而降低Cu的毒性效應。因此,可以通過利用堿性廢水與酸性含銅廢水進行一定比例的混合,來達到降低Cu毒性效應的作用,削弱其對污水廠生化池活性污泥微生物的沖擊,對污水廠的穩定運營具有實際的意義。
2.4 溫度對反應器DO變化產生的影響
實驗使用的污泥濃度為4808 mg/L,反應器混合液的溫度為23.3℃,控制系統反應條件,調節泥水比,使反應器的MLSS濃度為1202 mg/L,HRT為1 min。在此條件下運行時,通過改變進水溫度,使反應器混合的溫度升高,按照一定的梯度控制混合液的溫度分別為23.3、28.0、32.8、36.6、40.0、43.0℃,與溫度對應的DO變化情況見圖6。
從圖6可以看出,不同溫度使得Cu離子對系統產生不同程度的抑制最用。當溫度低于36.6℃時,Cu對系統的抑制作用隨著溫度的升高而增加,23.3℃時抑制作用最小,DO變化值為0.36 mg/L,當溫度升高至36.6℃時,Cu對系統的抑制作用達到最大,DO變化值為0.53 mg/L。而當溫度超過36.6℃時,DO變化值又逐漸減小。重金屬Cu的毒性隨著溫度升高而增加的現象可以解釋為活性污泥微生物隨著溫度的逐漸升高,其活性增強,對抑制性物質的敏感性提高,表現為抑制性逐漸增強。所以,當微生物處于最適宜溫度時,活性最大,對重金屬Cu的敏感性增加,而當溫度超過最適溫度時,微生物活性下降,對Cu離子毒性的敏感程度下降,DO變化值減小。
2.5 COD負荷對反應器DO變化產生的影響
實驗過程中使用的MLSS濃度為4464 mg/L,反應器混合液的溫度為22.3℃,調節泥水的流量及比例,控制系統的反應條件為HRT=2 min,MLSS為1116 mg/L。在條件不變的情況下,通過改變進水COD負荷,研究不同進水COD負荷條件下,8 mg/LCu對系統產生抑制的影響程度。隨著進水COD負荷增加,Cu對系統的抑制情況見下圖7。
由圖7可知,在此運行條件下,Cu對系統的抑制作用隨著進水COD負荷的增加呈現波動性的抑制現象。當進水COD負荷在219 mg/L到431 mg/L時,Cu對系統的毒性影響變化不明顯,DO變化值在0.7~0.72 mg/L之間;而當COD大于537 mg/L時,DO變化逐漸降低,進水COD為537 mg/L時,DO變化值為0.77 mg/L,進水COD分別為643、749、855 mg/L時,對應的DO變化值分別為0.76、0.68、0.65 mg/L,當進水COD為961 mg/L時,DO變化值最小為0.5 mg/L。所以,進水COD負荷對Cu的毒性具有一定程度的影響作用,適當的增加進水COD負荷可以一定程度的緩解重金屬Cu對活性污泥微生物的抑制作用,這與榮宏偉等研究的結論相一致[11]。
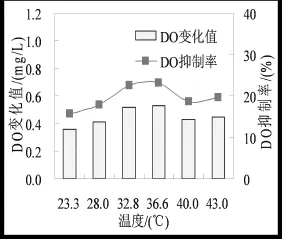
圖6 不同溫度對預警反應器DO的影響Fig.6 The effect of different temperature on DO in warning reactor
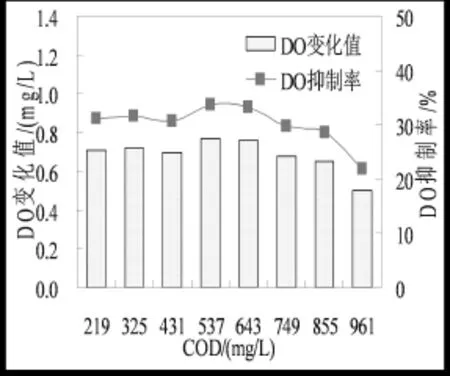
圖7 不同COD負荷對預警反應器DO的影響Fig.7 The effect of different COD on DO in warning reactor
3 結論
(1)一定條件下提高MLSS可以有效的削弱重金屬Cu對活性污泥微生物的抑制作用。當MLSS從572 mg/L增大至3520 mg/L時,Cu對活性污泥微生物的毒性減少了80%;一定程度提高進水COD負荷有利于污泥微生物對Cu離子的抵抗作用。
(2)進水為酸性條件時能夠促進Cu離子對活性污泥的毒性作用,原水pH為7.95降低至2.96時,Cu的毒性增加32.6%;而當進水為弱堿性條件時,可以一定程度的緩解Cu對污泥微生物的毒性作用,當進水pH為8.83時,Cu的毒性最小,毒性較原水條件下減小26.0%。
(3)一定范圍內Cu離子微生物的毒性效應隨溫度升高而增加,是因為適當提高溫度使微生物的活性增強,對Cu離子的敏感性提高,毒性增加;當溫度超過36.6℃時,微生物活性降低,敏感性隨之降低,毒性減小,表現為DO變化值減小。所以同等條件下,污水廠在夏季比冬季更易受重金屬類毒性物質影響;一定范圍內增加HRT會增加Cu離子對活性污泥微生物的抑制作用,當HRT從0.5 min增加到3 min時,沖擊作用增加80.9%。
[1]Hammaini A,Ballester A,Blázquez M L,et al.Effect of the presence of lead on the biosorption of copper,cadmium and zinc by activated sludge[J].Hydrometallurgy,2002,67:109-116
[2]You Sheng-jie,Tsai Yung-pin,Huang Ru-yi.Effect of heavy metals on nitrification performance in different activatedsludge processes[J].Journal of Hazardous Materials,2009,165(1/3):987-994
[3]Stasinakia A S,Mamais D,Thomaidis N S,et al.Effect of chromium(VI)on bacterial kinetics of heterotrophic biomass of activated sludge[J].Water Research,2002,36(13):3341-3349
[4]吳永貴,熊焱,林初夏,等.不同形態P對Cu、Zn、Cd聯合生物毒性效應的影響[J].環境科學學報,2006,26(12):2045-2051
[5]Pai T Y,Wang S C,Lo H.M,et al.Novel modeling concept for evaluating the effects of cadmium and copper on heterotrophic growth and lysis rates in activated sludge process[J].Journal of Hazardous Materials,2009,166(1):200-206
[6]Pamukoglu M Y,Kargi F.Mathematical modeling of copper(II)ion inhibition on COD removal in an activated sludge unit[J].Journal of Hazardous Materials,2007,146(1/2):372-377
[7]Pamukoglu M Y,Kargi F.Copper(II)ion toxicity in activated sludge processes as function of operating parameters[J]. Enzyme and Microbial Technology,2007,40(5):1228-1233
[8]Pamukoglu M Y,Kargi F.Removal of Cu(II)ions by biosorption onto powdered waste sludge(PWS)prior to biological treatment in an activated sludge unit:A statistical design approach[J].Bioresource Technology,2009,100(8):2348-2354
[9]榮宏偉,李健中,張可方.環境因素對銅離子毒性的影響[J].廣州大學學報(自然科學版),2011,10(2):74-78
The Judgement of the Influence Factors on Sludge Activity Inhibited by Copper Ion from Dissolved Oxygen Change
ZHAO Wen-yu1,2,WANG Qing1,LU Yan-qin1,2*,WANG Zhe1,LI Dong-hui1
1.College of Environmental Science and Engineering,Guilin University of Technology,Guilin 541004,China
2.Research Center of Guangxi Mining Industry and Environmental Science,Guilin University of Technology,Guilin 541004,China
In this paper,in order to provide reference for heavy metals wastewater treatment and wastewater treatment plant influent shock prevention,dissolved oxygen(DO)mutation index was used to study the effect of the toxicity of Cu2+on the microbial activity in different conditions by controlling environmental factors such as MLSS,HRT,pH,temperature and COD load.The results showed that increasing the concentration of activated sludge was obvious in improving the capacity of microorganism in resisting to the toxicity of Cu2+.When the system was impacted by 8 mg/L Cu2+,MLSS increased from 500 mg/L to 3000 mg/L,DO mutation decreased from 0.65 mg/L to 0.13 mg/L,inhibition rate decreased by 80%.When HRT of the system increased from 0.5 min to 3 min,DO mutation increased from 0.42 mg/L to 0.76 mg/L,inhibition rate increased by 80.9%.The pH was cooperative with the toxicity of copper ions at the condition of weak acid.The toxicity of Cu2+would reduce in the situation of alkalescence,because copper ions will react to precipitation as cupric hydroxide.Certain range of raising the temperature would increase the toxicity of copper ions,it would be the maximum toxicity when the temperature raised to 36.6℃.Increasing the COD in a certain range would be favorable for the system to resist the toxicity of Cu2+,DO mutation decreased steadily and the resistant enhanced gradually when the COD was more than 537 mg/L.
Dissolved oxygen mutation;Cu;biological inhibitory;influence factors
[TU992.3]
A
1000-2324(2015)01-0038-05
2013-03-11
2013-03-22
廣西高校科學技術研究重點項目(2013ZD032);“廣西危險廢物處置產業化人才小高地”資助
趙文玉(1973-),副教授,研究方向為水處理理論與技術.E-mail:zhaowenyu@glut.edu.cn
*通訊作者:Author for correspondence.E-mail:luyanqin@glut.eud.cn

