血紅蛋白在殼聚糖/納米金/APS/普魯士藍復合膜修飾電極上的直接電化學
□單彩霞 □趙飛燕
(1濮陽水文水資源勘測局 2安陽水文水資源勘測局)
0 引言
本法基于Hb-Chit/AuNPs/APS/PB多層膜修飾的玻碳電極為工作電極,研究了其制作、表征及對該修飾電極多層膜為基礎的生物傳感器的性能分析。通過電沉積的方法將PB修飾到GCE電極表面,制得PB/GCE電極;將帶正電荷、含有大量氨基的3-氨丙基三乙烯硅烷(APS)修飾到電極表面,并通過相反電荷之間的靜電相互作用將含有大量負電荷的納米金(AuNPs)固附于電極表面形成復合膜,最后,將Hb和殼聚糖溶液固載于多層膜修飾的電極上。由于PB特殊的催化特性,AuNPs和Hb分子的協同影響,這種生物傳感器具有良好的性能,即具有高的靈敏度、較強的穩定性和選擇性、響應時間短、線性范圍寬的優點,這種新型的修飾方法為研究蛋白質電化學提供了有效的功能界面,成功地用于測定H2O2。
1 實驗部分
1.1 傳感器的構制
玻碳電極依次用1.00,0.50,0.05μm的Al2O3漿在麓皮紙上拋光成鏡面以去除表面吸附有機物,每次拋光后先洗去表面污物,再用去離子水超聲清洗,重復三次,最后依次用HNO3溶液(1:1),乙醇溶液(1:1),去離子水超聲清洗(每次3-5min),將清洗好的電極晾干待用。
將含有2mmol/LFeCl3+2mmol/LK3[Fe(CN)6]+0.10mol/LKCl+0.10mol/LHCl的溶液通氬氣除氧10min,在氬氣氛圍內,將處理好的裸GCE置于此溶液中,以恒電壓+0.4 V進行電化學聚合120 s,即得到PB/GCE修飾電極。經過條件優化,將PB/GCE修飾電極置于含0.10mol/LKCl和0.10mol/LHCl的電解液中,并以50mV/s的掃描速率在-0.05V~+0.35 V范圍內掃描20圈,隨著聚合圈數增加,PB/GCE上的聚合峰電流逐漸增大,到一定程度時不再變化(見圖1),這表明電極表面形成了導電膜。由此產生的PB薄膜修飾電極用清水洗凈,并在氮氣氛圍下干燥。
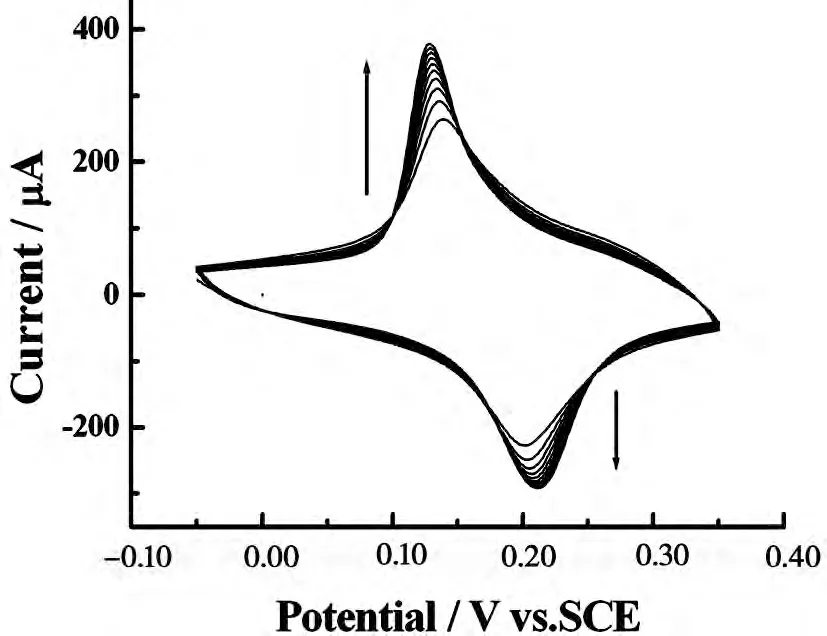
圖1 PB修飾電極的循環伏安圖
用以上方法修飾電極處理后,將修飾電極浸泡在2%的APS溶液中30min,以促使電極表面引入大量的氨基基團。然后,該修飾電極用二次水徹底沖洗并在4℃條件下在納米金溶液中浸泡10 h。為得到Hb-Chit復合膜的最佳響應,對Hb和Chit混合溶液修飾體積進行了優化。將Hb和Chit混合溶液滴涂到修飾電極表面,在電極上方罩上小燒杯,后將該修飾薄膜在空氣中干燥過夜,以便形成均勻的復合膜。
2 Hb-Chit/AuNPs/APS/PB復合膜的光譜表征
2.1 紫外可見吸收光譜表征
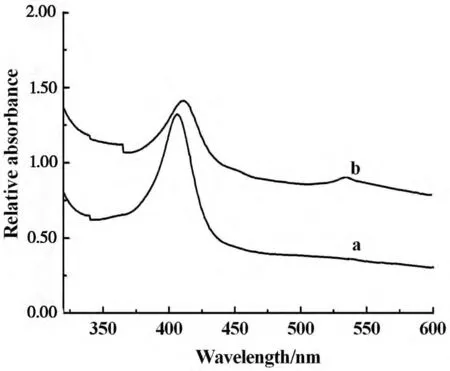
圖2 Hb(a),Hb-Chit/AuNPs/APS/PB修飾膜(b)的UV-vis光譜圖
圖2顯示了Hb(見圖2a曲線)及Hb在復合膜中(見圖2b曲線)的紫外可見光譜圖,對于包埋于Chit/AuNPs/APS/PB復合膜內的Hb,在413 nm處出現了明顯的Soret吸收帶,僅比Hb Soret吸收帶紅移了4 nm。Soret吸收帶輕微的移動及吸收率減小歸結于復合膜與蛋白質的交互作用,這種作用既不會破壞蛋白質結構,也不會破壞生物分子基本的微水環境。在Chit/AuNPs/APS/PB復合膜(見圖2b曲線)中大約在535 nm處出現了一個相對突出的吸收峰,而在Hb中(見圖2a曲線)卻未曾出現此類吸收峰,主要是納米金的特征吸收峰峰值大概在535 nm附近。
2.2 紅外光譜表征

圖3 Hb(a),Hb-Chit/AuNPs/APS/PB修飾膜(b)的紅外譜圖
Hb-Chit/AuNPs/APS/PB復合膜紅外光譜圖顯示了其組成部分的組合形狀(見圖3b曲線),可以看出復合膜中的酰胺I和酰胺II基團與天然Hb的酰胺I和酰胺II基團結構非常相似,說明在復合膜中,Hb的主要部分基本上保留了其天然結構,構象沒有發生大的變化。
3 修飾電極的直接電化學
3.1 循環伏安法測不同修飾電極的直接電化學行為
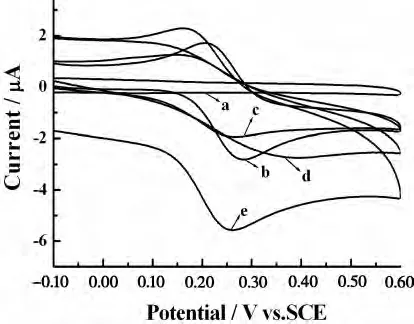
圖4 不同修飾電極的循環伏安圖
圖4顯示了在0.10mol/L pH7.00PBS中,在掃速100mV/s條件下,不同修飾電極的循環伏安行為。Hb-Chit/AuNPS/APS/PB/GCE電極得到了一對穩定而明確的氧化還原峰(見圖4e曲線),陽極峰電位(Epa)和陰極峰電位(Epc)分別位于160mV和250mV,式電勢Eo’=(Epa+Epc)/2=205mV。然而,在修飾膜中沒有Hb存在的條件下,只有PB/GCE電極得到一對可逆的氧化還原峰(見圖4b曲線),陽極峰電位和陰極峰電位分別位于210mV和276mV,式電勢為243mV,裸電極沒有任何氧化還原峰出現(見圖4a曲線),顯然,Hb-Chit/AuNPS/APS/PB/GCE電極反應的原因在于固載于電極表面的Hb的電化學氧化還原中心。另一方面,Hb-chit/PB修飾電極也出現了一對氧化還原峰(見圖4c曲線),然而,這對氧化還原峰較之Hb-Chit/AuNPS/APS/PB/GCE修飾電極出現的氧化還原峰小的多,AuNPS在Hb電極反應動力學中產生了巨大影響,在蛋白質與底層電極之間的電子轉移方面,AuNPS提供一個適宜的微環境。當不用PB修飾電極時,峰值電流范圍變得較為廣泛,波峰間隔值增大且峰電流較小(見圖4d曲線),可能是PB的存在促進了Hb與電極之間的電子轉移。
文章所用復合膜材料的生物相容性為Hb提供了一個與Hb本體天然狀態環境相似的微環境,Hb所處的微環境對其電子傳遞有較大的影響,電子傳遞過程與Hb在電極表面的取向有關,由于復合膜材料所帶電荷屬性不同,可以調節Hb在電極表面的取向,使其朝著利于電子受體或供體的方向進行,極大地促進了血紅蛋白與電極間的電子轉移過程。
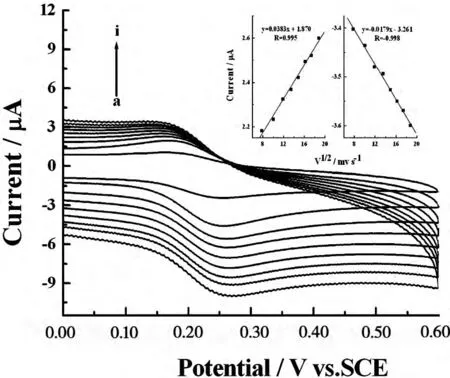
圖5 Hb-Chit/AuNPs/APS/PB修飾電極的峰電流與掃速的關系圖
3.2 Hb-Chit/AuNPs/APS/PB修飾電極電化學行為的影響因素
3.2.1 電極峰電流與掃速的關系
圖5研究了Hb-Chit/AuNPS/APS/PB/GCE電極峰電流與掃速的關系,掃速在20~350mV/s范圍內,隨著掃速的增加,氧化還原峰電流也隨之增加,氧化還原峰電位分別略有移動(還原峰正移,氧化峰負移),且式電勢變大,說明隨著掃速增加,電極電子轉移過程更加不可逆。在此掃速范圍內,峰電流與掃速成正比,表明電極反應受表面影響。在已選擇的掃速范圍內,氧化還原峰電流值幾乎相等,說明在復合材料修飾膜中的電活性HbFe(Ⅲ)在陰極掃描過程中轉化為HbFe(Ⅱ),而在陽極掃描過程中還原態的HbFe(II)又全部轉化為氧化態的HbFe(Ⅲ)。
當掃速在20~350mV/s范圍內時,峰電流與掃速呈良好的線性關系,結果如圖5所示。氧化還原峰電流Ip和掃描速度υ的線性回歸方程為Ipa(μA)=1.87+3.83×10-2υ(mV/s)(R=9.95×10-1)和Ipc(μA)=-3.26-1.79×10-2υ(mV/s)(R=9.98×10-1),所有這些結果與表面控制或單電子薄層電化學行為相符合。
3.2.2 溶液pH對生物傳感器電化學行為的影響
實驗研究了pH4.0-9.0范圍內Hb-Chit/AuNPS/APS/PB/GCE修飾電極的循環伏安行為,結果表明,隨著pH的增加,陰極峰和陽極峰均發生負移。此外陽極峰電勢Epa、陰極峰電勢Epc及式電勢Eo’(Epa/2+Epc/2)均與pH值呈線性關系,直線斜率分別為-48.00mV/pH、-44.50mV/pH和-46m V/pH,接近于1質子1電子可逆電極反應的理論值-59.00mV/pH,表明Hb和電極之間的電子傳遞過程伴隨有1質子的傳遞,質子參與主要是中和電化學還原過程中界面上積累過剩電荷,從而使靠近亞鐵血紅素的基團發生質子化作用,該過程可表示為:HbFe(III)+H++e-→HbHFe(II)。
陽極峰電勢Epa、陰極峰電勢Epc及式電勢Eo’(Epa/2+Epc/2)與pH值線性關系的直線斜率均與理論值59.00mV/pH有些偏離,可能是由于質子化是一個復雜的過程,受Hb配位基團和周圍的血紅素氨基酸共同影響。此外,在pH值為7.00左右時,在修飾電極上Hb氧化還原峰電流最大,其原因主要是Hb在pH值為7.00的PBS緩沖溶液中保持了高度的活性,故選擇pH值為7.00作為最佳底液pH值。
4 Hb-chit/AuNPS/APS/PB/GCE電極的重現性和穩定性
在pH7.00PBS中,于-0.10V-0.60V范圍內,對Hb-chit/AuNPS/APS/PB/GCE電極連續循環伏安掃描時,峰值電流基本保持不變,連續掃描80圈,氧化還原峰電流減小4.80%。該電極在4℃保存20 d,進行循環伏安掃描時發現電流沒有明顯的變化,僅比初始氧化還原電流降低6%左右,由此可見此修飾電極有較好的穩定性。比較8支不同的Hb-chit/AuNPS/APS/PB/GCE電極(制備方法相同)對10μmol/LH2O2的響應電流值,考察電極的重現性,測得RSD為5.20%,表明電極具有良好重現性。
5 結論
文章成功制備了一種新型的chit/AuNPS/APS/PB復合材料,并將其用于Hb的直接電化學研究。這一復合膜有極好的生物適應性和穩定性,能在電極表面為Hb提供合適的仿生微環境,保持了膜中Hb的活性,極大地促進Hb與電極間的電子轉移。該修飾膜修飾電極制備簡單、便捷且有良好穩定性和重現性。制備的Hb-chit/AuNPS/APS/PB/GCE復合膜修飾玻碳電極對H2O2有明顯的電催化活性,催化電流與較寬濃度范圍內的H2O2呈良好線性關系,且無需額外的電子介體,這將為電化學傳感和生物傳感提供一個優良的平臺。

