化學/酶復合催化法制備生物基化學品研究進展
肖竹錢,歐陽洪生,葛秋偉,王珍珍,蔣成君,楊瑞芹,計建炳,毛建衛
(1.浙江科技學院 生物與化學工程學院,浙江 杭州 310023;2.浙江省農產品化學與生物加工技術重點實驗室,浙江 杭州 310023;3.浙江工業大學 化學工程學院,浙江 杭州 310014)
生物質含有自然界最豐富的有機碳源(僅我國秸稈產量就達7 億t/年),在資源短缺的大背景下,利用生物質實現生產石油基化學品的替代產物,不僅需要從原料上實現“綠色”,還需要從溫和工藝條件下實現綠色生產,見圖1。生物基化學品是指利用可再生的生物質(淀粉、葡萄糖、木質纖維素等)為原料生產的大宗化學品和精細化學品等產品,見圖2,由于其并不是來源于化石原料,被認為是實現可持續發展的重要方向,引起國內外廣泛重視。在生物基化學品中丁二酸、3-羥基丙酸、葡萄糖二酸、2,5-呋喃二甲酸、天冬氨酸、谷氨酸、衣康酸、乙酰丙酸、甘油、木糖醇、3-羥基-γ-丁內酯等可能是未來最有價值的生物基化學品[1]。對于能源消耗迅速增長的中國,面臨著環境問題的巨大挑戰,在此背景下,開發利用生物基化學品具有重大意義。
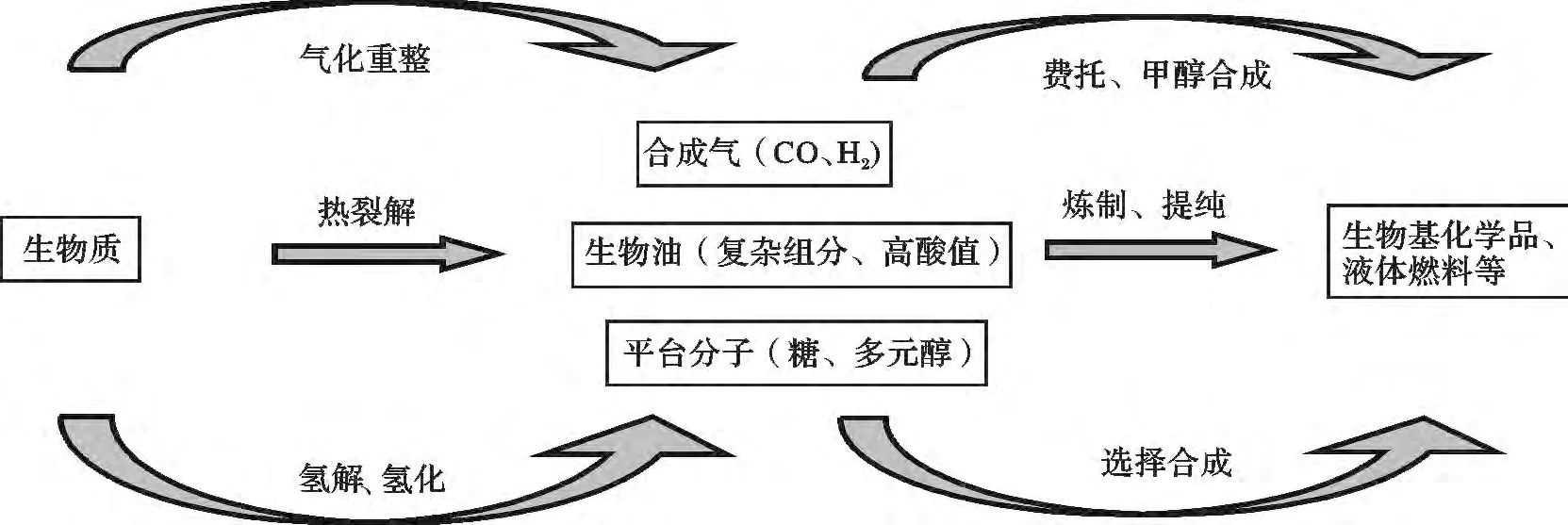
圖1 生物質轉化主要途徑Fig.1 The mian process for biomass conversion
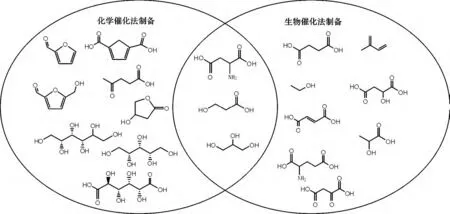
圖2 生物質基化學品[7]Fig.2 Bio-based chemicals
目前,由生物質轉化為化學品反應采用生物酶、Brnsted 和Lewis 酸等催化劑,主要進行的是單純生物催化或化學催化過程,其主要缺點是副反應較多、需要分離中間產物、對設備要求較高、耗能較大等[2-3]。化學/酶復合催化法應用于生物基化學品制備實現了原料與過程的綠色化。1980 年,van Bekkum 等[4]首次描述了化學催化(金屬催化劑)和生物催化(葡萄糖異構化酶)的兼容性,此法越來越多地應用于生物質煉制過程。化學/酶復合催化一步法反應延續了生物催化劑的高效、高選擇性和化學催化劑的穩定性(高溫下)等優點。若以水為溶劑,能使酶催化劑與化學催化劑在彼此協同作用下將多步轉化反應整合為一步反應,避免了中間產物的分離,節省了溶劑的消耗,極大地提高了空時收率[5-6],非常具有工業化潛力。本文主要論述化學/酶復合催化法在制備生物基化學品中的應用。
1 化學/酶復合催化法制備生物基糖醇
1.1 葡萄糖制備甘露醇
甘露醇是一種重要的六元醇,具有甜度適宜、熱量低、無毒副作用等特點[7-8]。因其重要的理化性質,在食品工業上,是一種重要的營養型甜味劑;在醫藥上,用作滲透性利尿劑、脫水劑以及醫藥添加劑;在精細化工方面,甘露醇及以其為原料合成的多種精細化工產品用于增塑劑、紡織輔助劑、油品分散劑、表面活性劑等。在自然界中,甘露醇主要貯存于海藻體內、水果和植物的根莖葉等。工業合成甘露醇方法有:從海帶中直接提取,葡萄糖電解還原法,葡萄糖異構法等,其中葡萄糖異構法應用最多。在金屬催化劑(如,Ni 催化劑)作用下,在溫度90 ℃,5.0 MPa 條件下,果葡糖漿加氫反應制備甘露醇的反應選擇性只有70%[9]。采用化學/酶復合催化法制備甘露醇工藝中,金屬加氫催化劑和異構化酶協同作用,甘露醇的收率可達84%[10],見圖3。此過程中可與葡萄糖異構化酶聯合催化的金屬催化劑有Pt/C、Y 型分子篩負載Ru 催化劑[11]、納米Pd[12]等。其中,Y 型分子篩負載Ru 催化劑和異構化酶協同作用下,在氫壓為6 MPa、反應時間為16 h 條件下,甘露醇的收率可達38%。而單獨用含Ru 催化劑催化葡萄糖氫化所獲得的甘露醇的收率只有1.5%,山梨醇的收率達到98%[13]。

圖3 由葡萄糖化學/酶復合催化一步法制備甘露醇Fig.3 Chemo-enzymatic one-step progress for glucose to mannitol
1.2 淀粉制備山梨醇
山梨醇是一種具有很高價值的平臺化合物,被美國能源部列為十二種最有價值的生物基單元化合物之一[14]。由山梨醇轉化而來的化學品涉及能源、化工、食品、制藥等重要領域。目前,絕大多數山梨醇都由淀粉水解成葡萄糖,再由葡萄糖加氫制得。淀粉水解催化劑主要有生物酶、Brnsted 酸和Lewis酸,葡萄糖加氫催化劑主要為金屬(如Ni,Pt,Ru等)或有機金屬催化劑[15-16],但酸性條件水解加氫對設備腐蝕嚴重,廢液污染環境。山梨醇也可在金屬催化劑作用下利用纖維素直接加氫制得,Joung Woo Han 等[17]直接以纖維素為原料,利用含Ru 催化劑,反應溫度為165 ℃,山梨醇收率為58. 7%。化學/酶復合催化一步法反應能夠簡化反應步驟,在低溫中性環境實現反應過程,并通過降低分離和精制成本,提高反應經濟性。Li Hui 等[18]利用糊精作原料,淀粉酶和Ru-B/mSiO2為催化劑,在348 K,氫壓6.0 MPa 條件下,通過一步反應制得的山梨醇收率達82%,反應過程見圖4。該方法以多孔SiO2為載體,將酶和化學催化劑整合成殼狀結構,通過控制孔徑大小,阻止了膠質物質吸附在催化劑表面,保護了催化劑的活性。因其具有殼狀結構,在微觀上就形成了眾多微反應器,促進了反應的進行[19]。

圖4 淀粉化學/酶復合催化一步法制備山梨醇Fig.4 Chemo-enzymatic one-step progress for starch to sorbitol
2 化學/酶復合催化法制備氨基酸
D 型氨基酸在20 世紀70 年代被科學家在人體中發現,被冠以“非天然”氨基酸之稱,價格十分昂貴。因其重要的功能性質,在醫藥、食品、農藥等方面具有廣泛的應用,還參與人體的重要新陳代謝[6]。目前,D 型氨基酸主要通過生物轉化法、物理化學拆分法等方法制備。前者特定酶催化劑成本較高,部分酶還對金屬具有一定的依賴性;后者拆分選擇性不高,純度不高,只有60% ~90%[20]。利用化學/酶復合催化法能夠“取長補短”,酶提高選擇性,化學催化劑適用于直接合成反應,并且溫度適應性強。Chen 等[21]以堿性蛋白酶、酰基轉移酶和5-磷酸吡哆醛為催化劑在高濃度有機溶劑中合成D 型氨基酸和多肽,使氨基酸和多肽收率提高了15%以上。
3 化學/酶復合催化法制備其它生物基化學品
3.1 葡萄糖制備縮水甘油和葡萄糖酸
縮水甘油中含有環氧基和羥基兩個具有反應活性的基團,是一種具有較高附加值的化工中間體或原料,它可作為合成表面活性劑、樹脂、染料等的中間體,也可廣泛用于各種溶劑的提取和分離。縮水甘油制備方法主要有甘油氯醇法、烯丙醇法、甘油/尿素法和甘油/3-氯-1,2-丙二醇法[22],甘油/3-氯-1,2-丙二醇法一般以甘油為起始原料在高溫、金屬催化劑條件下進行。劉學民等[23]以ZnSO4為催化劑,在溫度為215 ℃條件下合成目的產物的產率為83.8%,制備條件較為苛刻。而在以葡萄糖為原料制備葡萄糖酸工藝中,葡萄糖在氧化酶的作用下生成吡喃糖,副產物為H2O2,并以此為氧化劑,在SiO2負載Ti 催化劑作用下催化氧化烯丙醇制得縮水甘油,反應溫度僅為30 ℃,反應產率為30%[24],實現了上一個反應副產物的再利用。在反應初始,同時進料反應物和雙組分催化劑,實現以葡萄糖為原料一步法制備縮水甘油和葡萄糖酸,見圖5。

圖5 葡萄糖化學/酶復合催化制備縮水甘油和葡萄糖酸Fig.5 Chemo-enzymatic progress for producing epihydric alcohol and gluconic acid
3.2 葡萄糖制備2-羥基呋喃乙酸
2-羥基呋喃乙酸(FA)是一種具有芳香性的羥基酸,因其特有的呋喃環,在聚酯工業應用廣泛。它能與乳酸(LA)在一定條件下形成一種與聚苯乙烯(PS)性質非常相似的共聚物FA-LA,用于制造日常生活中的一次性餐具、汽車部件、包裝材料、玩具、建筑材料、電器和家庭用品等。葡萄糖化學/酶復合催化法制備2-羥基呋喃乙酸在工藝上更為簡便,目的產物的選擇性高[25],見圖6。

圖6 由葡萄糖化學/酶復合催化法制備2-羥基呋喃乙酸Fig.6 Chemo-enzymatic progress for producing glucose to 2-hydroxy furan acetic acid
3.3 甲基-D-吡喃半乳糖苷制備4-脫氧-D-葡萄糖
在甲基-D-吡喃半乳糖苷制備4-脫氧-D-葡萄糖需要多步反應[26],見圖7。

圖7 化學/酶復合催化一步法制備4-脫氧-D-葡萄糖Fig.7 Chemo-enzymatic one-step progress for glucose to 4-deoxy-D-glucose
反應時間較長,工藝步驟繁瑣,收率不高。為了提高目的產物的收率,將半乳糖氧化酶和金屬催化劑Pt/C 應用于一步合成反應[27]。前半部分反應在半乳糖氧化酶的作用下,大大提高了中間產物的選擇性,在中間產物不分離的前提下,后半部分反應將溫度升至70 ℃后,金屬加氫催化劑發揮催化作用。反應結果顯示,4-脫氧-D-葡萄糖的收率大于95%。
3.4 乳酸制備生物基化學品
乳酸是一種重要的生物基平臺化合物,由乳酸制得的生物基化學品具有良好的市場前景[5,28],見圖8。

圖8 由乳酸作為平臺化合物制備生物基化學品Fig.8 Use of lactic acid as a platform chemicals
乳酸可通過發酵法制備,發酵的原料一般是玉米、大米、甘薯等淀粉質原料或多糖[29]。乳酸發酵階段能夠產酸的乳酸菌種類很多,但產酸質量不高,需要將粗乳酸進一步提純[24-32]。乳酸也可以通過合成法制備,主要途徑有乳腈法、丙烯腈法、丙酸法、丙烯法等[33-34],但化學合成法過程工藝復雜,需要分解、精餾、濃縮等多步物理化學過程制得精乳酸。利用化學/酶復合催化一步法制備乳酸,選擇性高,不需分離中間產物,反應條件溫和,提高了反應的空時效率,見圖9。

圖9 化學/酶復合催化一步法制備乳酸Fig.9 Chemo-enzymatic one-step progress for preparation of lactic acid
4 結束語
化學/酶復合催化法為生物質煉制和生物質衍生物轉化為生物基化學品提供了一條更為綠色的工藝路徑。此法在簡化反應步驟、降低中間產物分離和精制過程的能耗等方面具有巨大優勢,過程經濟性好,符合綠色化學概念,在生物質煉制方面,將為我們帶來巨大的環境效益。然而,在生化催化劑的制備與重復利用、尋找聯合催化最適反應條件等方面需要進一步探索。生物催化劑和化學催化劑具有完全不同的催化機理,復合化學/酶催化劑于一步法制備工藝最根本的是要提高兩種催化條件的兼容性。尋找最優催化條件使兩種催化劑都能達到較好的催化性能,這是生物催化劑和化學催化劑復合的關鍵。
[1] 邢建民.2013 生物基化學品專刊序言[J].生物工程學報,2013,29:1351-1353.
[2] Kadokawa J. Precision polysaccaride synthesis catalyzed by enzymes[J]. Chemical Review,2011,111(7):4308-4345.
[3] Xiao Z H,Jin S H,Pang M,et al. Conversion of highly concentrated cellulose to 1,2-propanediol and ethy-lene glycol over highly efficient CuCr catalysts[J]. Green Chemistry,2013,15(4):891-895.
[4] Makkee M,Kieboom A P G,van Bekkum H,et al. Combined action of enzyme and chemical and metal catalyst,applied to the preparation of D-mannitol[J].Chem Commu,1980,19:930-931.
[5] Harald G,Werner H.Combing the‘two worlds’of chemocatalysis and biocatalysis towards multi-step one-pot processes in aqueous media[J]. Current Opinion in Chemical Biological,2014,19:171-179.
[6] 于平.生物轉化和手性拆分技術制備D-氨基酸研究進展[J].生物學通報,2005,40(9):3-5.
[7] Thomas J S,Brandon J O,Brent H,et al. Bridging the chemical and biological catalysis gap:Challenges and outlooks for producing sustainable chemicals[J].ACS Catalysis,2014,4:2060-2069.
[8] 林琳,岳敏,曹海龍,等. 產甘露醇菌株的育種研究進展[J].食品工業科技,2012,11:426-430.
[9] 朱建良,陳俊青,歐陽平凱,等. 果葡糖漿加氫制備甘露醇的選擇性[J]. 南京工業大學學報,2002,24(2):81-84.
[10]趙東輝,王關斌,李俊平,等. 雙異構法制備晶體甘露醇的研究[J].化工工程師,2005(3):53-55.
[11] Ruddlesden J F,Stewart A. Simultaneous action of Ru Yzeolite and glucose isomerase in the production of Dmannitol from D-glucose[J]. Chem RES,1981,8:378-379.
[12]Boffi A,Cacchi S,Ceci P,et al.The Heck reaction of alllic alcohols catalyzed by palladium nanoparticles in water:chemoenzymatic synthesis[J].Chem Cat Chem,2011,3:3347-3353.
[13] Marken J,Lizenzen S. Crystalline sugar alcohols:EP,T0-45598[P].2001-12-07.
[14] Werpy T,Petersen G. Top Value Added Chemicals from Biomass[M].Richland:Pacific Northwest National Laboratory,2004:6-13.
[15] Kadokawa J. Precision polysaccharide synthesis catalyzed by enzymes[J].Chemical Reviews,2011,111(7):4308-4345.
[16]Hu X T,Li H G,Wei B X,et al. Hydrolysis process of normal rice starch by 1-butanol-hydrochloric acid[J].Food Hydrocolloidds,2014,41:27-32.
[17]Joung Woo Han,Hyunjoo Lee.Direct conversion of cellulose into sorbitol using dual-functionalized catalysts in neutral aqueous solution[J]. Catalysis Communications,2012,19:115-118.
[18]Xu L,Wei W,Li H X,et al.Combination of enzyme and Ru-B amorphous alloy encapsulated in Yolk-Shell silica for one-pot dextrin conversion to sorbitol[J]. Chemical Research,2014,4:251-258.
[19] Santiso E E,George A M,Turner C H,et al. Adsorption and catalysis:The effect of confinement on chemical reactions[J]. Applied Surface Science,2005,252(3):766-777.
[20]梅樂和,姚善涇,關怡新,等. D-氨基酸的生物轉化與拆分技術研究的新進展[J]. 中國醫藥工業雜志,1999,30(5):235-238.
[21]Chen S T,Wang K T.Chemo-enzymatic synthesis of optically active amino acids and peptides[J]. Journal of the Chinese Chemical Society,1999,46(3):301-311.
[22]褚昭寧.甘油法合成縮水甘油的研究[D].無錫:江南大學,2009.
[23]劉學民,褚昭寧,劉志偉.甘油法合成縮水甘油[J].化工進展,2009,28(8):1445-1448.
[24] Vennestrom P N R,Taarning E,Christensen C H,et al.Chemoenzymatic combination of glucose oxidase with titanium silicalite-1[J].Chem Cat Chem,2010,2:943-945.
[25]Schwartz Thomas J,Goodman Samuel M,Osmundsen Christian M,et al.Integration of chemical and biological catalysis:Production of furylglycolic acid from glucose via cortalcerone[J]. ACS Catalysis,2014,3 (12):2689-2693.
[26] Heidlindemann M,Rulli G,Berkessel A,et al. Combination of asymmetric organo-and biocatalytic reactions in organic media using immobilized catalysts in different compartments[J].ACS Catalysis,2014,4(4):1099-1103.
[27]Rob S,Tom K.Combined catalytic conversion involving an enzyme,a homogeneous and a heterogeneous catalyst:onepot preparation of 4-deoxy-D-glucose derivatives from Dgalactose[J].Tetrahedron Lett,2002,43:3399-3400.
[28]Benjamin K,Paul S,Dumeignil F.Highly efficient catalyst for the decarbonylation of lactic acid to acetaldehyde[J].Green Chemistry,2010,12(11):1910-1913.
[29] Holm M S,Saravanamurugan S,Taarning E.Converion of sugars to lactic acids derivatives using heterogeneous aeotype catalysts[J].Science,2010,5978:602-605.
[30]胡永紅,管琚,楊文革,等. 發酵法生產D-乳酸的研究進展[J].食品與發酵工業,2007,33(12):98-103.
[31]許婷婷,柏中中,何冰芳.D-乳酸制備研究進展[J].化工進展,2009,28(6):991-996.
[32]金其榮,金豐秋.乳酸衍生物發展應用新動向[J]. 山西食品工業,2002,3:2-4.
[33]Srivastava A,Poonia A,Tripathi A D,et al. Optimization of nutritional supplements for enhanced lacticacid production utilizing sugar refinery by-products[J].Annal of Microbiology,2014,64(3):1211-1221.
[34]Jimenez B P,Salas A J,Esquivel M,et al.Optimization of microwave-assisted and conventional heating comparative synthesis of poly(lacticacid)by direct melt polycondensation from agroindustrial banana (Musa AAA Cavendish)and pineapple (Ananas comosus)fermented wastes[J].Journal of Polymers and the Environment,2014,22(3):393-397.

