硝基胍結晶過程介穩區寬度研究
徐其鵬,羅志龍,鄒高興,陳 松,康 超,楊 毅
(西安近代化學研究所,陜西西安710065)
?
硝基胍結晶過程介穩區寬度研究
徐其鵬,羅志龍,鄒高興,陳松,康超,楊毅
(西安近代化學研究所,陜西西安710065)
摘要:為了測試硝基胍在硝酸溶液中的介穩區寬度,采用重結晶儀測試溶液的濁度和溫度,經計算得到溶解度,分析了硝酸含量、降溫速率、飽和溫度和攪拌速率對介穩區寬度的影響。結果表明,在硝基胍結晶過程中,介穩區寬度隨降溫速率的增加和硝酸含量的升高而變寬;隨攪拌速率的增加, 介穩區寬度變窄;不同飽和溫度下,溫度越高,介穩區寬度越窄。在實際操作過程中,硝酸質量分數為45%,攪拌速率為150r/min, 飽和溫度為0℃,降溫速率為0.8℃/min時,結晶較宜。用經典成核理論推導了介穩區寬度的模型方程,結果與實驗值符合較好,成核級數為0.56。
關鍵詞:物理化學;硝基胍;濁度;溶解度;介穩區
引言
硝基胍是三基及多基發射藥的重要組分,由于其能量高、溫度系數低、燒蝕率低及炮口火焰較少,廣泛用于槍炮發射藥中。目前硝基胍的生產方法主要是濃硫酸與硝酸胍反應,再經稀釋分離獲得硝基胍[1-2]。該法制備的硝基胍粒度、純度和酸度均不滿足GJB1441A-2005《硝基胍規范》要求,需進行重結晶轉晶,且產生大量廢硫酸,對環境污染嚴重。西安近代化學研究所在20世紀80年代提出硝酸法制備硝基胍新工藝,可以一步制備滿足晶型、粒度、酸度和純度要求的硝基胍晶體[3-4]。
硝酸法制備硝基胍過程中,結晶粒度是至關重要的一步,結晶過程的控制直接影響產品的質量[5]。結晶操作的最佳過飽和度應該處于介穩區范圍內,以便控制結晶過程中的成核速率及晶體生長速率。為了得到理想的粒度及粒度分布產品,操作過程需要控制攪拌速率及降溫速率、選擇合適的結晶溫度及母液濃度[6-7]。本實驗研究了硝酸法制備硝基胍過程中硝酸含量、降溫速率、飽和溫度和攪拌速率對硝基胍結晶過程的影響,找出了這些條件對硝基胍結晶介穩區寬度的影響規律,為工業結晶器的設計和產品結晶過程的控制提供理論指導。
1實驗
1.1材料和儀器
硝基胍,陜西應用物理化學研究所;濃硝酸(質量分數98%),工業品,成都市科龍化工試劑廠;蒸餾水,自制。
Crystal scall型重結晶儀,含溫度檢測系統(精度0.01℃)、濁度檢測系統(精度0.01)、攪拌系統,英國HEL公司;FP50型加熱冷卻循環系統,德國Julabo公司。
1.2實驗方法
將配制的硝酸溶液500mL放入1000mL四口燒瓶中,開啟重結晶儀的濁度檢測系統、溫控系統和攪拌裝置,穩定10min后,記錄此時溶液的濁度。向溶液中加入硝基胍,初始每次1g,快達到飽和時,每次0.1g,每次平衡20min,當溶液的濁度未顯示變化時,再次加入定量的硝基胍,直到溶液的濁度發生變化,計算硝基胍的溶解量進而計算出硝基胍的溶解度。
將該溫度下的飽和溶液升溫5℃,穩定10min,記錄此時溶液的濁度,以一定速率降溫,當濁度增大時,記下此時的溫度。由此計算出該條件下的超溶解度或以溫差表示的介穩區寬度。
2結果與討論
2.1硝基胍的溶解度
用濁度檢測系統測定不同溫度和硝酸含量下硝基胍的溶解度,并與文獻值[8]進行對比,結果見表1。
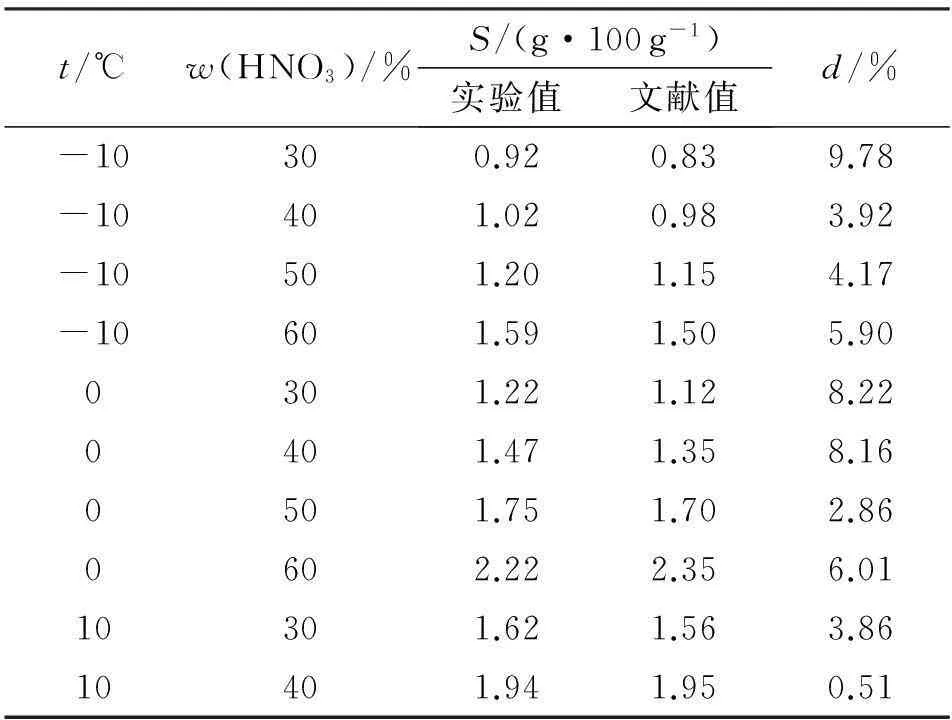
表1 硝基胍溶解度實驗值與文獻值的比較
續表1
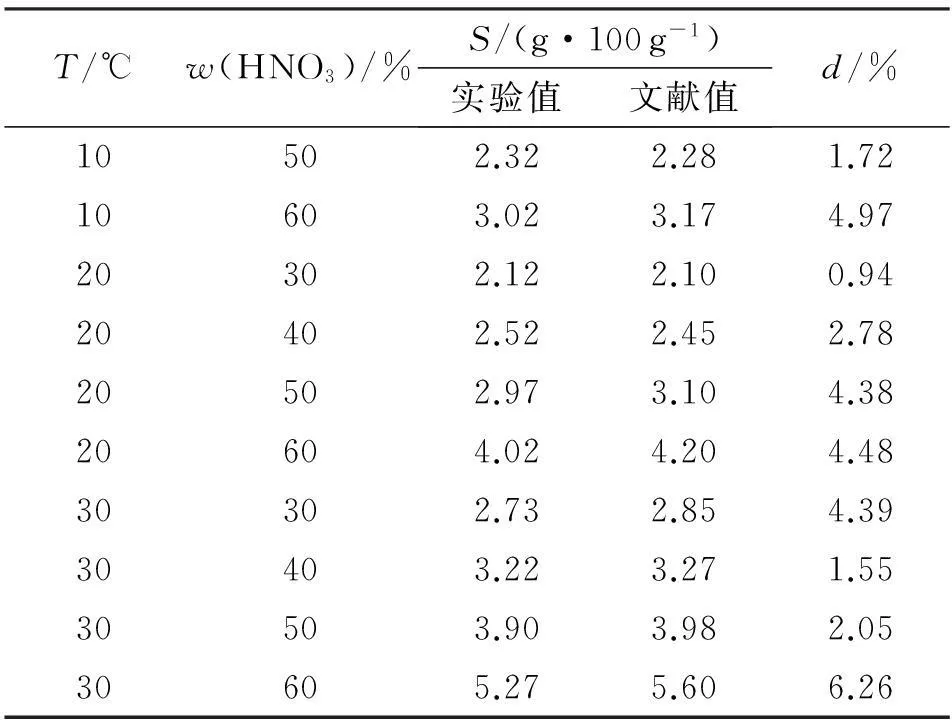
T/℃w(HNO3)/%S/(g·100g-1)實驗值文獻值d/%10502.322.281.7210603.023.174.9720302.122.100.9420402.522.452.7820502.973.104.3820604.024.204.4830302.732.854.3930403.223.271.5530503.903.982.0530605.275.606.26
注:t為飽和溶液的溫度;w(HNO3)為硝酸質量分數;d=|實驗值-文獻值|/實驗值。
表1顯示,文獻值與實驗值接近,相差絕對值均小于10%,證明該測試方法可行,數據準確。
2.2降溫速率對硝基胍結晶過程介穩區寬度的影響
根據經典成核理論[9]及Nyvlt等[10]的實驗結果,當攪拌速率一定時:
ln(tmax)=m′lnv+K1
(1)
將lnv與ln(tmax)作圖可得一直線,直線的斜率為成核級數的倒數。采用式(1)對不同降溫速率下硝基胍結晶的介穩區寬度進行關聯,得到不同飽和溫度下的模型方程:
當t=-5℃、w(HNO3)=45%、r=150r/min時,ln(tmax)=1.8015 lnv+1.2446;
當t=0℃、w(HNO3)=45%、r=150r/min時,
當t=5℃、w(HNO3)=45%、r=150r/min時,
當t=-10℃、w(HNO3)=45%、r=150r/min時,ln(tmax)=1.8786 lnv+1.0411
由模型方程可以看出,成核級數m值變化不大,說明溶液結晶的成核級數與飽和溫度基本無關,取平均值m=0.56。選擇上述3組模型方程的計算數據與實驗值作比較,結果見圖1。
從圖1可以看出,模型方程的計算值與實驗值相差不大,符合經典成核理論。另外,恒定的過飽和度是結晶過程中的最佳操作條件,而實際操作中很難做到,對于硝基胍結晶,控制在介穩區內更為實際[11]。在硝酸質量分數45%、攪拌速率150r/min、飽和溫度為0℃、降溫速率為0.8℃/min條件下,介穩區寬度為4℃,為硝基胍結晶的控制提供了便利。之后,隨著降溫速率的提高,介穩區寬度增長緩慢,而降溫速率的提高是以消耗動力為代價的,因此,選擇0.8℃/min的降溫條件較適宜。
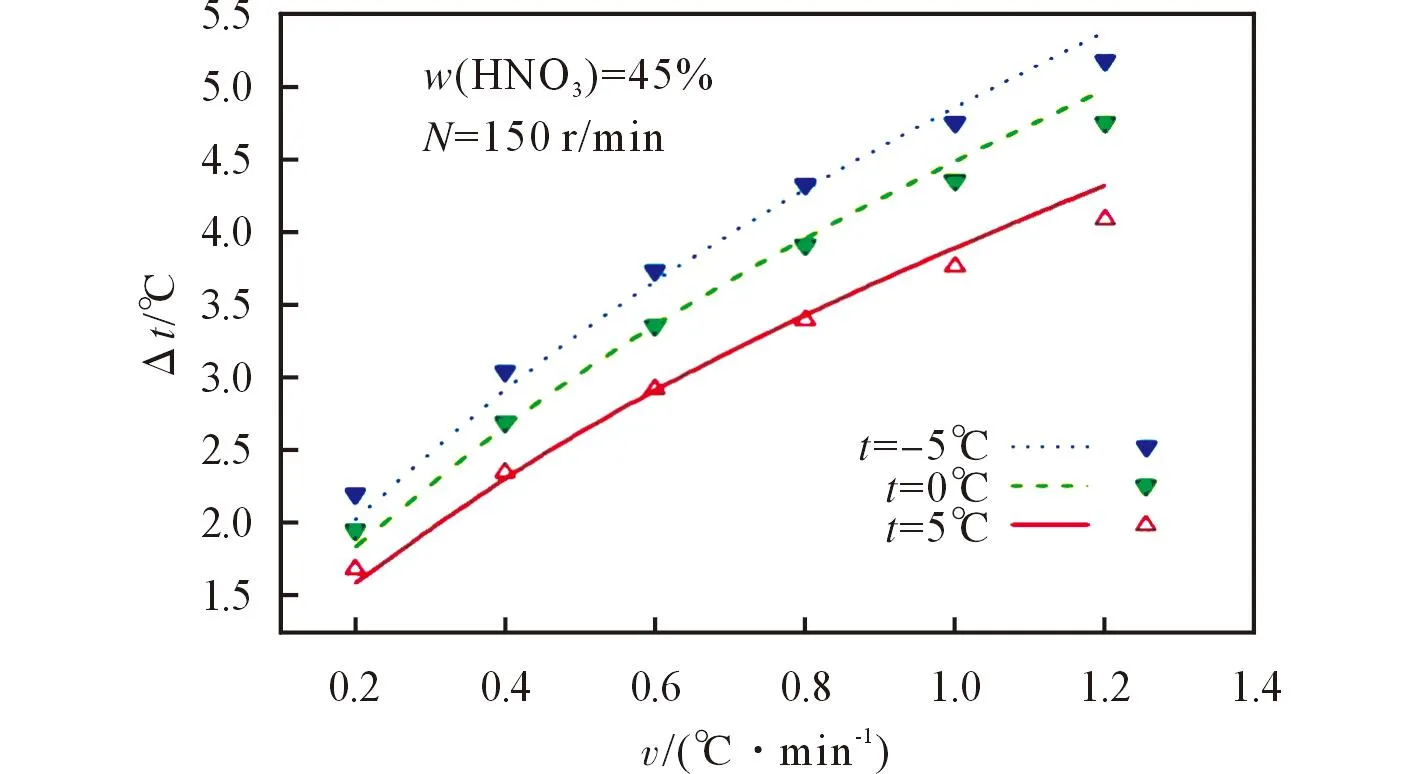
圖1 不同降溫速率下介穩區寬度模型方程計算值與實驗值的對比曲線Fig.1 Comparison equations of the model values with experimentones of metastable zone width under different cooling rates
2.3攪拌速率對硝基胍結晶過程介穩區寬度的影響
不同攪拌速率下硝基胍結晶過程介穩區寬度的變化曲線見圖2。
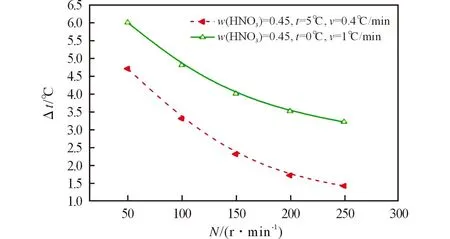
圖2 不同攪拌速率下硝基胍結晶過程介穩區寬度的變化曲線Fig.2 The change curves of the metastable zone width atdifferent stirring speeds
由圖2可以看出,硝基胍結晶過程的介穩區寬度均隨著攪拌速率的提高而變窄。這是因為提高攪拌速率,傳質速率增大,硝基胍分子碰撞成核的幾率增大;同時,傳熱速率增大,有利于結晶熱的擴散,結晶較容易,介穩區寬度變窄[12-13]。當攪拌速率大于150r/min時,介穩區變化平緩,這可能是由于此時的傳熱速率已達到硝基胍結晶的熱閾值。
2.4溫度對硝基胍結晶過程介穩區寬度影響
不同飽和溫度下硝基胍結晶過程介穩區寬度的變化曲線見圖3。
由圖3可以看出,在不同硝酸含量、攪拌速率及降溫速率下,硝基胍在硝酸溶液中的介穩區寬度均隨溫度的升高而降低。這是因為隨著溶液溫度的升高,黏度下降,導致溶質擴散系數增大,硝基胍分子熱運動加劇,分子間碰撞成核的幾率增強,并且飽和溫度越高,溶液中的硝酸含量也越高,成核更容易,因此溶液溫度升高導致介穩區寬度變窄。而在實際操作中,結晶過程的溫度不宜過高或過低,過高時硝基胍的溶解度增大,損失嚴重;過低時,增加額外動力成本,且介穩區寬度變化不明顯。綜合考慮,結晶溫度在0℃較適宜。
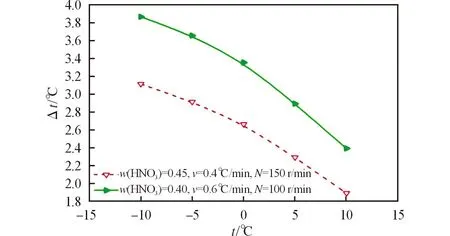
圖3 不同飽和溫度下硝基胍結晶過程介穩區寬度的變化曲線Fig.3 The change curves of the metastable zone widthof NQ at different saturation temperatures
2.5硝酸含量對硝基胍結晶過程介穩區寬度影響
不同硝酸含量下硝基胍結晶過程介穩區寬度的變化曲線見圖4。
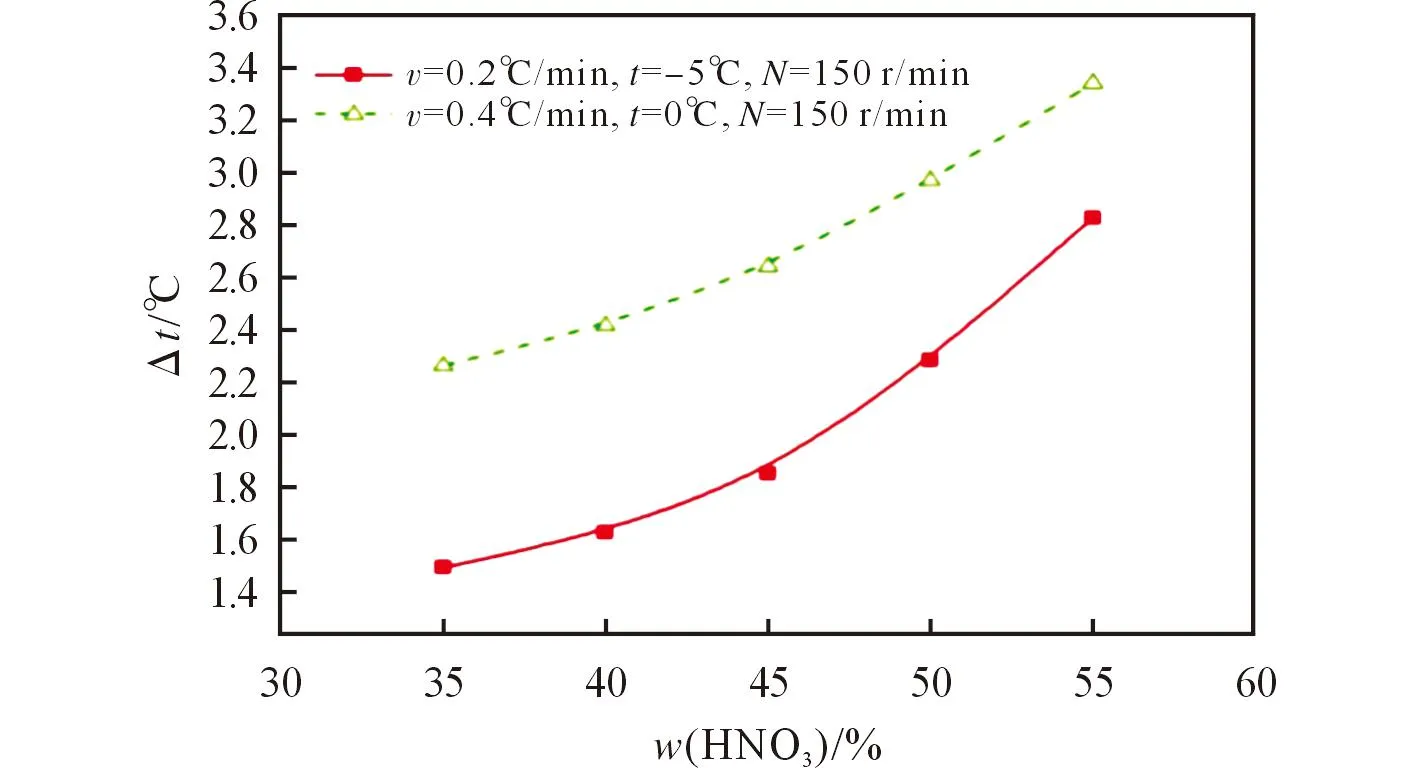
圖4 不同硝酸含量下硝基胍結晶過程介穩區寬度的變化曲線Fig.4 The change curves of the metastable zone widthof NQ at different content of nitrate acid
從圖4可以看出,硝基胍結晶過程的介穩區寬度隨硝酸含量的增大而變寬。這是因為,一方面,硝酸含量增大,黏度增加,溶質擴散系數減小,溶液中硝基胍分子熱運動降低,分子間成核幾率減小;同時,在較高含量下,硝基胍的溶解度增大,硝基胍在硝酸-水體系內的體積濃度增大,增加了碰撞成核幾率,兩者共同作用導致在硝酸含量較低時,介穩區寬度增長緩慢,而在含量較高時,介穩區寬度增長較快。在實際結晶過程中,選擇質量分數為45%的硝酸較適宜。
3結論
(1)用重結晶儀測試硝酸溶液的濁度和溫度,計算出硝基胍在硝酸溶液中的溶解度和以過冷度表示的介穩區寬度,溶解度數據與文獻值相差率小于10%,證明該測試方法的可行性及準確性。
(2)用經典成核理論對不同降溫速率下的模型參數進行擬合,得到不同飽和溫度下的模型方程,模型計算值與實驗值相符,成核級數為0.56。
(3)測定了硝基胍在硝酸溶液中結晶過程的介穩區寬度,介穩區寬度隨降溫速率的增加而變寬,隨攪拌速率的增加而變窄,隨硝酸含量的升高而變寬,且在不同飽和溫度下,溫度越高,介穩區寬度越窄。在實際結晶操作中,硝酸質量分數為45%,攪拌速率為150r/min,飽和溫度為0℃,降溫速率為0.8℃/min時較適宜。
參考文獻:
[1]Wardle R B,Braithwite P C,Haaland A C, et al. High energy OXETANE/HNIW Gun Propellants [C]∥ 27th International Annual Conference. Karlsruhe: ICT, 1996.
[2]魏學濤, 趙穎,李乃勤,等. 新型硝基胍發射藥研究[J]. 火炸藥學報, 2001, 24(4): 34-35.
WEI Xue-tao, ZHAO Yin, LI Nai-qin, et al. The study on a new kind of nitroguan idine propellant[J]. Chinese Journal of Explosives and Propellants, 2001, 24(4): 34-35.
[3]李文瑛,張萬君,宋景選. 均勻設計法優選球形硝基胍制備工藝[J]. 火炸藥學報, 2004, 27(4): 52-54.
LI Wen-ying, ZHANG Wan-jun, SONG Jing-xuan. Optimal technical conditions of preparing spherical nitroguanidine by uniform design[J]. Chinese Journal of Explosives and Propellants, 2004, 27(4): 52-54.
[4]陳超.硝基胍結晶控制工藝研究[D].北京:中國兵器科學研究院,2012.
CHEN Chao. Research of controlled crystallization of NQ[D].Beijing: China Weapons Science Research Institute,2012.
[5]Ulrich J, Strege C. Some aspects of metastable zone width and nucleation in industrial crystallizers[J].Journal of Crystal Growth,2002,237:2130-2135.
[6]Mullin J W,Jancic S J.Interpretation of metastable zone widths[J]. Trans Inst Chem Eng, 1979, 57(3):188-194.
[7]Srinivasan K, Meera K, Ramasamy P. A contemporary method to enhance the metastable zone width for crystal growth from solution[J].Materials Science and Engineering,2001,B84:233-236.
[8]陳超,楊毅,金建平,等.硝基胍結晶熱力學[J].化工進展,2012(S1):486-489.
CHEN Chao, YANG Yi, JIN Jian-ping,et al. Study on the ermodynamics of crystallization of nitroguanidine[J].Chemical Industry and Engineering Progress,2012(S1): 486-489.
[9]丁緒懷,談遒.工業結晶[M].北京:化學工業出版社,1985.
[10]Nyvlt J, Rychly R, Gottfried J, et al. Metastable zone-width of some aqueous solutions[J]. Crystal Growth, 1970(6):151-162.
[11]Melia T P, Moffitt W P. Crystallization from aqueous solution[J]. Colloid Science, 1964, 19: 433-447.
[12]林晶,黨亞固,費德君,等. 磷酸二氫銨結晶介穩區的研究[J].無機鹽工業,2007,39(10):21-23.
LIN Jing, DANG Ya-gu, FEI De-jun, et al. Research on crystallization metastable zone of ammonium dihydrogen phosphate[J]. Inorganic Chemicals Industry,2007,39(10):21-23.
[13]張磊,應漢杰,呂浩,等. 乙醇-水混合溶劑中5’-尿苷酸二鈉的結晶介穩區[J].化工學報,2008,59(6):1348-1352.
ZHANG Lei, YING Han-jie, Lü Hao, et al. Metastable zone of 5’-UMPNO2in ethanol-aqueous mixture[J]. Journal of Chemical Industry and Engineering,2008,59(6):1348-1352.
Study on the Metastable Zone Width of Nitroguanidine in Crystallization Process
XU Qi-peng, LUO Zhi-long, ZOU Gao-xing, CHEN Song, KANG Chao, YANG Yi
(Xi′an Modern Chemistry Research Institute, Xi′an 710065, China)
Abstract:To test the metastable zone width of nitroguanidine in nitric acid solution, the effects of content of nitric acid, cooling rate, saturation temperature and stirring speed on the metastable zone width were analyzed using test data obtained by recrystallization apparatus and calculated solubility. The results show that with the increase of cooling rate and nitric acid concentration, the metastable zone width of nitroguanidine in recrystallization process widens. With the increase of stirring speed, the metastable zone width narrows. In different saturation temperature, the higher the temperature, the more narrow the metastable zone width. In actual crystallization process, the crystallization is more appropriate when mass fraction of HNO3is 45%, stirring speed is 150r/min, saturation temperature is 0℃ and cooling rate is 0.8℃/min. The model equations of metastable zone width are derived by means of the classical nucleation theory. The results are in good agreement with the experimental ones. The nucleation ordermis 0.56.
Keywords:physical chemistry; nitroguanidine(NQ); turbidity;solubility;metastable zone
作者簡介:徐其鵬(1989-),男,工程師,從事含能材料工藝工程化研究。
基金項目:兵器裝備預先研究基金(40406040203);基礎產品創新火炸藥專項
收稿日期:2014-09-05;修回日期:2014-12-17
中圖分類號:TQ126; O64
文獻標志碼:A
文章編號:1007-7812(2015)01-0022-04
DOI:10.14077/j.issn.1007-7812.2015.01.005

