3個VHL綜合征家族的基因檢測及臨床調查
吳鑫堯,陳江明,趙義軍,謝 坤,劉付寶,耿小平
3個VHL綜合征家族的基因檢測及臨床調查
吳鑫堯1,陳江明2,趙義軍1,謝 坤1,劉付寶1,耿小平1
摘要目的 明確von Hippel-Lindau綜合征(VHL綜合征)家族基因突變及臨床表現特點,篩查出家族內基因突變攜帶者行臨床篩查,綜合家族發病特點行家族健康指導。方法
通過流行病學調查,共3例先證者臨床診斷VHL綜合征。抽取先證者及家族自愿者外周血,應用聚合酶鏈反應(PCR)體外擴增得到vhl基因片段,通過測序得到基因信息;再對家族內具有vhl基因突變的攜帶者進行頭顱MRI、腹部B超等對全身多系統行臨床篩查;綜合家族發病特點給出家族健康指導。結果 3例先證者均發現vhl基因發生突變,家族1 中5例成員基因陽性,突變方式為外顯子1 c.330C>A;家族2先證者外顯子3488delC;家族3發現7例基因陽性者,突變方式為外顯子1 c.233G>A。其中,家族成員1III3、3III1、3III4、3IV3確定為基因突變攜帶者,臨床檢查顯示其中3例成員已發病,1III3表現為雙腎多發囊腫,胰腺多發囊腫;3III1表現為胰腺多發囊腫;3III4表現為視網膜血管母細胞瘤、胰腺多發囊腫,視網膜血管母細胞瘤接受激光治療。3IV3由于年齡較小,臨床檢查未見明顯異常。所有基因攜帶者接受規范化隨訪。結論 基因檢測可早期確診VHL綜合征,臨床上對vhl基因突變患者需進行嚴密隨訪,從而提高患者治療效果、延長生存期或改善生活質量。
關鍵詞VHL綜合征;vhl基因;基因檢測
2015-02-13接收
作者單位:1安徽醫科大學第一附屬醫院器官移植中心,合肥230022
2安徽醫科大學第二附屬醫院普外科,合肥 230601
von Hippel-Lindau綜合征(VHL綜合征)是一種常染色體顯性基因遺傳性疾病,是染色體3P25 (OMIM 193300)長約10 bp的VHL腫瘤抑制基因突變所致。發生率約1/36 000,60歲之前,基因外顯率達95%[1]。臨床上常表現為視網膜及中樞神經系統的血管母細胞瘤、腎透明細胞癌、嗜鉻細胞瘤和胰腺腫瘤。盡管目前對該病分子生物學的認識以及手術時機的選擇有所進展,但VHL綜合征患者的平均生存年齡僅49歲[2]。該研究通過對3例臨床診斷VHL綜合征的患者及其家族內27例自愿者行vhl基因檢測,報道如下。
1 材料與方法
1.1 病例資料 安徽醫科大學第一附屬醫院2011 年1月~2013年12月有3例患者臨床診斷為VHL綜合征,3個家族共31例成員均自愿加入本項研究,簽署知情同意書,抽取每個家族成員外周血5 ml,于-80℃冰箱保存,并收集臨床資料。
1.2 實驗方法
1.2.1 DNA提取 用血液基因組DNA提取試劑盒Flexigene DNA kit(Qiagen,51204)提取外周血DNA,并以電泳檢測提取DNA純度,檢測條件為150 V、100 mA電脈20 min,見圖1。
1.2.2 聚合酶鏈式反應(polymerase chain reactions,PCR) 用Primer 5.0軟件設計引物,引物涵蓋VHL基因全部3個外顯子編碼區域,引物由上海生工生物工程技術有限公司合成,見表1。PCR將基因組DNA(100~200 ng)擴增,25 μl PCR反應體系包括:15.5 μl蒸餾水,5 μl 5×buffer緩沖液,1 μl脫氧核苷三磷酸(5 mmol/L),1 μl DNA模板,0.5 μl DNA聚合酶,40 mmol/L的上下游引物各1 μl。PCR反應擴增條件:外顯子1 95℃預變性10 min,95℃30 s,62℃30 s,72℃20 s,共35個循環,最終72℃下延伸10 min。外顯子2和外顯子3在60℃下行PCR擴增。1%瓊脂糖電泳,150 V、100 mA電泳20 min后使用紫外凝膠成像儀進行PCR結果檢測。
1.2.3 PCR反應純化及測序 PCR產物經AxyPrep-96 Kit純化后送生工測序。
1.2.4 測序結果分析 NCBI數據庫(http://www.ncbi.nlm.nih.gov/)中找到VHL基因,其包含3個外顯子共642個密碼子,編碼214個氨基酸(包含末端不翻譯氨基酸的3個終止密碼子),Multalin方法對測得DNA序列比對(http://multalin.toulouse.inra.fr/multalin/)。測得序列在http://web.expasy.org/translate/中將可能表達氨基酸翻譯,并與NCBI數據庫中進行比對。

表1 vhl基因外顯子片段大小和用于PCR擴增及測序的引物信息
1.3 臨床檢查方法 行VHL家族調查,并對家族內基因突變攜帶者行頭顱MRI、B超(肝、膽、胰、脾、腎、腎上腺及盆腔)、眼底、血尿常規及尿兒茶酚胺檢測。
2 結果
2.1 基因檢測結果 PCR產物瓊脂糖凝膠電泳結果顯示均獲得預期大小的擴增片段。3個家族31例健在成員均自愿接受基因分析,并繪制樹狀圖。結果包括先證者在內,家族1中5例成員vhl基因陽性,家族2中1例,家族3中7例。4例(1Ⅲ3、3Ⅲ1、3Ⅲ4、3Ⅳ3)家族成員確定為基因突變攜帶者,3個家族基因突變方式分別為:家族1外顯子1第330位堿基A替換為堿基C,導致vhl基因編碼的第110個氨基酸組胺酸變為脯氨酸。家族2外顯子3 第488位堿基C缺失,結果致vhl編碼的氨基酸162位以后全部紊亂。家族3外顯子1第233位堿基A轉換為堿基G,導致vhl基因編碼的第98個氨基酸天冬酰胺酸變為絲氨酸,見表2。
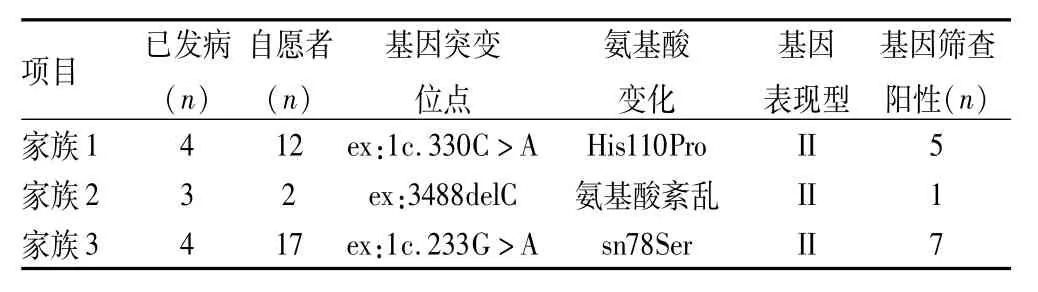
表2 3個家族基因突變位點、家系基因篩查結果以及VHL綜合征發病類型
2.2 臨床檢查
2.2.1 家族調查 家族1:先證者1Ⅱ1,男,48歲,
1991年因進行性的頭痛入安徽醫科大學第一附屬醫院行“小腦血管母細胞瘤切除”,術后恢復良好,至今無復發。患者2003年出現肉眼血尿,行“左腎透明細胞癌剜除術”,術后入安徽醫科大學第一附屬醫院泌尿外科二病區規范隨訪,2007年行“右腎透明細胞癌剜除術”,2012年行“左腰部轉移瘤切除+左側腎臟腫瘤射頻消融”,術后不久發現左側腰部腫塊復合,呈進行性增大,考慮腎透明細胞癌轉移,2014年1月行“左腰部腫瘤活檢+左腎腫瘤射頻消融術”,術后鏡檢于腰部脂肪組織見透明細胞腫瘤結節。患者1I1因多年頭痛,48歲去世。患者1 II3,47歲,10年前因頭暈發現腎上腺嗜鉻細胞瘤,雙腎多發囊腫,一直保守治療。2012年因雙腎囊腫于南京軍區總醫院行雙腎囊腫開窗引流術,治療效果不佳,囊腫無法完全根治,在患者診治期間,其女兒(1III6),23歲,醫生建議后體檢發現多囊肝,雙腎多發囊腫,至今尚無明顯臨床癥狀。先證者兒子(1III1),25歲,2年前因頭暈,行走不穩,入安徽醫科大學第一附屬醫院診斷小腦血管母細胞瘤,手術切除腫瘤,至今無復發。
家族2:先證者2II2,男,45歲,2013年12月因出現肉眼血尿半月余,安徽醫科大學第一附屬醫院診斷多發腎臟占位、肺部轉移可能、雙側腎上腺占位,失去治療時機,現腫瘤前列腺、骨多發轉移,于合肥市第五人民醫院保守對癥治療,一般狀況極差,見圖3A。患者2 I2,23歲體檢發現腎上腺占位、多發胰腺囊腫、多囊腎,并于上海市中山醫院行腎上腺嗜鉻細胞瘤切除術,胰腺囊腫未予處理。49歲出現血尿,診斷腎癌多發轉移,50歲去世。患者2II1,為先證者孿生哥哥,2011年因頭暈,行頭顱MRI見左側小腦半球囊性病變,于北京天壇醫院行小腦腫瘤切除術,術后證明為血管母細胞瘤。2013年因腎透明細胞癌多發轉移去世。
家族3:先證者3III2,女,27歲,2007年因行走不穩診斷小腦腫瘤,見圖3B。手術切除后2010年、2013年兩次復發,再次手術治療。先證者左眼視物不清7年,失明1年,一直未予診治,近期出現左眼脹痛,發作頻繁,經指導后檢查發現左眼眼底反光異常,正常紅光反射消失,網膜可見不規則滲出病灶,靜脈淤曲明顯,并見自視乳頭顳側生成粗大扭曲滋養血管,并見后極部增殖膜,遠端見瘤體,見圖3C。先證者父輩發病3例,患者3II1 58歲,2014年2月因肉眼血尿1 d于淮南市人民醫院就診,診斷雙腎多發腎癌晚期,失去治療時機,納入隨訪。患者3II2,1990年因頭暈行小腦腫瘤切除術,1993年腫瘤復發,再次手術切除,因術后出血死亡。患者3II5,15年前因頭痛、頭暈急性發作,入淮南市礦三院,診斷雙腎上腺嗜鉻細胞瘤、小腦腫瘤,治療期間顱內出血死亡。家族成員3III1平日偶感腹脹,癥狀可自行緩解,未予診治。
2.2.2 臨床檢查 對4例(1III3、3III1、3III4、3IV3)基因突變攜帶者進行頭顱MRI(3IV3年齡小于15歲未行MRI檢查)、B超(肝、膽、胰、脾、腎、腎上腺及盆腔)、眼底、血尿常規及尿兒茶酚胺檢測,其中3例(1III3、3III1、3III4)攜帶者檢查發現異常。1III3,21歲,腹部CT提示多發胰腺囊腫,見圖3D。3III1,33歲,平日偶感腹脹,未予重視,此次基因檢查突變陽性后行腹部CT發現胰腺及雙腎多發囊腫,見圖3E。3III4,22歲,基因檢測陽性情況下眼底檢查發現雙側眼底視網膜血管母細胞瘤,造影見瘤體及粗大扭曲的滋養血管,見圖3F。
3個家族共14例發病患者,男女發病比例4∶3,其中3例患者經基因篩查后臨床檢查證實已發病。14例發病患者首次出現癥狀的年齡為19~58(30.2±10.7)歲。病變部位包括中樞神經系統血管網狀細胞瘤6例、腎透明細胞癌5例、視網膜血管母細胞瘤2例、胰腺多發囊腫6例、腎臟多發囊腫8例,嗜鉻細胞瘤5例。中樞神經系統血管母細胞瘤患者除家系3中3II5未手術即死亡外,余患者共7次小腦腫瘤手術,腫瘤平均復發時間5.8年。5例腎透明細胞癌的患者,僅1例患者7年內連續行4次腎臟手術,腫瘤平均復發時間1.75年,余4例均因發現晚而延誤治療。3個家族共5例患者死亡,死亡率35.7%。2例死于中樞神經系統血管母細胞瘤,3例死于腎癌,平均死亡年齡33歲。
3 討論
VHL綜合征是常染色體顯性遺傳病,因vhl腫瘤抑癌基因突變所致,遺傳率50%,該抑癌基因包含3個外顯子,共轉錄213個氨基酸。外顯子2的表達(亞型I)或不表達(亞型II)導致基因轉錄為2種不同的剪接RNA。亞型I有2種轉錄結果:pVHL30和pVHL19,兩者在人體組織中均廣泛表達并扮演著控制轉錄伸展率的角色,二者統稱為pVHL。低氧誘導因子HIF1和HIF2是DNA結合轉錄因子,掌控基因轉錄激活促進細胞在低氧環境下適應及生長。pVHL可與elongin B、elongin C、cullin-2及Rbx1等其他蛋白結合形成復合物VCB-Cu12,
繼而作用于HIF1和HIF2ɑ亞基來調節泛素介導的蛋白降解。低氧的環境或pVHL喪失及活性下降時,HIF1和HIF2穩定并成為低氧反應的轉錄因子。這種低氧反應影響了葡萄糖的攝取和代謝,使血管生成,形成細胞外基質和細胞增殖,從而涉及VHL綜合征相關腫瘤的產生[3-6]。

表3 3個家族15例基因檢測陽性者臨床發病特點
張進等[7]完成了中國9個VHL家族的基因突變研究,其中錯義突變最多(7/9),突變的位置主要集中在第1外顯子的后1/3。有學者對中國各地共70個家族基因檢測結果進行總結,發現點突變80%,大片段缺失17.3%,18個突變位于外顯子1 (26個家族),7個突變位于外顯子2(7個家族),11個突變位于外顯子3(18個家族),1個突變位于外顯子2,1個突變位于3’-UTR。可見外顯子1和外顯子3為突變高發區域(51%)[8]。本組研究顯示第1、3家族均為點突變,家族突變位點均位于外顯子1后2/3,另1個家族外顯子3堿基C缺失。
臨床上VHL綜合征多采用Maher et al[2]提出的診斷標準:①有家族史,患中樞神經系統血管母細胞瘤或視網膜血管母細胞瘤、腎細胞癌、嗜鉻細胞瘤以及內囊淋巴瘤其中任一疾病,建立診斷。②無家族史,≥2種中樞神經系統血管母細胞瘤,或者有1種中樞神經系統血管母細胞瘤合并一處內臟病變建立診斷。本組3個先證者有明確家族史,已臨床診斷VHL綜合征。家族成員1Ⅲ3、3Ⅲ1、3Ⅲ4、3Ⅳ3,基因篩查陽性,臨床檢查表明3例家族成員已發病。前2例患者表現為胰腺和腎臟囊腫,可能為胰腺神經內分泌腫瘤及腎透明細胞癌的癌前病變,予之隨訪觀察。患者3Ⅲ4表現為視網膜血管母細胞瘤,為防止病灶逐漸擴大及相關并發癥影響視力,2014年7月在臨床指導下行激光治療。
研究[2]顯示,vhl基因型與臨床表現型存在相關性,基因錯義突變所編碼的蛋白常表現為嗜鉻細胞瘤。本組家族1因外顯子1第330位堿基A替換為
堿基C,發生錯義突變,家族3因外顯子1堿基A轉換為堿基G,導致錯義突變。但是同一家族之間可見發病的時間與病變累及部位不盡相同。如家族2,先證者與其孿生哥哥,都有腎臟病變及嗜鉻細胞瘤,但先證者未出現中樞神經系統血管母細胞瘤。
臨床調查表明VHL綜合征具有發病年齡輕、多呈隱匿發病、腫瘤易復發、死亡率高、患者生存時間短的特點。本組14例發病患者,首次出現癥狀的平均年齡為30.2歲,5例患者出現癥狀后無法手術治療。5例中樞神經系統血管母細胞瘤患者共7次小腦腫瘤手術,腫瘤平均復發時間5.8年。1例腎透明細胞癌患者7年內連續行4次腎臟手術,腫瘤平均復發時間1.75年。5例患者死亡,死亡率35.7%,平均死亡年齡33歲。
VHL綜合征表現為全身多系統病變,病變部分早期隱匿,臨床上難以早期診斷,導致患者治療效果不佳,死亡率高。該疾病在患者家族引起恐慌,基因檢測可明確診斷并篩選出基因突變攜帶者,消除家族成員恐慌情緒。對基因突變陽性成員進行臨床隨診,可以把握患者治療時機、提高治療效果、延長生存時間及提高生活質量。
參考文獻
[1] Maher E R,Iselius L,Yates J R,et al.von Hippel-Lindau disease:a geneticstudy[J].Med Genet,1991,28(7):443-7.
[2] Maher E R,Yates J R,Harries R,et al.Clinical features and natural history of von Hippel-Lindau disease[J].Q J Med,1990,77(283):1151-63.
[3] Richards F M,Phipps M E,Latif F,et al.Mapping the von Hippel-Lindaudisease tumour suppressor gene:identification ofgermline deletions by pulsed field gel electrophoresis[J].Hum Mol Genet,1993,2(7):879-82.
[4] McNeill A,Rattenberry E,Barber R,et al.Genotype-phenotype correlationsin VHL exon deletions[J].Am J Med Genet A,2009,149A(10):2147-51.
[5] Richards F M,Schofield P N,Fleming S,et al.Expression of the von Hippel-Lindau disease tumour suppressor gene during humanembryogenesis[J].Hum Mol Genet,1996,5(5):639-44.
[6] Kaelin W G Jr.The von Hippel-Lindau tumour suppressor protein:O2sensing and cancer[J],Nat Rev Cancer,2008,8(1):865-73.
[7] 張 進,黃翼然,潘家驊,等.中國人von Hippel-Lindau綜合征種系突變研究[J].中華醫學遺傳學雜志,2007,24(2):124-7.
[8] Wu P,Zhang N,Wang X,et al.Family history of von Hippel-Lindau disease was uncommon in Chinese patients:suggesting the higher frequency of de novo mutations in VHL gene in these patients[J].J Hum Genet,2012,57(4):238-43.
Mutation analysis and clinical investigation of three Chinese families with VHL disease
Wu Xinyao1,Chen Jiangming2,Zhao Yijun1,et al
(1Organ Transplantation Center,The First Affiliated Hospital of Anhui Medical University,Hefei 230022;2Dept of General Surgery,The Second Affiliated Hospital of Anhui Medical University,Hefei 230601)
AbstractObjective To detect the genetic mutations of vhl gene of three families who were diagnosed in clinical,and screen the carriers for clinical guiding treatment.Methods The vhl gene was screened for mutation using a direct DNA sequencing analysis for 31 members from three families.The genetic mutations carriers were required to undergo further clinical examination,surveillance and treatment.Results The genetic testing results were based on positive three probands.5 members of family 1 had positive genes,1 member in family 2,7 members in family 3.The position of three von Hippel-Lindau syndrome(VHL)families genes mutations sites was separately on c.330C>A in exon1,488delC in exon3 and c.233G>A in exon1.In DNA sequencing analysis,we found four potential carriers(1Ⅲ3,3Ⅲ1,3Ⅲ4,3Ⅳ3),and combined with clinical examination,three(1Ⅲ3,3Ⅲ1,3Ⅳ3)of them had disease.1Ⅲ3 was diagnosed with multi-cysts on kidney and pancreas,3Ⅲ1 was diagnosed with pancreatic multi-cysts.3Ⅲ4 was diagnosed with retinal hemangioblastoma.We had guided the member 3IV3 for eye surgery.3IV3 was not found with abnormal symptoms because of her young age.And all of the gene carriers should have the follow-up visit.Conclusion Genetic testing can diagnose VHL syndrome early.To improve patients'treatment,prolong survival and improve the quality of life,the patients with vhl gene mutations need follow-up closely.
Key wordsvon Hippel-Lindau syndrome;vhl gene;gene detection
作者簡介:吳鑫堯,男,碩士研究生;劉付寶,男,副教授,副主任醫師,碩士生導師,責任作者,E-mail:liufubao88@163.com
基金項目:安徽省自然科學基金(編號:1308085MH133)
文獻標志碼A
文章編號1000-1492(2015)05-0635-05
中圖分類號R 394.3

