菜籽油生物柴油化學動力學機理的構建
毛功平,王 忠,倪培永
(江蘇大學汽車與交通工程學院,江蘇 鎮江 212013)
生物柴油的組分非常復雜,如以大豆油和菜籽油為原料制備的生物柴油,含有油酸甲酯、亞油酸甲酯、棕櫚酸甲酯、硬脂酸甲酯、亞麻酸甲酯等組分,且主要組分的相對分子質量較大,分子的碳鏈長度較長,一般為碳鏈長度17~19的大型酯類,因而很難針對單一組分建立一種可以完全表達生物柴油化學動力學特性的模型[1-3]。
目前對于生物柴油化學動力學機理的研究主要有兩種方法:一是對與生物柴油主要組分結構類似的小分子甲酯(如甲酸甲酯、丁酸甲酯等)進行試驗和動力學的研究,研究它們的氧化性能;二是研究癸酸甲 酯 (Methyl Decanoate,MD)、硬 脂 酸 甲 酯(Methyl Stearate,MS)等大分子酯類的氧化機理,將其作為生物柴油的替代機理。國內外學者對生物柴油機理開展了研究,并取得了一定的成果。美國Cornell大學的Fisher等人[4]認為丁酸甲酯與生物柴油中的主要組分都含有代表烷基或者烯基),因而可用來替代生物柴油。Fisher在低溫低壓密閉容器中進行了丁酸甲酯的燃燒試驗,建立了包含279種組分和1 259個基元反應的丁酸甲酯機理,這是生物柴油替代機理的較早報道。法國國家科學研究院(CNRS)的Dagaut[5]等人采用射流反應器進行了不同壓力、溫度、時間和空燃比等條件下菜籽油甲酯的氧化試驗,以碳原子個數為2~6的烯烴作為菜籽油甲酯的替代物質,建立了菜籽油甲酯氧化的簡化模型,提出了由225種物質和1 841個基元反應組成的菜籽油甲酯氧化機理。美國勞倫斯·利弗摩爾國家實驗室(Lawrence Livermore National Laboratory,LLNL)的 Herbinet[6]等人將正庚烷、異辛烷和丁酸甲酯的機理組合在一起,建立了包含高溫和低溫反應部分的癸酸甲酯詳細化學動力學氧化模型。將發動機燃用癸酸甲酯、菜籽油甲酯在射流攪動反應器中反應的試驗數據與癸酸甲酯模型計算結果進行了對比,驗證了機理的有效性,發現癸酸甲酯機理模擬生物柴油燃燒的效果要優于丁酸甲酯。美國加利福尼亞大學的Seshadri[7]等人采用直接關系圖法(DRG,Directed Relation Graph)對3 036種物質、8 555個基元反應組成的詳細癸酸甲酯機理進行簡化,得到包含713個基元反應和125種組分的主干機理,通過對比模擬結果和試驗結果驗證了簡化機理的有效性。
1 替代物質的組成和比例的確定
采用酯交換法,以菜籽油為原料制備了生物柴油。采用6890GC氣-質譜聯用儀,測量了生物柴油的酯類組成。表1列出檢測結果。
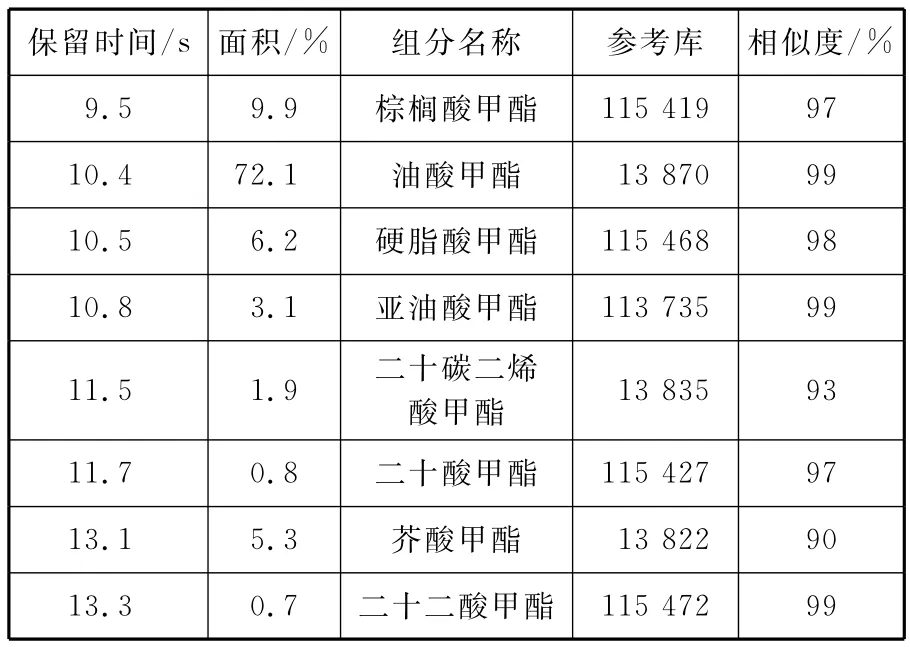
表1 生物柴油組分測量結果
根據測量結果中各組分所占比例,擬合得到生物柴油的分子式(C19H36O2),并計算出氧質量分數(10.8%)。
選取摩爾比為1∶2的MB和NH組成的混合燃料(記為MBNH)作為生物柴油的替代物質,表2列出3種燃料的理化特性。由表2可以看出,丁酸甲酯的熱值僅為生物柴油的75%左右,相對分子質量為35%左右,氧質量分數和化學式與生物柴油差別較大,不能完全體現生物柴油的燃燒特征。混合燃料MBNH與生物柴油的特性接近,且分子結構中包含了結構,是比MB更合適的生物柴油的替代物。
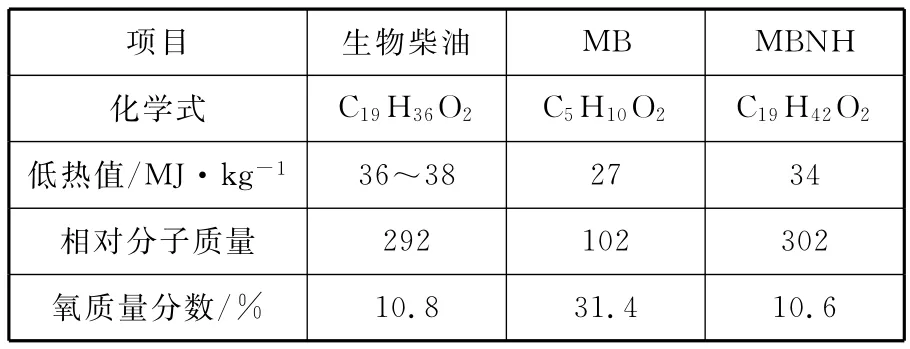
表2 生物柴油、MB、MBNH的理化特性
2 替代物質的化學動力學機理
構建多組分燃料機理的常用方法是將各燃料組分的機理“疊加”在一起,去掉重復的部分。采用類似的方法構建生物柴油的機理,得到包含356種物質、1 937個基元反應的生物柴油新機理。構建步驟如下:
1)將Fisher[2]提出的包含264種物質、1218個基元反應的丁酸甲酯機理,Patel[8]提出的包含29種物質和52個基元反應的正庚烷簡化機理疊加起來,得到組合機理。
2)對柴油機來說,熱力NOx途徑是主要途徑,快速NOx途徑也占一部分,生物柴油不含氮元素,故不考慮燃料NOx途徑。因此,在組合機理的基礎上,再加入熱力NO、快速NO、NO2的機理。添加的 NOx機理部分見表3[9]。
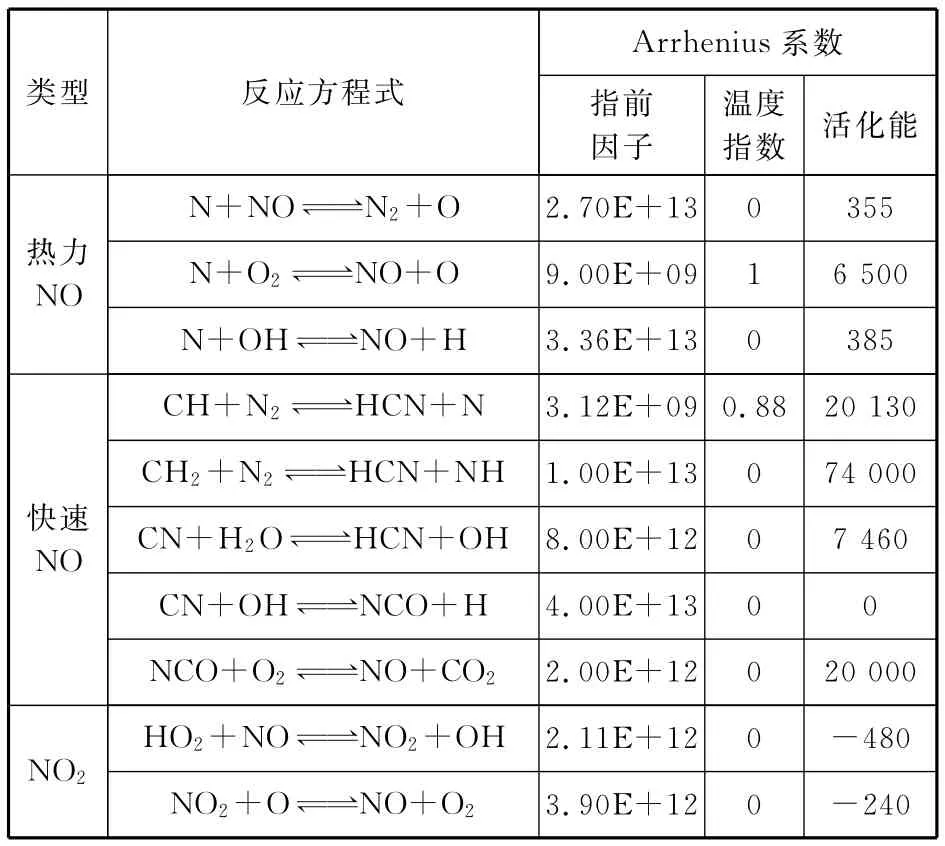
表3 NOx生成機理
3 新機理的修正
研究發現,“疊加法”構建的機理的特征時間尺度差別較大,微分方程的特征值差別明顯,特征矩陣的條件數很大,各基元反應的化學反應速率常數直接來自各組分的機理,必然帶來在“擬穩態假設”、“部分平衡假設”等基礎上得到的新機理對各燃料組分機理的偏離,形成了計算的“剛性”問題,導致計算精度降低[10]。因此,需要對新機理中基元反應的化學反應速率常數進行修正。
3.1 待修正基元反應的確定
采用Chemkin軟件中的均質零維反應器模型與構建的機理耦合,對基元反應進行敏感性分析,對全局敏感性較高的基元反應的化學反應速率常數進行修正。
以文獻[11]中的試驗條件為計算邊界條件,選定初始溫度為1 650K,壓力為3MPa。根據計算結果,篩選出對主要污染物生成敏感性較高的基元反應。參考的主要污染物有可揮發性有機化合物(VOC,Volatile Organic Compound),未燃碳氫化合物(UHC,Unburned Hydrocarbons),NO,CO2,NO2,CO。影響各污染物生成基元反應的敏感性系數見表4。
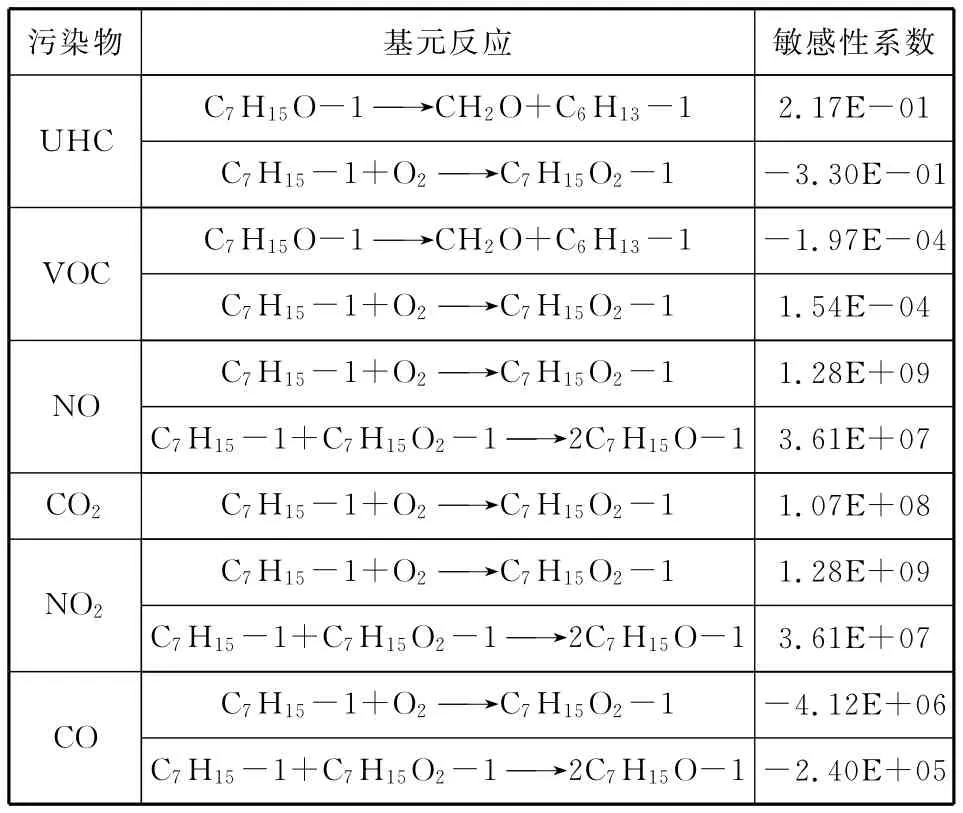
表4 敏感性較高的基元反應
根據表4中的結果,篩選出化學反應速率常數需要修正的基元反應(見表5),重點對這3個基元反應的化學反應速率常數進行優化。
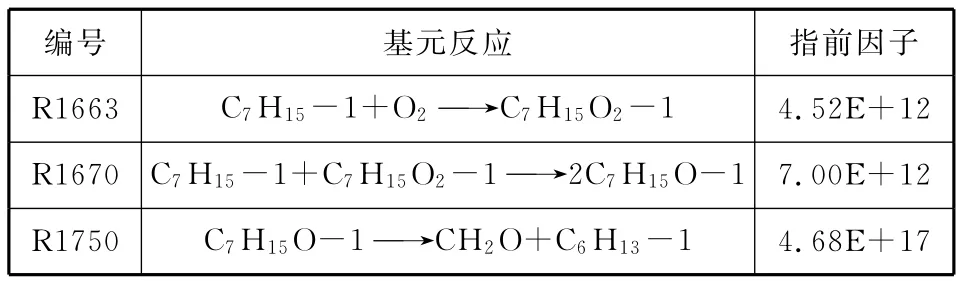
表5 需要修正的基元反應
3.2 化學反應速率常數的修正
通過調整化學反應速率常數中的指前因子對篩選出的基元反應的化學反應速率常數進行修正。采用對其施加擾動的方法,設定6種反應速率常數指前因子的變化范圍(見表6)。擾動變量V1~V2表示關于反應速率的指前因子的敏感性,V3~V6強調由于活化能不確定對溫度的影響。在溫度較低時,變量選擇與基準值接近,溫度升高后,變量在V4~V5間。
選取6種不同的指前因子變化量(見表7)。運用Chemkin軟件中的攪拌反應器模型,模擬不同擾動變量情況下CO2和C2H4的摩爾分數,與文獻[3]中的試驗數據進行對比分析。

表6 化學反應速率常數的變化范圍
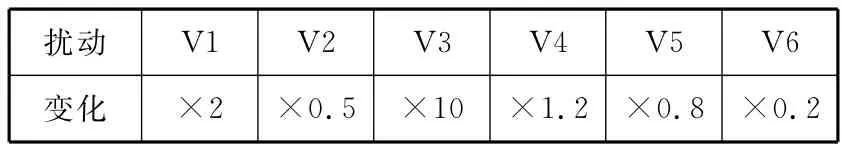
表7 指前因子的變化量
4 新機理的驗證與分析
4.1 驗證試驗數據
Dagaut在射流攪拌反應器中進行了菜籽油甲酯的燃燒試驗[5],采用其試驗數據進行機理驗證。反應器容積為30.5cm3,燃料的摩爾濃度為0.05%,燃料溫度保持在290℃,載氣氮氣的流速為100L/h。采用在線色譜-質譜聯用儀、熱傳導式探測器、火焰離子檢測器等設備測量了壓力為1~10MPa,反應時間分別為0.07s,0.1s,1s,當量比為0.25~1.5,溫度為800~1 400K 條件下,H2,O2,CO,CO2,CH4,C2H4,C3H6,C4H8等燃燒產物的摩爾分數。本研究選取壓力0.1MPa、反應時間0.07s、當量比0.25作為計算邊界條件。由于試驗結果中CO2和C2H4的摩爾分數較高,且這兩種物質涉及到C,H,O 3種主要元素,故通過比較CO2和C2H4摩爾分數的計算值和試驗值,驗證新機理的有效性。
4.2 計算結果與分析
圖1和圖2示出CO2和C2H4摩爾分數的試驗結果與計算結果的對比。EXP為文獻[5]中的試驗數據,V0為未修正機理的模擬結果;V1~V6分別表示對指前因子施加表7中的擾動后,運用新機理模擬得到的數據。由圖可以看出,對表5中基元反應化學速率常數的指前因子施加V4,V5擾動后,計算結果與試驗結果較為接近。
為了較方便地評價試驗與模擬結果的差異,引入“平均誤差”的概念,定義平均誤差Err為
式中:N為不同溫度對應的試驗數據總數;φVi為不同擾動下模擬得到的燃燒產物的摩爾分數;φV0為試驗測量得到的摩爾分數。
計算得到的CO2和C2H4摩爾分數和試驗值之間的平均誤差見圖3。
從圖3可以看出:對于CO2,V3和V6擾動下的平均誤差較大,分別為9.53×10-3和3.99×10-3,V4和V5擾動下的平均誤差較小,分別為0.62×10-3和0.91×10-3,未修正機理的計算平均誤差較大,為1.15×10-3;對于C2H4,平均誤差較大的 擾 動 為 V3 和 V6,分 別 為1.08×10-3和0.47×10-3,V4的平均誤差較小,為0.07×10-3,而未修正機理的計算平均誤差也較小,為0.09×10-3。可見,在 V4擾動下,CO2和C2H4的計算平均誤差均較小,與試驗結果較接近。
5 結論
a)根據氣質聯用儀測量的生物柴油酯類組成,得到生物柴油的擬合分子式為C19H36O2,丁酸甲酯和正庚烷按1∶2的比例組成的混合燃料在分子式、分子量、黏度等方面較丁酸甲酯與實際的生物柴油更為接近,可用來替代生物柴油;
b)對影響主要污染物生成的基元反應進行敏感性分析,篩選出編號為R1663,R1670,R1750的基元反應,修正其化學反應速率常數;
c)采用對待修正基元反應的化學反應速率常數指前因子施加不同大小的擾動的方法,模擬不同擾動下燃燒產物CO2和C2H4的摩爾分數,并與試驗結果對比,發現V4(指前因子略微增大)擾動下新機理的計算平均誤差較小。
[1] Chung K Law.Combustion at a crossroads:status and prospects[J].Proceedings of the Combustion Institute,2007,31:1-29.
[2] 毛功平,王 忠,許廣舉,等.內燃機燃料化學動力學機理的研究進展[J].車用發動機,2011(6):7-11.
[3] 裴毅強,鄭朝蕾,張 博.生物柴油替代混合物化學動力學模型構建及路徑分析[J].物理化學學報,2014,30(2):217-226.
[4] Fisher E M,Pitz W J,Curran H J,et al.Detailed chemical kinetic mechanisms for combustion of oxygenated fuels[J].Proceedings of the combustion institute,2000,28:1579-1586.
[5] Dagaut P,Gail S,Sahasrabudhe M.Rapeseed oil methyl ester oxidation over extended ranges of pressure,temperature,and equivalence ratio:Experimental and modeling kinetic study[J].Combustion and flame,2007,31:2955-2961.
[6] Herbinet O,Pitz W J,Westbrook C K.Detailed chemical kinetic oxidation mechanism for a biodiesel surrogate[J].Combustion and flame,2008,154:507-528.
[7] Seshadri K,Tianfeng Lu,Herbinet O,et al.Experimental and kinetic modeling study of extinction and ignition of methyl decanoate in laminar nonpremixed flows[J].Proceedings of the Combustion Institute,2009,32:1067-1074.
[8] Patel A,Kong S C,Reitz R D.Development and Validation of a Reduced Reaction Mechanism for Hcci Engine Simulations[C].SAE Paper 2004-01-0558.
[9] 毛功平,王 忠,許廣舉,等.生物柴油燃燒過程中氧、氮元素的遷移歷程分析[J].車用發動機,2011(4):37-42.
[10] 王彬彬,蔣 勇,邱 榕.CSP分析方法在簡化燃燒化學反應系統中的應用[J].物理化學學報,2008,24(12):2221-2228.
[11] 袁銀南,張 恬,梅德清,等.柴油機燃用生物柴油燃燒與排放[J].江蘇大學學報:自然科學版,2006,27(3):216-219.

