多層螺旋CT血管成像在乳腺癌手術計劃中的臨床應用研究
范惠文 史訊 時坤 邱鋁 穆向明
乳腺癌是女性最常見的惡性腫瘤之一,近年來,其發病率呈上升趨勢且逐漸趨于年輕化。目前乳腺癌最有效的治療手段仍然是手術切除[1-2],但還是有少數乳腺癌患者就診時,由于腋靜脈受侵,導致術中不易分離而放棄手術切除。近年來隨著血管吻合技術及人工血管的應用,可實施受侵腋靜脈切除后的端端吻合或人工血管置換,從而為手術徹底切除掃清了障礙。但實際工作中常發現,由于乳腺、腋窩毗鄰關系相對復雜,術前判斷腋血管有無浸潤及其受侵程度存在困難,而影像學檢查中多層螺旋CT(MSCT)憑借其短時間、薄層面、大范圍的數據采集優勢,重建后圖像可達到各向同性,可精細顯示大血管及主要分支,其CT血管成像(CTA)技術更是成為術前評估癌腫侵犯大血管的最重要手段之一[3-4]。本研究目的在于初步探討MSCT腋血管成像在乳腺癌手術計劃中的臨床應用價值。
1 資料與方法
1.1 一般資料 搜集本院2011年4月-2013年3月經術前MSCT檢查、術后病理確診的乳腺癌患者共51例,均為女性,年齡27~75歲,平均57.2歲。原發病灶直徑0.8~5.1 cm,平均2.3 cm。患乳為右側22例,左側29例;病灶位于外上象限27例,其中包括副乳腺癌2例,內上象限10例,外下象限3例,內下象限2例,中央區5例,病灶分布于兩個或兩個以上象限4例。病理診斷:導管內癌5例,浸潤性導管癌39例,浸潤性小葉癌7例。TNM分期:Ⅰ期7例,Ⅱa期17例,Ⅱb期11例,Ⅲa期10例,Ⅲb期4例,Ⅳ期2例。并對其中42例患者進行電話及書信隨訪,隨訪截至日期為2012年3月。
1.2 方法 采用Siemens 128層螺旋CT機(Siemens Definition AS,Germany),配備工作站Leonardo(Siemems Medical Solutions)。檢查包括平掃與增強,所有患者均采用仰臥位,目的是與手術體位基本一致,易于病灶術前準確定位。對比劑選用碘海醇,濃度為300 mg I/mL,對比劑總量為100 mL,速率為3.0 mL/s,分別延遲30~35 s及180 s螺旋掃描。平掃掃描范圍同常規肺部,增強掃描范圍上界包括腋窩,下界達乳房下緣。掃描參數為:準直器寬度0.75 mm,重建層厚6 mm,管電壓為120 kV,管電流165 mAs,pitch 3~6。將原始圖像數據傳至工作站后按層厚0.75 mm,層距0.5 mm行薄層重建。血管成像方法采用多平面重建(multiplanar reformation,MPR)、容積成像(volume rendering,VR)、表面遮蓋重建(surface shaded display,SSD)、最大密度投影(maximum intensity projection,MIP)。
當前,CT在評判腋血管受侵方面報道甚少,筆者目前主要參考了研究較為成熟的胰腺癌侵犯胰周大血管的CT評判標準[5],初定:CTA圖像中顯示病灶包繞腋靜脈>1/2管徑時,判斷血管受侵。圖像評價均由兩位副高及以上職稱影像診斷醫師以盲法閱片,評價內容為腋靜脈有無侵犯及其程度。所有手術均由從事普外科工作15年且從事乳腺外科5年以上的2名醫生主持,術中均由術者仔細探查并分離腋血管,遇到判斷血管是否受侵及能否切除,是否切除后行端端吻合或人工血管置換,則由兩位醫生商量決定。
2 結果
MPR圖像(圖1)除清楚顯示51例患者病灶的大小、形態、邊緣、密度以及鄰近乳頭、乳暈皮膚、乳腺后間隙等之外,還可清晰顯示病灶及與鄰近組織結構的關系,且CT所見與手術所見相符合。此外,MPR對乳腺癌的沙礫狀鈣化及囊變的顯示尤為明顯,同時還可顯示肺部及縱隔情況,4例乳腺癌可見肺部多發轉移,2例見胸椎、肋骨轉移。
VR圖像(圖2)能夠更直觀顯示病灶的位置、形態及與周圍組織的關系。調節閾值可選擇性去除乳腺組織后的胸部組織,分層次顯示乳腺病灶、腋部淋巴結,特別對病灶內鈣化灶易于觀察,本組中有9例可見砂礫樣、不定形鈣化。
SSD圖像能多角度較好地顯示病灶形態及腋窩淋巴結的情況,立體感、直觀性強。本組中有33例在SSD圖像上可見大小不一淋巴結顯影。
MIP(圖3)、VR(圖2)圖像能較好顯示腋動、靜脈以及胸肩峰動、靜脈和胸外側動、靜脈及其主要分支。18例CT診斷腋窩淋巴結有轉移乳腺癌患者均見病灶圍繞腋靜脈、胸外側動、靜脈周圍分布,2例副乳腺癌病灶均與腋靜脈分界不清。
CTA圖像中顯示病灶包繞腋靜脈>1/2管徑為標準,術前CT判斷有16例腋靜脈受累,其中14例系腋窩轉移淋巴結累及腋靜脈,2例副乳腺癌病灶直接侵犯腋靜脈,CTA顯示32條腋靜脈中,CT診斷腋靜脈受累陽性計數25條,手術證實26條。以手術結果為標準,MSCT判斷腋靜脈受侵情況見表1,準確性、靈敏性、特異性分別為90.6%、92.3%、83.3%,陽性預測值、陰性預測值分別為96.0%、71.4%。
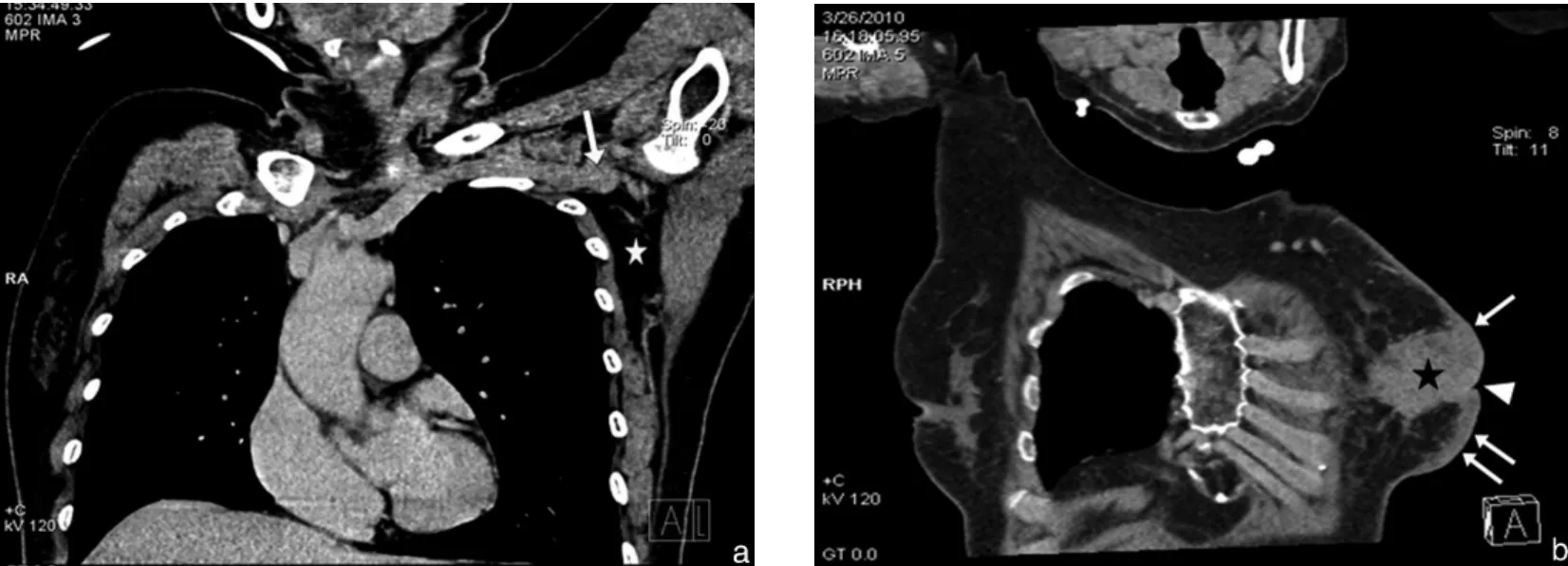
圖1 多層面重建圖像(MPR)
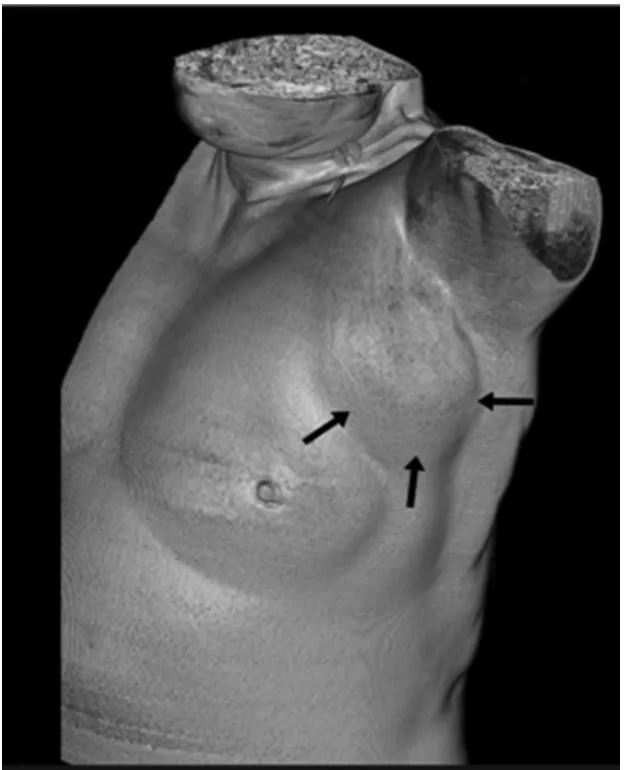
圖2 容積重建(VR)圖像

圖3 MIP圖像
乳腺癌腋靜脈侵犯的手術探查標準為:手術暴露所見或觸診發現血管被腫瘤侵犯包繞或阻塞等,為不能分離。若僅發現血管與腫瘤粘連尚可分離,則不屬于血管受侵。16例均常規行乳腺癌根治術,行腋窩淋巴結清掃及受侵腋靜脈切除,其中6例腋靜脈受侵長度小于2.0 cm行腋靜脈端端吻合術,8例超過2.0 cm者采用聚四氟乙烯(PIFE)人工血管移植進行腋靜脈重建。4例血管端端吻合、5例人工血管移植術后患側上肢輕度水腫,后均逐漸消退,3例行人工血管移植,術后未出現患側上肢水腫。術后1個月,每周彩超檢查未見腋靜脈及移植人工血管內血栓形成,術后1個月后予化療。術后隨訪4~12個月,腋靜脈及移植血管血流通暢,未見血栓。

表1 18例乳腺癌腋窩淋巴結轉移患者CT判斷腋靜脈受累與手術結果比較 條
3 討論
MSCT憑借其自身優勢[6-8],術前評判乳腺癌有無腋靜脈侵犯及其程度對制定合理的治療方案、選擇適當的手術術式有重要意義。
3.1 CTA對腋靜脈受侵的評判 淋巴轉移是乳腺癌最常見的轉移途徑,腋窩淋巴結則是乳腺癌最為好發轉移的第一站淋巴[9],解剖學上,腋窩淋巴結多位于腋靜脈及其分支周圍,當其發生轉移時,腋靜脈管壁常被侵犯,本組病例CTA重建證實,腫大的腋窩淋巴結多圍繞腋動靜脈、胸外側靜脈分布,增多、增大的淋巴結可將腋靜脈、胸外側靜脈包繞,使患側靜脈回流障礙,導致患側上肢、胸壁皮膚水腫,增強檢查發現患側血管變細、增強延遲。以往認為,當腫大的轉移性淋巴結已侵犯腋靜脈壁時,術中常不易分離,故不能強行剝離,以免造成血管損傷,可在術后行放療來彌補。但近年來隨著乳腺癌術式不斷改進,特別是血管再造技術的逐漸成熟,現在一定范圍內血管受侵仍可實施受侵血管切除及重建,達到手術徹底切除的目的,因此,對該類手術而言,評估腋靜脈受侵是術前準備之關鍵。
當前由于各研究單位采用的MSCT檢查技術及評判標準的不同,使得文獻報道CT診斷癌腫侵犯周圍大血管敏感性和特異性存在差異,而有關MSCT在評判腋靜脈受侵方面報道甚少。本研究目前主要參考了研究較為成熟的胰腺癌侵犯胰周大血管的CT標準[10-11],并結合筆者研究的初步結果后認為:當病灶組織包繞腋靜脈>1/2管徑時,判為血管受侵的結果較為滿意,其準確性、靈敏性、特異性分別達到90.6%、92.3%、83.3%,陽性預測值、陰性預測值分別為96.0%、71.4%。因此,CTA圖像在術前評判乳腺癌累及腋靜脈情況方面有具有較高的臨床價值。研究中還發現,CTA重建圖像并不能體現出橫斷面圖像上顯示的血管受累情況,因此,筆者認為,在實際工作中應將重建圖像與原始橫斷面像相結合來減小這種誤差。
3.2 CTA各種后處理技術的優缺點 CTA常用的重建方法包括:二維MPR、三維VR、SSD及MIP[12]。本組研究顯示,由于MPR具有較高組織分辨率,因此對乳腺癌的形態、邊界及受累周邊結構的顯示較好,對癌灶內的沙礫狀鈣化及囊變的顯示尤為明顯,對乳腺癌的診斷起到非常重要的作用(圖1);此外,MPR還可顯示肺部、縱隔、胸骨、肋骨等有無轉移,有助于術前腫瘤分期的判定。但由于MPR是二維重建方法,空間分辨率較差,對于腋靜脈等大血管的全景顯示不如三維的MIP、VR、SSD重建。VR重建有投影功能,經過不同的閾值選擇可以將乳腺本身及腋窩的病灶投影在體表上,可多方位明確腫瘤瘤供血管、腋窩淋巴結與腋靜脈間的關系(圖2),為術前定位、評估提供直接的影像依據。但筆者也發現,VR在顯示病灶的內部結構及皮膚、Cooper韌帶、基底膜、胸大肌侵犯等方面不如其他重建方法。
SSD可以立體感、直觀地顯示腫瘤形態、腫瘤血管與淋巴結轉移[12],但需要選擇合適的閾值以顯示腫瘤、腫瘤血管及淋巴結。其缺點是有時候由于圖像上結構有重疊而需要進行手動切割,人為操作的失誤時則會產生假象。
MIP重建是在薄層基礎上根據需要擴大空間分辨率進行,重建方法簡單易行,能充分顯示腫瘤血管數量、走行,對于外科手術提供了非常有用的信息(圖3);對于乳腺癌破壞正常結構所顯示的結構扭曲及星芒狀改變顯示較清晰,有利于對乳腺癌的診斷。其缺點是不能對深度關系進行編碼,立體感較差。比較而言,三維重建較二維重建在顯示血管和腫瘤關系方面更具優勢,相比較MIP、SSD而言,VR能提供更豐富的信息,且通過調節窗寬、窗位可顯示掃描腫塊內不同密度的組織結構,并能多方位明確腫瘤與血管間的關系。因此實際工作中,筆者認為重建應以VR成像為主,MPR、MIP圖像為補充。
總之,乳腺癌易發生癌腫和/或轉移淋巴結浸潤腋靜脈,術前CTA檢查能立體再現病灶、評判腋窩淋巴結、腋靜脈,便于手術醫師確定手術路徑、制定手術計劃,并在術中對照定位,明顯提高了手術的成功率[11,13],是一種非常重要的術前評估手段,但目前CTA成像檢查中,仍存在碘劑過敏、檢查價格較昂貴及CT輻射劑量大等缺陷,有待乳腺外科、影像科醫師經驗的不斷積累來克服。
[1]Cheville A.Prevention of lymphoedema after axillary surgery for breast cancer[J].BMJ,2010,340(15):b5235.
[2]Yip C H,Taib N A,Tan G H,et al.Predictors of axillary lymph node metastases in breast cancer:is there a role for minimal axillary surgery?[J].World J Surg,2009,33(1):54-57.
[3]苗華棟,深津博.多排螺旋CT在乳腺癌術前評估中的應用[J].中國醫學計算機成像雜志,2007,13(5):343-347.
[4]朱明霞,羅天友,歐陽羽,等.64層螺旋CT后處理技術對乳腺病變的顯示及診斷價值[J].臨床放射學雜志,2007,26(6):561-565.
[5]Nakayama Y,Yamashita Y,Kadota M,et al.Vascular encasement by pancreatic cancer:correlation of CT findings with surgical and pathologic results[J].J Comput Assist Tomogr,2001,25(3):337-342.
[6]Kang D K,Kim E J,Kim H S,et al.Correlation of whole-breast vascularity with ipsilateral breast cancers using contrast-enhanced MDCT[J].AJR Am J Roentgenol,2008,190(2):496-504.
[7]Perrone A,Lo M L,Sassi S,et al.MDCT of the breast[J].AJR Am J Roentgenol,2008,190(6):1644-1651.
[8]Tozaki M.Diagnosis of breast cancer:MDCT versus MRI[J].Breast Cancer,2008,15(3):205-211.
[9]Uematsu T,Sano M,Homma K,et al.Value of Three-Dimensional Helical CT Image-Guided Planning for Made-to-Order Lumpectomy in Breast Cancer Patients[J].Breast J,2004,10(1):33-37.
[10]Nakayama Y,Yamashita Y,Kadota M,et al.Vascular encasement by pancreatic cancer:correlation of CT findings with surgical and pathologic results[J].J Comput Assist Tomogr,2001,25(3):337-342.
[11]Shien T,Akashi-Tanaka S,Yoshida M,et al.Usefulness of preoperative multidetector-row computed tomography in evaluating the extent of invasive lobular carcinoma in patients with or without neoadjuvant chemotherapy[J].Breast Cancer,2009,16(1):30-36.
[12]Baek S Y,Sheafor D H,Keogan M T,et al.Two-dimensional multiplanar and three-dimensional volume-rendered vascular CT in pancreatic carcinoma:interobserver agreement and comparison with standard helical techniques[J].AJR Am J Roentgenol,2001,176(6):1467-1473.
[13]Tozaki M.Diagnosis of breast cancer:MDCT versus MRI[J].Breast Cancer,2008,15(3):205-211.

