光、溫限制后銅綠微囊藻和斜生柵藻的超補償生長與競爭效應
謝曉玲, 周 蓉, 鄧自發
(南通大學生命科學學院, 南通 226007)
光、溫限制后銅綠微囊藻和斜生柵藻的超補償生長與競爭效應
謝曉玲, 周 蓉, 鄧自發*
(南通大學生命科學學院, 南通 226007)
研究了銅綠微囊藻(Microcystisaeruginosa)和斜生柵藻(Scenedesmusobliquus)低溫和低光照限制后的超補償效應,以及共培養條件下的競爭效應。結果表明,低溫和低光照均顯著抑制微藻的生長發育,但低溫對銅綠微囊藻的抑制效應更強,而斜生柵藻則對低光脅迫更敏感。經過低光和低溫培養后,銅綠微囊藻和斜生柵藻在恢復正常培養時藻細胞密度短期內都表現出超補償增長效應, 但不同藻類超補償模式不同,斜生柵藻補償生長時間不超過1周,而銅綠微囊藻的補償效應可以持續10天;此外,統計結果表明銅綠微囊藻細胞密度對低溫限制解除表現出更顯著的補償生長,斜生柵藻則在低光解除后表現出更強的超補償效應。微藻葉綠素a指標在光恢復條件下都表現出顯著的補償效應,但溫度恢復過程中葉綠素a含量與藻密度增長不同步,低溫脅迫對恢復正常培養后微藻葉綠素a的形成產生了一定的負效應;銅綠微囊藻產毒株(912) 在兩種恢復模式下脫氫酶活性顯著高于對照,產毒株(912)脫氫酶活性的補償響應明顯高于其它兩種材料。共培養實驗結果表明斜生柵藻同銅綠微囊藻產毒株(912)相比處于競爭劣勢,而在同無毒株(469)的共培實驗中,盡管連續正常培養情況下兩者競爭能力差異不顯著,但在恢復培養條件下斜生柵藻競爭能力顯著高于后者。因此產毒型銅綠微囊藻低溫和低光后的補償生長效應以及對斜生柵藻的競爭優勢可能是藍藻爆發的內源性機制之一。
銅綠微囊藻(Microcystisaeruginosa);斜生柵藻(Scenedesmusobliquus);超補償效應;競爭效應;藍藻爆發
藍藻爆發是包括海洋在內所有水體最嚴重的環境問題之一,爆發后果不僅影響生態系統本身的結構和功能,更為重要的是它將嚴重威脅區域環境質量和水安全,因此有關藍藻爆發的機制及控制等方面的研究長期以來都是水體生態學關注的熱點之一[1- 4]。眾所周知,水體富營養化是導致藍藻爆發的主要原因,然而多項研究指出藍藻爆發與氣候因素存在著密切關系,當營養物質足夠維持藍藻水華的形成時氣候因素將是導致藍藻水華事件的關鍵[5- 6]。有研究表明溫度與光照等氣候因子對太湖藍藻群落種類組成的影響大于營養鹽[7],其中溫度可能是驅動溫帶和亞熱帶湖泊藻類群落更替的主要因子[8]。在全球氣候變暖的大背景下藍藻爆發頻繁更受到溫度等氣候變量短期變化影響[9- 10]。
溫度和光照是影響水生微藻的重要環境變量,而低溫和低光照是其常常遇到的脅迫因素,不同藻類對這些脅迫具有不同的耐受性[11- 12],并表現出不同生長策略[13]。研究發現一些微藻在遭受低光照等脅迫時生長速度和活力顯著降低,但在脅迫解除后藻細胞密度都表現出超補償生長響應[14- 17]。銅綠微囊藻(Microcystisaeruginosa)是引起藍藻水華的最重要藻種,盡管已有大量研究證明光照和溫度顯著影響其種群生長和發育[5,18- 20],但有關低溫和低光照脅迫后的補償生長及其對種群競爭力的影響研究少有報道,而這有可能是藍藻爆發的重要內源性因素。
本項研究通過比較不同株系銅綠微囊藻以及斜生柵藻(Scenedesmusobliquus)在光溫脅迫后的生長過程,探究其是否存在超補償響應,同時采用共培養實驗評估這一過程對其種群競爭力的影響,從而解析藍藻復蘇和爆發機制,并為有效控制水華提供理論依據。
1 材料與方法
1.1 實驗材料
本實驗所用銅綠微囊藻(Microcystisaeruginosa)產毒株系912和無毒株系469,以及斜生柵藻(Scenedesmusobliquus)均購自中國科學院武漢水生生物研究所淡水藻種庫。
1.2 實驗方法
1.2.1 藻類的培養
實驗選用BG- 11培養基培養[21]。所有培養基和所用器皿均于121℃在高壓蒸汽滅菌鍋滅菌15min。實驗前將銅綠微囊藻和斜生柵藻進行擴大培養。預處理實驗設3個組,低光組,低溫組和正常對照組;補償實驗設3組:低光組光恢復、低溫組溫度恢復,正常對照組,同時分為3種藻種獨立恢復培養與共培養(競爭實驗)兩種模式(912+斜生柵藻;469+斜生柵藻), 具體實驗條件見表1。光暗比為12 h∶12 h,恒溫培養箱靜置培養,每天定時人工搖瓶3次。每一實驗組合4個重復。
1.2.2 藻細胞密度的測定
自接種之日起每隔72h取樣,用血球計數板在顯微鏡下分別記錄銅綠微囊藻和斜生柵藻細胞密度,取樣前充分搖動培養瓶使培養液均勻,從而保證取樣代表性,每次每瓶鏡檢3張計數板。前期預處理起始接種密度分別為5.4×105個/mL(912)、5.5×105個/mL(469)和6.3×105個/mL(斜生柵藻);恢復培養與競爭實驗起始接種密度分別為4.6×105個/mL(912)、4.7×105個/mL(469)和5.6×105個/mL(斜生柵藻),保證各培養瓶中起始藻密度基本一致。
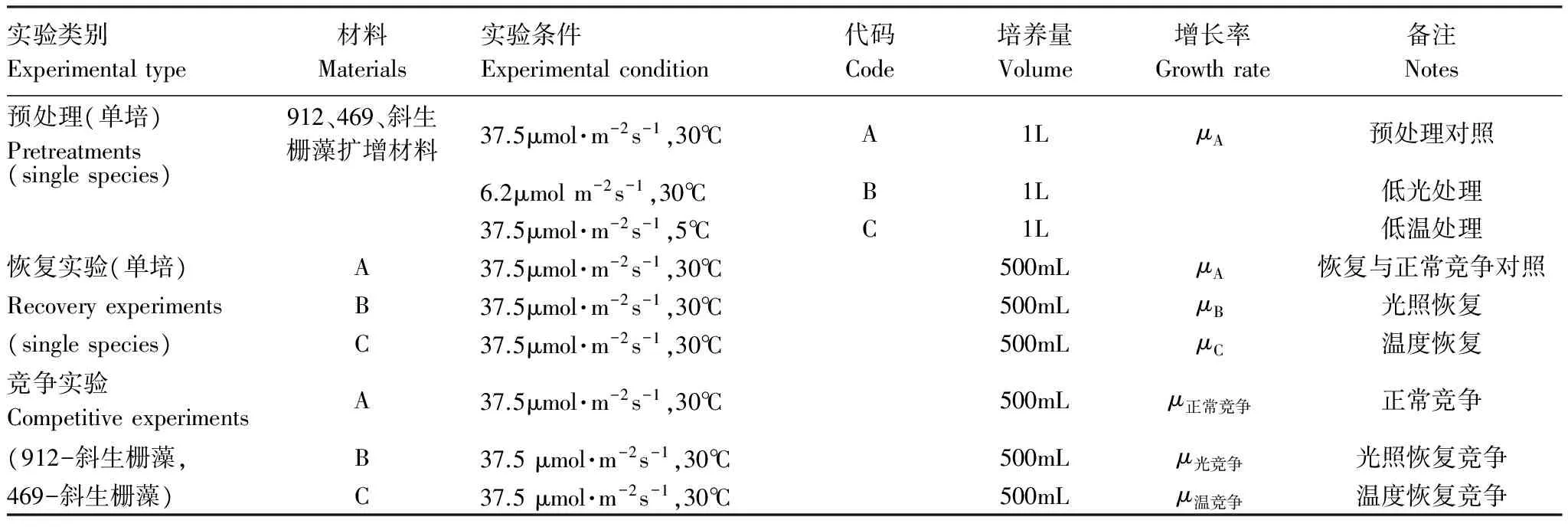
表1 實驗設計表
在不同時段統計的藻密度數據基礎上,計算不同處理藻細胞比增長率(μ):
μ=ln(xn-xn-1)/(tn-tn-1)
式中,xn為本計數期的細胞密度(個/mL);xn-1為前一計數期的細胞密度(個/mL);tn為對應于xn的培養天數;tn-1為對應于xn-1的培養天數,具體計算以3d為時間周期。
1.2.3 補償效應和競爭效應的量化分析
根據補償指數[22]和競爭指數[23]的計算原理,以未經預處理的不同藻種單獨正常培養時藻細胞最大比增長率(μA)為基準,分別按照以下公式計算光照和溫度恢復培養處理的補償效應與正常競爭時的競爭效應:
補償效應光=(μ恢復B-μA)/μA×100%
補償效應溫=(μ恢復C-μA)/μA×100%
競爭效應正常競爭=(μ競爭競爭-μA)/μA×100%
以單獨培養的恢復實驗時藻細胞最大比增長率(μB和μC)為基準,按照以下公式計算光照和溫度恢復時的競爭效應,
競爭效應光恢復=(μ光競爭-μB)/μB×100%
競爭效應溫恢復=(μ溫競爭-μC)/μC×100%
式中,μA,μB和μC具體含義見表1。
1.2.4 光合色素含量和脫氫酶活性測定
銅綠微囊藻為藍藻,沒有葉綠素b,所以每次取樣50mL混合均勻的藻液抽濾并參照文獻測定不同培養條件下葉綠素a含量[14], 3次重復; 采用TTC(2,3,5-氯化三苯基四氮唑)-脫氫酶還原法測定藻細胞活性: 取混合均勻藻液50mL離心、棄上清夜, 在三(羥甲基)氨基甲烷鹽酸鹽(Tris-HCl)緩沖溶液、pH=8.4的反應環境中,加入lmL0.8%的TTC溶液,水浴溫度(32±1)℃、發色培養1h,使用雙組分萃取劑4mL丙酮和5mL石油醚的混合溶劑進行萃取;同時設置對照;3次重復;用紫外分光光度計(UV- 1200)測定[21]。
1.3 數據處理與統計分析
數據統計分析應用SPSS 18.0軟件:在多因素方差分析的基礎上,藻細胞密度采用t檢驗分析不同處理與對照間,以及不同處理間差異顯著性,同時應用Mann-Whitney U-test對各密度變化曲線進行差異性檢驗,并根據差異性的顯著程度評估敏感性;以單獨正常培養未經預處理的藻種生長數據為對照,計算恢復培養的補償效應和共培時正常競爭效應,以恢復實驗的單獨培養數據為對照計算恢復期共培養處理競爭效應,并進行統計分析; 用單因素方差分析(One-way ANOVA)比較不同培養條件下葉綠素a含量與脫氫酶活性,當差異顯著時(P<0.05),進一步應用Duncan多重比較檢驗處理之間的差異性。同時以藻細胞密度為協變量進行協方差分析,從而檢驗不同培養條件下單個藻細胞相關指標的差異性。繪圖應用Origin 8.5。
2 結果與分析
2.1 低光照和低溫對不同藻種生長的影響
實驗結果表明,同正常培養相比低光照和低溫脅迫顯著影響銅綠微囊藻和斜生柵藻的正常生長發育。在不同培養條件下銅綠微囊藻兩個株系和斜生柵藻表現出類似的生長曲線,12d后密度增加幅度顯著降低,逐漸呈水平趨勢(圖1),期間正常培養條件下的藻密度增加了約25倍,而低光照和低溫條件下藻密度僅增加了1倍。同樣正常培養體系藻細胞比增長速率顯著高于兩種逆境處理體系中的。此外,統計分析結果表明銅綠微囊藻和斜生柵藻對這兩種脅迫因素的響應也表現出一定的差異:通過對密度變化曲線各時間點藻密度的顯著性檢驗,發現與斜生柵藻相比,銅綠微囊藻在低溫條件下表現出更強的抑制效應,而斜生柵藻則對低光更敏感(圖1)(Mann-Whitney U-test,P<0.05)。

圖1 低光照和低溫對銅綠微囊藻和斜生柵藻生長的影響(均值±標準誤,n=4)Fig.1 The effects of lower illumination and temperature on the growth of M. aeruginosa and S. obliquus (Mean±S.E, n=4)912: 銅綠微囊藻產毒株系912; 469:銅綠微囊藻無毒株系469;
2.2 不同藻株藻細胞密度對光照和溫度的補償效應
從圖2可以看出,同正常培養的藻株相比,經過低光和低溫培養的銅綠微囊藻和斜生柵藻細胞密度在恢復正常培養條件時都表現出一定的超補償效應,但不同藻類呈現出不同的超補償模式。兩株銅綠微囊藻在培養的前10d都呈現一定超補償生長,細胞密度顯著高于對照(One-way ANOVA ,P<0.05),但隨著培養時間的延長這種補償生長逐漸消失,第12天時不同處理的藻株基本達到相同的密度;無毒株系469低光和低溫解除后較產毒株912的超補償效應更顯著 (圖2)(P<0.05)。與銅綠微囊藻相比,斜生柵藻低光和低溫解除后正常培養的超補償效應僅在培養的前7天表現出來,到第8天連續正常培養的藻株密度已經接近光恢復培養材料的藻株,統計結果表明補償效應持續時間顯著短于銅綠微囊藻的(圖2)。同樣,從圖3中可以看出,實驗初期恢復培養材料的比增長速率顯著高于對照。此外,不同藻類對低光和低溫后的超補償敏感性存在一定的差異性,銅綠微囊藻對低溫限制解除表現出更高的敏感性,而斜生柵藻則在低光解除后表現出更強的超補償效應(P<0.05)。
2.3 不同條件下銅綠微囊藻與斜生柵藻的競爭效應
斜生柵藻分別與產毒(912)和不產毒的銅綠微囊藻(469)共培養實驗結果表明,與單獨培養相比,共培養體系中無論銅綠微囊藻還是斜生柵藻的藻細胞比增長速率μ和最大密度都顯著降低(P<0.05)(圖3,圖4)。比較3種共培養模式的結果可以看出,經過低光或低溫預處理的藻種在恢復正常培養過程中藻細胞密度都較連續正常培養樣品的高。從斜生柵藻與兩種不同株系的銅綠微囊藻的競爭關系分析,在斜生柵藻與無毒株(469)的共培養體系中藻細胞密度顯著高于其同有毒株(912)共培養中的密度,產毒株912產生的微囊藻毒素可能對共培養的斜生柵藻產生了一定的競爭性抑制(圖4)。
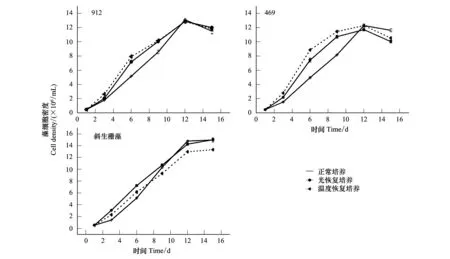
圖2 銅綠微囊藻和斜生柵藻光和溫度恢復下的補償生長(均值±標準誤,n=4)Fig.2 Overcompensation ofM. aeruginosa and S. obliquus experienced low light and temperature stress (Mean±S.E, n=4)
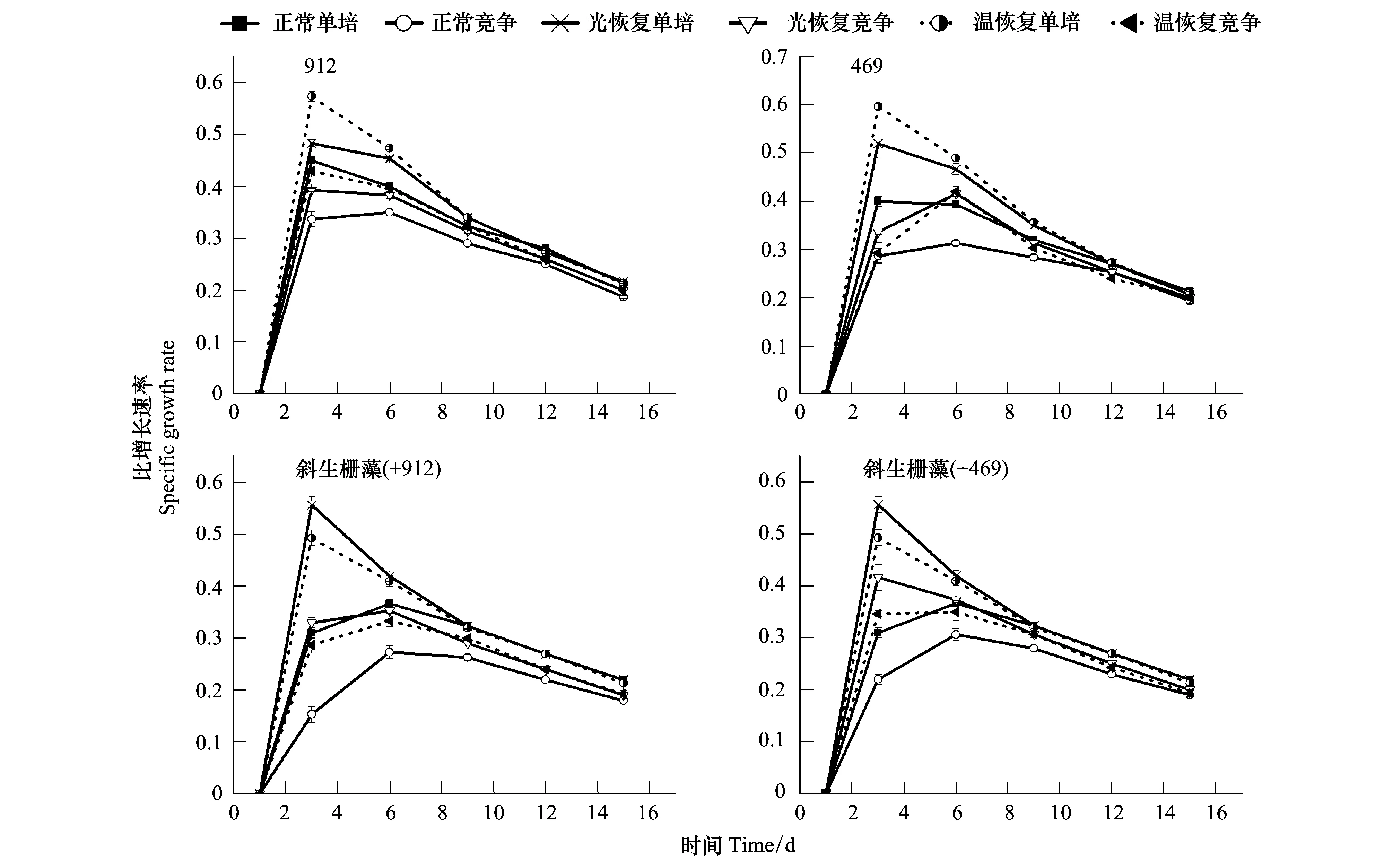
圖3 不同條件下銅綠微囊藻與斜生柵藻的藻密度比增長率 (均值±標準誤,n=4)Fig.3 Thespecific growth rate of Microcystis aeruginosa and Scenedesmus obliquus under different culture conditions (Mean±S.E, n=4)
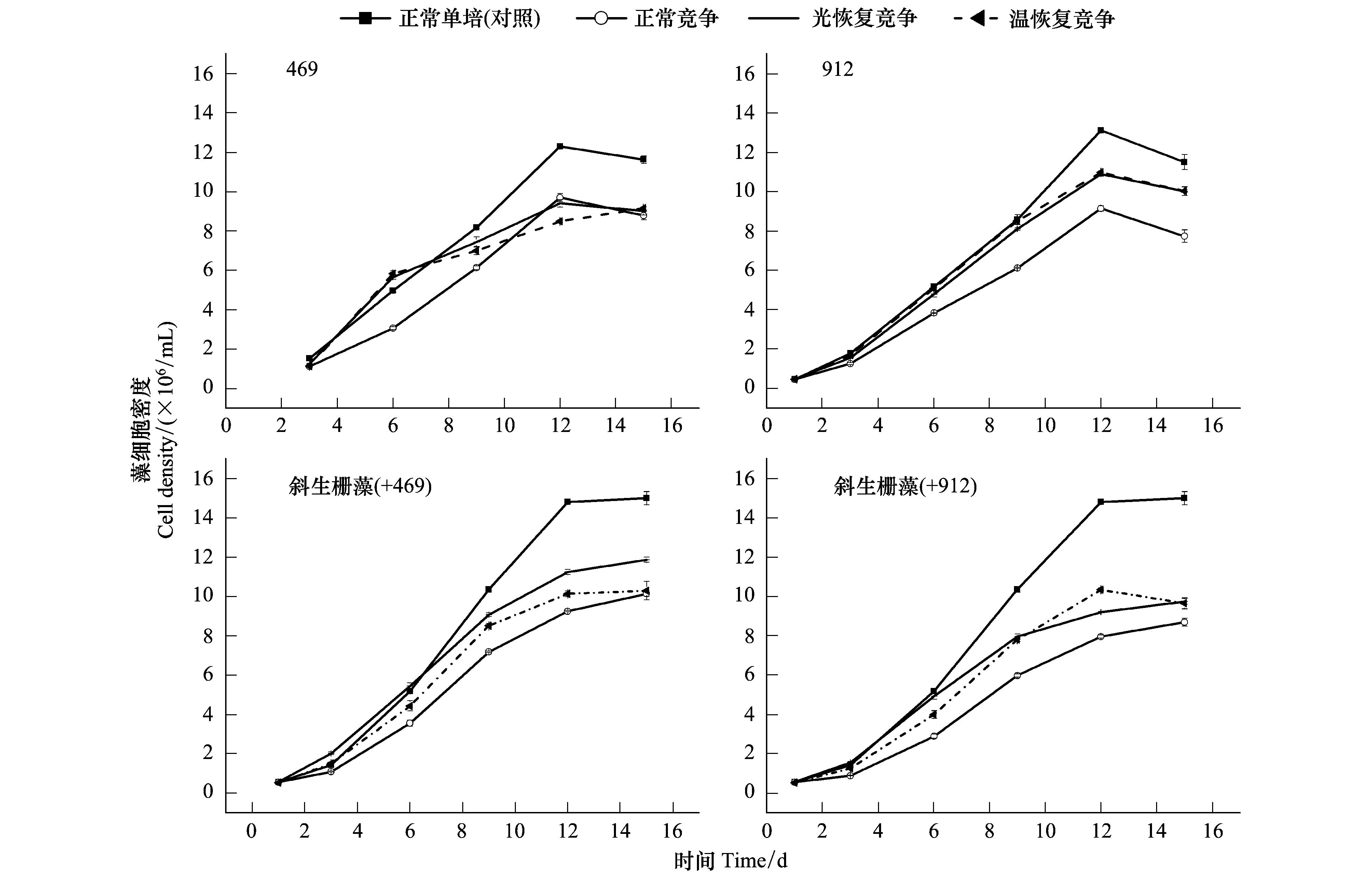
圖4 不同條件下銅綠微囊藻與斜生柵藻的競爭效應 (均值±標準誤,n=4)Fig.4 The competition effects of Microcystis aeruginosa and Scenedesmus obliquus under different culture conditions (Mean±S.E, n=4)
量化分析補償期內不同藻株的補償生長結果表明,斜生柵藻在光照恢復的情況下補償效應顯著高于銅綠微囊藻的,而溫度恢復時與產毒株912的差異不顯著,但顯著低于無毒株469的補償效應(圖5);無毒株469在光照和溫度恢復正常后的補償生長能力顯著高于產毒株912的。敏感性分析結果表明銅綠微囊藻對溫度表現出更高的敏感性(圖5),而斜生柵藻對光照強度更敏感(圖5)(P<0.05)。
量化分析結果表明,未經脅迫預處理的共培體系中斜生柵藻細胞增殖被競爭抑制的幅度顯著高于共培的產毒株912的,而與共培的無毒株469差異不顯著。盡管在經過低光或低溫脅迫預處理后的共培體系中斜生柵藻的抑制程度降低,但還是顯著高于產毒株被抑制率(P<0.05)。與無毒株469相比,兩種藻類在連續正常培養情況下競爭能力相當,而在恢復培養的處理中斜生柵藻對469生長和擴增的抑制效應遠大于469對斜生柵藻的,即斜生柵藻具有更強的競爭能力(P<0.05)。
2.4 不同培養條件對銅綠微囊藻和斜生柵藻葉綠素a含量的影響
同正常培養相比,限光和低溫處理都顯著降低了培養體系單位體積中葉綠素a的含量;兩種脅迫處理比較限光培養體系顯著低于低溫處理下的;3種藻株之間差異不顯著(圖6)。結合不同培養體系中藻密度數據進行協方差分析結果表明,在限光和低溫處理下單個藻細胞葉綠素a含量與正常培養條件下的差異不顯著(P>0.05)。
在光恢復培養的條件下,實驗藻葉綠素a含量都顯著高于連續正常培養的和經過低溫處理后溫度恢復的相應樣品,而溫度恢復培養的藻株葉綠素a含量顯著低于另外兩類相應樣品的,其中尤以產毒株912葉綠素a含量差異最顯著(圖6)。光恢復培養的條件下3個藻株葉綠素a含量都表現出一定程度的超補償效應,而經過低溫處理后即使恢復正常溫度,葉綠素a含量并未表現出超補償效應,而藻密度在此情況下表現出較強的超補償效應(圖5),兩個指標表現出不同步性,說明低溫預處理直接影響了后期正常培養時藻類葉綠素a的合成。
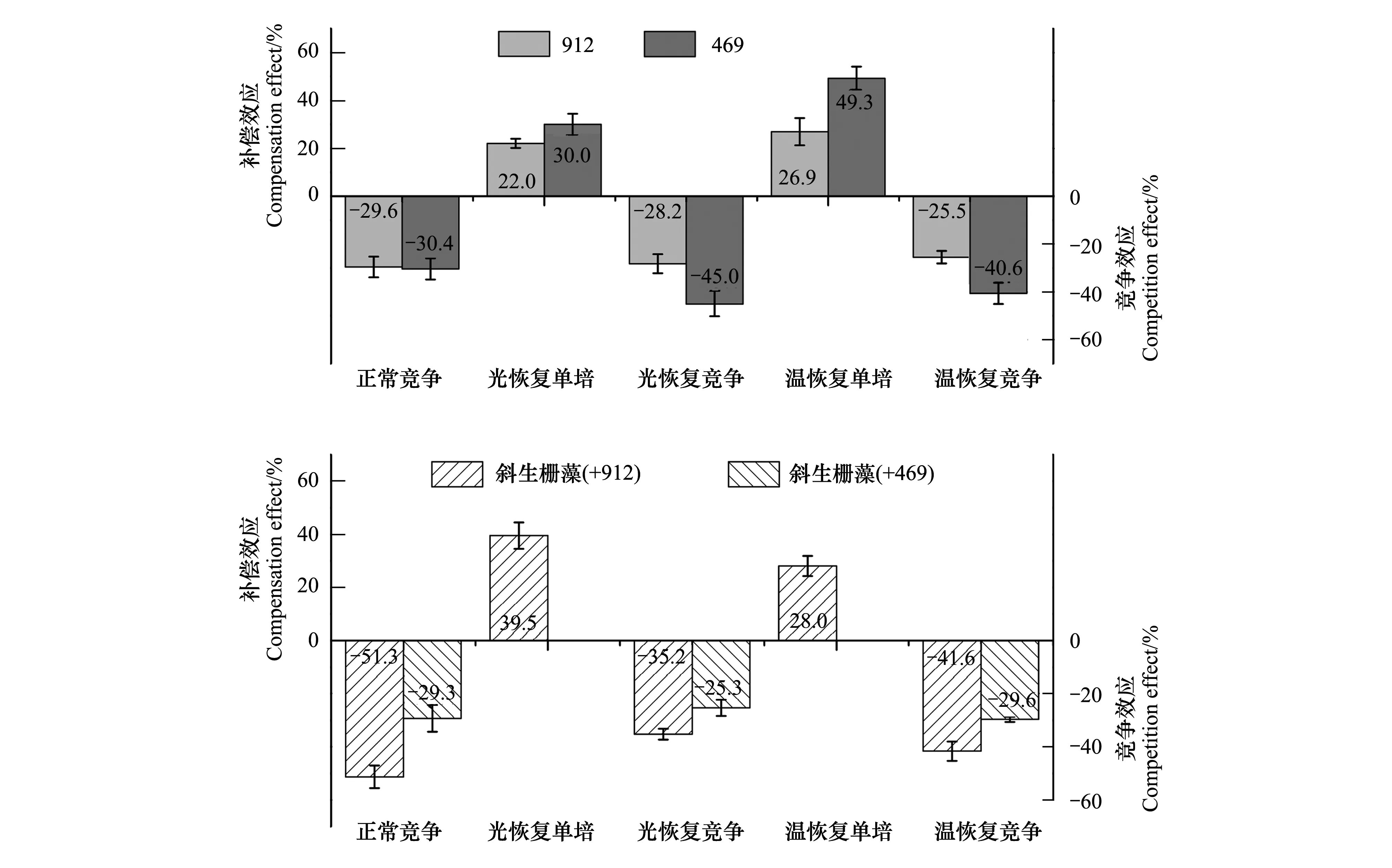
圖5 不同培養體系中銅綠微囊藻和斜生柵藻的補償效應和抑制效應(均值±標準誤,n=4)Fig.5 The compensation effects and inhibitory effects of M. aeruginosa and S. obliquus under different culture systems (Mean±S.E, n=4)
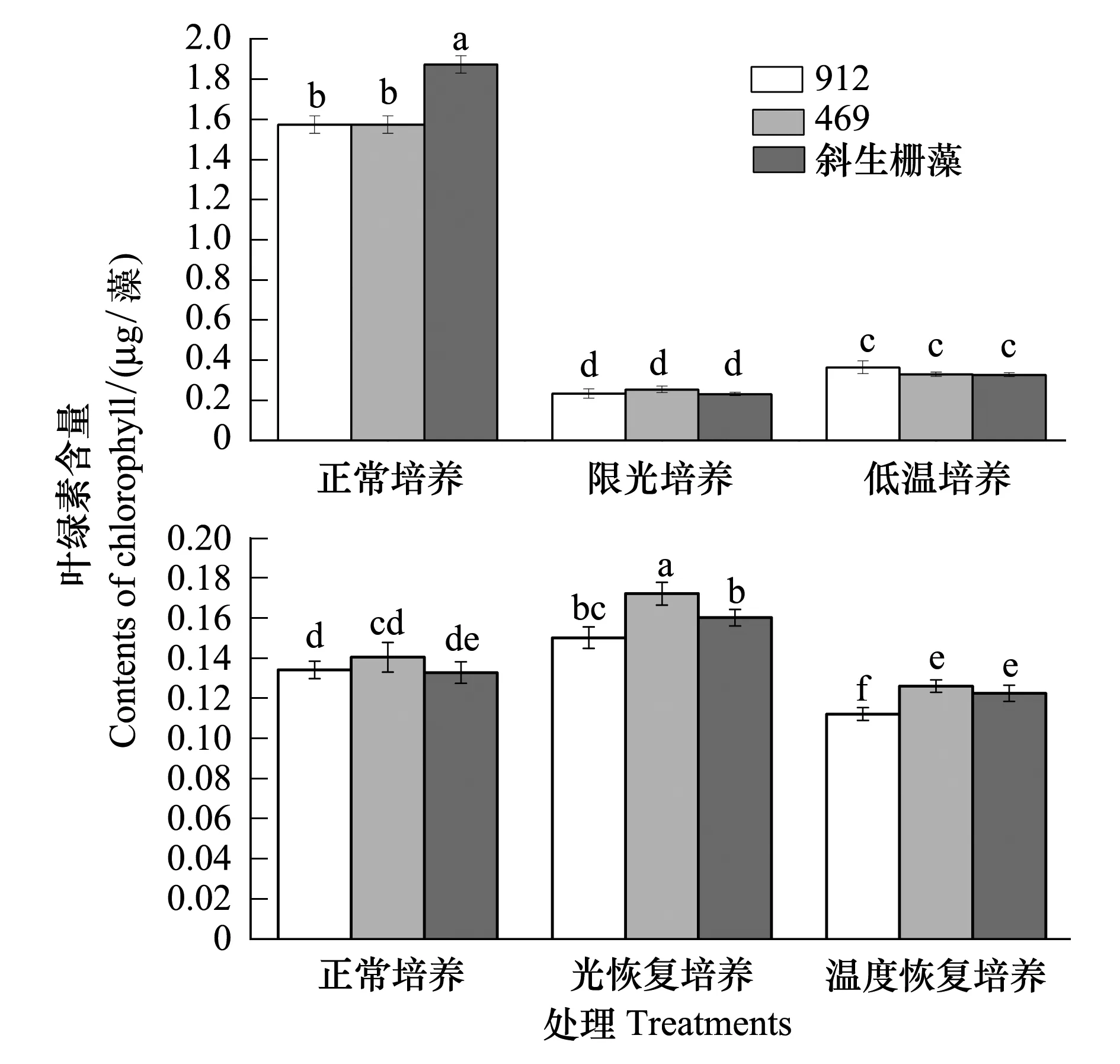
圖6 不同培養條件下銅綠微囊藻和斜生柵藻葉綠素含量的差異Fig.6 The differences of content of chlorophyll of M. aeruginosa and S. obliquus under different culture systems平均值±標準誤,不同字母表示差異顯著, P<0.05, n=4
2.5 不同培養條件對銅綠微囊藻和斜生柵藻脫氫酶活性的影響
低溫和限光培養體系中3種藻細胞脫氫酶活性都顯著低于正常培養體系中的,而兩種脅迫處理間差異不顯著;3種藻株之間比較可以看出限光和低溫脅迫下銅綠微囊藻產毒株(912)藻細胞脫氫酶活性都顯著高于其它兩種藻細胞脫氫酶活性(圖7)。協方差分析結果表明在限光和低溫脅迫條件下單個藻細胞脫氫酶活性顯著高于正常培養的(P<0.05)。單個藻細胞脫氫酶活性的提高可能是對限光和低溫脅迫的應急響應。
在單獨培養體系中,銅綠微囊藻和斜生柵藻脫氫酶活性對不同恢復條件響應模式不完全相同,而且銅綠微囊藻不同株系的響應也存在差異。產毒株912在兩種恢復培養模式下脫氫酶活性都有極顯著提高(P<0.01),而無毒株469僅在光恢復條件下極顯著提高(P<0.01),在溫度恢復條件下脫氫酶活性與對照(正常培養)相比差異不大(P>0.05),斜生柵藻脫氫酶對不同處理的響應模式與469相似(圖7)。
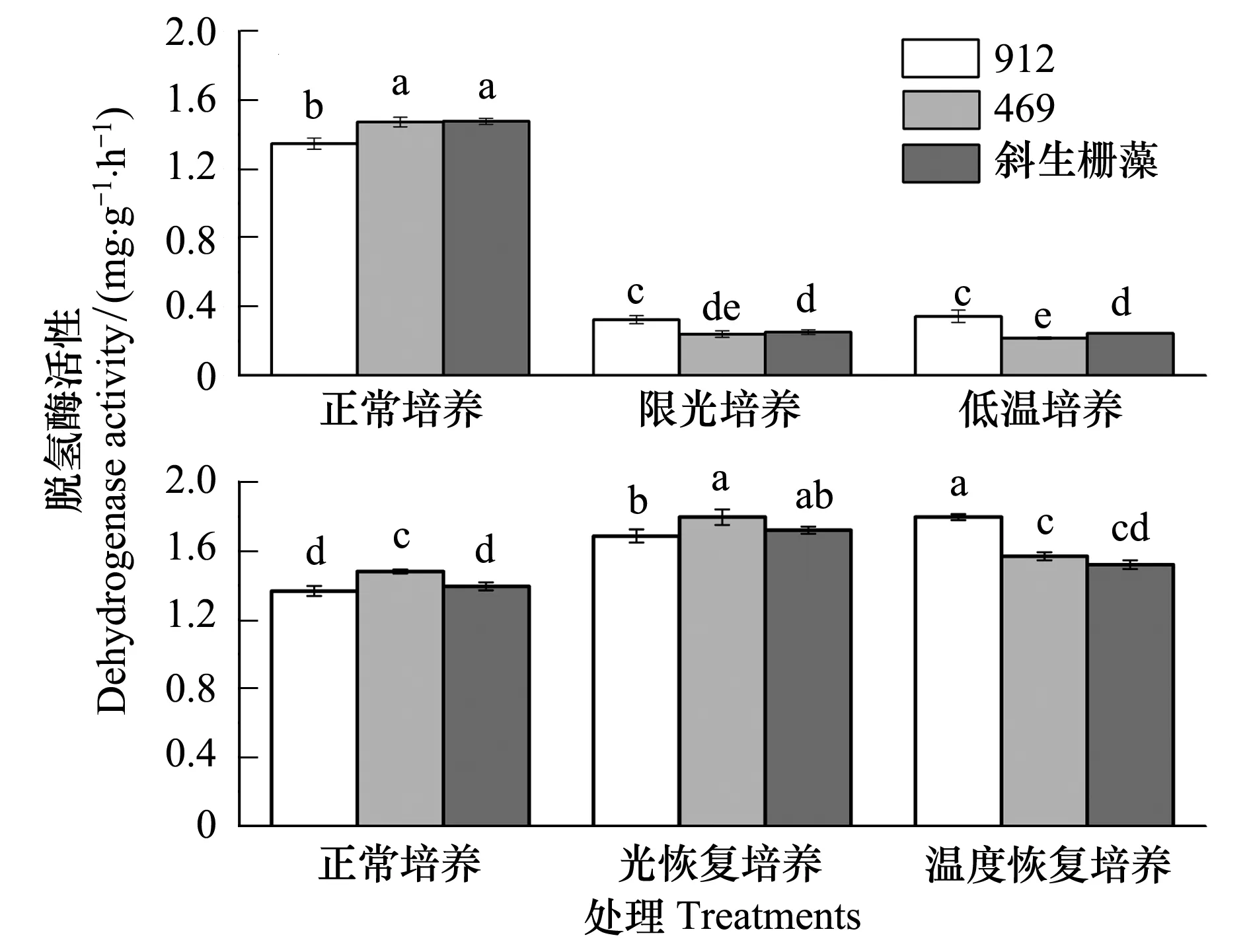
圖7 不同培養條件下銅綠微囊藻和斜生柵藻脫氫酶活性的差異 Fig.7 The differences of activity of dehydrogenase of M. aeruginosa and S. obliquus under different culture systems
3 討論
植物在逆境脅迫下生長速率往往表現出一定程度降低,在脅迫解除之后, 植物將逐漸恢復其生長能力,甚至表現出超過正常生長速率的現象,即超補償生長。超補償反應是植物對抗波動環境的一種適應對策,是植物在與環境的長期博弈中形成的抗逆機理的重要組成部分[22]。藻細胞密度是表征浮游植物種群生物量最真實的指標,研究發現蛋白核小球藻(Chlorellapyrenoidosa)、三角褐指藻(Phaeodactylumtricornutum)、綠色巴夫藻(Pavlovaviridis)、四列藻(Tetraselmistetrethele)等在暗處理等脅迫解除后藻細胞密度都表現出超補償生長現象[14- 17]。本研究表明銅綠微囊藻和斜生柵藻在低溫和低光照逆境解除后的恢復生長過程中藻細胞密度短期內都表現出顯著的超補償生長效應。與斜生柵藻相比,銅綠微囊藻補償性生長雖然啟動稍晚,但啟動后藻細胞密度快速增加,且持續時間長于斜生柵藻,尤其是低溫解除后藍藻的補償生長效應更加明顯,這將為高溫情況下藍藻優勢地位的建立和維持奠定基礎,這和譚嘯等[24]模擬升溫對藻類復蘇研究結果基本一致。盡管低溫和低光照顯著抑制了銅綠微囊藻的生長,但9℃以上銅綠微囊藻和斜生柵藻都可復蘇,但前者復蘇后的生長速率高于后者,并且隨著溫度的升高藍藻的優勢更加明顯[25]。在全球氣候變化的大背景下,溫度短期變化的幅度和頻率明顯增加,這種短期變溫刺激將誘發藍藻超補償生長,藻類群落組成結構將發生改變,藍藻數量顯著增加,因此在營養足夠的情況下藍藻爆發頻率和規模很有可能增加。
種間競爭在植物群落構建和維持中扮演著極其重要的角色,不同植物針對某一種或某些生態因子往往具有不同的競爭能力,而競爭能力強的物種將在群落組成和功能作用上占主導地位。一般情況下生物群落的物種組成處于動態平衡中,但當環境發生變化而導致某一種或某幾種生物在種間競爭中占絕對優勢時其數量將快速增長,藍藻爆發就是典型的例證,研究發現春末夏初氣溫回暖時太湖藻類群落組成發生了顯著改變:藍藻取代了綠藻成為優勢種[26- 27]。本實驗結果中,與單種培養對照相比,銅綠微囊藻和斜生柵藻共培養時兩種藻類的細胞增長速率和最大密度呈現出顯著降低趨勢,說明兩種藻類存在明顯的相互競爭。綠藻、硅藻和藍藻是大多數淡水水體最主要的藻類,當氣溫較低時綠藻和硅藻更占優勢,隨著溫度的升高藍藻更具競爭優勢[28]。通過比較斜生柵藻分別與產毒株912和無毒株469競爭結果可以看出,同912共培養過程中產生的微囊藻毒素對斜生柵藻可能產生了毒害作用,銅綠微囊藻可通過產生微囊藻毒素增強其競爭能力[29- 33]。因此,微囊藻毒素可能是產毒性微囊藻在群落中優勢地位建立和鞏固的重要機制之一。
應用葉綠素a含量表征浮游植物初級生產力和水體營養化水平已有很長的歷史,盡管有研究表明用葉綠素a含量表征浮游藻類生物量存在一定的問題[33],但到目前為止還沒有一個更快速、簡便而相對準確的指標來替代它[35- 37]。葉綠素a是浮游植物中最主要的光合色素,占浮游藻類干重的1%—2%,其含量的高低與藻類對光能吸收效率和利用效率都顯著相關,其值越大說明光合同化率越高[34]。葉綠素a含量又隨藻類種類、溫度、光照等因素的變化而異,低溫和低光照都直接降低了浮游植物種群葉綠素含量[38]。同對照相比,低光照脅迫解除后3種實驗藻葉綠素a含量與細胞密度的增長幅度基本一致,因此低光照脅迫并未影響葉綠素a的生物合成能力,研究表明雖然大多數植物葉綠素合成的通路是光依賴性的,但部分藻類還具有在黑暗條件下合成葉綠素的輔助通路[39]。盡管低溫脅迫下單個藻細胞葉綠素a含量沒有顯著變化,但在低溫脅迫解除后的恢復性生長過程中葉綠素含量顯著低于相應對照,由此說明低溫預處理仍然對藻細胞葉綠素合成能力造成了影響,在恢復培養的過程中藻細胞密度表現出了補償性生長,葉綠素a的合成能力未能完全恢復,從而表現出葉綠素a增長幅度與細胞密度增加并非同步。這一結果也證明有些情況下葉綠素a含量并不能很好的表征藻細胞密度[34]。
脫氫酶是一類氧化還原酶,參與了生物體氨基酸合成和降解、丙酮酸的氧化、光合作用、戊糖磷酸途徑、氧化磷酸化、脂肪的氧化和合成等過程,是生物生命活動過程中極其重要的酶類[21]。由于脫氫酶只有活細胞體才能產生,所以生物體的脫氫酶活性(DHA)是細胞活力的最重要表征指標之一,通過檢測藻細胞脫氫酶活性可以體現出藻細胞生命力[21,40- 41]。同對照相比,經過低光照或低溫預處理后恢復生長的藻細胞脫氫酶活性都有一定程度的提高,尤其是產毒株912經過低溫脅迫解除后的恢復生長過程中脫氫酶活性顯著提高。同時3種藻響應模式表現出一定的差異,在低溫脅迫解除后銅綠微囊藻無毒株469和斜生柵藻脫氫酶活性都顯著低于光恢復培養狀態的。結合低溫和低光照脅迫解除后3種藻細胞密度的增長可以發現,雖然斜生柵藻和無毒株469藻細胞密度都呈現出較明顯的補償生長,但經過低溫后的恢復生長過程藻細胞活性并未達到正常水平,而銅綠微囊藻產毒株不僅藻細胞密度增長迅速,細胞活力也得到恢復或提高,由此可見其抗低溫脅迫能力明顯高于另外兩種藻類。因此銅綠微囊藻產毒株低溫和低光照逆境脅迫后的補償性生長和對其它藻類的競爭優勢可能是藍藻爆發的重要內源性機制。
4 結論
藍藻生長和水華形成歷經休眠、復蘇、增殖和爆發四個階段,在營養保證的前提下溫度和光照是促進藍藻細胞迅速增殖,種群密度急劇增加的關鍵因素,不同藻類對環境變化的響應以及種間競爭能力的差異是藍藻爆發的內源機制。本研究中低溫和低光照均顯著抑制微藻的生長發育,但銅綠微囊藻在低溫條件下表現出更強抑制,而斜生柵藻則對低光脅迫更敏感。在光溫恢復正常的條件下各種藻細胞密度增長短期內都表現出超補償效應,但不同藻類超補償模式不同,斜生柵藻補償生長時間不超過1周,而銅綠微囊藻的補償效應可以持續10d;銅綠微囊藻細胞密度對低溫限制解除表現出更顯著的補償生長,而斜生柵藻則在低光解除后表現出更強的超補償效應。競爭實驗結果表明銅綠微囊藻產毒株(912)對斜生柵藻具有顯著的競爭優勢,而無毒株(469)對斜生柵藻則不具有競爭優勢,因此微囊藻毒素可能是產毒型微囊藻在群落中優勢地位建立和鞏固的重要機制之一。溫度恢復條件下藻類葉綠素a含量并未表現出與藻密度增長同步,低溫脅迫可能對微藻葉綠素a的形成產生了一定的負效應。脫氫酶是表征藻類細胞活力的重要指標,產毒株(912)脫氫酶活性的補償響應顯著高于無毒株(469)和斜生柵藻的。因此產毒型銅綠微囊藻低溫和低光后的補償生長效應以及對斜生柵藻的之一競爭優勢可能是藍藻爆發的重要內源性機制。
致謝:感謝美國北卡大學教堂山分校(University of North Carolina at Chapel Hill)生物系Peter S. White教授潤色英文摘要;南通大學孫政璽、于珍、趙莉莉、汪情等同學參與部分實驗工作,特此致謝。
[1] Kong F X, Gao G. Hypothesis on cyanobacteria bloom-forming mechanism in large shallow eutrophic lakes. Acta Ecologica Sinica, 2005, 925(3): 589- 595.
[2] Kong F X, Ma R H, Gao J F, Wu X D. The theory and practice of prevention, forecast and warning on cyanobacteria bloom in Lake Taihu. Journal of Lake Science, 2009, 21(3): 314- 328.
[3] Paerl H W, Otten T G. Harmful Cyanobacterial Blooms: Causes, Consequences, and Controls. Microb Ecology, 2013, 65: 995- 1010.
[4] Wang C Y, Yu Y, Sun Y K, Li H L,Kong F X, Zhang M, Shi X L, Yang Z. The discussion of the early forecasting of cyanobacteria bloom in the Lake Taihu based on ELCOM-CAEDYM model. China Environmental Science, 2013, 33(3): 491- 502.
[5] Paul V J. Global warming and cyanobacterial harmful algal blooms. Advances in Experimental Medicine and Biology, 2008, 619: 239- 257.
[6] Zhang M,Duan H, Shi X, Yu Y, Kong F X. Contributions of meteorology to the phenology of cyanobacterial blooms: implications for future climate change. Water Research, 2012, 46(2): 442- 452.
[7] Gu T T, Kong F X, Tan X, Yu Y. Investigation on spatio-temporal pattern of cyanobacterial community structure by T-RFLP during overwinter and recruitment period in Taihu Lake. Acta Ecologica Sinica, 2011, 31(1): 21- 30.
[8] Grover J P, Chrzanowski T H. Seasonal dynamics of phytoplankton in two warm temperate reservoir: association of taxonomic composition with temperature. Journal of Plankton Research, 2005, 27(10): 1- 7.
[9] Huber V, Wagner C, Gerten D, Adrian R. To bloom or not to bloom: contrasting responses of cyanobacteria to recent heat waves explained by critical thresholds of abiotic drivers. Oecologia, 2012, 169(1): 245- 256.
[10] Paerl H W, Otten T G. Harmful cyanobacterial blooms: causes, consequences, and controls. Microb Ecology, 2013, 65(4): 995- 1010.
[11] Eilertsen H C, Degerlund M. Phytoplankton and light during the northern high-latitude winter. Journal of Plankton Research, 2010, 32(6): 899- 912.
[12] Clegg M R, Gaedke U, Boehrer B, Spijkerman E. Complementary ecophysiological strategies combine to facilitate survival in the hostile conditions of a deep chlorophyll maximum. Oecologia, 2012, 169(3): 609- 622.
[13] Laabir M, Jauzein C, Genovesi B, Massere E, Grzebyk D, Cecchi P, Vaquer A,Perrin Y, Collos Y. Influence of temperature, salinity and irradiance on the growth and cell yield of the harmful red tide dinoflagellateAlexandriumcatenellacolonizing Mediterranean waters. Journal of Plankton Research, 2011, 33(10): 1550- 1563.
[14] Duan S S, Guo Y F, Liu Z Q,Li A F, Xu N, Zhang Y N, Chen H. Overcompensatory growth of Tetraselmistetretheleunder the stress of nutrients deficiency. Acta Ecologica Sinica, 2003, 23(7) : 1297- 1304.
[15] Zhang Z P, Duan S S, Liu Z Q,Li A F, Xu N. Overcompensation response ofNannochloropsisoculataunder the darkness stress. Journal of Jinan University (Natural Science) , 2005, 26(3): 412- 416.
[16] Liu X J, Duan S S, Li A F. The effect of overcompensatory growth inPavlovaviridisafter UV-B stress treatments. Acta Ecologica Sinica , 2006, 26(6): 1763- 1771.
[17] Cai Z P, Duan S S, Wei W. Darkness and UV radiation provoked compensatory growth in marine phytoplanktonPhaeodactylumtricornutum(Bacillariophyceae). Aquaculture Research, 2009, 40(13): 1559- 1562.
[18] Chen X C, Sun Y C, Zeng X W, Li C J, Kong H N. The inhibition of low light intensity on the growth ofMicrocystisaeruginosain raw water. China Environmental Science, 2007, 27(3): 352- 355.
[19] Wu R, Cui L F, Lou S, Shi Y. The influence of temperature and illumination on theMicrocystisproduction. Environmental Science & Technology, 2010, 33(6): 33- 36.
[20] Zeng J, Wang W X.Temperature and irradiance influences on cadmium and zinc uptake and toxicity in a freshwater cyanobacterium,Microcystisaeruginosa. Journal of Hazardous Materials, 2011, 190: 922- 929.
[21] Xie J, Hu W R, Pei H Y. Detection of amount and activity of living algae in fresh water by dehydrogenase activity (DHA). Environ Monit Assess, 2008, 146: 473- 478.
[22] Tommy L, Tuomi J, Nilsson P. Evidence for an evolutionary history of overcompensation in the grassland biennialGentianellacampestris(Gentianaceae). American Naturalist, 1997, 149, 6: 1147- 1155.
[23] Weigelt A, Jolliffe P. Indices of plant competition. Journal of ecology, 2003, 91: 707- 720.
[24] Tan X, Kong F X, Yu Y, Shi X L. Effects of enhanced temperature on algae recruitment and phytoplankton community succession. China Environmental Science, 2009, 29(6): 578- 582.
[25] Tang J, Song L R, Sun S S, Wei H H, Wan N. Recruitment ability ofMicrocystisaeruginosaunder low light-low temperature combination. Enviromental Science (Chinese), 2010, 31(12): 2933- 2937.
[26] Hu X Z, Jin X C, Chu Z S, Ma Z Y, Yi L W. Light competition betweenMicrocystisaeruginosaandScendesmusquadricaudafrom Taihu lack and the dominance process simulation in microcosm. Journal of Agro-Environment Science, 2005, 24(3): 538- 543.
[27] Xing P, Kong F X, Cao H S, Zhang M. Relationship between bacterioplankton and phytoplankton community dynamics during late spring and early summer in lake Taihu. Acta Ecologica Sinica, 2007, 27(5): 1696- 1702.
[28] Zhang Z B, Shi X L, Liu G J, Yang X Y, Wang Y N, Liu X J. The relationship between planktonic algae changes and the water quality of the West Lake, Hangzhou, China. Acta Ecologica Sinica, 2009,29(6): 2980- 2987.
[29] Deblois C P, Juneau P. Comparison of Resistance to Light Stress in Toxic and Non-Toxic Strains ofMicrocystisaeruginosa(Cyanophyta). Journal of Phycology, 2012, 48(4): 1002- 1011.
[30] El-Shehawy R, Gorokhova E, Fernandez-Pinas F, del Campo F F. Global warming and hepatotoxin production by cyanobacteria: What can we learn from experiments?. Water Research, 2012, 46: 1420- 1429.
[31] Li D M, Kong F X, Shi X L, Ye L L,Yu Y, Yang Z. Quantification of microcystin-producing and non-microcystin producingMicrocystispopulations during the 2009 and 2010 blooms in Lake Taihu using quantitative real-time PCR. Journal of Environmental Sciences, 2012, 24(2) 284- 290.
[32] Li Y X , Li D H. Competition between toxicMicrocystisaeruginosaand nontoxicMicrocystiswesenbergiiwith Anabaena PCC7120. Journal of Applied Phycology, 2012, 24: 69- 78.
[33] Harel M, Weiss G, Lieman-Hurwitz J, Lebendiker M,Temper V, Block C,Sukenik A, Zohary T, Braun S, Carmeli S, Kaplan A. Interactions betweenScenedesmusandMicrocystismay be used to clarify the role of secondary metabolites. Environmental Microbiology Reports, 2013, 5(1): 97- 104.
[34] Kruskopf M, Flynn K J. Chlorophyll content and fluorescence responses cannot be used to gauge reliably phytoplankton biomass, nutrient status or growth rate. New Phytologist, 2006, 169: 525- 536.
[35] Huot Y, Babin M, Bruy`ant F. Does chlorophyll a provide the best index of phytoplankton biomass for primary productivity studies? Biogeosciences Discuss, 2007, 4: 707- 745.
[36] Todd V R, Mark B D, Lowell E G. Chlorophyll-a as a criterion for establishing nutrient standards in the streams and rivers of Illinois. Journal of Environmental Quality, 2008, 37: 437- 447.
[37] Boyer J N, Kelble C R, Ortner P B, Rudnick D T. Phytoplankton bloom status: Chlorophyll a biomass as an indicator of water quality condition in the southern estuaries of Florida, USA. Ecological Indicators, 2009, 9: 56- 67.
[38] Shaaban A M, Mansour H A, Saber A A. Relationships between total chlorophyll and phytoplankton individuals of Rosetta branch of River Nile, Egypt. International Research Journal of Biochemistry and Bioinformatics, 2011, 1(10) : 257- 265.
[39] Wu Q Y, Vermaas W F J. Light-dependent chlorophyll a biosynthesis upon chlL deletion in wild-type and photosystem I-less strains of the cyanobacteriumSynechocystissp. PCC 6803. Plant Molecular Biology, 1995, 29: 933- 945.
[40] Liang W Y, Wang K, Ruan Q Y, Wang J L. Viability determ ination ofMicrocystisaeruginosaby TTC-dehydrogen as eassay. Acta Scientiae Circumstantiae, 2008, 28 (9): 1745- 1750.
[41] Hoch M P, Dillon K S, Coffin R B, Cifuentes L A. Sensitivity of bacterioplankton nitrogen metabolism to eutrophication in sub-tropical coastal waters of Key West, Florida. Marine Pollution Bulletin, 2008, 56: 913- 926.
參考文獻:
[1] 孔繁翔, 高光. 大型淺水富營養化湖泊中藍藻水華形成機理的思考. 生態學報, 2005, 25(3): 589- 595.
[2] 孔繁翔, 馬榮華, 高俊峰, 吳曉東. 太湖藍藻水華的預防、預測和預警的理論與實踐. 湖泊科學, 2009, 21(3): 314- 328.
[4] 王長友, 于洋, 孫運坤, 李洪利, 孔繁翔, 張民, 史小麗, 陽振. 基于ELCOM- CAEDYM模型的太湖藍藻水華早期預測探討. 中國環境科學 2013, 33(3): 491- 502.
[7] 顧婷婷, 孔繁翔, 譚嘯,于洋. 越冬和復蘇時期太湖水體藍藻群落結構的時空變化. 生態學報, 2011, 31(1): 21- 30.
[14] 段舜山, 郭羽豐, 劉振乾, 李愛芬, 徐寧, 張亞楠, 陳潔. 四列藻在營養限制脅迫下的超補償生長研究. 生態學報, 2003, 27(7): 1297- 1304.
[15] 張珍萍, 段舜山, 劉振乾, 李愛芬, 徐寧. 眼點擬微綠球藻在黑暗脅迫下的超補償生長響應. 暨南大學學報(自然科學與醫學版), 2005, 26(3): 412- 416.
[16] 劉曉娟,段舜山,李愛芬. 綠色巴夫藻在UV- B脅迫后的生長補償效應.生態學報, 2006, 26(6): 1763- 1771.
[18] 陳雪初, 孫揚才, 曾曉文, 李春杰, 孔海南. 低光照度對源水中銅綠微囊藻增殖的抑制作用. 中國環境科學, 2007, 27(3): 352- 355.
[19] 吳溶, 崔莉鳳, 盧珊, 時寅. 溫度光照對銅綠微囊藻生長及藻毒素釋放的影響. 環境科學與技術, 2010, 33(6): 33- 36.
[22] 王海洋,杜國禎,任金吉. 種群密度和施肥對垂穗披堿草刈割后補償作用的影響. 植物生態學報,2003, 27(4): 477- 483.
[24] 譚嘯, 孔繁翔, 于洋, 史小麗,張民. 升溫過程對藻類復蘇和群落演替的影響.中國環境科學,2009, 29(6):578- 582.
[25] 湯俊, 宋立榮, 孫松松, 魏海慧, 萬能. 低光低溫聯合作用對銅綠微囊藻復蘇能力的影響. 環境科學, 2010, 31(12): 2933- 2937.
[26] 胡小貞, 金相燦, 儲昭升, 馬祖友, 易文利. 太湖銅綠微囊藻與四尾柵藻的光競爭及模擬優勢過程初探. 農業環境科學學報, 2005, 24(3): 538- 543.
[27] 邢鵬, 孔繁翔, 曹煥生, 張民. 太湖浮游細菌與春末浮游藻類群落結構演替的相關分析. 生態學報, 2007, 27(5): 1696- 1702.
[28] 張志兵,施心路, 劉桂杰, 楊仙玉,王婭寧, 劉曉江. 杭州西湖浮游藻類變化規律與水質的關系. 生態學報,2009,29(6): 2980- 2987.
[40] 梁文艷, 王珂, 阮清鴛, 王金麗. TTC- 脫氫酶還原法測定銅綠微囊藻活性. 環境科學學報, 2008, 28 (9): 1745- 1750.
Overcompensation and competitive effects ofMicrocystisaeruginosaandScenedesmusobliquusafter low temperature and light stresses
XIE Xiaoling, ZHOU Rong, DENG Zifa*
SchoolofLifeScience,NantongUniversity,Nantong226007,China
Changes of temperature and light significantly influence the growth and activity of phytoplankton. To explore the effects of these two variables on the cyanobacterial blooms, we analyzed the growth ofMicrocystisaeruginosaandScenedesmusobliquus, as well as the competition between the two species, under conditions of low temperature and low light, and under conditions of release from these two stress factors. The results showed that low temperature and low light significantly inhibited the growth of microalgae. Low temperature led to a stronger inhibitory effect onM.aeruginosathan low light did; however, the growth inhibition ofS.obliquuswas more sensitive to low light than to low temperature. After release from low temperature or limiting light, all of the experimental taxa exhibited the overcompensation growth within a limited time and this response varied by species. TwoM.aeruginosastrains showed a greater response to increased temperature than increased light. However, overcompensation ofS.obliquuswas greater in response to increased light than increased temperature. When the species were grown together, results showed that under all culture conditions, the toxicMicrocystisstrains (912) had a competitive advantage overS.obliquus. Although there was no significant difference between the competitive ability of the nontoxicMicrocystisstrain (469) andS.obliquusunder the normal, the former (469) showed a competitive disvantage toS.obliquusunder conditions of release from low light and low temperature. Chlorophyll-a content of all experimental algae overcompensated when released from light limitation. In the temperature experiments, the increase of chlorophyll-a content and algal density were asynchronism for all species, and cryogenic pre-treatment had a negative after-effect on microalgae chlorophyll-a content under release from low temperature. The response of dehydrogenase activity of algae when released from low temperature or low light stress varied with algae species, and the compensating increase of dehydrogenase activity of toxic strains (912) was significantly higher than that of the other two taxa. The results suggested that higher the compensatory growth of toxicMicrocystisas well as its competitive advantage overS.obliquuswhile released from low temperature and light stresses, might be the important mechanisms that result in blue-green algae bloom.
Microcystisaeruginosa;Scenedesmusobliquus; overcompensation; competitive effect; Cyanobacterial bloom
國家重點研究發展計劃(2008CB418201); 江蘇省高校“青藍工程-中青年學術帶頭人”項目;南通大學“創新人才”項目
2013- 06- 13;
2013- 10- 28
10.5846/stxb201306131698
*通訊作者Corresponding author.E-mail: dengzifa@126.com
謝曉玲, 周蓉, 鄧自發.光、溫限制后銅綠微囊藻和斜生柵藻的超補償生長與競爭效應.生態學報,2014,34(5):1224- 1234.
Xie X L, Zhou R, Deng Z F.Overcompensation and competitive effects ofMicrocystisaeruginosaandScenedesmusobliquusafter low temperature and light stresses.Acta Ecologica Sinica,2014,34(5):1224- 1234.

