反硝化脫硫工藝中生物硫分布特征及分離方法
遠(yuǎn) 野,王愛(ài)杰,馬素麗,陳 川,趙友康,譚文勃,黃 聰,徐熙俊,孫德智
反硝化脫硫工藝中生物硫分布特征及分離方法
遠(yuǎn) 野1,2,王愛(ài)杰1,2,馬素麗1,2,陳 川1,2,趙友康1,2,譚文勃1,2,黃 聰1,2,徐熙俊1,2,孫德智1,2
(1.哈爾濱工業(yè)大學(xué)市政環(huán)境工程學(xué)院,150090哈爾濱;2.哈爾濱工業(yè)大學(xué)城市水資源與水環(huán)境國(guó)家重點(diǎn)實(shí)驗(yàn)室,150090哈爾濱)
為探尋反硝化脫硫工藝生物硫分離方法,運(yùn)行反硝化脫硫系統(tǒng)獲得生物硫在系統(tǒng)中分布特征,并對(duì)生物硫進(jìn)行粒徑分布、Zeta電位、能譜及電鏡掃描分析,確定了一種分離生物硫的新方法.結(jié)果表明,生物硫在反硝化脫硫系統(tǒng)中水相占65%,污泥相占35%.能譜分析表明,生物硫硫元素占60%以上,電鏡分析顯示生物硫表面具有多聚糖、蛋白質(zhì)等官能團(tuán),生物硫Zeta電位平均為-20 mV帶負(fù)電(在±30 mV之間),得出生物硫具有膠體特性.進(jìn)一步用陽(yáng)離子絮凝劑實(shí)驗(yàn)分離生物硫獲得99%分離率.混凝沉淀方法能有效地分離回收生物硫.
生物硫;分布特征;膠體特性;混凝沉淀
含硫含氮廢水毒性高、腐蝕性強(qiáng)、污染性大,對(duì)環(huán)境造成嚴(yán)重破壞[1-4].王愛(ài)杰等[5-8]成功將反硝化脫硫工藝應(yīng)用于含硫、氮、碳廢水的處理,通過(guò)在生態(tài)位上調(diào)節(jié)反硝化自養(yǎng)和異養(yǎng)的協(xié)同作用,實(shí)現(xiàn)了反硝化脫硫工藝中硫化物向單質(zhì)硫(簡(jiǎn)稱(chēng)“生物硫”)的定向轉(zhuǎn)化,在同步去除硫、氮、碳污染物的同時(shí)獲得了較高單質(zhì)硫轉(zhuǎn)化率.然而,單質(zhì)硫易被空氣氧化,如果在反硝化脫硫工藝后續(xù)處理中,單質(zhì)硫不能被有效分離出來(lái),將被繼續(xù)氧化為硫酸鹽等硫系污染物,對(duì)水體造成二次污染[9-14].陳川等[15-16]對(duì)反硝化脫硫工藝中碳氮比、硫氮比和進(jìn)水負(fù)荷等工藝參數(shù)進(jìn)行了研究,討論了影響單質(zhì)硫轉(zhuǎn)化率的因素.但是,目前關(guān)于單質(zhì)硫在反硝化脫硫工藝系統(tǒng)中分布情況的研究未見(jiàn)報(bào)道.反硝化脫硫微生物產(chǎn)生的生物硫分散在水相和污泥相中,研究其分布情況有助于生物硫的分離回收,可作為再生資源應(yīng)用于農(nóng)業(yè)和工業(yè)生產(chǎn)中.
本文成功運(yùn)行反硝化脫硫反應(yīng)器實(shí)現(xiàn)了單質(zhì)硫最大產(chǎn)率,通過(guò)單質(zhì)硫的實(shí)測(cè)和物料平衡分析得出生物硫在反硝化脫硫工藝水相和污泥相的分布情況,并對(duì)生物硫進(jìn)行了粒徑分布、Zeta電位、能譜元素分析以及電鏡掃描等物化特性的分析,得出生物硫具有膠體特性的重要結(jié)論.進(jìn)而提出可利用混凝沉淀的方法進(jìn)行生物硫的分離回收,為下一步生物硫的分離優(yōu)化提供理論基礎(chǔ).
1 實(shí) 驗(yàn)
1.1實(shí)驗(yàn)裝置
反硝化脫硫反應(yīng)器采用顆粒污泥膨脹污泥床反應(yīng)器EGSB,裝置如圖1所示.內(nèi)徑50 mm,總高度120 cm,反應(yīng)區(qū)高度140 cm,總?cè)莘e5.0 L,主反應(yīng)區(qū)1.0 L,高徑比為18.反應(yīng)器外側(cè)纏繞電熱絲通過(guò)溫控儀控制溫度在(35±1)℃.進(jìn)水采用蠕動(dòng)泵從反應(yīng)器底部連續(xù)打入,并在反應(yīng)器沉淀區(qū)設(shè)有回流口,通過(guò)蠕動(dòng)泵回流實(shí)現(xiàn)內(nèi)循環(huán),回流比控制在10∶1,上升流速vup為1.5 m/h.產(chǎn)生的氣體經(jīng)2 mol/L的堿液吸收后進(jìn)入濕式氣體流量計(jì)測(cè)量體積.
1.2接種污泥
反硝化脫硫反應(yīng)器接種污泥取自哈爾濱太平污水處理廠(chǎng)二沉池,污泥的生物量指標(biāo)分別為:懸浮物質(zhì)量濃度(SS)27.48 g/L,揮發(fā)性懸浮物(VSS)1.75 g/L,VSS與SS比0.75.在接入反應(yīng)器之前,采用不同孔徑的泰勒式標(biāo)準(zhǔn)篩對(duì)接種污泥進(jìn)行淘洗和篩選,以去除污泥中較大的無(wú)機(jī)顆粒和金屬沉淀物質(zhì).將經(jīng)過(guò)淘洗粒徑均勻且小于0.2 mm的污泥接入反應(yīng)器中.
1.3反應(yīng)器的啟動(dòng)
反硝化脫硫反應(yīng)器進(jìn)水組成為硫化物200 mg/L、硝酸鹽90 mg/L、乙酸鹽78 mg/L.根據(jù)微生物生長(zhǎng)代謝的需要,每升進(jìn)水加入1 mL微量元素溶液,組成為:EDTA,50 g/L;NaOH,11 g/L;CaCl2·2H2O,7.34 g/L;CuCl2·2H2O,0.14 g/L;(NH4)6Mo7O24·4H2O,0.5 g/L;MnCl2·2H2O,2.5 g/L;ZnCl2,1.06 g/L;FeCl2·4H2O,3.58 g/L;CoCl2·6H2O,0.5 g/L.進(jìn)水調(diào)節(jié)pH至7.5~8.5,溫度保持在25℃.水力停留時(shí)間(HRT)從12 h逐漸縮短到8、6、4 h以提高反應(yīng)器進(jìn)水負(fù)荷,以硫化物、硝酸鹽和乙酸鹽的去除率及單質(zhì)硫生成率作為考察反應(yīng)器處理效果的依據(jù).
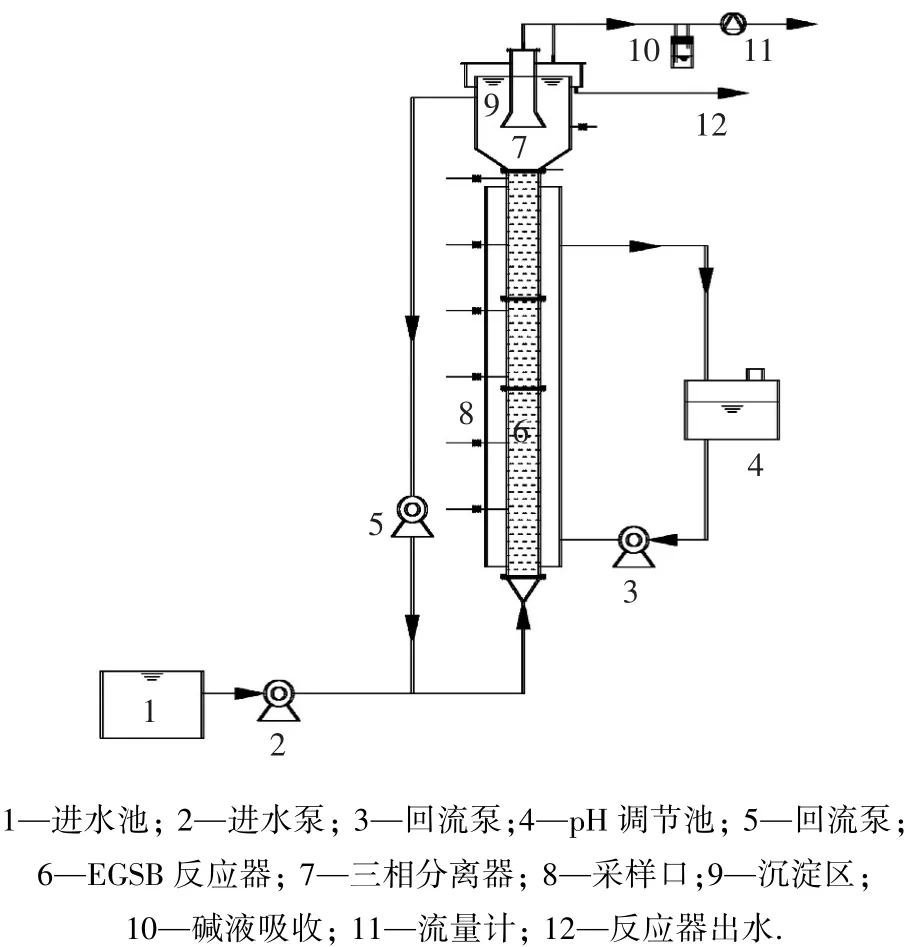
圖1 反硝化脫硫EGSB反應(yīng)器
1.4分析方法
一出門(mén),丁香就給權(quán)箏打電話(huà)避開(kāi)一切與自殺相關(guān)的敏感話(huà)題,直接切入“結(jié)婚”。她要求權(quán)箏別人說(shuō)什么都別想,就問(wèn)問(wèn)自己對(duì)何東的感覺(jué),他是不是比較接近你條件的男人?權(quán)箏想了一下說(shuō)是,我長(zhǎng)的不美,傻博一個(gè),還不會(huì)持家,能找到他這樣的,很滿(mǎn)意。丁香就說(shuō),那還等什么?女人是性別上的弱勢(shì)群體,八十歲的男人還能傳種接代呢,八十歲的女人你試試?
硝酸鹽和乙酸鹽采用離子色譜法測(cè)定[17];硫化物采用亞甲基藍(lán)分光光度法測(cè)定[18];單質(zhì)硫的測(cè)定采用亞硫酸鹽法[8,19],單質(zhì)硫與亞硫酸鹽在高pH下轉(zhuǎn)化為硫代硫酸鹽,利用離子色譜法測(cè)定硫代硫酸鹽含量間接得到生物硫含量.生物硫特性測(cè)定方法:粒徑分布采用激光粒度分布儀測(cè)定,Zeta電位采用Zeta電位分析儀測(cè)定.SEM圖片采用Quanta 200環(huán)境掃描電鏡.
2 結(jié)果與討論
2.1反硝化脫硫反應(yīng)器運(yùn)行效能
反硝化脫硫反應(yīng)器運(yùn)行效能見(jiàn)圖2.第Ⅰ階段(0~30 d),反應(yīng)器啟動(dòng)期的水力停留時(shí)間(HRT)為12 h,在進(jìn)水硫化物、硝酸鹽和乙酸鹽負(fù)荷為0.40,0.18和0.15 kg·m-3·d-1條件下,硫化物的去除率逐漸達(dá)97%,單質(zhì)硫的轉(zhuǎn)化率達(dá)93%.硝酸鹽和乙酸鹽的去除率分別達(dá)97%和96%.在反應(yīng)器底部發(fā)現(xiàn)直徑在0.5~2.0 mm的顆粒污泥,顆粒污泥外面包裹著一層白色的單質(zhì)硫.反應(yīng)器啟動(dòng)期馴化出具有高效反硝化脫硫功能的顆粒污泥.

圖2 反硝化脫硫反應(yīng)器運(yùn)行效能
第Ⅱ階段(30~50 d),HRT縮短到8 h,進(jìn)水硫化物、硝酸鹽和乙酸鹽負(fù)荷提高到0.61,0.29和0.22 kg·m-3·d-1,硫化物、硝酸鹽和乙酸鹽的去除率依然可達(dá)94%以上,并在氣相中檢測(cè)到N2和CO2,未檢出H2S和N2O.為繼續(xù)提升反硝化脫硫反應(yīng)器的效率,在第Ⅲ階段(50~70 d)縮短HRT到6 h,進(jìn)水硫化物、硝酸鹽和乙酸鹽負(fù)荷提高到0.80,0.37和0.31 kg·m-3·d-1,單質(zhì)硫轉(zhuǎn)化率仍然達(dá)95%,同時(shí)硫化物、硝酸鹽和乙酸鹽的去除率保持在95%以上.在第Ⅳ階段(70~80 d),HRT進(jìn)一步縮短到4 h,進(jìn)水硫化物、硝酸鹽和乙酸鹽負(fù)荷進(jìn)一步提高到1.23,0.52和0.45 kg·m-3·d-1,硫化物、硝酸鹽和乙酸鹽去除率下降到81%,69%和57%,單質(zhì)硫轉(zhuǎn)化率下降到80%以下.式(1)~(3)是由Reyes?Avila和陳川等[4,16,20]提出的自養(yǎng)反硝化微生物和異養(yǎng)反硝化微生物生化反應(yīng)式:

第Ⅳ階段(70~80 d),負(fù)荷進(jìn)一步提高,反應(yīng)器出水檢測(cè)到0.11 kg·m-3·d-1亞硝酸鹽,同時(shí)乙酸鹽去除率下降,說(shuō)明異養(yǎng)反硝化細(xì)菌活性受到抑制,這與陳川等[21]得到的結(jié)果一致.過(guò)量的亞硝酸鹽具有生物毒性,亞硝酸鹽的不斷積累也逐漸影響自養(yǎng)反硝化細(xì)菌的活性,破壞了自養(yǎng)微生物和異養(yǎng)微生物的協(xié)同作用,從而導(dǎo)致硫化物的去除率和單質(zhì)硫的轉(zhuǎn)化率逐漸下降[21].所以,當(dāng)HRT為4 h,反應(yīng)器體系超出所能承受的最大負(fù)荷.因此,該反應(yīng)器體系最適宜的運(yùn)行參數(shù)為HRT=6 h,進(jìn)水硫化物負(fù)荷0.80 kg·m-3·d-1、硝酸鹽負(fù)荷0.37 kg·m-3·d-1和乙酸鹽負(fù)荷0.31 kg·m-3·d-1.
2.2系統(tǒng)碳、氮、硫平衡及單質(zhì)硫分布
系統(tǒng)碳、氮、硫平衡及單質(zhì)硫分布情況在反應(yīng)器最適宜的運(yùn)行參數(shù)下進(jìn)行(HRT=6 h,硫化物負(fù)荷0.80 kg·m-3·d-1、硝酸鹽負(fù)荷0.37 kg·m-3·d-1和乙酸鹽負(fù)荷0.31 kg·m-3·d-1).反應(yīng)器系統(tǒng)運(yùn)行穩(wěn)定下的單質(zhì)硫產(chǎn)率見(jiàn)圖3,系統(tǒng)硫平衡見(jiàn)表1,平均94%的硫化物(S2--S)轉(zhuǎn)化為單質(zhì)硫S0.然而,在反硝化脫硫反應(yīng)器出水中只檢測(cè)到0.49 kg·m-3·d-1的單質(zhì)硫S0,約占單質(zhì)硫總量的65%.這是由于35%的單質(zhì)硫附著在顆粒污泥上沉淀在反應(yīng)器的底部.陳川等[4]利用一個(gè)EGSB反應(yīng)器同時(shí)去除硝酸鹽1.45 kg·m-3·d-1,硫化物3.1 kg·m-3·d-1和有機(jī)碳2.77 kg·m-3·d-1,并獲得了90%的單質(zhì)硫產(chǎn)率2.79 kg·m-3·d-1,高于本系統(tǒng)獲得的單質(zhì)硫產(chǎn)率.Reyes?Avila等[16]利用CSTR反應(yīng)器處理負(fù)荷0.29 kg·m-3·d-1Acetate?C,0.2 kg·m-3·d-1N3-?N和0.294 kg·m-3·d-1S2-?S,獲得了99%的單質(zhì)硫產(chǎn)率0.291 kg·m-3·d-1,低于本系統(tǒng)獲得的單質(zhì)硫產(chǎn)率.這些脫硫反硝化工藝只針對(duì)單質(zhì)硫的轉(zhuǎn)化率進(jìn)行討論,并未給出單質(zhì)硫在工藝系統(tǒng)中水相和污泥相的分布.本研究對(duì)反硝化脫硫系統(tǒng)單質(zhì)硫的分布進(jìn)行研究,得出單質(zhì)硫在水相約占65%,污泥相約占35%.這些研究為分別從水相和污泥相分離單質(zhì)硫提供基礎(chǔ)數(shù)據(jù).由表2可見(jiàn),每消耗1 g NO3--N產(chǎn)生0.797 g N2.在氣相中檢測(cè)出CO2和N2,未檢測(cè)出N2O和H2S.出水中沒(méi)有積累過(guò)量的有機(jī)碳和硝酸鹽,去除率均達(dá)94%以上.
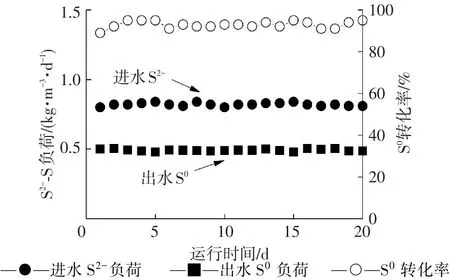
圖3 反硝化脫硫反應(yīng)器單質(zhì)硫產(chǎn)率
2.3生物硫特性及其分離方法的確定
2.3.1 生物硫的粒徑分布

表1 反硝化脫硫反應(yīng)體系中硫平衡
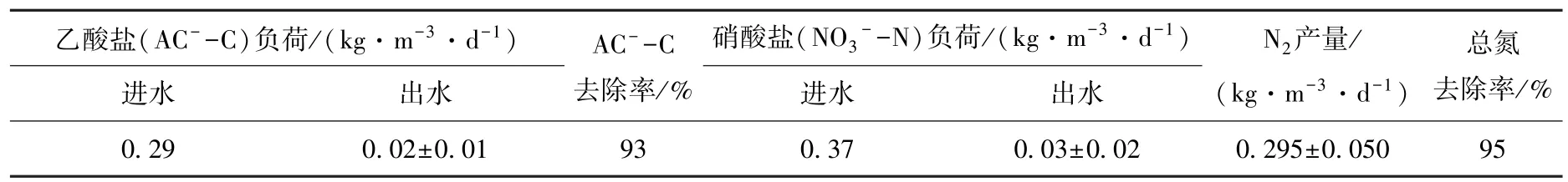
表2 反硝化脫硫反應(yīng)體系中碳、氮平衡

圖4 反硝化脫硫系統(tǒng)含生物硫出水
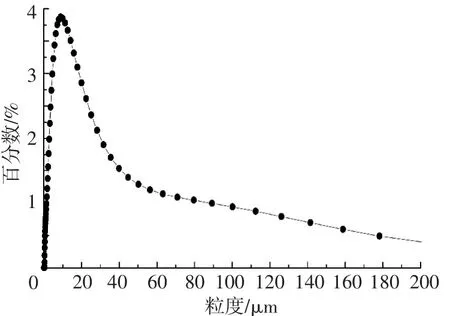
圖5 生物硫粒徑體積分布
2.3.2 生物硫掃描電鏡分析
通過(guò)電鏡掃描(SEM)對(duì)出水中生物硫顆粒的形貌特征進(jìn)行分析.由圖6可以看出,出水中線(xiàn)條、顆粒狀等多種形狀的物質(zhì)相互交錯(cuò)形成立體網(wǎng)狀結(jié)構(gòu),利于出水中生物硫的網(wǎng)捕凝聚和絮凝沉淀作用[23].圖7為生物硫顆粒的放大形貌,呈表面粗糙的球狀,攜帶大分子的聚糖、蛋白質(zhì)等多種官能團(tuán),官能團(tuán)帶電可使不同帶電物質(zhì)凝集形成絮體[24],生物硫的這些特點(diǎn)為其分離奠定了基礎(chǔ).

圖6 反應(yīng)器出水中生物硫形貌圖

圖7 生物硫顆粒的放大形貌圖
2.3.3 生物硫能譜分析
通過(guò)能譜分析得出生物硫顆粒的元素分布為:硫元素(S)質(zhì)量分?jǐn)?shù)約60.07%,同時(shí)含有碳(C)14.51%、氧(O)18.95%和鎂(Mg)6.47%等元素,這是因?yàn)樯锪蝾w粒外表面具有大分子有機(jī)物質(zhì)[24].
2.3.4 生物硫Zeta電位
Zeta電位是對(duì)顆粒之間相互排斥或吸引力強(qiáng)度的度量,是表征膠體體系穩(wěn)定性的重要指標(biāo)[25-26].分子或分散粒子越小帶有較多正或負(fù)同性電荷,Zeta電位(正或負(fù))越高,體系越穩(wěn)定,即溶解或分散可以抵抗聚集.反之,Zeta電位(正或負(fù))越低,越傾向于凝結(jié)或凝聚,即吸引力超過(guò)了排斥力,分散被破壞而發(fā)生凝結(jié)或凝聚[27].Moiler等[28]得出,膠體體系的Zeta電位絕對(duì)值大于30 mV可以獲得較好的穩(wěn)定體性,隨著Zeta絕對(duì)值增大,穩(wěn)定性越高.
本反硝化脫硫反應(yīng)器含生物硫出水的Zeta電位在±30 mV之間,平均為-20 mV,見(jiàn)圖8.表明生物硫的膠體分散體系不穩(wěn)定,同時(shí)由測(cè)定值得出生物硫顆粒帶負(fù)電荷.進(jìn)一步推斷,生物硫膠體顆粒可與正電荷物質(zhì)如陽(yáng)離子絮凝劑作用發(fā)生絮凝沉淀.生物硫顆粒的膠體特性進(jìn)一步為生物硫的絮凝分析提供了條件.
2.3.5 生物硫分離方法初探
取反硝化脫硫反應(yīng)器含生物硫出水放入燒杯中(如圖9(a)),將一束匯光線(xiàn)垂直照射含有生物硫燒杯,出現(xiàn)一條貫穿燒杯的乳紅色光柱,產(chǎn)生了丁達(dá)爾效應(yīng)現(xiàn)象,表明含生物硫出水具有懸濁液性質(zhì).通過(guò)投加1.67 mg/L的聚合氯化鋁,生物硫獲得了很好的分離,乳白色生物硫沉淀到燒杯底部(見(jiàn)圖9(b)).通過(guò)檢測(cè)上浮水單質(zhì)硫含量,獲得了99%的絮凝率和濁度去除率.證明利用混凝方法進(jìn)行生物硫的分離是可行的.

圖8 生物硫出水Zeta電位

圖9 混凝方法分離生物硫的效果
3 結(jié) 論
1)反硝化脫硫反應(yīng)器實(shí)現(xiàn)了94%的單質(zhì)硫最大產(chǎn)率,生物硫在反硝化脫硫工藝系統(tǒng)的分布為水相65%和污泥相35%.
2)通過(guò)對(duì)生物硫進(jìn)行粒徑分布、Zeta電位、能譜元素分析以及電鏡掃描等物化特性分析,得出生物硫具有膠體特性.初步利用陽(yáng)離子絮凝劑進(jìn)行生物硫的分離回收,獲得99%的分離率.為下一步生物硫的分離優(yōu)化工作提供了理論基礎(chǔ).
[1]DORMAN D C,STRUVE M F,GROSS E A,et al.Respiratory tract toxicity of inhaled hydrogen sulfide in Fischer?344 rats,Sprague?Dawley rats,and B6C3F1mice following subchronic(90?day)exposure[J].Toxicology and Applied Pharmacology,2004,198(1):29-39.
[2]JICKELLS T.External inputs as a contributor to eutrophication problems[J].Journal of Sea Research,2005,54(1):58-69.
[3]LIU Y,YANG S F,XU H,et al.Biosorption kinetics of cadmium(Ⅱ)on aerobic granular sludge[J].Process Biochemistry,2003(38):997-1001.
[4]CHEN C,REN N Q,WANG A J,et al.Simultaneous biological removal of sulfur,nitrogen and carbon using EGSB reactor[J].Applied Microbiology and Biotechnology,2008,78(6):1057-1063.
[5]REYES J,RAZO E,GOMEZ J.Simultaneous biological removal of nitrogen,carbon and sulfur by denitrification[J].Water Research,2004,38(14/15):3313-3321.
[6]王愛(ài)杰,杜大仲,任南琪,等.脫氮硫桿菌在廢水脫硫、脫氮處理工藝中的應(yīng)用[J].哈爾濱工業(yè)大學(xué)學(xué)報(bào),2004,36(4):423-425.
[7]CHEN C,REN N Q,WANG A J,et al.Enhanced performance of denitrifying sulfide removal process under micro?aerobic condition[J].Journal of Hazardous Materials,2010,179:1147-1151.
[8]JIANG GM,KELLER J.Sulfur transformation in rising main sewers receiving nitrate dosage[J].Water Research,2009,43(17):4430-6574.
[9]胡亮,何艷明,陳加希.硫酸鹽水污染狀況與控制技術(shù)[C]//中國(guó)環(huán)境科學(xué)學(xué)會(huì)學(xué)術(shù)年會(huì)優(yōu)秀論文集,2008:810-815.
[10]胡亮,陳加希,何艷明.硫酸鹽污水的污染狀況分析[J].云南冶金,2010,39(2):102-105.
[11]繆應(yīng)祺.廢水生物脫硫機(jī)理及技術(shù)[M].北京:化學(xué)工業(yè)出版社,2004.
[12]郝曉地,戴吉,魏麗.生物除硫理論與技術(shù)研究進(jìn)展[J].生態(tài)環(huán)境,2006,15(4):844-853.
[13]于文波,胡明成.硫酸鹽的環(huán)境危害及含硫酸鹽廢水處理方法[J].科技信息,2011(11):10401-10402.
[14]胡明成.硫酸鹽的環(huán)境危害及含硫酸鹽廢水處理技術(shù)[J].成都大學(xué)學(xué)報(bào):自然科學(xué)版,2012,31(2):181-184.
[15]CHEN C,WANG A J,REN N Q,et al.High?rate denitrifying sulfide removal process in expanded granular sludge bed reactor[J].Bioresource Technology,2009,100(7):2316-2319.
[16]REYES?AVILA J,RAZO?FLORES E,GOMEA J.Simultaneous biological removalofnitrogen,carbon and sulfur by denitrification[J].Water Research,2004,38(14):3313-3321.
[17]GOMMERS P J F,BULEVELD W,ZUIJDERWIJK F J M,et al.Simultaneous sulfide and acetate oxidation in a denitrifying fluidized bed reactor?II.measurements of activities and conversion[J].Water Research,1988,22(9):1085-1092.
[18]KRISHNAKUMAR B,MAJUMDAR S,MANILAL V B,et al.Treatment of sulphide containing wastewater with sulphur recovery in a novel reverse fluidized loop reactor(RFLR)[J].Water Research,2005,39(4):639-647.
[19]ZHOU X,LIU L,CHEN C,et al.Reduction of produced elementary sulfur in denitrifying sulfide removal process[J].Applied Microbiology and Biotechnology,2011,90(3):1129-1136.
[20]MANCONI I,CARUCCI A,LENS P,et al.Simultaneous biological removal of sulphide and nitrate by autotrophic denitrification in an activated sludge system[J].Water Science&Technology,2006,53(12):91-99.
[21]CHEN C,WANG A J,REN N Q,et al.Biological breakdown of denitrifying sulfide removal process in high?rate expanded granular bed reactor[J].Applied Microbiology and Biotechnology,2008,81(4):765-770.
[22]陶麗霞,王成端,向迎洪,等.絮凝沉淀處理含241Am廢水時(shí)絮凝體粒徑分布的影響因素初探[J].輻射防護(hù),2006,26(3):177-180.
[23]鄭懷禮,張會(huì)琴,蔣紹階,等.聚磷硫酸鐵的形貌結(jié)構(gòu)與絮凝機(jī)理[J].光譜學(xué)與光譜分析,2011,31(5):1409-1413.
[24]JANSSEN A J H.Sufrace characteristics and aggregation of microbiologically produced sulfur particles in relation to the process conditions[J].Colloids and Surfaces B:Biointefaces,1996,6:115-129.
[25]HUNTER,R J.Zeta potential in colloid science:principles and applications[M].San Diego:Academic Press Inc,1981:386.
[26]RUNKANA V,SOMASUNDARAN P,KAPUR P C.Mathematical modeling of polymer?induced flocculation by charge neutralization[J].Journal of Colloid and Interface Science,2004,270:347-358.
[27]楊錦,黃志杰,侯善華,等.磷酸銨鎂結(jié)石患者尿微晶組分分析及其與結(jié)石形成的關(guān)系[J].光譜學(xué)與光譜分析,2011,31(1):168-172.
[28]MOILER R H,JACOBS C.Buparvaquone mucoadhesive nanosuspension:preparation,optimisation and long?term stability[J].International Journal of Pharmaceutics,2002,237(1/2):151-161.
(編輯劉 彤)
Distribution characteristics and separation of biological sulfur in denitrifying sulfide removal process
YUAN Ye1,2,WANG Aijie1,2,MA Suli1,2,CHEN Chuan1,2,ZHAO Youkang1,2,TAN Wenbo1,2,HUANG Cong1,2,XU Xijun1,2,SUN Dezhi1,2
(1.School of Municipal and Environmental Engineering,Harbin Institute of Technology,150090 Harbin,China;2.State Key Laboratory of Urban Water Resource and Environment,Harbin Institute of Technology,150090 Harbin,China)
To better separate biologicalsulfur from denitrifying sulfide removal(DSR)process,we determined a new method by researching on the distribution characteristics of biological sulfur in this process system,Zeta potential,particle size distribution,scanning electron microscope and energy spectrum analysis.The results showed that the biological sulfur in the effluent and sludge accounted for 65%and 35%of the total sulfur production,respectively.S content of biological sulfur particles is no less than 60%.Zeta potential value is approximately-20 mV(between±30 mV);Biological sulfur particles are spherical with rough surfaces,with many functional groups on the surface such as polysaccharide and proteins.The above biological properties indicate that it has characteristics of colloid.The biological sulfur flocculation rate is approximately 99%when using cationic coagulant to separate biological sulfur.Coagulation is an effective method ofseparating biological sulfur form(DSR)process.
biological sulfur;distribution characteristics;characteristics of colloid;coagulation
X703.1
A
0367-6234(2014)08-0034-06
2013-03-15.
國(guó)家高技術(shù)研究發(fā)展計(jì)劃(863計(jì)劃)主題項(xiàng)目(2011AA060904).
遠(yuǎn) 野(1984—),男,博士研究生;
王愛(ài)杰(1972—),女,教授,博士生導(dǎo)師.
遠(yuǎn) 野,yuanye-19840915@163.com.

