UV法測定清潔驗證中殘留物依帕司他的含量
楊玉琴 季洪英 洪麗萍 黃加秀 李競梅 包衛國
依帕司他為醛糖還原酶抑制藥, 以可逆地抑制與糖尿病性并發癥的發病機制相關的多元醇代謝中葡萄糖轉化為山梨醇的醛糖還原酶而發揮作用, 其制劑唐林(依帕司他片)是本公司生產的主打暢銷品種, 由于其對糖尿病神經性病變的治療中的顯著療效而受到廣大患者的一致好評。本文主要圍繞依帕司他清潔驗證中的殘留物開展研究, 本文參考藥典方法[1]對主活性成分依帕司他的定量分析進行了研究和驗證,結果表明UV法簡便, 準確, 可以用于依帕司他的定量分析。
根據擦拭取樣的殘留量、設備中的總殘留限度、設備總內表面積計算得出依帕司他的殘留量LD值為5.3 μg/cm2,試驗中模擬設備材質的平板面積為100 cm2, 取樣回收率為100%, 換算為理論取樣量為530 μg, 于50 ml量瓶中以無水乙醇溶解并稀釋至刻度, 得到濃度約為10.6 μg/ml的溶液, 作者以此濃度開展相關研究和驗證。
1 儀器與試藥
瑞士Mettler Toledo XP205 電子分析天平, 美國Agilent8453紫外分光光度計等。
依帕司他對照品(批號為:100618-200401)購于中國藥品生物制品檢定所, 試劑均為分析純, 水為超純水。
2 方法與結果
2.1 紫外條件與方法 石英比色池規格:1 cm;檢測波長:292 nm;溶劑:無水甲醇;狹縫寬度:1.0 nm。
2.2 對照品溶液的配制 精密稱取依帕司他對照品適量,加流動相溶解制成每1 ml含265 μg的對照品貯備液。
2.3 線性關系試驗 分別精密吸取上述對照品貯備液適量,用無水乙醇稀釋制成濃度分別為:2.6 μg/ml、5.3 μg/ml、10.6 μg/ml、21.2 μg/ml、26.5 μg/ml、53 μg/ml的溶液 , 分別在 292 nm的波長處測定吸光度, 平行試驗兩份, 建立標準曲線, 以依帕司他濃度為橫坐標(X), 其吸光度值為縱坐標(Y), 得回歸方程為: Y=0.0358X-0.0061 相關系數r=1.0000.
結果表明依帕司他在 2.67 μg/ml~53.74 μg/ml范圍內 , 依帕司他對照品溶液濃度和其吸光度值具有良好的線性關系。2.4 檢測限(LOD)和定量限(LOQ) 以無水乙醇的空白溶液校零后, 測定空白的吸光度值11次, 對11次的結果求標準偏差值, 作為背景噪音。檢測限對應的信噪比為3:1, 定量限對應的信噪比為10:1, 將所得結果與線性關系試驗中所得標準曲線的斜率相除即得檢測限和定量限, UV法測定依帕司他的檢測限 (LOD)為 :0.013 μg/ml, 定量限 (LOQ)為 0.044 μg/ml。
2.5 精密度試驗 取濃度為10.608 μg/ml的依帕司他對照品溶液, 按樣品測定項下方法操作, 重復測定6次, 結果依帕司他的吸光度的均值為0.37653, RSD值為0.1%, 表明該方法精密度良好。
2.6 穩定性試驗 取濃度為10.808 μg /ml的供試品溶液,按樣品測定項下方法在25℃下放置考察, 在放置0、2、4、6、8 h后分別測定一次, 共測定5次, 5次吸光度值的RSD值為1.0%, 表明供試品溶液在8h內穩定。
2.7 重復性試驗 取批號為13070111的樣品, 按照“2.9”項下方法制備6份供試液, 結果依帕司他含量均值為100.40%,RSD為0.3%。
2.8 加樣回收率試驗 采用加樣回收法。計算得平均回收率為99.60%, RSD為0.2%, 結果見表1。
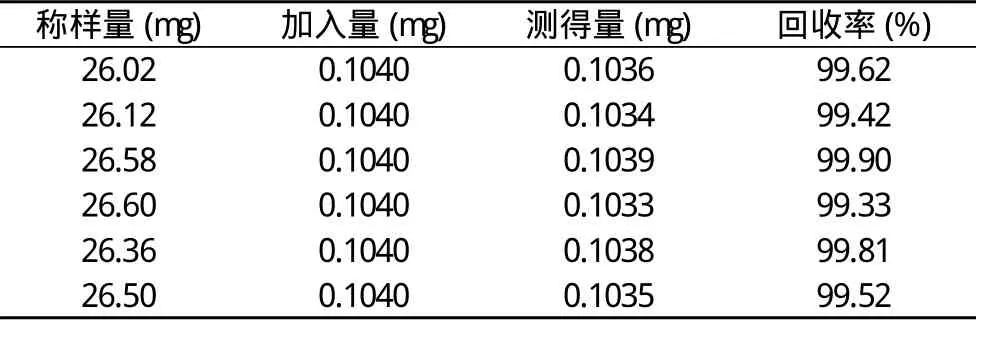
表1 加樣回收率試驗結果(n=6)
2.9 樣品含量測定 取本品, 精密稱定適量, 置100 ml量瓶中, 加無水乙醇振搖使依帕司他溶解并稀釋至刻度, 搖勻,再精密量取2 ml, 置50 ml量瓶中, 加無水乙醇稀釋制成每1ml溶液中約含10.6 μg的溶液, 作為供試品溶液。
3 小結
上述試驗的驗證結果表明UV法測定依帕司他清潔驗證中的殘留物依帕司他的含量可行, 該方法可用于依帕司他的定量分析。分別選取不同廠家和不同種類的溶劑作為擦拭溶劑, 結果選擇無水乙醇為擦拭溶劑較適宜, 因為依帕司他在無水乙醇中溶解完全, 且無水乙醇為揮發性溶劑, 可以在將殘留物依帕司他擦拭完全的同時有效減少溶劑殘留。
[1] 國家藥典委員會、中國藥典(二部) .北京:化學工業出版社,2010.

