十氫萘溶液中聚苯乙烯與常規載體的作用過程研究
黃輝,周俊濤,朱健煬,陶士英
(1.寧波工程學院 化工學院,浙江寧波 315016;2.寧波諾丁漢大學工程系,浙江 寧波 315100)
本文選用或制備聚苯乙烯加氫催化劑的常規載體,采用XRD和低溫氮氣吸附對其結構進行了分析表征,并在十氫萘溶液中考察了吸附溫度、聚苯乙烯初始濃度和吸附時間對載體與聚苯乙烯作用過程的影響,建立了載體對聚苯乙烯的吸附動力學模型,從聚苯乙烯分子結構的角度進行了分析,以期進一步了解聚苯乙烯與載體作用過程的機理,為開發聚苯乙烯加氫制聚環己基乙烯高效非均相催化劑提供理論依據。
1 實驗部分
1.1 試劑與儀器
十氫萘,優級純;聚苯乙烯、擬薄水鋁石、硅膠均為工業品。
SX2-4-10箱式電阻爐;D8 Advance X射線粉末衍射儀;ASAP 3020物理吸附儀;CGF-50微型高壓反應釜;UV7504紫外-可見光分光光度計。
1.2 載體的制備[3]
擬薄水鋁石在500℃焙燒4 h。自然冷卻,研磨、過篩,待用。大孔硅膠干燥、研磨、過篩后待用。
1.3 聚苯乙烯濃度的測定
在261.5 nm處,聚苯乙烯中的苯環對紫外光有吸收,而環己烷基則對紫外光無吸收,可以通過測定十氫萘溶液中苯環的吸光度計算苯環濃度。配制不同濃度的苯環溶液,分別測得其對應的吸光度,經線性擬合得到吸光度a與苯環溶度CPS的標準曲線方程為 CPS= -1.071 14 ×10-4+0.005 64a(R=0.999 1)。
1.4 實驗方法
取一定量的聚苯乙烯,溶于一定體積的十氫萘溶液中,并投入到50 mL微型高壓反應釜,升溫到150℃后,快速加入載體,用氮氣進行空氣置換,于封閉、1 000 r/min攪拌轉速下吸附24 h后,樣品經離心分離、稀釋定容后用紫外-可見光分光光度計測苯環濃度。并計算吸附率、吸附量。
聚苯乙烯吸附率=(溶液中聚苯乙烯初始濃度-吸附后溶液中聚苯乙烯的濃度)/溶液中聚苯乙烯初始濃度。
聚苯乙烯的吸附量=被吸附的聚苯乙烯質量/投入溶液中的所有聚苯乙烯質量。
2 結果與討論
2.1 載體表征
2.1.1 XRD Cu 靶,波長 λ =0.154 056 nm,Kα 輻射線,電壓 40 kV,電流 450 mA,掃描速率 10(°)/min,掃描步寬0.02°,2θ掃描范圍10~90°。焙燒后的擬薄水鋁石和預處理過的硅膠樣品的XRD圖譜見圖1。
由圖1可知,衍射峰分別為γ-Al2O3和SiO2的典型特征峰。
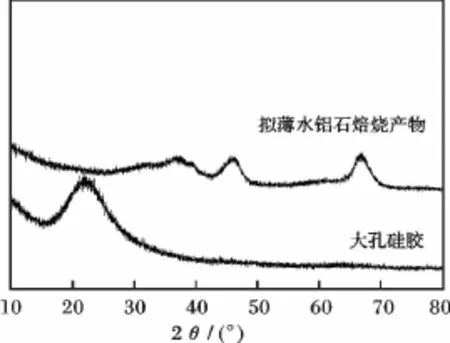
圖1 載體γ-Al2O3和SiO2的XRD圖譜Fig.1 XRD patterns of γ-Al2O3and SiO2
2.1.2 低溫氮氣吸附 圖2為載體 γ-Al2O3和SiO2的氮氣吸附-脫附等溫線(a)和對應的孔徑分布圖(b)。

圖2 載體γ-Al2O3和SiO2的氮氣吸附-脫附等溫線和孔徑分布圖Fig.2 N2Adsorption-desorption isotherm and pore size distribution of γ-Al2O3and SiO2
由圖2可知,兩者均呈現出典型的IV型等溫線和H1滯后環,其中SiO2的孔徑分布較窄,主要集中在10 nm左右,而γ-Al2O3的孔徑分布則較寬,主要分布在5~30 nm。經計算,γ-Al2O3載體的BET比表面積為233.21 m2/g,孔容為 0.02 cm3/g,平均孔徑為16.35 nm;SiO2載體的 BET 比表面積為319.83 m2/g,孔容為 0.02 cm3/g,平均孔徑為 9.45 nm。
2.2 聚苯乙烯與載體的作用
2.2.1 吸附溫度的影響 在聚苯乙烯初始濃度為1.5%,吸附時間為24 h的條件下,分別考察了吸附溫度與SiO2、γ-Al2O3上聚苯乙烯的吸附量的關系,結果見圖3。

圖3 吸附溫度對不同載體上聚苯乙烯吸附量的影響Fig.3 Effect of adsorption temperature on adsorbed polystyrene over different carriers
由圖3可知,當吸附溫度從25℃上升到150℃時,SiO2對聚苯乙烯的吸附量從0.023 g/g逐漸增大到0.274 g/g,γ-Al2O3對聚苯乙烯的吸附量則從0.016 g/g增加到0.152 g/g。這是因為隨著溫度的上升,聚苯乙烯十氫萘溶液的粘度會逐漸下降,聚苯乙烯在溶液中的傳質阻力變小,擴散速率增大[4],使得在較高吸附溫度下的載體能夠吸附更多的聚苯乙烯分子。
2.2.2 初始濃度的影響 在吸附溫度為150℃、吸附時間為24 h的條件下,研究了聚苯乙烯初始濃度與SiO2、γ-Al2O3上聚苯乙烯的吸附量的關系,結果見圖4。
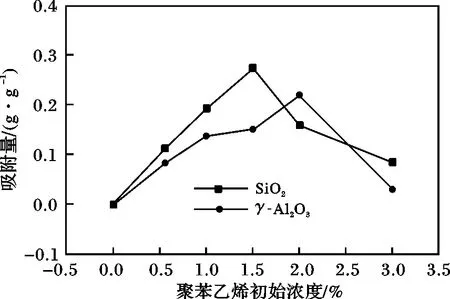
圖4 聚苯乙烯初始濃度對不同載體上聚苯乙烯吸附量的影響Fig.4 Effect of initial concentration on adsorbed polystyrene over different carriers
由圖4可知,在聚苯乙烯初始濃度為0~3.0%的范圍內,載體上聚苯乙烯的吸附量均經歷先增大,后又變小的過程,其中γ-Al2O3上聚苯乙烯的吸附量在聚苯乙烯初始濃度為2.0%時達到最大值0.22 g/g,而SiO2上聚苯乙烯的吸附量則在聚苯乙烯初始濃度為1.5%時即已經達到最大值0.274 g/g。在前面階段,聚苯乙烯的傳質驅動力濃度差隨著聚苯乙烯初始濃度的增大而增大,傳質速率越快,載體上吸附的聚苯乙烯量也就越多。而Gandhi等[5]發現,聚苯乙烯在十氫萘中的粘度ηr與聚苯乙烯濃度c及聚苯乙烯的數均分子量Mn呈一定的函數關系ηr=f(cM0.5n),因此在吸附溫度一定、聚苯乙烯分子量不變的情況下,聚苯乙烯十氫萘溶液粘度就會隨著聚苯乙烯初始濃度的增加而增大,聚苯乙烯在溶液中的傳質阻力變大,導致后面階段中載體上的聚苯乙烯吸附量減少。
2.2.3 吸附時間的影響 在溫度為150℃,濃度為2%的聚苯乙烯十氫萘溶液中,考察了聚苯乙烯和載體作用過程中吸附率與吸附時間的關系,結果見圖5。
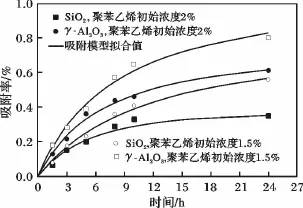
圖5 不同聚苯乙烯初始濃度下聚苯乙烯吸附率與吸附時間的關系Fig.5 Polystyrene adsorption rate vs.adsorption time under different initial concentrations
由圖5可知,十氫萘溶液中聚苯乙烯被載體γ-Al2O3和SiO2吸附的量均分別隨著時間的延長而增大,在 24 h時達到最值,分別為 γ-Al2O3時的61.4%和SiO2時的34.8%。吸附率的差異既與載體的用量有關,也會受到載體結構性質影響。在24 h的吸附時間下,γ-Al2O3和SiO2對聚苯乙烯的吸附量分別為 0.22 g/g和 0.158 g/g,說明 γ-Al2O3比SiO2能吸附更多的聚苯乙烯分子。
2.2.4 吸附動力學 根據文獻[6],十氫萘溶液中聚苯乙烯在載體上的吸附速率可以表示為:
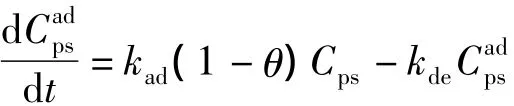
kad和kde——聚苯乙烯的吸附和脫附速率常數;
Cps——溶液中液相內聚苯乙烯的濃度,mol/L;
θ——聚苯乙烯在載體表面的覆蓋率。
為便于分析,忽略載體上聚苯乙烯的脫附過程,則kde為0。進一步將吸附在載體表面的聚苯乙烯分子簡化成寬l、高h的橢圓形,那么聚苯乙烯在載體表面的覆蓋率θ可定義為:

式中 V——溶液體積,L;
NAV——阿伏伽德羅常數,6.02 ×1023mol-1;
S——溶液中載體的表面積,m2;
A——橢圓形聚苯乙烯分子的橫截面
(A= πl2/4),m2。
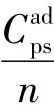
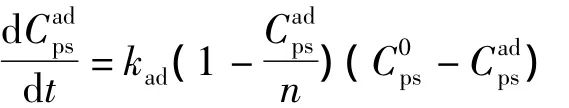
將上式積分,并代入初始條件,得到:
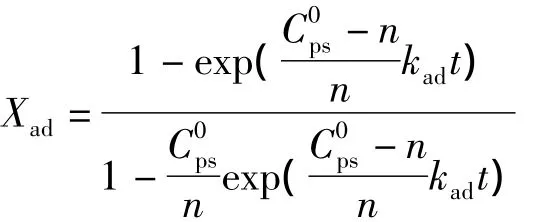
根據圖5中的實驗數據,經優化擬合得到吸附動力學模型常數及擬合效果,分別見表1和圖5。

表1 吸附動力學模型常數Table 1 Constants of the adsorption kinetic model
由表1和圖5可知,模型相關系數R均在0.98以上,實驗值與吸附動力學模型擬合值較為吻合;對于γ-Al2O3而言,聚苯乙烯初始濃度較高時的吸附速率更大,橢圓形聚苯乙烯分子的橫截面大小相近;而對于SiO2,聚苯乙烯初始濃度較高時,其吸附速率反而比低濃度的小,橢圓形聚苯乙烯分子的橫截面則比低濃度時的大。
假定吸附在載體上的橢圓形聚苯乙烯分子的體積與其在十氫萘溶液中的水力體積不變,那么存在:
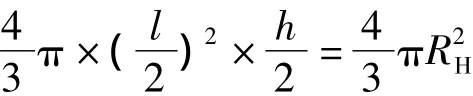
式中 RH——十氫萘溶液中聚苯乙烯分子的水力半徑,nm。
聚苯乙烯的水力半徑RH與聚苯乙烯的重均分子量的 0.588 次方成正比[7],再結合文獻[8]及表1中的A值,可得到吸附在載體上的聚苯乙烯分子的幾何尺寸情況,結果見表2。
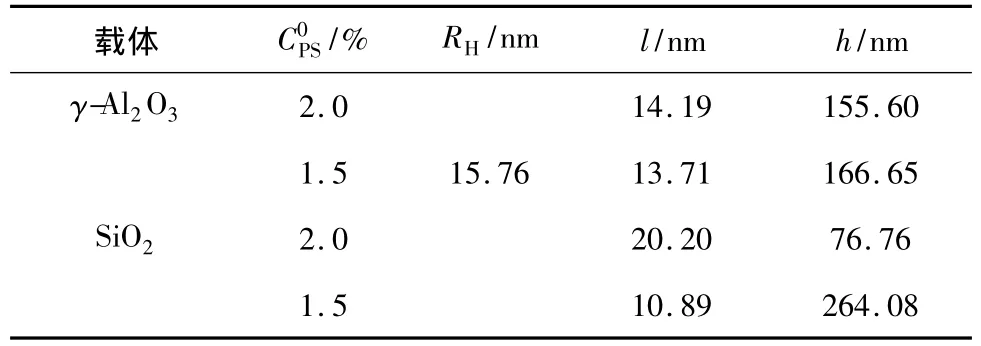
表2 載體吸附的聚苯乙烯分子的尺寸Table 2 Dimensions of adsorbed polystyrene molecules on carriers
由表2可知,聚苯乙烯初始濃度的高低對于最后吸附在γ-Al2O3上面的聚苯乙烯分子幾何形狀影響不大,而對吸附在SiO2上面的聚苯乙烯分子幾何形狀影響較大。聚苯乙烯的初始濃度較高時,其吸附的聚苯乙烯分子形狀顯得較低濃度時吸附的聚苯乙烯分子更寬、更矮。同時,2種載體上吸附的橢圓形聚苯乙烯分子的高度h均大于2RH,說明聚苯乙烯分子從十氫萘溶液中被吸附到載體上時,經歷構象變化,最后形成被拉伸的橢圓形結構,使得載體表面可以吸附更多的聚苯乙烯分子。
3 結論
(1)選用或制備了常規載體γ-Al2O3和SiO2,考察其在十氫萘溶液對聚苯乙烯的吸附過程。在吸附溫度25~150℃、聚苯乙烯初始濃度0~3.0%、吸附時間0~24 h等實驗研究范圍內,載體對聚苯乙烯的吸附量均隨著吸附溫度的升高而增大、隨著聚苯乙烯初始濃度的增大而出現先增大后減小的變化、隨著吸附時間的延長而增大。
(2)建立了載體γ-Al2O3和SiO2對十氫萘溶液中聚苯乙烯的吸附動力學模型,聚苯乙烯在吸附過程中經歷構象變化,最后在載體上呈現拉伸狀橢圓形分子結構。
[1]Scheirs J,Priddy D B.Modern Styrenic Polymers:Polystyrenes and Styrenic Copolymers[M].England:John Wiley& Sons Ltd,2003:533-556.
[2]黃輝,樊一帆,陶士英,等.聚苯乙烯催化加氫制備聚環己烷基乙烯的研究進展[J].化工新型材料,2013,41(4):178-179,181.
[3]Levin I,Brandon D.Metastable alumina polymorphs:Crystal structures and transition sequences[J].Journal of the American Ceramic Society,1998,81(8):1995-2012.
[4]Whittier R E,Xu D W,Zanten J H,et al.Viscosity of polystyrene solutions expanded with carbon dioxide[J].Journal of Applied Polymer Science,2006,99(2):540-549.
[5]Gandhi K S,Williams M C.Solvent effects on the viscosity of moderately concentrated polymer solutions[J].Journal of Polymer Science Part C:Polymer Symposia,1971,35(1):211-234.
[6]Kislenko V N,Berlin A A,Kawaguchi M,et al.Mathematical models of polymer adsorption at a porous adsorbent surface[J].Langmuir,1996,12(3):768-773.
[7]Akcasu A Z,Han C C.Molecular weight and temperature dependence of polymer dimensions in solution[J].Macromolecules,1979,12(2):276-280.
[8]Han K Y,Zuo H R,Zhu Z W,et al.High performance of palladium nanoparticles supported on carbon nanotubes for the hydrogenation of commercial polystyrene[J].Ind Eng Chem Res,2013,52(50):17750-17759.

