黃酒及其酸敗組分的高效毛細管電泳檢測方法的研究
陳乃東,胡 平,羅志強,馬 莉,李望遠
(1.皖西學院生物與制藥工程學院,安徽六安237012;2.皖西中藥與天然藥物工程技術研究中心,安徽六安237012;3.植物細胞工程安徽省工程技術研究中心,安徽六安237012)
黃酒及其酸敗組分的高效毛細管電泳檢測方法的研究
陳乃東1,2,3,胡 平1,羅志強1,馬 莉1,李望遠1
(1.皖西學院生物與制藥工程學院,安徽六安237012;2.皖西中藥與天然藥物工程技術研究中心,安徽六安237012;3.植物細胞工程安徽省工程技術研究中心,安徽六安237012)
黃酒生產與陳化過程中發生酸敗變質,是黃酒業面臨的頭等難題。本文中以黃酒原酒為對象,從檢測波長、緩沖液組成、分離電壓等方面對高效毛細管區帶電泳法檢測黃酒組分的條件進行研究。結果表明,選擇檢測波長215nm、0.075nmol/L的pH=10.0的磷酸氫二鈉-四硼酸鈉緩沖液、分離電壓8kV檢測,可以得到理想的黃酒原酒、黃酒料酒與酸敗黃酒原酒的高效毛細管區帶電泳圖譜。通過對比分析,確定導致酸敗的可能組分峰位于保留時間27.0~31.0min區段。研究結果為黃酒酸敗組分的檢出、質量標準構建及黃酒生產過程中的質量控制奠定基礎,具有一定的應用價值。
黃酒,高效毛細管電泳,酸敗
黃酒因酒精含量較低,在生產、陳化和儲運過程中易感染細菌而導致變酸甚至發臭,這種現象稱為酸敗,俗稱“起醭”。酸敗是我國黃酒業面臨的頭等難題[1-2]。輕度酸敗既降低原料出酒率,又損害了黃酒應有的風味,直接影響了黃酒的品質。重度酸敗時黃酒因變質而無法飲用,造成了大量的人力、物力損失,還會引發因清理困難而導致的環境污染[3-4]。酸敗現象已成為困擾黃酒生產企業、使黃酒生產成本居高不下的主要技術難題之一[5]。運用現代分析技術,建立黃酒酸敗組分檢測方法進而構建酸敗預警機制對降低黃酒酸敗的發生具有重要意義。
在黃酒生產中,多以味道是否變酸、發臭、目測是否“起醭”等感官手段判斷黃酒是否發生酸敗,這種全靠經驗的做法一旦發現已是深度酸敗。李勇波[1]、馮德明等[2]運用高效液相色譜法對黃酒的酸敗組分進行了探討,本實驗室[6]在前期實驗也對酸敗黃酒原酒的酸敗組分HPLC法檢測條件進行了研究,由于發生酸敗的黃酒pH較低(本實驗使用的酸敗黃酒原酒的pH=1~2),在色譜柱使用允許的pH范圍內,酸性較強的酸敗組分多以離子狀態存在,很難建立有效的酸敗組分檢出HPLC分析方法。
高效毛細管電泳技術以毛細管柱為分離通道,以高壓直流電源為驅動力對物質分子等進行高效分離和檢測[7-8],由于其進樣量少,分析速度快、效率高和樣品消耗少等優點,已廣泛應用于食品、藥品等的成分分析、質量標準的制定及質量控制[9-12],在緩沖液為堿性條件下,黃酒的組分尤其是酸敗組分均以離子狀態存在,在高壓電場驅動下,在毛細管柱中按荷質比不同實現分離。然而高效毛細管電泳用于黃酒酸敗組分研究尚未見報道。本文以黃酒原酒為研究對象,構建黃酒組分的HPCE檢測方法。在此基礎上,對酸敗的黃酒原酒進行對比分析,確定導致黃酒酸敗的可能組分,為進一步探討酸敗的基源、建立預防黃酒酸敗的質量控制方法、對黃酒釀造的各個環節中建立酸敗預警系統及黃酒生產工藝改進提供參考依據。
1 材料與方法
1.1 材料與儀器
硼酸 上海實意化學試劑有限公司;磷酸二氫鈉 南京化學四試劑一廠;四硼酸鈉 新科電化劑廠;氫氧化鈉 隴西化工股份有限公司,均為國產分析純;黃酒原酒、酸敗黃酒原酒、黃酒料酒 由黃酒原酒加入適當的調味品并稀釋而成的直接投入市場銷售的料酒,2012年4月26日從安徽禾裕黃酒集團有限公司生產車間隨機抽取,每種樣品抽取10個,采回后于4℃冰箱保存、備用。
TU1901紫外-可見分光光度計 北京普析;K1060型高效毛細管電泳儀 北京凱奧;42.8cm×45μm未涂層石英毛細管的毛細管 北京凱奧;精密pH試紙 上海三愛思。
1.2 實驗方法
1.2.1 樣品預處理 緩沖液、樣品黃酒原酒、黃酒料酒、酸敗黃酒原酒,測定前以稀鹽酸、碳酸鈉溶液調pH=3.0后,以0.45μm纖維素膜過濾后備用。
1.2.2 毛細管電泳的條件優化
1.2.2.1 電泳緩沖液的選擇 由于黃酒中含有大量的酸性成分,參考相關文獻[7-10]選擇硼砂、磷酸氫二鈉-四硼酸鈉作為候選緩沖溶液。
1.2.2.2 檢測波長的選擇 在200~400nm范圍掃描黃酒原酒,獲吸收光譜,進而確定HPCE檢測最佳波長。
1.2.2.3 分離電壓的選擇 在1.2.2.2確定的波長下,考察分離電壓為5.0、6.0、7.0、8.0、9.0、10.0、20.0kV時黃酒原酒的HPCE譜,對比分析,確定適合黃酒組分分析的分離電壓。
1.2.2.4 緩沖溶液pH的選擇 實驗選擇測定緩沖液的pH分別為8.0、9.0、10.0、11.0時黃酒原酒HPCE譜,根據測定結果選擇適合黃酒組分分離的緩沖液pH。
1.2.2.5 緩沖溶液離子濃度的選擇 在前幾步檢測的基礎上,考察緩沖液離子濃度對黃酒組分分離的影響。參考相關文獻[7-12],實驗考察離子濃度為0.025、0.05、0.075、0.1mmol/L時,黃酒原酒的HPCE譜,根據測定結果,選擇最佳緩沖液離子濃度。
2 結果與分析
2.1 緩沖體系的選擇
緩沖液體體系測定結果見圖1。用硼砂做緩沖液時,運行電流過大,有漏電現象,基線不穩,峰形不好,遷移時間重現性差。用磷酸氫二鈉-四硼酸鈉緩沖液時,黃酒各組分分離效果較好,峰面積和遷移時間的重現性好,基線也很穩定。因此選擇磷酸氫二鈉-四硼酸鈉作為緩沖溶液。
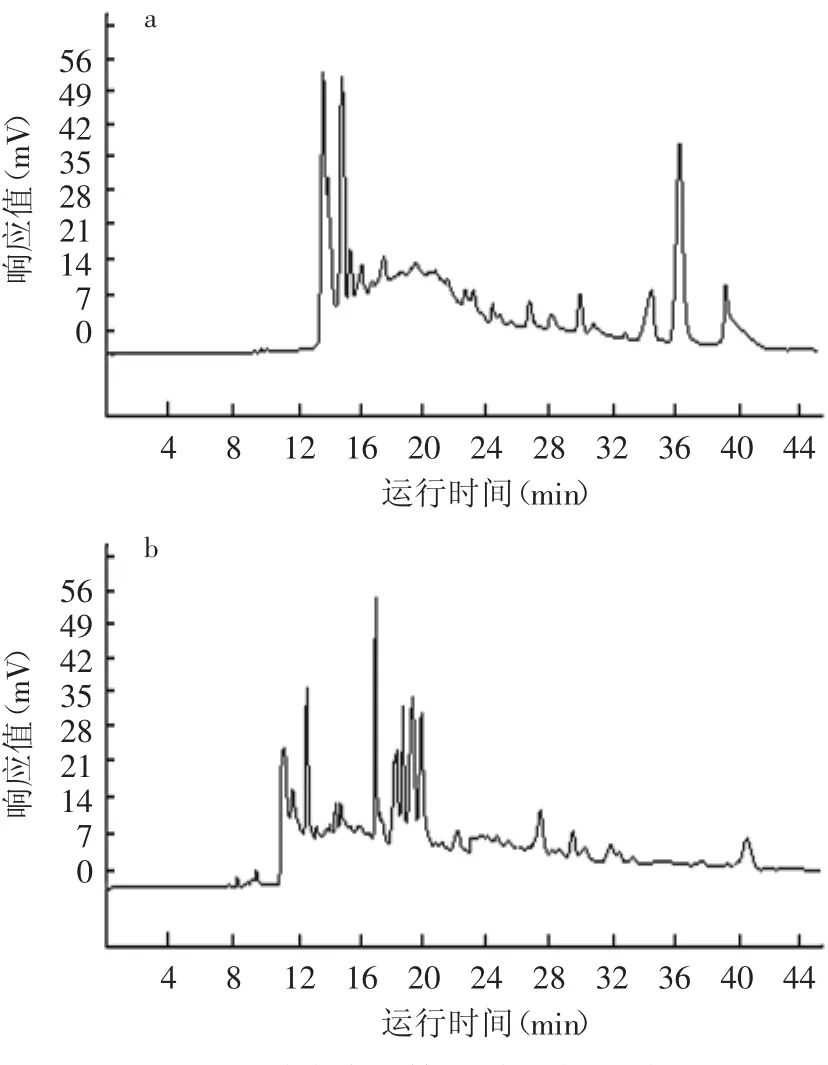
圖1 緩沖液對檢測結果的影響Fig.1 The HPCE graphs detected with different buffers
2.2 檢測波長的選擇
黃酒的200~400nm紫外掃描結果如圖2所示。
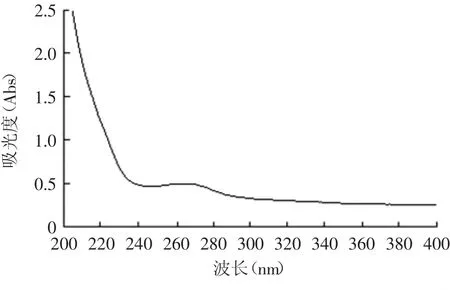
圖2 黃酒原酒的紫外吸收光譜Fig.2 The UV absorption spectrum of wine base
黃酒原酒在200~240nm,250~280nm波長范圍內有較強吸收,另外在365nm附近亦有弱吸收。實驗選擇了215、235、265和365nm作為檢測波長。分析檢測結果(圖3)可知,檢測波長在235、265和365nm時檢測不夠靈敏,峰面積較小。綜合考慮,選擇215nm作為黃酒組分分析的檢測波長。
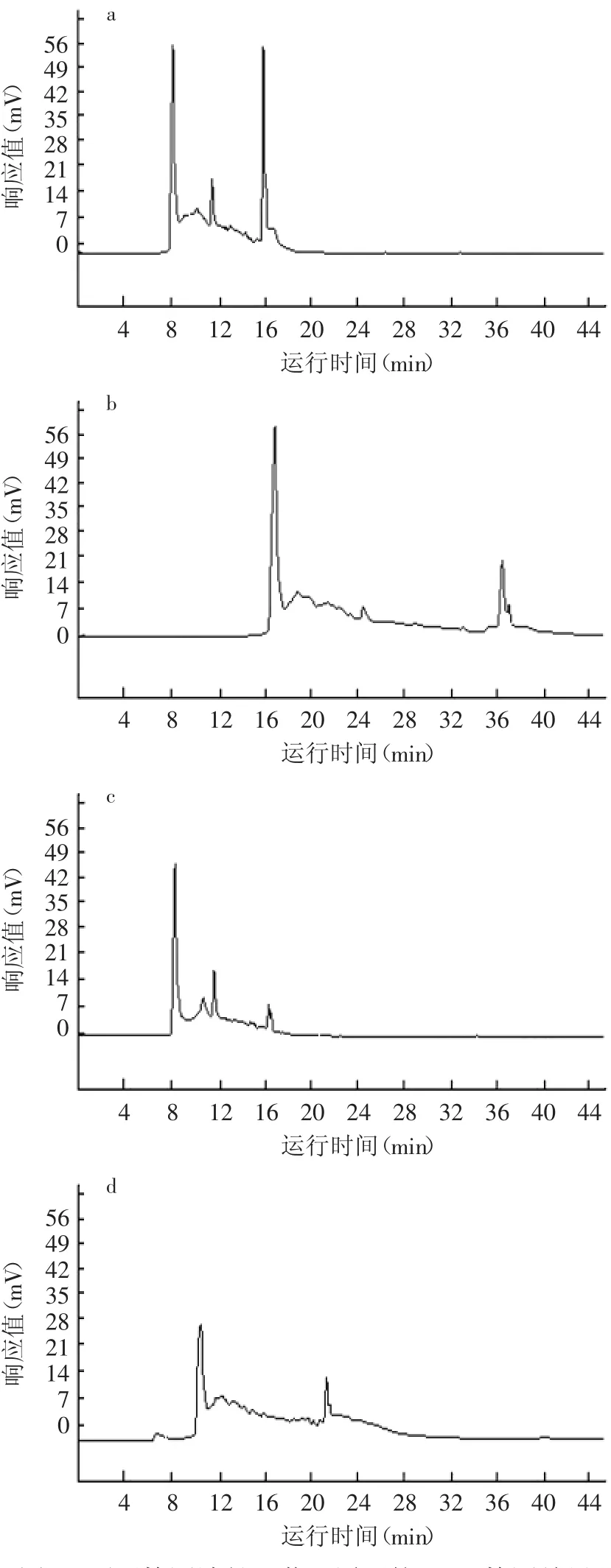
圖3 不同檢測波長下黃酒原酒的HPCE檢測結果Fig.3 The electrophoretograms of wine base detected with different wavelengths
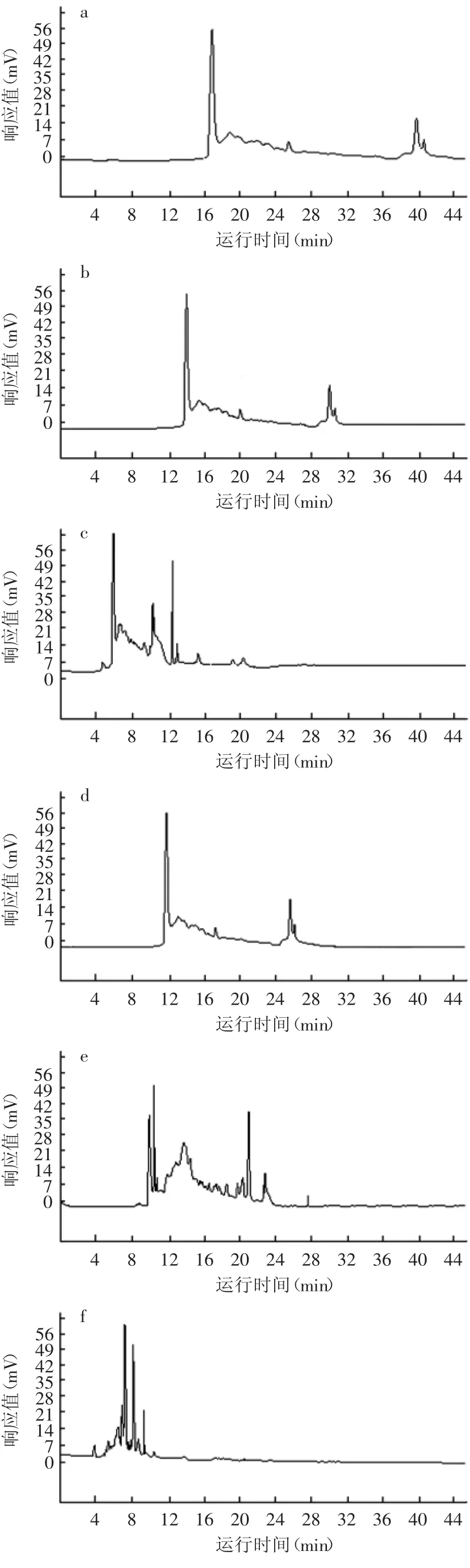
圖4 電壓對黃酒原酒組分分離的影響Fig.4 The electrophoretograms of wine base detected with different voltages
2.3 分離電壓的選擇
黃酒原酒在分離電壓分別為5.0、6.0、7.0、8.0、9.0、10.0、20.0kV時的HPCE測定結果如圖4所示。
分析測定結果,黃酒原酒各組分的出峰時間隨分離電壓的增加而提前。電壓10.0kV時,毛細管內電流過大,引起毛細管電解質產生自熱,柱效明顯下降;分離電壓達20.0kV時(圖4),各組分信號堆疊無法辨認;當電壓過低于7.0kV時,遷移時間延長,譜帶展寬,峰高降低,靈敏度下降。綜合考慮,選擇8.0kV作為分離電壓。
2.4 緩沖溶液pH選擇
由于黃酒中的物質多以酸性物質為主[13-18],導致了它在酸性和中性條件下基本不能電離,電泳中的遷移速度與溶劑相等,其吸收峰與溶劑峰重疊,從而使精確度和重現性變差。實驗選擇pH為8.0、9.0、10.0及11.0進行檢測。結果(圖5)表明,pH為10.0時,峰形較好,基線正常,峰面積和遷移時間的重現性好。因此選擇緩沖液的pH為10.0。
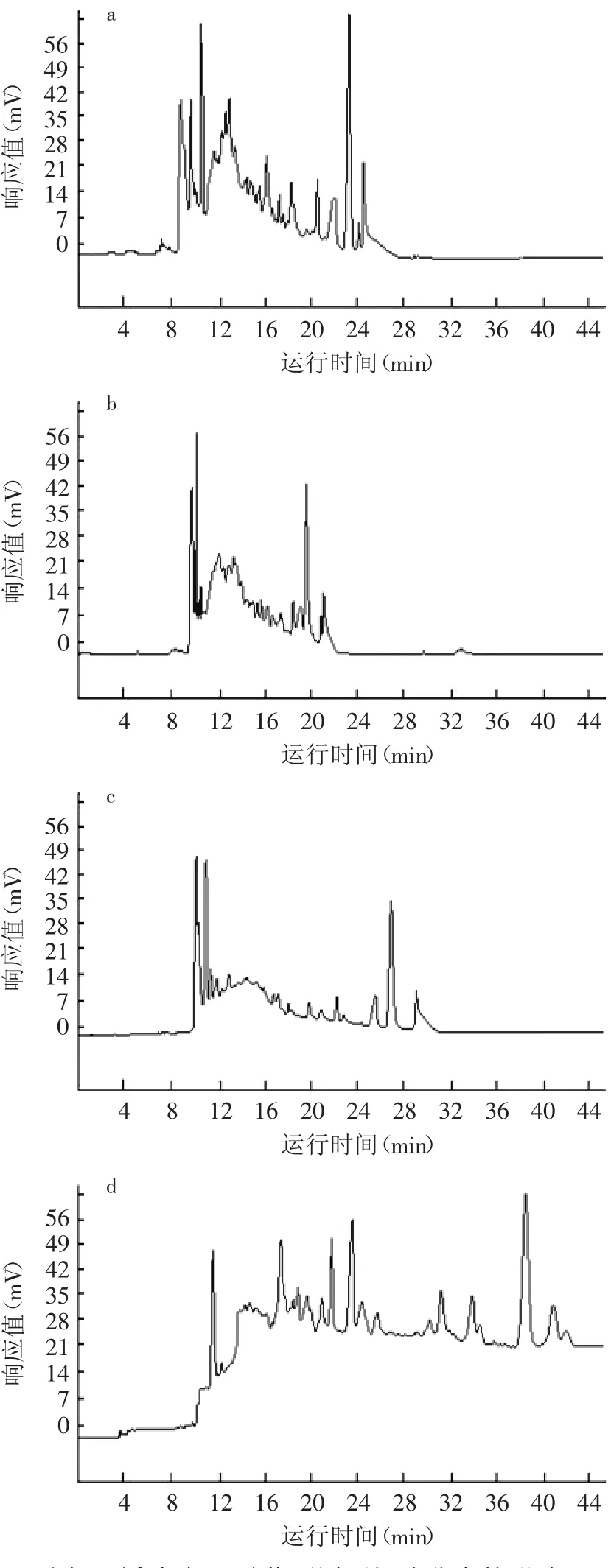
圖5 緩沖液pH對黃酒原酒組分分離的影響Fig.5 The electrophoretograms of wine base detected with different pH values of buffers
2.5 緩沖溶液離子濃度選擇
實驗考察了磷酸氫二鈉的濃度在0.025、0.05、0.075、0.1mmol/L時的基線、峰形、遷移時間和峰面積的重現性。實驗結果如圖6所示,可見,隨著濃度的增加,基線逐漸漂移,各組分保留時間延長;在低濃度時,峰形有拖尾且峰高逐漸增加的現象,在高濃度時出現基線漂移;整個過程中,遷移時間和峰面積的重現性都較好。綜合以上因素,選擇緩沖液離子濃度為0.075mmol/L。
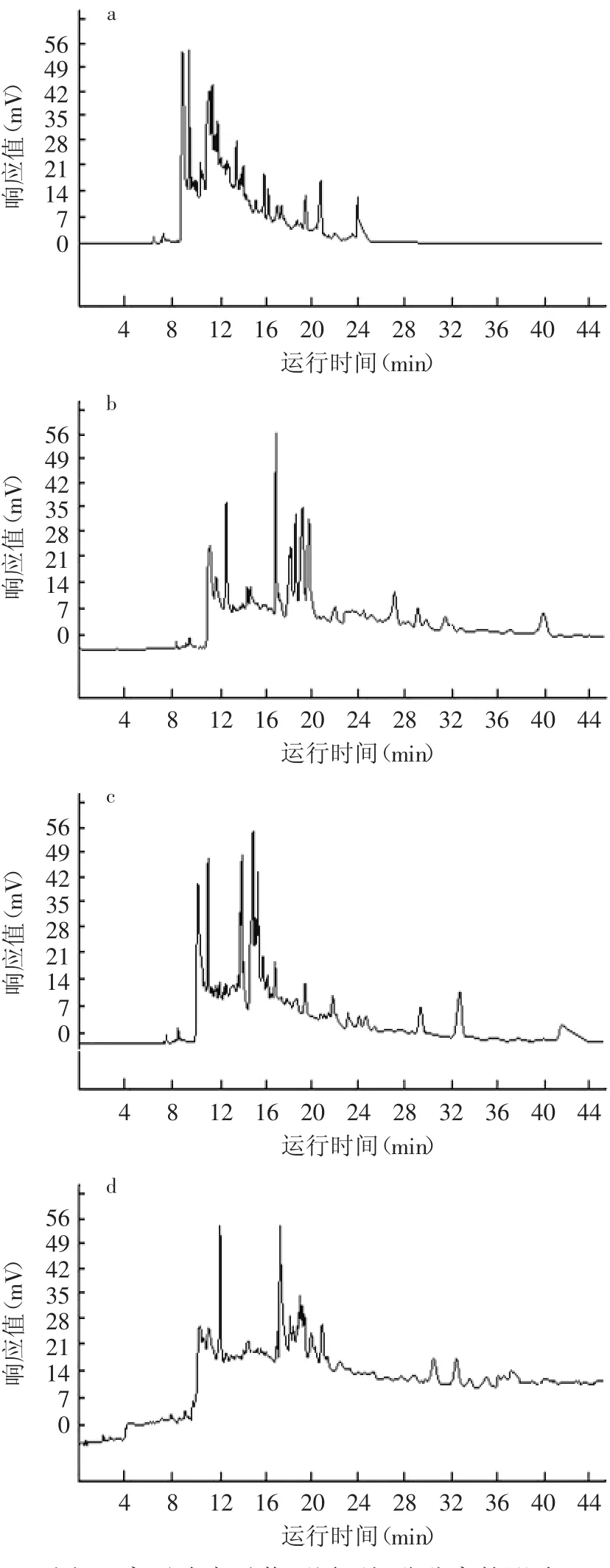
圖6 離子濃度對黃酒原酒組分分離的影響Fig.6 The electrophoretograms of wine base detected with different ion concentration of buffers
綜合上述實驗結果,確定黃酒組分HPCE分析條件為:pH=10.0的0.075mmol/L磷酸氫二鈉-四硼酸鈉、檢測波長215nm、分離電壓8.0kV。在此檢測條件下,大部分黃酒原酒組分達到基線分離。
2.6 黃酒原酒、酸敗黃酒原酒原酒、黃酒料酒組分分析
為了驗證依據上述實驗建立的分析條件的穩定性與重現性,采用上述最佳HPCE條件下,測得黃酒原酒結果如圖7a所示。在該條件下,黃酒原酒各組分基本實現基線分離,各組分出峰時間主要集中在11.0~14.0min(7個組分峰)和17.0~24.0min(11個組分峰)。此外,7.0~9.0min之間存在5個弱峰。多次重復測定,檢測到黃酒原酒的物質峰數量、各組分的保留時間、峰面積等重現性良好,證明實驗建立的黃酒原酒HPCE檢測方法穩定性、重現性較好。
同樣條件檢測黃酒料酒(圖7b),與黃酒原酒對比分析保留時間、相對峰位置、峰形等,在7.0~27.0min具有相同數量的組分峰,且均為共有峰。主要差別體現在黃酒料酒HPCE譜的37.0~44.0min增加了3個組分峰,可能是原酒加工成料酒過程中增加的風味組分。黃酒料酒是由黃酒原酒稀釋并加入適當的調味組分勾兌而來,其化學成分與黃酒原酒基本類似。二者的HPCE譜的相似性進一步證明實驗建立檢測方法的穩定性和重現性。
相同條件下檢測酸敗黃酒原酒(圖7c),與黃酒原酒對比分析其保留時間、相對峰位置、峰形,在11.0min前,未檢測到明顯組分峰,在11.0~14.0min只有三個峰(僅有一個為共有峰,tR=11.8min),17.0~ 24.0min部分僅有2個共有峰(tR=22.4min,23.6min)及三個小峰。在27.0~31.0min間,增加了5個峰,在tR= 46.3min處,新增了1個較強的峰。酸敗黃酒原酒與黃酒原酒、黃酒料酒HPCE檢測結果存在顯著差異。酸敗黃酒原酒是在生產黃酒原酒過程中混進有害微生物,其生長代謝消耗醪液中的營養物質,產生導致酸敗的物質形成的。因此,酸敗黃酒原酒的HPCE圖中新增的峰包含導致黃酒酸敗的部分或全部物質,在11~27.0min內缺失的共有峰代表有害微生物發酵所消耗的組分。生產過程滅菌不徹底導致有害微生物殘留或侵入是黃酒酸敗的主要原因。建立酸敗黃酒原酒組分高效毛細管電泳檢測方法,可用于黃酒生產環節中監控酸敗的產生及黃酒的質量評價和質量控制。此外,可從酸敗醪液中分離純化微生物,采用本實驗建立的檢測方法檢測這些微生物的發酵產物,通過檢測其在27.0~31.0min內及46.5min處與酸敗黃酒原酒共有峰的存在與否,追蹤可能導致黃酒酸敗的基源微生物,根據該微生物的習性,在生產過程中改進生產工藝,采取針對性滅菌或預防措施,抑制有害微生物侵入或生長,從而有效降低酸敗的發生,降低黃酒生產成本。本實驗可為這些后續研究奠定了基礎。
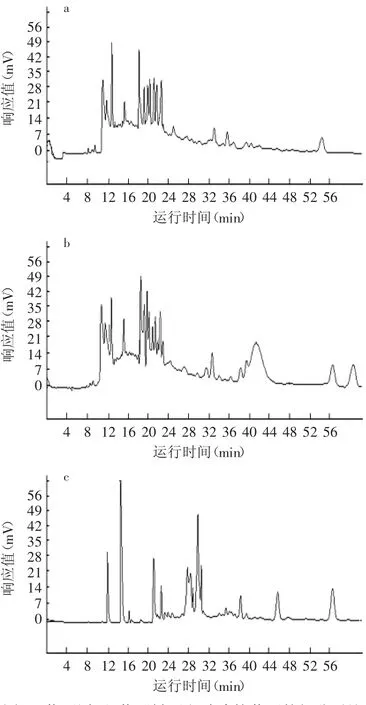
圖7 黃酒原酒、黃酒料酒和酸敗的黃酒的組分對比Fig.7 The HPCE analysis of wine base,marked and rancid Chinese rice wine detected with the established HPCE method
3 結論與展望
高效毛細管電泳法可有效檢測黃酒原酒、黃酒料酒及酸敗黃酒原酒的組分,其最適檢測條件為:pH=10.0的0.075mol/L磷酸氫二鈉-四硼酸鈉、檢測波長215nm、分離電壓8.0kV,在此條件下,可實現黃酒原酒、黃酒料酒及酸敗黃酒原酒組分的有效分離和檢出。在本實驗確立的最適檢測條件下,安徽禾裕黃酒有限責任公司生產中產生的酸敗黃酒原酒在HPCE圖上主要表現為在保留時間27.0~31.0min內及46.5min檢測到信號峰,可據此判斷黃酒或生產某個環節中的醪液是否發生酸敗。
[1]李勇波,賴櫻花,成堅,等.HPLC檢測客家黃酒酸敗前后有機酸變化及工藝優化[J].中國釀造,2011(11):178-182.
[2]馮德明,剝峙清,馬紅霞,等.黃酒酸敗時主要有機酸種類及含量分析[J].中國釀造,2010(1):125-128.
[3]蔡明迪,陳希,李汴生,等.超高壓處理對黃酒陳化的影響[J].食品與發酵工業,2011,37(1):26-31.
[4]朱一松,趙光鰲,帥桂蘭,等.超濾法生產的純生黃酒非生物穩定性的研究[J].食品與發酵工業,2005,31(2):26-29.
[5]夏艷秋,朱強,汪志君.黃酒醪液酸敗的影響因素及控制[J].食品與發酵工業,2004,30(7):33-37.
[6]陳乃東,陳乃富,王慶紅,等.黃酒成分HPLC分析[J].安徽農學通報,2012,18(13):177-178.
[7]朱金花,陳興國,劉繡華.高效毛細管電泳分離測定水中的乙酸和氯代乙酸[J].化學研究,2011,22(2):56-60.
[8]彭進進,羅澤嬌,李龍媛.高效毛細管電泳-二極管陣列檢測法測定土壤中的苯酚[J].分析科學學報,2012,28(1):98-100.
[9]汪紅,王強,羅輝明,等.丹參多糖的含量測定及高效毛細管電泳法測定其單糖組分[J].中華中醫藥·學刊,2007,25(4):827-829.
[10]王辰,黃慧玲,莫麗冬,等.腦蛋白水解物中多肽組分的高效毛細管電泳分析[J].中國醫藥,2012,7(5):603-605.
[11]陳盛余,鄧光輝,張桂華,等.高效毛細管電泳紫外檢測法分離檢測射干苷和鳶尾黃素[J].分析實驗室,2011,30(3):80-82.
[12]祝仕清,牛長群.高效毛細管電泳法/液質聯用分離與測控硫酸卷曲霉素各組分[J].中國抗生素雜志,2009,34(7):416-418.
[13]呂旭聰,黃志清,黃若蘭,等.反相高效液相色譜法同時快速測定黃酒和葡萄酒中有機酸的含量[J].食品與發酵工業,2010,36(6):132-136.
[14]鐘其頂,姚亮,熊正河.采用GC/MS和HPLC-ELSD 2種方法測定黃酒中的EC含量[J].食品與發酵工業,2007,33(3):115-119.
[15]江超,林峰,鄒慧君,等.陳年紹興黃酒的成分分析與品質鑒定[J].食品與發酵工業,2009,35(10):119-123.
[16]江偉,蘭玉倩,黃毅,等.固相微萃取與氣相色譜-質譜聯用法對不同酒齡黃酒的微量風味分析與應用[J].食品與發酵工業,2011,37(2):144-150.
[17]戴軍,謝廣發,陳尚衛,等.紹興黃酒中一種ACE活性抑制肽的分離和鑒定[J].食品與發酵工業,2005,31(5):98-101.
[18]俞關松.黃酒pH指標范圍的探討及超標的預防控制[J].食品與發酵工業,2002,28(1):76-78.
Study on establishment of HPCE method on the possible rancid constituents of yellow rice wine
CHEN Nai-dong1,2,3,HU Ping1,LUO Zhi-qiang1,MA Li1,LI Wang-yuan1
(1.College of Biotechnology and Pharmaceutical Engineering,West Anhui University,Liu’an 237012,China;2.West Anhui Biotechnology Research Center of Natural Medicine,West Anhui University,Liu’an 237012,China;3.Anhui Biotechnology Research Center of Plant Cell Engineering,Liu’an 237012,China)
Rancidity is a large challenge commonly encountered in Chinese rice wine business.In order to establish a convenient and operable assaying method for detecting main components and rancid constituents of yellow rice wine,HPCE zone electrophoresis was primarily explored involving wavelength,voltage and buffer solution including its kinds,the pH values and the ionic concentration.It was found that ideal electrophoretograms of wine base and its corresponding rancid sample as well as the marketed yellow rice wine could be obtained with wavelength 215nm,0.075nmol/L of disodic phosphate-sodium tetraborate buffer and 8.0kV of separation voltage.The remarkable differences existed between the rancid sample and the other two.These peaks represented potential rancid constituents of metamorphous Chinese rice wine could be determined by the established HPCE method.The result was helpful for the detection of rancid constituents,the establishment of quality standards and the quality control of Chinese rice wine in the future.
yellow rice wine;high performance capillary electrophoresis(HPCE);rancidity
TS255.1
A
1002-0306(2014)06-0069-06
10.13386/j.issn1002-0306.2014.08.006
2013-08-05
陳乃東(1972-),男,博士后,副教授,主要從事食品化學、天然藥物活性成分分離鑒定、中藥與天然藥物質量標準與質量控制方面的研究。
安徽省教育廳重點項目(KJ2012A277,KJ20108259);國家自然科學基金(81274021);安徽省自然科學基金(090413113);六安市定向委托皖西學院市級研究重點項目(2011LWA001);皖西學院研究性學習項目(WXXYX2013061,WXXYX2012064,WXXYX2012066)。

