超高效液相色譜-同位素稀釋質譜法測定配方奶粉中的泛酸
渠 巖,崔亞娟,李全霞,陳兆天,李 東,梁敏慧
(1.北京市營養源研究所,北京 100050;2.北京工業大學生命科學與生物工程學院,北京 100022)
超高效液相色譜-同位素稀釋質譜法測定配方奶粉中的泛酸
渠 巖1,崔亞娟1,李全霞1,陳兆天1,李 東1,梁敏慧2
(1.北京市營養源研究所,北京 100050;2.北京工業大學生命科學與生物工程學院,北京 100022)
建立測定配方奶粉中泛 酸的超高效液相色譜-同位素稀釋質譜方法。樣品經乙酸銨溶液提取、三氯甲烷除蛋白后,進行超高效液相色譜-串聯質譜分析,采用HSS T3液相色譜柱分離,以10 mmol/L乙酸銨溶液(含0.1%甲酸)和乙腈為流動相進行梯度洗脫,多反應監測模式,內標法定量。結果表明:方法定量限為0.040 mg/100 g,線性范圍內低、中、高3 個標準添加水平的回收率為96.9%~104.3%,相對標準偏差為3.78%~5.04%。該方法操作過程簡單、分析周期短、靈敏度高、重復性好,適用于奶粉中泛酸的測定。
泛酸;超高效液相色譜-同位素稀釋質譜方法;配方奶粉
泛酸又稱VB5或遍多酸,廣泛存在于生物體內,是生理代謝所必需的酸類物質。泛酸在酸、堿、熱及光等條件下都不穩定。泛酸是輔酶A的組成部分,參與體內蛋白質、碳水化合物的生理代謝,尤其是對脂肪的合成和代謝起著十分重要的作用[1]。根據《中國居民膳食營養素參考攝入量》[2],泛酸每日適宜攝入量為:嬰幼兒1.7~1.8 mg,未成年人2.0~4.0 mg,成年人5.0 mg,孕婦6.0 mg,乳母7.0 mg。
目前,配方奶粉中泛酸的國家標準檢測方法是微生物法和高效液相色譜法[3]。其中,微生物法[4-5]是測定泛酸的經典方法,但是該方法復雜費時,對環境條件要求高。高效液相色譜法[6-12]常用來檢測強化食品中的泛酸,但其所用的流動相均為磷酸鹽緩沖溶液,需要調節溶液pH值,過程復雜且容易受到其他添加劑的影響。除此以外,也有報道用免疫法、氣相色譜-質譜聯用法、高效毛細管電泳法、超臨界流體色譜法等[13-17]方法檢測泛酸。超高效液相色譜串聯質譜(ultra performance liquid chromatography-tandem mass spectrometry,UPLC-MSMS)法是一種在定性和定量方面都具有優勢的方法,具有較高的靈敏度和較強的分離能力,可以在短時間內分析低含量、多組分的樣品[18-20]。近年來,國外有報道利用泛酸的穩定同位素結合UPLC-MS-MS法測定食品中的泛酸[21-25],該方法被證實是一種快速、準確、靈敏的方法,然而國內相關研究卻鮮有報道。
1 材料與方法
1.1 材料與試劑
泛酸鈣(純度≥98.0%) 美國Supelco公司;泛酸鈣-[13C3,15N](純度≥99.5%) 美國IsoSciences公司;乙酸銨、甲酸(均為色譜純) 美國Sigma公司;乙腈(色譜純) 美國Fisher公司;三氯甲烷(分析純)北京化學試劑公司;實驗用水為超純水。
1.2 儀器與設備
Acquity@UPLC-Xevo TQ 型超高效液相色譜-串聯質譜聯用儀、Acquity@HSS T3柱 美國Waters公司;高速冷凍離心機 日本Hitachi公司;Vortex-Genie 2型漩渦振蕩器 美國Scientific Industries公司;BS224S型分析天平 德國Sartorius公司。
1.3 方法
1.3.1 溶液配制
泛酸標準溶液(100 μg/mL):稱取泛酸鈣10.87 mg,加水溶解至100 mL(泛酸質量濃度=泛酸鈣質量濃度×0.92);泛酸同位素標準溶液(100 μg/mL):稱取泛酸鈣-[13C3,15N] 1.09 mg,加水溶解至10 mL;10 mmol/L乙酸銨緩沖液:稱取乙酸銨0.385 4 g于500 mL容量瓶中,加水溶解并定容。
1.3.2 樣品處理
稱取奶粉樣品約5 g(精確至0.000 1 g)于150 mL三角瓶中,加入100 mL 40~50 ℃溫水,振搖溶解后超聲萃取10 min。取試樣溶液1 mL于50 mL離心管中,加入泛酸同位素標準溶液(由初步實驗確定添加量,確保試樣中泛酸和同位素泛酸質量相近),用10 mmol/L乙酸銨緩沖液定容至20 mL。渦旋振蕩1 min,超聲10 min。加入10 mL三氯甲烷,渦旋振蕩1 min,10 000 r/min離心10 min。上清液用0.22 μm gHP濾膜過濾,并轉移至棕色自動進樣瓶中。
1.3.3 色譜條件
色譜柱:HSS T3柱(2.1 mm×100 mm,1.8 μm);流速0.4 mL/min;柱溫40 ℃;樣品溫度15 ℃;進樣量10 μL;流動相A:10 mmol/L乙酸銨(含0.1%甲酸)溶液;流動相B:乙腈。梯度洗脫條件見表1。

表1 流動相梯度洗脫條件Table 1 Elution conditions for PA
1.3.4 質譜條件
電噴霧離子源;正離子模式;多反應監測模式;毛細管電壓1.5 kV;離子源溫度150 ℃;脫溶劑氣溫度500 ℃;錐孔氣流量(氮氣)50 L/h;脫溶劑氣流量(氮氣)1 000 L/h;碰撞氣流速(氬氣)0.17 mL/min。
泛酸和同位素泛酸的定量和定性離子對、錐孔電壓、碰撞能量等參數見表2。
表2 泛酸和同位素泛酸的定性和定量離子對、錐孔電壓和碰撞能量Table 2 Qualitative and quantitative ion pairs, cone voltages and collision energy for PA and PA-
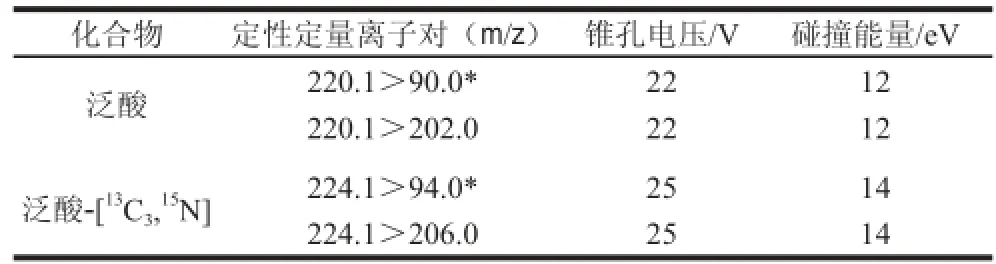
表2 泛酸和同位素泛酸的定性和定量離子對、錐孔電壓和碰撞能量Table 2 Qualitative and quantitative ion pairs, cone voltages and collision energy for PA and PA-
注:*.定量離子對。
化合物 定性定量離子對(m/z)錐孔電壓/V碰撞能量/eV泛酸220.1>90.0*2212 220.1>202.02212泛酸-[13C3,15N]224.1>94.0*2514 224.1>206.02514
2 結果與分析
2.1 樣品處理的優化
考察了不同提取劑的提取效果,用水和乙酸銨緩沖液分別提取,泛酸的回收率均在90%~110%之間。但由于不同樣品在水中的pH值不同,會影響泛酸在色譜柱上的保留時間和峰形。而利用乙酸銨緩沖液提取可以得到較穩定的保留時間和較好的峰形,因此選擇其作為提取劑。
奶粉中含有大量蛋白質,如不除去會使樣品混濁、無法進樣,更會縮短色譜柱壽命。因此,考察了三氯甲烷、高氯酸和調節pH值的除蛋白效果和對泛酸回收率的影響。結果顯示,3種方式都可以使蛋白沉淀,獲得澄清的樣品溶液。但高氯酸對泛酸的破壞性很大,處理過后的泛酸響應值顯著降低。而三氯甲烷和調節pH值這2種方式均對泛酸回收率無顯著影響,回收率分別為99.3%和96.3%。考慮到操作簡易省時,選擇添加三氯甲烷去除蛋白。
2.2 色譜與質譜條件的優化
2.2.1 色譜柱的選擇
比較了BEH C18柱(100 mm×2.1 mm,1.7 μm)、BEH Amide柱(100 mm×2.1 mm,1.7 μm)和HSS T3柱(100 mm×2.1 mm,1.8 μm)的分離效果(圖1)。因為泛酸屬于極性較強的化合物,它在C18柱和Amide柱上的保留較差,峰形也較差。而在對極性化合物有特殊保留能力的HSS T3柱上得到了較好的分離效果,且峰形好,響應值高,因此選擇HSS T3柱。

圖1 泛酸在3種色譜柱上的離子色譜圖Fig.1 Ion chromatograms of PA by using three columns
2.2.2 多反應監測條件的選擇
本研究使用UPLC-MS-MS方法,通過多反應監測方式進行采集。選擇目標物質的2對母離子>子離子,其中響應值較強的離子對作為定量離子對,另一對作為定性離子對。泛酸和同位素泛酸的多反應監測色譜圖、子離子掃描圖見圖2、3。
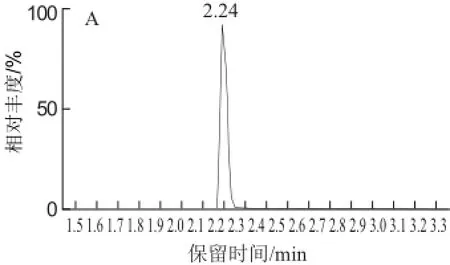

圖2 泛酸和同位素泛酸的離子色譜圖Fig.2 Ion chromatograms of PA and PA-[13C3,15N]

圖3 泛酸(A)和同位素泛酸(B)的子離子掃描圖Fig.3 Mass spectra of PA (A) and PA-[13C3,15N] (B)
2.3 方法的驗證
2.3.1 回收率
取已知泛酸含量的奶粉樣品,進行3 個標準添加水平(樣品中泛酸含量的50%、100%、150%)的回收率實驗,每個添加水平重復測定6次,分別計算加標回收率和相對標準偏差,結果見表3。泛酸3個水平的加標回收率在96.9%~104.3%,相對標準偏差在3.78%~5.04%,能夠滿足檢測實際樣品需要。

表3 泛酸加標回收實驗結果Table 3 Average recoveries and relative standard deviations of PA
2.3.2 線性范圍、檢出限和定量限
準確吸取泛酸標準溶液,分別添加泛酸同位素標準溶液,用10 mmol/L乙酸銨緩沖液稀釋成質量濃度為1、50、100、200、300、400、500 ng/mL的泛酸標準工作液,以峰面積比(A泛酸/A同位素)和同位素質量濃度的乘積為縱坐標、泛酸質量濃度為橫坐標,繪制標準曲線。結果表明,泛酸在1~500 ng/mL范圍內線性關系良好,線性回歸方程為Y=1.038 56X+0.953 334,相關系數r=0.999 9。根據定量離子信噪比(RSN)結合定量限加標回收實驗(回收率92.9%),確定檢出限(RSN≥3)為0.4 ng/mL,定量限(RSN≥10)為1.0 ng/mL。當取樣量為5 g、最終定容體積為20 mL時,檢出限和定量限分別為0.016 mg/100 g和0.040 mg/100 g。
2.3.3 方法精密度
取奶粉樣品按照1.3節中的方法,每日平行測定6次(n=6),連續測定3 d(n=3),考察方法的精密度,結果見表4。

表4 樣品中泛酸的測定結果Table 4 Results of PA determination in samples
2.3.4 與微生物方法的比對
微生物法是檢測泛酸的經典方法,同時也是GB 5413.17—2010《嬰幼兒食品和乳品中泛酸的測定》[3]的第一法。用微生物法和UPLC-MS-MS法同時對10種奶粉樣品做比對實驗(表5)。對實驗結果做t檢驗:平均差的95%置信區間,假設平均差=0(與平均差≠0),t=-0.519,P=0.309>0.05,表明2種方法測定結果無顯著差異,同時也證明了UPLC-MS-MS法測定結果的準確性。
然而由于微生物法操作復雜、培養耗時等因素,導致其檢測周期較長(3~4 d),不適于大量樣品的快速檢測。而UPLC-MS-MS法的樣品處理步驟簡單、操作省時,在保證分析結果準確的前提下,可以大幅縮短樣品的檢測周期,有利于提高檢測效率。

表5 泛酸含量測定微生物法和UPLC-MS-MS法對比Table 5 Comparison of microbiological method and UPLC-MS-MS mg/100 g
3 結 論
本研究通過對樣品前處理方法和UPLC-MS-MS條件優化,建立了一種可以快速檢測配方奶粉中泛酸的方法。本方法利用乙酸銨緩沖液提取、采用三氯甲烷除蛋白,得到了較好的提取效果。同時利用泛酸同位素作為內標,通過多反應監測模式進行信號采集,樣品回收率較高且穩定。本方法結果準確,與傳統的微生物法相比沒有顯著差異,而且方法操作過程簡單、分析周期短、靈敏度高、重復性好,適用于奶粉中泛酸的測定。
[1] 楊延輝, 肖春玲. 泛酸的功能和生物合成[J]. 生命的化學, 2008, 28(4): 448-452.
[2] 中國營養學會. 中國居民膳食營養素參考攝入[M]. 北京: 中國輕工業出版社, 2000: 350-356.
[3] 衛生部. GB 5413.17—2010 嬰幼兒食品和乳品中泛酸的測定[S]. 北京: 中國標準出版社, 2010.
[4] ANGYAL G. Methods for microbiological analysis of selected nutrients[J]. Journal of AOAC International, 1996, 8 (1): 41-45.
[5] 張旭, 馬妮, 鄭洪. 微生物法測定食品中泛酸 的含量[J]. 中國微生態學雜志, 2012, 24(7): 654-655.
[6] 林麗琴, 楊直, 石云峰. HPLC測定泛酸鈣的有關物質[J]. 中國現代應用藥學, 2012, 29(11): 10135-1038.
[7] 杜彥山, 張志國, 賈云虹, 等. 高效液相色譜法測定奶粉中泛酸[J].食品研究與開發, 2007, 28(6): 121-124.
[8] 劉志楠, 喻東威, 宋曉東, 等. 煙酸和泛酸不同方法檢測的對比[J].食品研究與開發, 2011, 32(11): 90-93.
[9] 楊發樹, 劉耀敏, 陳照. 反相高效液相色譜法測定預混合飼料中的D-泛酸[J]. 飼料研究, 2012, 35(8): 73-75.
[10] 劉志楠, 喻東威, 趙源, 等. 牛奶中泛酸含量測定[J]. 食品科學, 2012, 33(2): 177-180.
[11] 李少旦, 彭衛芳. 反相高效液相色譜法同時測定維生素B6、煙酰胺和泛酸鈣[J]. 理化檢驗: 化學分冊, 2009, 45(7): 800-802.
[12] PAKIN C, BERGAENTZLE M, HUBSCHER V, et al. Fluorimetric determination of pantothenic acid in foods by liquid chromatography with post-column derivatization[J]. Journal of Chromatography A, 2004, 1035(1): 87-95.
[13] HAUGHEY S A, O’KANE A A, BAXTER G A, et al. Determination of pantothenic acid in foods by optical biosensor immunoassay[J]. Journal of AOAC International, 2005, 88(4): 1008-1014.
[14] BANNO K, MATSUOKA M, HORIMOTO S, et al. Simultaneous determination of pantothenic acid and hopantenic acid in biological samples and natural products by gas chromatography-mass fragmentography[J]. Journal of Chromatography B, 1990, 525: 255-264.
[15] RYCHLIK M. Quantification of free and bound pantothenic acid in foods and blood plasma by a stable isotope dilution assay[J]. Journal of Agricultural and Food Chemistry, 2000, 48(4): 1175-1181.
[16] ZHANG Q, QIU J, LIAO N S. Simultaneous determination of calcium pantothenate and calcium-amino propionate and γ-butyrolactone by high performance capillary zone electrophories[J]. Chinese Journal of Analysis Laboratory, 2001, 20(1): 91-92.
[17] 程劼, 謝建春, 蘇曉鷗. 飼料中D-泛酸鈣的超臨界流體色譜測定[J].分析測試學報, 2010, 29(4): 418-420.
[18] LEPORATI A, CATELLANI D, SUMAN M, et al. Application of a liquid chromatography tandem mass spectrometry method to the analysis of water-soluble vitamins in Italian pasta[J]. Analytica Chimica Acta, 2005, 531(1): 87-95.
[19] CHEN Z, CHEN B, YAO S Z. High-performance liquid chromatography/ electrospray ionization-mass spectrometry for simultaneous determination of taurine and 10 water-soluble vitamins in multivitamin tablets[J]. Analytica Chimica Acta, 2006, 569(1): 169-175.
[20] LU B Y, REN Y P, HUANG B F, et al. Simultaneous determination of four water-soluble vitamins in fortified infant foods by ultraperformance liquid chromatography coupled with triple quadrupole mass spectrometry[J]. Journal of Chromatographic Science, 2008, 46(3): 225-232.
[21] RYCHLIK M, FREISLEBEN A. Quantification of pantothenic acid and folates by stable isotope dilution assays[J]. Journal of Food Composition and Analysis, 2002, 15(4): 399-409.
[22] RYCHLIK M. Simultaneous analysis of folic acid and pantothenic acid in foods enriched with vitamins by stable isotope dilution assays[J]. Analytica Chimica Acta, 2003, 495(1/2): 133-141.
[23] RYCHLIK M. Pantothenic acid quantification by a stable isotope dilution assay based on liquid chromatography-tandem mass spectrometry[J]. Analyst, 2003, 128(7): 832-837.
[24] GUTZEIT D, KLAUBERT B, RYCHLIK M, et al. Effects of processing and of storage on the stability of pantothenic acid in sea buckthorn products (Hippophaё rhamnoides L. ssp. rhamnoides) assessed by stable isotope dilution assay[J]. Journal of Agricultural and Food Chemistry, 2007, 55(10): 3978-3984.
[25] RYCHLIK M, ROTH-MAIER D. Pantothenic acid quantification: method comparison of a stable isotope dilution assay and a microbiological assay[J]. International Journal for Vitamin and Nutrition Research, 2005, 75(3): 218-223.
Determination of Pantothenic Acid in Formula Milk Powder Using Ultra Performance Liquid Chromatography-Isotope Dilution Mass Spectrometry
QU Yan1, CUI Ya-juan1, LI Quan-xia1, CHEN Zhao-tian1, LI Dong1, LIANG Min-hui2
(1. Beijing Research Institute for Nutritional Resources, Beijing 100050, China; 2. College of Life Science and Bio-enginee ring, Beijing University of Technology, Beijing 100022, China)
An ultra performance liquid chromatography-isotope dilution mass spectrometry (UPLC-IDMS) method has been developed for the determination for pantothenic acid (PA) in formula milk powder. Samples were extracted with ammonium acetate solution, and precipitated protein by adding chloroform for analyzing by UPLC-MS-MS. The analyte was separated using an HSS T3 column. The mobile phase consisted of 10 mmol/L ammonium acetate with 0.1% formic acid and acetonitrile. The PA was identified by multiple reaction monitoring (MRM) and quantified by internal standard method. The results showed that the limit of quantification for PA was 0.040 mg/100 g. The recoveries at three spiked levels and the relative standard deviations were 96.9%–104.3% and 3.78%–5.04%, respectively. This method proved to be simple, timesaving, sensitive and accurate for the determination of PA in formula milk powder.
pantothenic acid; ultra performance liquid chromatography-isotope dilution mass spectrometry; formula milk powder
TS207.3;O657.63
A
1002-6630(2014)08-0212-05
10.7506/spkx1002-6630-201408042
2013-08-01
北京市科技新星計劃項目(2011059);衛生行業科研專項項目(201202012);
北京市科委“雙十計劃”項目(Z121106002812109);北京市優秀人才培養資助項目(2011D002022000001)
渠巖(1984—),男,工程師,碩士,研究方向為食品分析。E-mail:quyan_0220@163.com

