S-8大孔吸附樹脂富集紫膠色酸
陳智勇
(中國林業科學研究院資源昆蟲研究所,國家林業局特色森林資源工程技術研究中心,云南 昆明 650224)
S-8大孔吸附樹脂富集紫膠色酸
陳智勇
(中國林業科學研究院資源昆蟲研究所,國家林業局特色森林資源工程技術研究中心,云南 昆明 650224)
以提取液中紫膠色酸的含量為指標,通過靜態吸附-解吸和動態吸附-解吸紫膠色酸提取液,確定S-8大孔吸附樹脂富集紫膠色酸的工藝參數。結果表明:S-8大孔吸附樹脂對紫膠色酸有良好的吸附性能,靜態吸附過程中S-8大孔吸附樹脂在30 ℃條件下吸附4.5 h后達到對紫膠色酸的最佳飽和吸附,吸附液流速為2 mL/min時,S-8大孔吸附樹脂達到動態飽和最佳吸附;解吸液為95%乙醇溶液、100 mL乙醇中加1.0 mL 2 mol/L的鹽酸溶液、解吸液流速3 mL/min時色酸富集效果好,解吸率大于90%;經20 次重復吸附/解吸后對紫膠色酸的解吸率依然達到89.50%,樹脂可多次重復使用;經大孔吸附樹脂富集精制后的紫膠色酸含量由24.77%提高至62.92%,純度提高了1.54 倍,富集后紫膠色酸的得率(以原膠質量計)達到0.52%,說明采用S-8大孔吸附樹脂富集紫膠色酸是可行的。
紫膠色酸;大孔吸附樹脂;富集
紫膠色酸是紫膠紅色素中蒽醌類化合物的統稱,是紫膠紅色素中的有效顯色物質[1-3]。紫膠色酸是一系列蒽醌衍生物的混合物,由于其多數衍生物均含有羧基,而呈現一定酸性[4-6]。目前已經發現的紫膠色酸有5 種,分別是紫膠色酸A、B、C、D、E,其基本結構極為類似,主要區別在于取代基的種類與位置不同[7-11]。由于紫膠色酸理化性質非常穩定,加之其天然、安全、無毒的優良特性,是食品、化妝品、醫藥及紡織品的優良著色劑[12-16],為我國允許用于食品添加劑的天然色素[17-18]。
紫膠色酸主要由紫膠蟲體經水洗、沉降、結晶而得到,由于紫膠蟲體中含有的糖、蛋白、灰分等雜質不可避免地進入到提取物中,因此需對其進行精制,以提高產品中紫膠色酸的含量[19-20]。然而,一直以來人們對紫膠色酸的提取技術關注較多,相關報道也較為常見[21-23],而對紫膠色酸的精制技術研究還不夠細致,尤其高純度紫膠色酸產品還很鮮見[24]。本研究以S-8大孔吸附樹脂為填料,采用樹脂吸附的方法將蒽醌類物質保留,實現紫膠色酸與雜質的有效分離,從而達到精制紫膠色酸的目的,為高純度紫膠色酸產品的開發和制備提供參考方法和理論依據。
1 材料與方法
1.1 材料與試劑
紫膠原膠,由中國林業科學研究院資源昆蟲研究所景東南亞熱帶實驗站提供,為云南紫膠蟲(K. yunnanensis Ou et Hong)原膠[25]。
S-8大孔吸附樹脂 天津市海光化工有限公司;鹽酸 天津市風船化學試劑廠;乙醇 天津市大茂化學試劑廠。
1.2 儀器與設備
CPC-505電導率儀 德國斯瑪特公司;AB204-S精密型電子天平 Mettler Tole
do中國有限公司;DU-800型紫外-可見分光光度計 美國Beckman-Coulter公司;SHZ-82恒溫振蕩器 金壇市富華儀器有限公司;HHS-11-2型電熱恒溫水浴鍋 江蘇省醫療器械廠;SLEVA-2轉盤離心機 德國Hermle Labortechnik公司;BCD-208K BS冰箱 青島海爾股份有限公司。
1.3 方法
1.3.1 大孔吸附樹脂的預處理
將S-8大孔吸附樹脂以無水乙醇浸泡3~4 h,然后以無水乙醇洗滌樹脂并放凈洗滌液,重復洗滌多次,直至向洗滌液中加入3 倍體積水不顯渾濁時停止。最后以去離子水淋洗樹脂至無乙醇氣味后離心脫水,并于冰箱中冷藏備用。
1.3.2 紫膠色酸原液制備
取原膠顆粒粉碎成1~6 mm顆粒后稱質量,按照紫膠與去離子水比1∶5(g/mL)取樣后,機械攪拌2 h,并以200 目細紗布過濾洗色液,重復提取6 次后,合并洗色液,以檸檬酸調整洗色液pH 3.5~4,攪拌澄清后采用濾膜過濾,取濾液備用。
1.3.3 S-8大孔吸附樹脂的吸附實驗
1.3.3.1 吸附溫度對S-8大孔吸附樹脂吸附能力的影響
精確稱量1.00 g經1.3.1節中預處理的S-8大孔吸附樹脂并置于100 mL三角瓶中,加入1.3.2節中制備的紫膠色酸原液50 mL,設置恒溫振蕩器溫度分別為20、30、40、50 ℃后,每30 min取一次上清液測定其吸光度并計算其質量濃度,直至紫膠色酸質量濃度不再降低為止,并按照式(1)、(2)計算各溫度條件下紫膠色酸的吸附量及吸附率隨時間的變化。
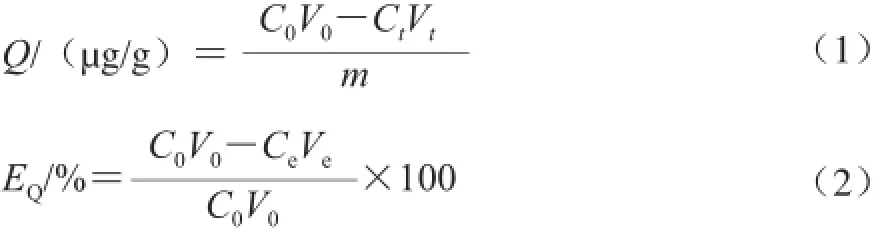
式中:Q為紫膠色酸在S-8大孔吸附樹脂上的吸附量/(?g/g);EQ為紫膠色酸在S-8大孔吸附樹脂上的吸附率/%; C0、Ct、Ce分別為吸附前、t時間和吸附后原液中紫膠色酸的質量濃度/(?g/mL);V0、Vt、Ve分別為吸附前、t時間和吸附后吸附液的體積/mL;m為S-8大孔吸 附樹脂的質量/g。
1.3.3.2 吸附液流速對S-8大孔吸附樹脂吸附能力的影響
精確稱量5.00 g經1.3.1節中預處理的S-8大孔吸附樹脂,采用濕法裝柱。取1.3.2節中已預處理的紫膠色酸原液,分別在吸附液流速為1.0、2.0、3.0、4.0、5.0 mL/min條件下流過上述預裝的吸附柱,每隔5 min取樣并測定流出液的吸光度At,并計算流出液中紫膠色酸的質量濃度Ct。以Ct=1/10C0為始漏點,合并到達始漏點前的流出液,以流出液中紫膠色酸的質量濃度Ct和體積Vt,計算吸附量和吸附率。
1.3.4 S-8大孔吸附樹脂的解吸實驗
1.3.4.1 乙醇體積分數對S-8大孔吸附樹脂解吸能力的影響精確稱量1.00 g經1.3.1節中預處理的S-8大孔吸附樹脂并置于100 mL三角瓶中,加入1.3.2節中制備的紫膠色酸原液50 mL,設置恒溫振蕩器溫度為30 ℃恒溫振蕩6 h,以去離子水洗滌去除殘余色素后吸干水分。配制體積分數分別為20%、40%、60%、80%和95%的乙醇溶液各50 mL,并以其解吸S-8大孔吸附樹脂12 h;在每50 mL不同體積分數的乙醇溶液中各加0.5 mL 2mol/L的鹽酸溶液,以提高解吸液對S-8大孔吸附樹脂的解吸能力。測定其吸光度并計算其質量濃度,按式(3)、(4)計算解吸量和解吸率。

式中:D為紫膠色酸在S-8大孔吸附樹脂上的解吸量/(?g/g);Cd為解吸液中紫膠色酸的質量濃度/(?g/mL);Vd為解吸液體積/mL;m為S-8大孔吸附樹脂的質量/g;ED為紫膠色酸在S-8大孔吸附樹脂上的解吸率/%;Q為紫膠色酸在S-8大孔吸附樹脂上的吸附量/(?g/g)。
1.3.4.2 鹽酸加入量對S-8大孔吸附樹脂解吸能力的影響
精確稱量1.00 g經1.3.1節中預處理的S-8大孔吸附樹脂并置于100 mL三角瓶中,加入1.3.2節中制備的紫膠色酸原液50 mL,設置恒溫振蕩器溫度為30 ℃恒溫振蕩6 h,以去離子水洗滌去除殘余色素后吸干水分。量取1.3.4.1節中洗脫效果較好的乙醇溶液50 mL,加不同體積2 mol/L的鹽酸溶液調酸,并以其解吸S-8大孔吸附樹脂12 h。測定其吸光度并計算其質量濃度,計算不同鹽酸加入量的乙醇溶液解吸量和解吸率。
1.3.4.3 解吸液流速對S-8大孔吸附樹脂解吸能力的影響精確稱量5.00 g經1.3.1節中預處理的S-8大孔吸附樹脂,采用濕法裝柱。按1.3.3.2節較佳流速動態吸附的條件上柱;采用1.3.4.1節及1.3.4.2節中較佳的洗脫液分別在1.0、1.5、2.0、2.5、3.0 mL/min流速條件下洗脫。每隔5 min測定流出液的吸光度At,并計算流出液中紫膠色酸的質量濃度Ct,以流出液的紫膠色酸質量濃度Ct為初始流出液吸光度的1/10時為終點,合并到達終點前所有流出液,測流出液中紫膠色酸的質量濃度Cd和體積Vd,計算解吸量和解吸率。
1.3.5 最佳條件下S-8大孔吸附樹脂對紫膠色酸的富集效果
在1.3.3節及1.3.4節中確定的最佳吸附、解吸條件下,取紫膠色酸原液50 mL,按照文獻[24]中方法測定其紫膠色酸含量T0后,以S-8大孔吸附樹脂對紫膠色酸原液進行吸附和解吸實驗,收集解吸液后測定解吸液的體積V1和解吸液的質量濃度C1,并計算紫膠色酸的含量T1,并以原膠質量m0為基準計算富集后紫膠色酸的得率Y1。

1.3.6 S-8大孔吸附樹脂的動態重復性實驗
精確稱量5.00 g經1.3.1節中預處理的S-8大孔吸附樹脂,采用濕法裝柱。取1.3.2節中已預處理的紫膠色酸原液,在1.3.3.2節中較佳的流速條件下,進行動態吸附。待S-8大孔吸附樹脂達到吸附飽和后,先以質量分數0.01% HCl溶液洗滌,目的是除去極性較強、水可以解吸的物質,再以乙醇溶液在上述得到的最佳解吸條件下解吸。分別收集上述動態吸附過程的解吸液及紫膠色酸原液,測定其吸光度At,并計算解吸液中紫膠色酸的質量濃度和解吸率。同一樹脂柱重復上述操作20 次,考察S-8大孔吸附樹脂的重復使用性能。
1.3.7 分析方法
按照文獻[24]中提供的方法進行如下步驟的吸光度測試:以移液管精確移取吸附液/解吸液,將含有紫膠色酸的吸附液/解吸液置于水浴鍋上蒸干,再按照文獻[24]中以質量分數0.5%醋酸鎂-甲醇溶液溶解顯色,在540 nm波長條件下測定吸光度,并帶入標準曲線計算測試樣中的紫膠色酸質量濃度。
2 結果與分析
2.1 S-8大孔吸附樹脂的吸附實驗
2.1.1 吸附溫度對S-8大孔吸附樹脂吸附能力的影響
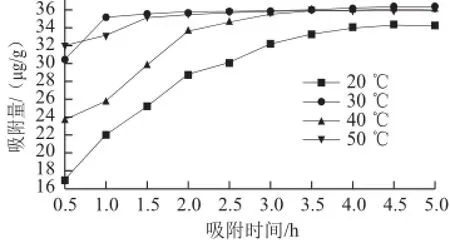
圖1 不同溫度條件下S-8大孔吸附樹脂吸附量隨時間的變化Fig.1 Adsorption quantity vs curves of S-8 at different temperatures
如圖1所示,在不同溫度條件下、5 h的吸附時間內,S-8大孔吸附樹脂對紫膠色酸的吸附量呈增大的趨勢,但就達到飽和吸附的速度而言,溫度對S-8大孔吸附樹脂有著較大的影響,溫度為30 ℃時大孔吸附樹脂的吸附量較高,且更快達到飽和吸附。

圖2 不同溫度條件下S-8大孔吸附樹脂吸附率隨時間的變化Fig.2 Adsorption rate vs time curves of S-8 at different temperatures
如圖2所示,隨吸附時間延長,S-8大孔吸附樹脂對紫膠色酸吸附率增加;5 h內S-8大孔吸附樹脂在30~50 ℃條件下逐漸趨于吸附飽和,吸附率均大于95%;而由吸附率曲線可見,S-8大孔吸附樹脂在30 ℃條件下吸附率達到最大,趨于飽和后隨著時間的延長吸附率基本維持穩定。綜合圖1與圖2的結果可知,S-8大孔吸附樹脂在30 ℃條件下吸附4.5 h后達到對紫膠色酸的最佳飽和吸附。
2.1.2 吸附液流速對S-8大孔吸附樹脂吸附能力的影響

圖3 吸附液流速對S-8大孔吸附樹脂吸附量的影響Fig.3 Effect of flow rate of the sample solution on adsorption quantity onto S-8
如圖3所示,隨著吸附時間的延長,S-8大孔吸附樹脂的吸附量逐次降低,總體來看,流速越快,曲線斜率越大,說明流速越快,吸附量降低的也就越快,這是因為吸附液流速越快時,單位時間內流過樹脂的紫膠色酸也就越多,因而大孔樹脂也就越容易達到飽和,但這并不意味著流速越大,樹脂吸附效果越好,因為樹脂的累積吸附量也是必須考慮的重要因素。
由圖4可以看出,隨著吸附液流速增加,S-8大孔吸附樹脂對紫膠色酸的累積吸附量增加,但大孔吸附樹脂的動態吸附過程不僅要考慮吸附量的大小,由于吸附率的高低決定了紫膠色酸原液的利用率和吸附效率,因此,吸附率的大小是動態吸附過程中吸附液流速考量的重要因素。各流速下,紫膠色酸吸附液的吸附量及吸附率如表1所示。
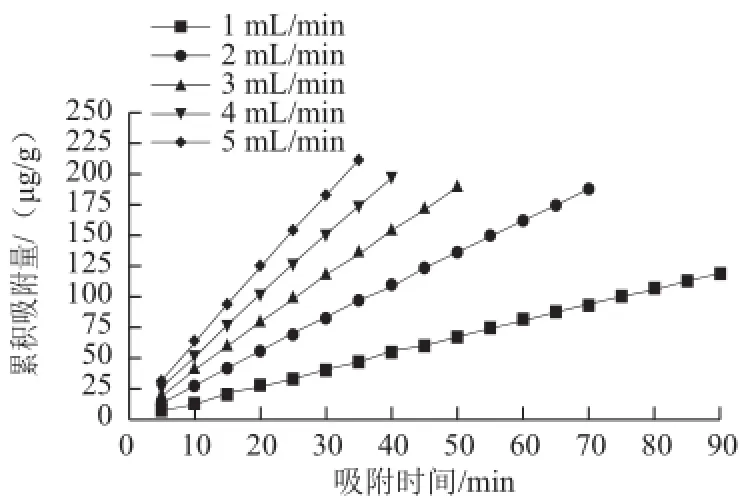
圖4 吸附液流速對S-8大孔吸附樹脂累積吸附量的影響Fig.4 Effect of flow rate of the sample solution on cumulative adsorption quantity onto S-8

表1 S-8大孔吸附樹脂達到始漏點的吸附參數Table 1 Adsorption parameters of S-8 at the starting leakage point
由表1可知,當吸附液流速為2 mL/min時,S-8大孔吸附樹脂對紫膠色酸的吸附率達到最高,而隨著吸附原液流速繼續增大,吸附率明顯降低。此外,當動態吸附過程中流速過快時,由于吸附液與大孔吸附樹脂表面接觸的時間過短,原液中的溶質分子來不及擴散至樹脂表面時就會發生樹脂漏液現象,從而降低了樹脂對原液的吸附效率。綜上可見,吸附液流速為2 mL/min時,S-8大孔吸附樹脂對紫膠色酸的吸附效率最佳。
2.2 S-8大孔吸附樹脂的解吸實驗
2.2.1 乙醇體積分數對S-8大孔吸附樹脂解吸能力的影響
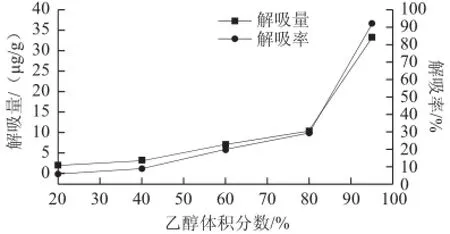
圖5 不同體積分數的乙醇解吸液對S-8大孔吸附樹脂解吸能力的影響Fig.5 Effect of ethanolconcentration on desorption rate
由圖5可以看出,乙醇體積分數對S-8大孔吸附樹脂的解吸影響顯著,隨著乙醇體積分數的增大,樹脂解吸率由5.76%增加至92.36%。可見,增大解吸液中乙醇的體積分數有利于S-8大孔吸附樹脂中紫膠色酸的高效解吸。
2.2.2 解吸液加酸量對S-8大孔吸附樹脂解吸能力的影響
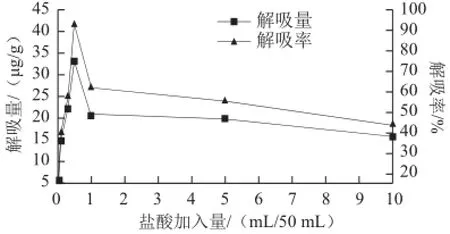
圖6 加酸量對S-8大孔吸附樹脂解吸能力的影響Fig.6 Effect of different amounts amount of hydrochloric acid added to aqueous ethanol on desorption capability of S-8
由圖6可知,鹽酸的加入明顯改變乙醇溶液對S-8大孔吸附樹脂的解吸能力。由圖6可以看出,少量鹽酸的加入即可達到較好的解吸效果,在每50 mL 95%乙醇鹽酸用量為0.5 mL時,解吸能力達到最大,解吸率達到92.36%,而后隨著鹽酸濃度的持續增大,解吸率明顯降低。可見,50 mL 95%乙醇中加入0.5 mL 2 mol/L的鹽酸時,其解吸效果最好,解吸率最高。
2.2.3 解吸液流速對樹脂解吸能力的影響
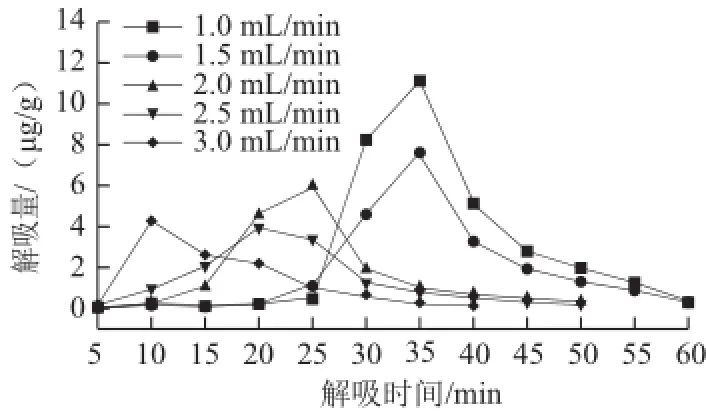
圖7 解吸液流速對S-8大孔吸附樹脂解吸量的影響Fig.7 Effect of flow rate of the desorption solution on desorption quantity of S-8
如圖7所示,隨著解吸液流速的增大,解吸曲線整體向左平移,即從S-8大孔吸附樹脂上解吸相同量的紫膠色酸所用的時間越短,可見適當增大解吸液流速有利于縮短解吸時間,但解吸液流速并非越大越好,因為還必須得考慮解吸的效率,為方便計算解吸率,各流速條件下S-8大孔吸附樹脂的累積解吸量曲線如圖8所示。
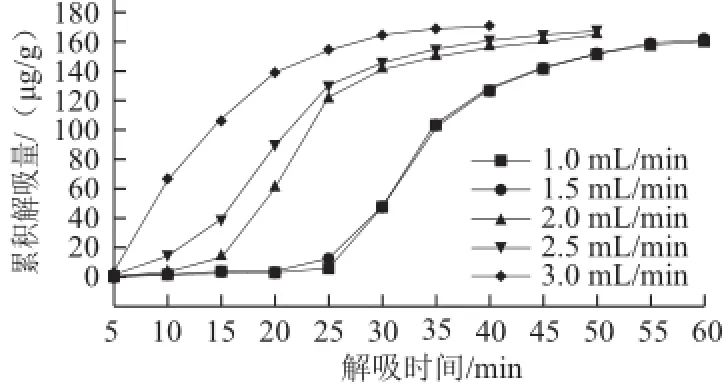
圖8 解吸液流速對S-8大孔吸附樹脂累積解吸量的影響Fig.8 Effect of flow rate of the desorption solution on cumulative desorption of S-8
由圖8可以看出,隨著解吸液流速的依次增大,S-8大孔吸附樹脂的累積解吸量依次增加,且當解吸液流速越大時,達到相同累積解吸量所需解吸時間也就越短,可見增大解吸液流速有利于S-8大孔吸附樹脂對紫膠色酸的解吸。各流速梯度下,S-8大孔吸附樹脂的解吸效率如表2所示。
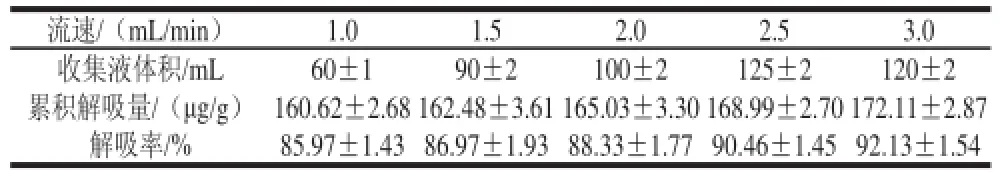
表2 S-8大孔吸附樹脂達到解吸終點解吸參數Table 2 Adsorption parameters of S-8 macroporous resin at the end of desorption
由表2可知,當解吸液流速為3 mL/min時,S-8大孔吸附樹脂對紫膠色酸的累積解吸量和解吸率達到最高,可將S-8大孔吸附樹脂中吸附的90%以上紫膠色酸成分充分洗脫下來,而隨解吸液流速減小,吸附量和吸附率均有所下降。
2.3 最佳吸附/解吸條件下S-8大孔吸附樹脂對紫膠色酸的富集效果
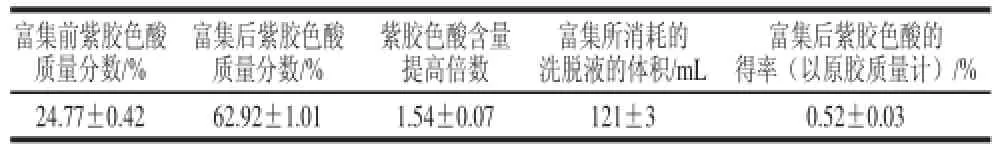
表3 S-8大孔吸附樹脂對紫膠色酸的富集效果Table 3 Enrichment performance of laccaic acid by S-8
由表3可見,在上述所得的最佳吸附、解吸條件下,S-8大孔吸附樹脂對紫膠色酸有較好的富集效果,紫膠色酸樣品質量分數由富集前的24.77%提高至62.92%,提高1.54倍,富集后紫膠色酸的得率達到了0.52%。
2.4 動態吸附/解吸驗證性實驗

圖6 S-8大孔吸附樹脂的重復使用性能驗證Fig.6 Reusability of S-8
由圖6可見,S-8大孔吸附樹脂重復吸附/解吸20 次,結果表明:以2.0 mL/min流速、140 mL紫膠色酸原液在30 ℃條件下吸附上柱,吸附時間4.5 h后達到動態飽和最佳吸附;然后用質量分數0.01% HCl溶液進行洗柱,再用濃度2 mol/L的鹽酸,按照鹽酸與95%乙醇 溶液體積比1∶100進行調和,120 mL調和液以3.0 mL/min流速解吸20次重復后,雖然解吸液中蒽醌平均質量濃度和解吸率有所下降,但變化幅度不大,經20 次重復吸附/解吸后對紫膠色酸的解吸率依然達到89.50%,表明S-8大孔吸附樹脂重復使用性好。
3 結 論
S-8大孔吸附樹脂對紫膠色酸有良好的吸附性能,靜態吸附過程中S-8大孔吸附樹脂在30 ℃條件下吸附4.5 h后達到對紫膠色酸的最佳飽和吸附;柱上動態吸附時,吸附液流速為2.0 mL/min,140 mL紫膠色酸原液在30 ℃條件下吸附上柱,吸附時間4.5 h后達到動態飽和最佳吸附。
S-8大孔吸附樹脂的最佳解吸條件為解吸液95%乙醇溶液、100 mL乙醇中加1.0 mL 2 mol/L鹽酸溶液、解吸液流速3 mL/min,此時色酸富集效果好,解吸率大于90%;經20 次重復吸附/解吸后對紫膠色酸的解吸率依然達到89.50%,樹脂可多次重復使用。
經S-8大孔吸附樹脂富集精制后的紫膠色酸含量由24.77%提高至62.92%,純度提高了1.54倍,富集后紫膠色酸的得率(以原膠質量計)達到0.52%,說明采用S-8大孔吸附樹脂富集紫膠色酸是可行的。
[1] 陳曉鳴, 陳又清, 張弘, 等. 紫膠蟲培育與紫膠加工[M]. 北京: 中國林業出版社, 2008: 44-46.
[2] 鄭華, 張弘, 張忠和. 天然動植物色素的特性及其提取技術情況[J].林業科學研究, 2003, 16(5): 628-635.
[3] 王祥榮, 侯學妮, 丁雷, 等. 紫膠紅色素的穩定性[J]. 紡織學報, 2008, 29(8): 67-70.
[4] 盧艷民, 周梅村, 鄭華, 等. 蒽醌類色素的特性和研究進展[J]. 林產化學與工業, 2007, 27(B10): 147-152.
[5] 張弘, 房桂干, 鄭華, 等. 紫膠紅色素穩定性研究[J]. 食品科學, 2009, 30(23): 65-69.
[6] 廖亞龍, 劉中華. 國內外紫膠深加工狀況及研發趨勢[J]. 食品工業科技, 2007, 28(8): 190-193.
[7] HIRATA K, UEMATSU Y, SUZUKI K, et al. Analysis of main pigments and other ingredients in lac color product[J]. Journal of the Food Hygienic Society of Japan, 2001, 42(2): 109-113.
[8] KATSUHIRO W, TAKATOSHI K, HIROMITSU A. Analytical and preparative separation of kaoliang and lac colors by pH-zone-refining CCC[J]. Journal of Liquid Chromatography and Related Technologies, 2005, 28(12/13): 2097-2106.
[9] OKA H, ITO Y, YAMASA S, et al. Identification of lac dye components by electrospray high performance liquid chromatographytandem mass spectrometry[J]. Journal of the Mass Spectrometry Society of Japan, 1998, 46(1): 63-68.
[10] 梅梅, 楊聞翰, 杜文霞. 果汁中天然色素紫膠紅的UPLC-TUV定量檢測及UPLC-MS-MS結構確證[J]. 分析測試學報, 2011, 30(12): 1338-1344.
[11] ITAKURA Y, UENO E, ITO Y, et al. Analysis of lac and cochineal colors in foods using reversed-phase thin-layer chromatography/ scanning densitometry[J]. Journal of Food Hygienic Society of Japan, 1999, 40: 183-188.
[12] 劉新民. 頗值得化妝品界開發利用的紫膠紅色素[J]. 廣西輕工業, 1994(4): 27-31.
[13] DIVYA R P, SINGH B, BABOO K M, et al. Evaluation of coloring efficacy of lac dye in comminuted meat product[J]. Journal of Food Science and Technology, 2011, 48(3): 378-381.
[14] DUBE D K, LOCH-CARUSO R, TROSKO J, et al. Assessment of the carcinogenic potential of a proposed food coloring additive, laccaic acid, using short term assays[J]. Cell Biology and Toxicology, 1984, 1(11): 111-125.
[15] HIRATA C, UEMATSU Y, SUZUKI K, et al. Analysis of lac color in diets and feces of rats for toxicity studies[J]. Journal of the Food Hygienic Society of Japan, 2002, 43(2): 110-113.
[16] CHIKKO S, NAOKO N, MASAYUKI T, et al. Inhibition of plasma hyaluronan-binding protein autoactivation by laccaic acid[J]. Bioscience, Biotechnology and Biochemistry, 2010, 74(11): 2320-2322.
[17] 凌關庭. 食品添加劑手冊[M]. 3版. 北京: 化學工業出版社, 2003: 988. [18] 廖亞龍, 劉中華. 國內外紫膠深加工狀況及研發趨勢[J]. 食品工業科技, 2006, 27(8): 190-195.
[19] 張弘, 房桂干, 鄭華, 等. 大孔吸附樹脂精制紫膠紅色素的研究[J].食品科學, 2010, 31(22): 232-236.
[20] 陳億遠, 劉佳銘, 莊全火, 等. 紫膠紅色素提取及其廢液治理的研究[J].齊齊哈爾輕工業學院學報, 1993, 9(2): 11-17.
[21] 劉躍明, 盧貴忠. 天然紫膠紫膠色素的特性及提取技術研究進展[J].云南農業大學學報, 2005, 20(1): 120-123.
[22] 鄭君秀. 紫膠紅色素提取工藝條件的優選[J]. 福州師專學報: 自然科學版, 1996, 16(1): 38-42.
[23] 曹銘, 周梅村, 唐莉英, 等. 紫膠色素提取方法的研究[J]. 食品科技, 2005, 30(2): 45-47.
[24] ZHANG Hong, FANG Guigan, ZHENG Hua, et al. Determination of anthraquinone content in lac dye through combined spectrophotometry and HPCE[J]. Procedia Engineering, 2011, 18: 86-94.
[25] 歐炳榮, 洪廣基. 云南紫膠蚧新種記述[J]. 昆蟲分類學報, 1990, 7(1): 16-17.
Enrichment of Laccaic Acid by S-8 Macroporous Resin
CHEN Zhi-yong
(Research Center of Engineering and Technology on Forest Resources with Characteristics, State Forestry Administration, Research Institute of Resources Insects, Chinese Academy of Forestry, Kunming 650224, China)
The conditions for static and dynamic adsorption and desorption by S-8 macroporous resin for enri ching laccaic acid were investigated by measuring the laccaic acid concentration in crude extract and eluates. The results showed that adsorption capability of S-8 macroporous resin was favorable to laccaic acid. In the static adsorption process, the resin exhibited maximum saturated adsorption at 30 ℃ after 4.5 hours. When the fl ow rate of the sample solution was 2 mL/min the dynamic adsorption achieved the maximum saturation level. The best enrichment results (more than 90% desorption rate) were obtained when the adsorbed laccaic acid was desorbed using 100 mL of 95% aqueous ethanol with 1.0 mL of 2 mol/L hydrochloric acid at a flow rate of 3 mL/min. The desorption rate remained as high as 89.50% after twentieth repeated use, suggesting good reusability of the sorbent. After the enrichment process, the purity of laccaic acid was increased from 24.77% to 62.92% with a purification factor of 2.54, and the yield of laccaic acid from lac was 0.52%. This study demonstrates the applicability of S-8 macroporous resin for enriching laccaic acid.
laccaic acid; macroporous adsorbent resin; enrichment
TQ028.3;TS264.4;S759.7;S899.2
A
1002-6630(2014)22-0017-05
10.7506/spkx1002-6630-201422004
2014-07-14
國家高技術研究發展計劃(863計劃)項目(2014AA021801)
陳智勇(1967—),男,高級工程師,博士,主要從事林業生物資源開發工程研究。E-mail:zychen@263.net

