催化熒光法測(cè)定蔬菜中痕量亞硝酸根的研究
劉永濤,云霞,那廣水*
(1.大連工業(yè)大學(xué)生物工程學(xué)院,遼寧大連116034;2.國(guó)家海洋環(huán)境監(jiān)測(cè)中心,遼寧大連116023)
催化熒光法測(cè)定蔬菜中痕量亞硝酸根的研究
劉永濤1,2,云霞1,那廣水2*
(1.大連工業(yè)大學(xué)生物工程學(xué)院,遼寧大連116034;2.國(guó)家海洋環(huán)境監(jiān)測(cè)中心,遼寧大連116023)
該研究建立了催化熒光分析法測(cè)定蔬菜中痕量NO2-的方法。NO2-可以催化中性紅的熒光褪色反應(yīng),且其含量與褪色反應(yīng)速率成正比。通過(guò)單因素試驗(yàn)以及均勻試驗(yàn)優(yōu)化了實(shí)驗(yàn)條件,確定了最佳的試劑因素組合。實(shí)驗(yàn)結(jié)果表明:在激發(fā)波長(zhǎng)λex=537 nm和發(fā)射波長(zhǎng)λem=595 nm,試劑因素組合中性紅900 μL,溴酸鉀1 850 μL,硫酸1 050 μL時(shí),方法NO2-測(cè)定的工作曲線為y=1.58x+0.46,相關(guān)系數(shù)r=0.999 5,線性范圍為0.02~0.11 mmol/L,檢出限0.001 2 mmol/L,變異系數(shù)為6.5%,平均回收率為100.2%,此法適合于根莖類蔬菜中微量NO2-含量的測(cè)定。
催化熒光法;亞硝酸根;均勻試驗(yàn)
亞硝酸鹽作為食品添加劑是允許使用的,常作為發(fā)色劑,具有一定的抗菌防腐作用。但是人體過(guò)量攝入亞硝酸鹽后,可將低鐵血紅蛋白氧化成為高鐵血紅蛋白,使之失去輸送氧的能力,且亞硝酸根(NO2-)易與仲胺類化合物反應(yīng)生成強(qiáng)致癌性物質(zhì)亞硝胺,會(huì)對(duì)人體產(chǎn)生較強(qiáng)的毒性,并有可能引發(fā)致癌、致畸等后果,因而測(cè)定亞硝酸鹽是環(huán)境、食品分析中的重要指標(biāo)[1-2]。目前國(guó)內(nèi)外測(cè)定亞硝酸鹽的標(biāo)準(zhǔn)方法仍為重氮耦合比色法,此法顯色反應(yīng)穩(wěn)定性較差,所需試劑本身也都是毒性很大的致癌物質(zhì),同時(shí)樣品中的銅、鐵、硫、碘等離子都會(huì)對(duì)測(cè)定有干擾作用[3-5]。鮑所言等[6]選用的熒光催化劑為高毒且具有致癌性的吖啶橙,通過(guò)對(duì)其改進(jìn),本實(shí)驗(yàn)將熒光劑選擇為安全無(wú)毒的中性紅,以提高實(shí)驗(yàn)的安全性。本研究根據(jù)NO2-可以催化中性紅氧化使其褪色的反應(yīng),建立了測(cè)定NO2-的新體系。NO2-本身不發(fā)熒光,但它可以催化中性紅和溴酸鉀的熒光發(fā)生褪色反應(yīng),反應(yīng)速率與NO2-的含量呈正比[7-8]。該方法可用于測(cè)定河水、地下水和根莖類農(nóng)作物中痕量NO2-的含量。從而建立了生物或食品類樣品中痕量亞硝酸鹽的熒光檢測(cè)方法。
1 材料與方法
1.1 材料與試劑
圓蔥、馬鈴薯:市售;硫酸、亞硝酸鈉(分析純)、中性紅(指示劑):天津科密歐化學(xué)試劑開(kāi)發(fā)中心;溴酸鉀(分析純):國(guó)藥集團(tuán)化學(xué)試劑有限公司;三氯甲烷(分析純):天津市大茂化學(xué)試劑廠。
1.2 儀器與設(shè)備
FR-540熒光光度計(jì):日本島津公司;HH-S超級(jí)恒溫水浴鍋:鞏義市英峪予華儀器廠;感量0.000 1 g電子天平:梅特勒-托利多儀器上海有限公司;101-2電熱鼓風(fēng)干燥箱:天津?qū)嶒?yàn)儀器廠;單道可調(diào)移液槍:大龍興創(chuàng)實(shí)驗(yàn)儀器有限公司。
1.3 試驗(yàn)方法
1.3.1 試劑的配制
1 mg/mL NO2-標(biāo)準(zhǔn)儲(chǔ)備液:精密稱取1 g于硅膠干燥器中干燥24 h的亞硝酸鈉,加去離子水溶解移入1 000 mL容量瓶中,加2 mL氯仿作保護(hù)劑,以抑制細(xì)菌生長(zhǎng)并防止HNO3釋出,然后用去離子水稀釋至刻度。
10 μg/mL NO2-標(biāo)準(zhǔn)使用液:臨用前,吸取NO2-標(biāo)準(zhǔn)儲(chǔ)備液1 mL,置于100 mL容量瓶中,加去離子水稀釋至刻度。
1.0 mmol/L中性紅溶液:稱取約29 mg中性紅,用去離子水溶解后,定容至100 mL。
0.2 mol/L溴酸鉀溶液:稱取3.34 g溴酸鉀,用去離子水溶解后,定容至100 mL。
0.18 mol/L硫酸溶液:量取約4.9 mL 98%硫酸,倒入100 mL去離子水的燒杯,然后加水至500 mL。
1.3.2 熒光強(qiáng)度測(cè)定方法
在10 mL具塞比色管中依次加入1.0 mmol/L中性紅溶液1 000 μL,0.2 mol/L溴酸鉀溶液1 800 μL,0.18 mol/L硫酸1 000 μL,10 μg/mL NO2-標(biāo)準(zhǔn)溶液3 000 μL或待測(cè)溶液適量,用去離子水定容至10 mL,同時(shí)做試劑空白實(shí)驗(yàn)。將配制好的溶液搖勻后,置于55℃水浴中反應(yīng)10 min,然后轉(zhuǎn)入20℃水浴10 min。在最佳激發(fā)波長(zhǎng)和發(fā)射波長(zhǎng)處,分別測(cè)定空白體系和催化體系溶液的熒光強(qiáng)度F0和F,并計(jì)算△F=(F0-F)的值。
1.3.3 均勻試驗(yàn)方案設(shè)計(jì)
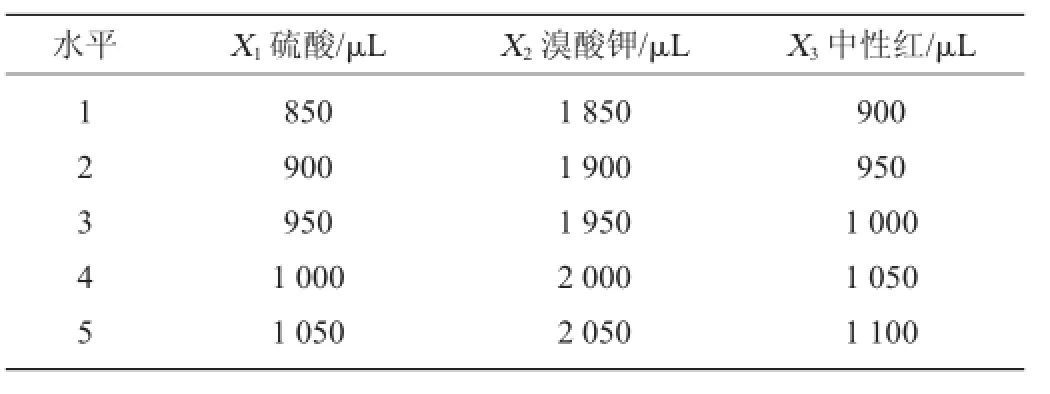
表1 熒光強(qiáng)度優(yōu)化均勻試驗(yàn)因素與水平Table 1 Factors and levels of uniform experiment for fluorescence intensity optimization
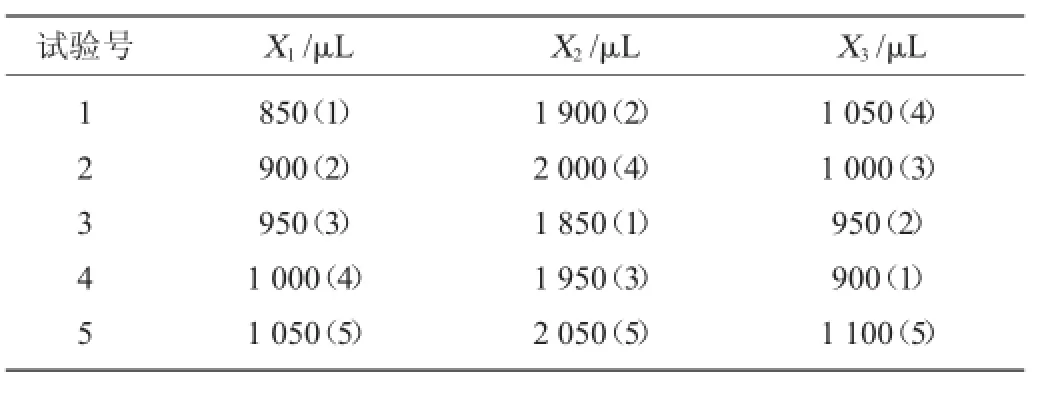
表2 熒光強(qiáng)度優(yōu)化均勻試驗(yàn)設(shè)計(jì)方案Table 2 Design program of uniform experiment for fluorescence intensity optimization
以硫酸用量X1、溴酸鉀用量X2和中性紅用量X33個(gè)因素,采用5水平作均勻試驗(yàn)設(shè)計(jì),其因素與水平列于表1中。其中每個(gè)因素的水平范圍選擇以單因素試驗(yàn)中所得的最佳試驗(yàn)條件為依據(jù)。根據(jù)因素?cái)?shù)和因素的水平數(shù),選擇U5(54)均勻試驗(yàn)設(shè)計(jì)表與使用表進(jìn)行表頭設(shè)計(jì)和試驗(yàn)方案設(shè)計(jì)。表頭設(shè)計(jì)選擇均勻試驗(yàn)設(shè)計(jì)表的1、2、4列安排X1、X2和X33個(gè)因素,得到均勻試驗(yàn)設(shè)計(jì)方案表2。
2 結(jié)果與分析
2.1 測(cè)定波長(zhǎng)的選擇
在10 mL具塞比色管中加入1.0 mmol/L的中性紅溶液1 000 μL,用去離子水定容至10 mL,掃描其激發(fā)波長(zhǎng)與發(fā)射波長(zhǎng)。激發(fā)光在450~570 nm內(nèi)的最佳值為λex=537 nm,發(fā)射光在530~640 nm內(nèi)的最佳值為λem=595 nm,掃描結(jié)果見(jiàn)圖1。
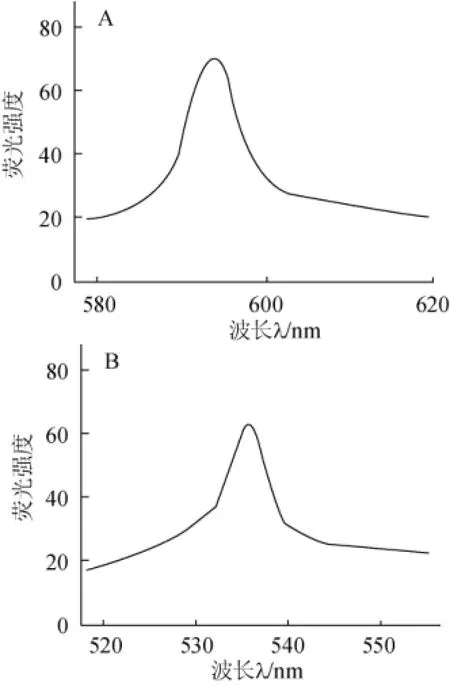
圖1 中性紅激發(fā)光譜(A)與發(fā)射光譜(B)Fig.1 Excitation spectra(A)and emission spectrum(B)of neutral red
2.2 單因素試驗(yàn)
2.2.1 中性紅用量的選擇

圖2 中性紅用量對(duì)熒光強(qiáng)度的影響Fig.2 Effect of neutral red addition on fluorescence intensity
分別吸取1.0 mmol/L中性紅溶液700 μL、800 μL、900 μL、1 000 μL、1 100 μL,按照1.3.1試驗(yàn)方法配制溶液并測(cè)定熒光強(qiáng)度,結(jié)果如圖2所示。
隨著中性紅用量的增加,△F值也逐漸增大,在中性紅用量為800~1 000 μL時(shí),△F值達(dá)到最大,并基本保持平穩(wěn)。繼續(xù)增加中性紅用量,△F值反而逐漸下降。實(shí)際測(cè)量的中性紅用量宜選擇催化強(qiáng)度最大且變化較平穩(wěn)的范圍,也即選擇900 μL作為中性紅的最佳用量。
2.2.2 溴酸鉀用量的選擇
首先在各比色管中加入900μL中性紅溶液(1.0mmol/L),然后分別加入1500μL、1600μL、1700μL、1800μL、1900 μL溴酸鉀溶液(0.2 mol/L),再依照1.3.1試驗(yàn)方法配制溶液并測(cè)定熒光強(qiáng)度,結(jié)果圖3所示。
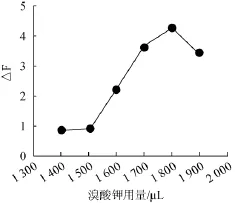
圖3 溴酸鉀用量對(duì)熒光強(qiáng)度的影響Fig.3 Effect of potassium borate addition on fluorescence intensity
由圖3可以看出,溴酸鉀用量的增加會(huì)使△F值也增大,當(dāng)溴酸鉀用量在1 700~1 900 μL之間時(shí)△F值變化緩慢并較穩(wěn)定,溴酸鉀用量為1 800 μL時(shí)△F值達(dá)到最大,繼續(xù)增大溴酸鉀用量,△F值反而會(huì)減小。所以溴酸鉀用量為1 800 μL時(shí),亞硝酸根的催化強(qiáng)度可達(dá)到最大,此為最佳的溴酸鉀用量。
2.2.3 硫酸用量的選擇
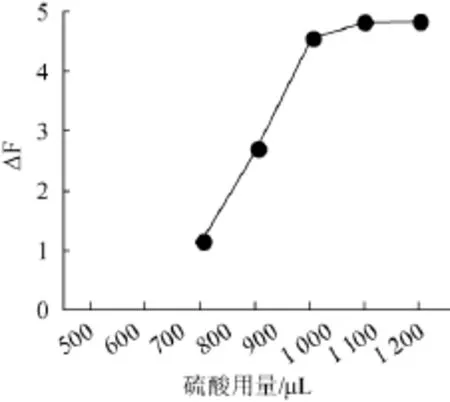
圖4 硫酸用量對(duì)熒光強(qiáng)度的影響Fig.4 Effect of sulfuric acid addition on fluorescence intensity
在各比色管中取900 μL中性紅溶液(1.0 mmol/L)和1 800 μL溴酸鉀溶液(0.2 mol/L),再依次加入700 μL、800 μL、900 μL、1 000 μL、1 100 μL不同量的硫酸溶液(0.18 mol/L),再按照1.3.1試驗(yàn)方法配制溶液并測(cè)定△F值。
從圖4可以看出,在硫酸用量為1000~1050μL時(shí),△F值變化緩慢并達(dá)到最大值,在硫酸用量為1 050~1 100 μL時(shí),△F值又開(kāi)始減小。故硫酸用量為1 050 μL時(shí),亞硝酸根的熒光催化程度達(dá)到最大,此即為硫酸的最佳加入量。
2.2.4 水浴時(shí)間對(duì)反應(yīng)體系的影響
反應(yīng)時(shí)間是影響△F值的一個(gè)關(guān)鍵因素,試驗(yàn)考察了55℃水浴中,不同反應(yīng)時(shí)間5 min、6 min、7 min、8 min、9min、10 min、11 min被測(cè)體系的△F值的變化情況。圖5的結(jié)果表明,在5~10 min之間,隨反應(yīng)時(shí)間的增加,體系的反應(yīng)速率也增大,在水浴10 min時(shí)反應(yīng)體系達(dá)到最大,當(dāng)反應(yīng)時(shí)間超過(guò)10 min,△F值開(kāi)始減小,故水浴10 min為最佳的水浴時(shí)間。
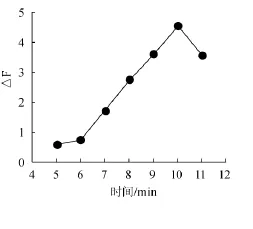
圖5 水浴時(shí)間對(duì)反應(yīng)體系的影響Fig.5 Effect of bath time on fluorescence intensity
2.2.5 水浴溫度對(duì)反應(yīng)體系的影響
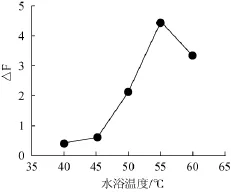
圖6 水浴溫度對(duì)反應(yīng)體系的影響Fig.6 Effect of bath temperature on the reaction system
試驗(yàn)考察了反應(yīng)溫度40℃、45℃、50℃、55℃、60℃時(shí)體系△F值的化情況,發(fā)現(xiàn)溫度對(duì)反應(yīng)體系△F測(cè)定的結(jié)果影響很大,結(jié)果見(jiàn)圖6。由圖6可知,當(dāng)反應(yīng)溫度<45℃時(shí),催化作用不明顯。但隨著溫度的升高,催化反應(yīng)速度逐漸加快,△F值也逐漸增大,至55℃時(shí),催化效果最為明顯。繼續(xù)升高溫度,反應(yīng)的速率反而降低。故水浴55℃
是亞硝酸根催化強(qiáng)度達(dá)到最大時(shí)的溫度。
2.3 通過(guò)均勻試驗(yàn)確定最佳反應(yīng)條件
完全從所選試驗(yàn)點(diǎn)的均勻性出發(fā),即從全面試驗(yàn)點(diǎn)中挑選出部分具有代表性的試驗(yàn)點(diǎn),來(lái)反映體系的主要特征。此設(shè)計(jì)方法最大的特點(diǎn)是使試驗(yàn)工作量更少。本研究?jī)H選5個(gè)有代表性的試驗(yàn)點(diǎn),設(shè)計(jì)方案見(jiàn)表2所示。
2.3.1 均勻試驗(yàn)直觀分析結(jié)果
根據(jù)均勻試驗(yàn)設(shè)計(jì)方案表2,得到試驗(yàn)結(jié)果見(jiàn)表3。從表3結(jié)果可以看出,5個(gè)試驗(yàn)中4號(hào)試驗(yàn)△F值最強(qiáng)。所以直觀分析結(jié)果認(rèn)為較佳的試驗(yàn)方案為:中性紅(1.0 mmol/L)用量900 μL、溴酸鉀(0.2 mol/L)用量1 950 μL、硫酸(0.18 mol/L)用量1 000 μL。
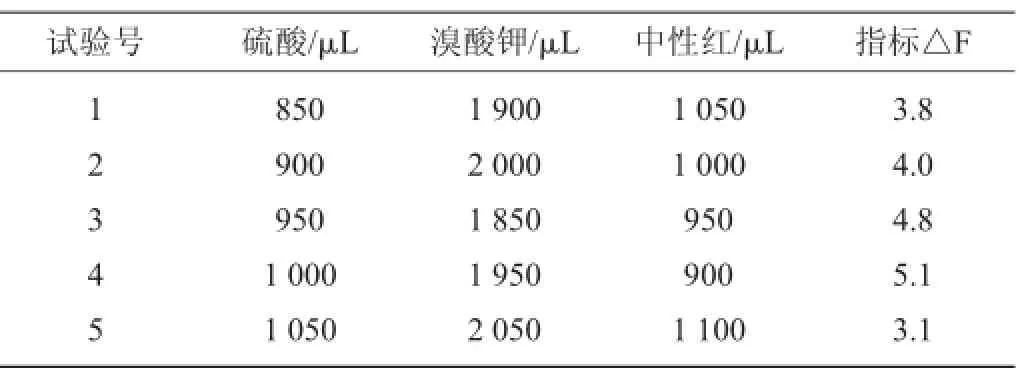
表3 均勻試驗(yàn)結(jié)果Table 3 Results of uniform test
2.3.2 均勻試驗(yàn)多元回歸分析結(jié)果
利用SPSS軟件對(duì)試驗(yàn)結(jié)果進(jìn)行多元回歸分析用求條件極值的強(qiáng)約束化法對(duì)回歸方程進(jìn)行優(yōu)化,用Matlab編程,最小二乘法尋優(yōu)。按照表2的試驗(yàn)方案來(lái)填寫(xiě)軟件的運(yùn)行參數(shù)。即考察指標(biāo)數(shù)為1,試驗(yàn)因素?cái)?shù)為3,運(yùn)行次數(shù)為5,因素X1硫酸的上下限為850~1 050,因素X2溴酸鉀的上下限為1850~2050,因素X3中性紅的上下限為900~1100,置信水平選擇95%。得回歸方程Y=17+0.42X1-2.2X2-9.0X3。
回歸方程的變量分析見(jiàn)表4。樣本容量N=5,顯著性水平α=0.05,檢驗(yàn)值Ft=342.6,臨界值Fα(3,1)=215.7,由于Ft>Fα(3,1),所以回歸方程顯著。經(jīng)優(yōu)化處理,當(dāng)中性紅取900 μL,溴酸鉀取1 850 μL,硫酸取1 050 μL時(shí),指標(biāo)熒光強(qiáng)度△F值最大,即中性紅被氧化的最徹底,此為更好的反應(yīng)條件,不在表2的5個(gè)試驗(yàn)方案當(dāng)中,因此需要驗(yàn)正試驗(yàn)。
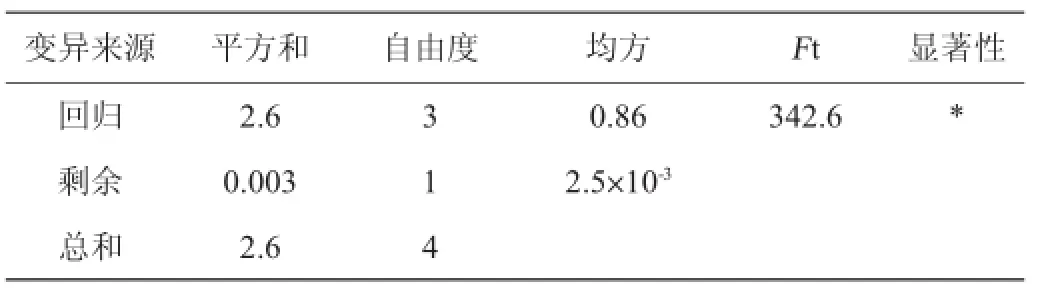
表4 回歸方程變量分析Table 4 Variable analysis of regression equation
經(jīng)過(guò)以上回歸分析,確定了3種試劑的加入量,并重新選取新的試驗(yàn)參數(shù)進(jìn)行了兩次試驗(yàn),試驗(yàn)數(shù)據(jù)如下:△F1=5.31,△F2=5.28,平均△F=5.30,在所有試驗(yàn)數(shù)據(jù)中為最高值,驗(yàn)證了在該條件下,中性紅被氧化的最徹底。
2.3.3 標(biāo)準(zhǔn)曲線的繪制及檢出限
在5支比色管中依次加入900μL中性紅溶液(1.0 mmol/L),1 850 μL溴酸鉀溶液(0.2 mol/L),1 050 μL硫酸溶液(0.18 mol/L),再分別加入1 000 μL、2 000 μL、3 000 μL、4000μL、5000μLNO2-標(biāo)準(zhǔn)使用液(10 μg/mL),以去離子水定容至10 mL。55℃下水浴10 min,然后轉(zhuǎn)入20℃水浴保持10 min后,同時(shí)做試劑空白試驗(yàn),測(cè)其熒光強(qiáng)度△F值。以NO2-用量為橫坐標(biāo),△F值為縱坐標(biāo),得標(biāo)準(zhǔn)曲線見(jiàn)圖7。按5次空白實(shí)試驗(yàn)標(biāo)準(zhǔn)偏差(σ)的3倍除以工作曲線的斜率得到此種方法的檢出限0.001 2 mmol/L。5次空白試驗(yàn)測(cè)得值的相對(duì)標(biāo)準(zhǔn)偏差2.7%。
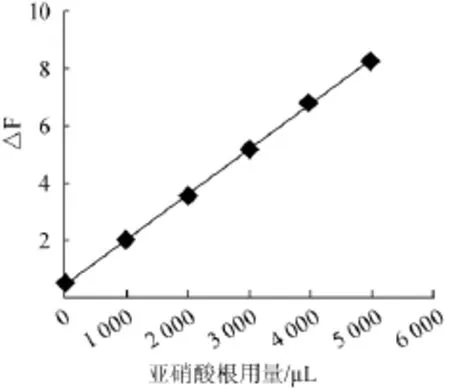
圖7 NO2-標(biāo)準(zhǔn)曲線Fig.7 Standard curve of NO2-
標(biāo)準(zhǔn)曲線的回歸方程y=1.58x+0.46的相關(guān)系數(shù)r=0.999 5,表明當(dāng)NO2-濃度為0.02~0.11 mmol/L時(shí),體系的熒光強(qiáng)度△F與NO2-濃度呈現(xiàn)良好的線性關(guān)系。可進(jìn)一步進(jìn)行樣品的測(cè)定。
2.3.4 樣品的預(yù)處理及測(cè)定
取新鮮馬鈴薯與圓蔥洗凈、晾干。分別準(zhǔn)確稱取帶皮與無(wú)皮馬鈴薯2.0g放入研缽中,加入80mL蒸餾水搗碎勻漿,過(guò)濾,濾液于100 mL容量瓶中定容。另分別準(zhǔn)確稱取帶皮與無(wú)皮圓蔥5.0 g,放入研缽中,加入80 mL蒸餾水搗碎勻漿,過(guò)濾,濾液于100 mL容量瓶中定容。配制成的四種溶液按中性紅取900 μL,溴酸鉀取1 850 μL,硫酸取1 050 μL進(jìn)行樣品測(cè)定,平行做2組試驗(yàn),測(cè)得的結(jié)果如表5所示。將平均△F值代入回歸方程中,可計(jì)算出兩種蔬菜NO2-的含量。
由表5可知,帶皮蔬菜中的NO2-含量比不帶皮的蔬菜中NO2-含量高,說(shuō)明蔬菜中的表皮中也含有NO2-,所以根莖類蔬菜在食用時(shí)最好去皮食用。根據(jù)蔬菜中亞硝酸鹽的含量標(biāo)準(zhǔn),本試驗(yàn)中樣品的NO2-含量低于國(guó)家標(biāo)準(zhǔn),由此可得本試驗(yàn)中樣品的亞硝酸鹽含量沒(méi)有超標(biāo)。
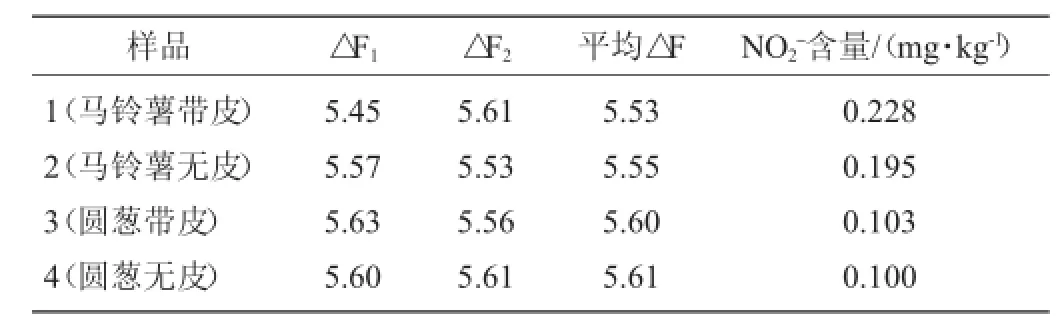
表5 樣品NO2-含量試驗(yàn)結(jié)果Table 5 NO2-content results of samples
2.3.5 精密度試驗(yàn)與加標(biāo)回收率試驗(yàn)
取5只10 mL具塞比色管,向其中依次加入中性紅900 μL,溴酸鉀1 850 μL,硫酸1 050 μL和待測(cè)液1 000 μL,在55℃水浴中加熱10 min,轉(zhuǎn)入20℃水浴10 min后,做精密度試驗(yàn),結(jié)果見(jiàn)表6所示。回收率加標(biāo)試驗(yàn)結(jié)果見(jiàn)表7所示。

表6 NO2-含量精密度試驗(yàn)結(jié)果Table 6 Precision experiment results of NO2-content
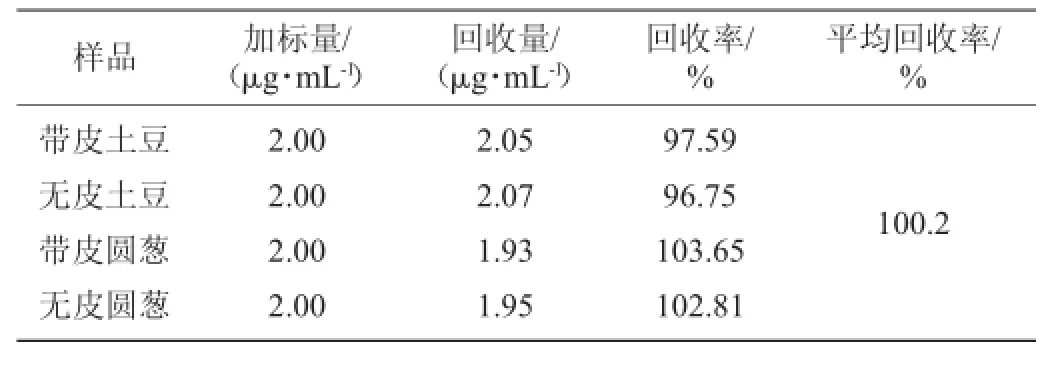
表7 NO2-含量回收率試驗(yàn)結(jié)果Table 7 Recovery experiment results of NO2-content
由表6和表7可見(jiàn),用催化熒光法測(cè)定NO2-偏差小,變異系數(shù)(coefficient of variation,CV)低,回收率接近100%,適合根莖類植物中所含的微量NO2-濃度的測(cè)定。
3 結(jié)論
利用中性紅氧化反應(yīng)體系中的NO2-可以起到催化作用的原理,根據(jù)中性紅熒光強(qiáng)度的變化與NO2-含量成正比的關(guān)系來(lái)測(cè)定NO2-的含量。通過(guò)單因素試驗(yàn)和均勻試驗(yàn)證明中性紅溶液(1.0 mmol/L)加量900 μL,溴酸鉀溶液(0.2 mol/L)加量1 850 μL,硫酸(0.18 mol/L)加量1 050 μL時(shí),催化程度最明顯。
在微量NO2-的熒光分析中建立了最佳分析條件:激發(fā)波長(zhǎng)λex=537.0 nm,發(fā)射波長(zhǎng)λem=595.0 nm,最佳測(cè)定工作曲線為y=1.58x+0.46,相關(guān)系數(shù)r=0.999 5。亞硝酸鹽的線性范圍為0.02~0.11 mmol/L,檢出限為0.001 2 mmol/L,相比吖啶橙法(0.000 3 mmol/L)略高。
通過(guò)對(duì)馬鈴薯和圓蔥兩種蔬菜樣品的分析測(cè)定,所得數(shù)據(jù)的標(biāo)準(zhǔn)偏差為0.029,變異系數(shù)為6.5%,此方法測(cè)定蔬菜中亞硝酸根含量的平均回收率為100.2%。并通過(guò)研究證實(shí)蔬菜的表皮中也含有一部分亞硝酸鹽。在通常情況下,由于根莖類蔬菜中的亞硝酸鹽主要來(lái)自于所吸收的水分,所以其含量較低,對(duì)人體無(wú)害。本法也適用于其他蔬菜中亞硝酸鹽農(nóng)藥殘留的檢測(cè),還為無(wú)熒光物質(zhì)的熒光檢測(cè)奠定了基礎(chǔ),開(kāi)闊了熒光分析方法的應(yīng)用途徑。
[1]吳小春,吳友誼.環(huán)境水樣及食品中亞硝酸根的分析進(jìn)展[J].分析測(cè)試技術(shù)與儀器,2003,9(4):227-233.
[2]MOORCROFT M J,DAVIS J,COMPTON R G.Detection and determination of nitrate and nitrite:a review[J].Talanta,2001,54(5):785-803.
[3]齊小玲,富新權(quán),謝君創(chuàng).催化光度法測(cè)定水中微量亞硝酸根[J].湖北化工,2001,3(1):45-46.
[4]MINAKATA K,OKMAOTO N,NOZAWA H,et al.Determination of nitrite in bio1ogical fluids by use of electron spin resonance[J].Anal Biochem,2004,325(1):168-170.
[5]ZUO Y G,WANG C G,VAN T.Simultaneous determination of nitrite and nitrate in dew,rain,snow and lake water samples by ion-pair highperformance liquid chromatography[J].Talanta,2006,70(2):281-285.
[6]鮑所言,劉衛(wèi)潔,胡漢芳.催化熒光法測(cè)定痕量亞硝酸根[J].光譜學(xué)與光譜分分析,2004,24(3):342-344.
[7]劉常增.鋅試劑-NO2-/KBrO3催化體系測(cè)定痕量亞硝酸根[J].光譜學(xué)與光譜分析,2003,23(3):348-350.
[8]徐遠(yuǎn)金,李海云,姚志雄,等.水中亞硝酸根的表面活性劑增敏催化動(dòng)力學(xué)流動(dòng)注射熒光法測(cè)定[J].分析測(cè)試學(xué)報(bào),2003,22(4):32-34.
[9]韓志輝,呂昌銀.吖啶紅熒光碎滅法測(cè)定痕量亞硝酸根[J].中國(guó)衛(wèi)生檢驗(yàn)雜志,2004,14(3):287-288.
[10]李書(shū)華,蒲彪,陳封政.VC和發(fā)酵溫度對(duì)泡仔姜中亞硝酸鹽的影響[J].中國(guó)釀造,2006,25(2):34-36.
[11]ZHANG M,YUAN D X,HUANG Y M.Sequential injection spectrophotometric determination of nanomolar nitrite in seawater by on-line preconcentration with HLB cartridge[J].Acta Oceanologica Sinica,2010,29(1):100-107.
[12]張瑩,孫君社,張京聲,等.溶氧對(duì)巨大芽孢桿菌發(fā)酵亞硝酸還原酶的影響[J].中國(guó)釀造,2011,30(6):43-47.
[13]WEI C.Analysis of the influence of free ammonia on the accumulation ofnitriteinthe nitrite nitrification system[J].Chinese J Geochem,2009, 28:440-444.
[14]范亞娜,蓋軻.幾種腌制蔬菜中亞硝酸鹽含量的測(cè)定[J].寶雞文理學(xué)院學(xué)報(bào):自然科學(xué)版,2008(1):41-43
[15]YU D B,YONG D M,DONG S J.Toxicity detection of sodium nitrite, borax and aluminum potassium sulfate using electrochemical method [J].J Environ Sci,2013,25(4):785-790.
[16]韓彬,曹磊,鄭立,等.夾管電磁閥定量-流動(dòng)注射分析系統(tǒng)測(cè)定海水中亞硝酸鹽和硝酸鹽氮[J].分析化學(xué),2010,38(12):1832-1837.
Determination of trace nitrite in vegetables by catalytic fluorescence method
LIU Yongtao1,2,YUN Xia1,NA Guangshui2*
(1.College of Biological Engineering,Dalian Polytechnic University,Dalian 116034,China; 2.National Marine Environmental Monitoring Center,Dalian 116023,China)
A method for trace nitrite determination in vegetables by catalytic fluorimetry was established.The neutral red fluorescence bleaching reaction could be catalyzed by nitrite,and the reaction rate was in direct proportion to nitrite content.The optimal reaction conditions and reagent combinations were determined by single factor and uniform experiment.Result showed that under the condition of excitation wavelengthλex=537 nm,emission wavelengthλem=595 nm,combination of reagent factors were neutral red 900 μl,potassium bromate 1 850 μl and sulfuric acid 1 050 μl.The standard curve for nitrite determination of the present method wasy=1.58x+0.46,(r=0.999 5).The linear range was 0.02~0.11 mmol/L,detection limit was 0.001 2 mmol/L,variation coefficient was 6.5%and average recovery rate achieved 100.2%.The method is suitable for micro nitrite content determination in root vegetables.
fluorescence analysis method;nitrite;uniform test
O657.3
A
0254-5071(2014)07-0113-05
10.11882/j.issn.0254-5071.2014.07.026
2014-05-04
國(guó)家海洋局青年海洋科學(xué)基金(20090507)
劉永濤(1990-),男,碩士研究生,研究方向?yàn)樯锎呋c生物分析。
*通訊作者:那廣水(1977-),男,副研究員,博士,研究方向?yàn)闄z測(cè)技術(shù)研究與應(yīng)用。

