UPLC 法同時測定三葉片中4 種成分的溶出度
劉亭亭, 張德芹, 王 萌* , 金秀麗
(1. 天津中醫藥大學,天津市現代重點實驗室-省部共建國家重點實驗室培育基地,天津300193;2. 天津國際生物醫藥聯合研究院,天津300457;3. 現代中藥發現與制劑技術教育部工程研究中心,天津300193)
三葉片是由張伯禮院士主持研制的治療二型糖尿病的中藥新藥,由桑葉、荷葉、山楂葉等五味藥材組成。中藥復方是通過組方藥材及其中多種成分的共同或協調作用起效的,具有多成分、多靶點的作用特點。藥物的溶出是固體藥物吸收的前提條件,藥物吸收又是口服藥物發揮全身作用的第一步。研究和考察復方中藥,特別是復方中藥口服制劑的體外溶出特征應遵循其作用特點,選取藥物中多個具有代表性的藥效活性成分進行研究。以多種代表性成分為指標,對中藥復方口服制劑體外溶出特征進行研究是反映其體內吸收情況,表征和衡量中藥復方制劑藥效和質量的重要手段之一。
針對三葉片用于糖尿病早期糖耐量低及糖脂代謝紊亂的療效,本研究查閱文獻篩選制劑中具有降糖和降脂藥效活性報道的主要成分,并綜合考慮制劑中成分含有量因素,確定選取蘆丁[1-4]、荷葉堿[5-6]、金絲桃苷[7-8]、芍藥苷[9-11]等成分作為三葉片體外溶出度研究指標成分。
本研究以UPLC 作為研究分析手段,選取多種藥效活性成分為指標,建立專屬性強、快速、高效的三葉片中多指標性成分UPLC 同時定量測定的方法。并以此進行中藥復方制劑三葉片體外溶出研究,以期較為真實的對復方中藥口服制劑中多種成分的復雜體內吸收過程進行預判。在此過程中,對各成分溶出特征同步性進行考察,從而在一定程度上反映多成分體內吸收過程和藥效作用過程中的相互作用,從溶出角度詮釋中藥復方口服制劑配伍機制和復方中藥口服制劑中多成分的協同作用。
1 材料
H class 超高效液相色譜儀 (美國Waters);CH-4123 溶出儀(瑞士Sotax 公司);Milli-Q 超純水儀(美國Millipore 公司);H1650-W 離心機(長沙湘儀離心機儀器有限公司);HHS 型電熱恒溫水浴鍋(上海博訊實業有限公司醫療設備廠)。
三葉片(由天津中醫藥大學中醫藥研究院制得);芍藥苷、蘆丁、荷葉堿對照品(中國藥品生物制品檢定所,批號分別為110736-101035,100080-200707,111566-200703),金絲桃苷對照品(中新藥業,批號2013.5.14);乙腈(CHROMASOLV,色譜純);甲酸(天津市大茂化學試劑廠,色譜純);無水乙醇(天津市大茂化學試劑廠,分析純)。
2 方法與結果
2.1 成分測定
2.1.1 色譜條件 Waters BEH RP C18色譜柱(2.1 mm × 100 mm,1.7 μm),流動相為乙腈(A) -0.3%甲酸水(B),梯度洗脫(0 ~4 min,13%A;4 ~5 min,13% ~15% A;5 ~10 min,15%A;10 ~10.5 min,15% ~16% A;10.5 ~16 min,16%A);體積流量0.3 mL/min;柱溫35 ℃;檢測波長0 ~12 min,225 nm;12 ~16 min,360 nm。
2.1.2 對照品溶液的制備 分別精密稱取芍藥苷、荷葉堿、蘆丁、金絲桃苷對照品適量,加30%乙醇制成每1 mL 含芍藥苷、荷葉堿、蘆丁、金絲桃苷分別為103.5、28.3、5.062 5、20.25 μg 的混合對照品溶液。
2.1.3 供試品溶液的制備 取三葉片一粒,照《中國藥典》2010 年版二部附錄XC[12]溶出度測定法槳法,以500 mL 經脫氣處理的純水為溶出介質,轉速120 r/min,4 h 時取出溶出液適量,10 000 r/min下離心5 min,取上清液進樣。
上述色譜條件下測定芍藥苷,荷葉堿,蘆丁,金絲桃苷對照品和供試品的色譜圖如圖1 所示,由圖可知三葉片中4 種指標成分分離良好,且其他成分及雜質不干擾其測定。
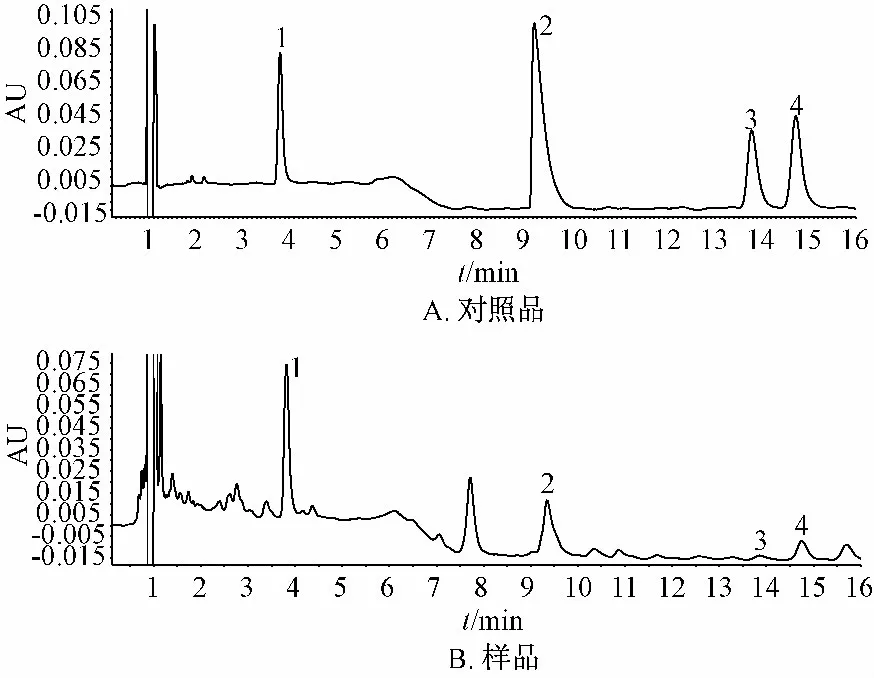
圖1 UPLC 色譜圖Fig.1 UPLC chromatograms
2.1.4 標準曲線的建立 將“2.1.2”項下的對照品混合溶液依次精密稀釋成系列混合對照品溶液,10 000 r/min 離心5 min,注入超高效液相色譜儀,按“2.1.1”項下的色譜條件測定峰面積,以峰面積為縱坐標,質量濃度為橫坐標,質量繪制標準曲線,計算回歸方程、r 值及線性范圍見表1,結果表明各成分在以下線性范圍內線性良好。
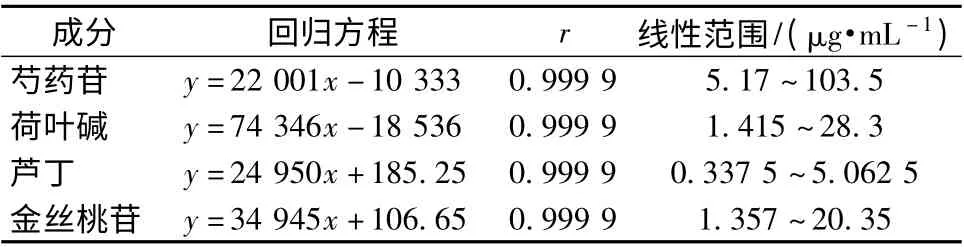
表1 線性關系考察Tab.1 Linear corelation
2.1.5 精密度試驗 將供試品溶液重復進樣6 次,按方法測定計算峰面積,芍藥苷、荷葉堿、蘆丁、金絲桃苷峰面積的RSD 值分別為0.5%、2.3%、0.2%、0.3%,符合溶出度試驗要求。
2.1.6 穩定性試驗 將供試品溶液分別于2、4、8、12、18、24 h 進樣,記錄各考察成分峰面積,芍藥苷、荷葉堿、蘆丁、金絲桃苷峰面積的RSD值分別為1.2%、2.9%、1.8%、1.1%,表明樣品在24 h 內穩定。
2.1.7 重復性試驗 取同一批三葉片,按“2.1.3”項下方法制備6 份供試品溶液,依次進樣,記錄各考察成分峰面積,芍藥苷、荷葉堿、蘆丁、金絲桃苷的重復性考察結果RSD 值分別為1.6%、4.3%、0.8%、1.8%,表明方法重復性良好。
2.1.8 加樣回收試驗 精密稱定80 目三葉片細粉6 份,置于50 mL 錐形瓶中,各精密加入與三葉片細粉中芍藥苷,荷葉堿,蘆丁,金絲桃苷質量相等的對照品溶液,加入適量30%乙醇溶液至20 mL,超聲處理2 h 取出放至室溫,10 000 r/min 下離心5 min,按方法測定計算峰面積,計算加樣回收率。測得芍藥苷、荷葉堿、蘆丁、金絲桃苷的平均回收率分別為 96.3%、101.4%、100.6%、100.5%,RSD 分 別 為 0.5%、0.7%、2.0%、2.4%。表明方法準確度良好。
2.2 溶出度的測定
2.2.1 溶出條件的篩選 分別考察pH 7.2、pH 6.8、pH 4.5 磷酸鹽緩沖溶液,超純水,0.1 mol/L鹽酸,30%乙醇等溶出介質中三葉片4 種藥效成分的溶出度,通過比較芍藥苷、荷葉堿、蘆丁、金絲桃苷的溶出量,以30%乙醇為溶出介質時各成分的溶出量最大,其他溶出介質稍小,但溶出百分率均在70%以上,選擇超純水作為溶出介質。另外轉速對溶出度也有一定的影響,以水為溶出介質對比100 r/min 和120 r/min 下的溶出情況,溶出量差別不大,120 r/min 時重復性更好,故將轉速定為120 r/min。
2.2.2 三葉片溶出曲線的繪制 根據《中國藥典》2010 年版二部附錄XC 溶出度測定法,選用第二法槳法進行三葉片溶出度研究。取三葉片6片,以經脫氣處理后的超純水500 mL 為溶出介質,轉速為120 r/min,溫度(37 ±0.5)℃,依法測定,不同時間點取樣1 mL,經10 000 r/min 離心5 min,每次取樣后補加同體積同溫度的溶出介質,UPLC測定樣品中芍藥苷、荷葉堿、蘆丁、金絲桃苷的量,計算各時間點藥效成分的平均累積溶出百分率和標準差,繪制溶出曲線 (含誤差線)結果見圖2。
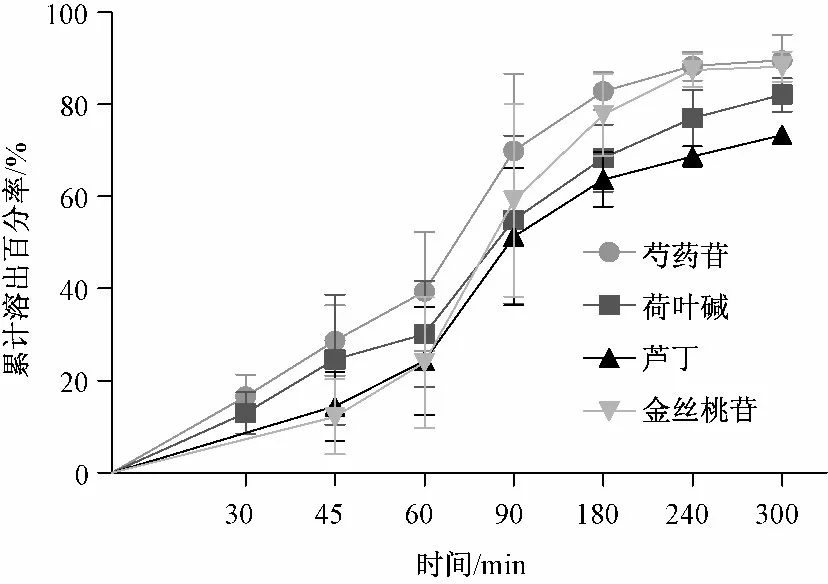
圖2 三葉片各成分平均累積溶出百分率Fig.2 Average cumulative dissolution rates foreach component of Sanye Tablets
2.2.3 相似因子法(f2)比較三葉片中4 種活性成分溶出曲線一致性 比較兩條釋放曲線差異的方法有很多,其中f2相似因子法是一種較好的區分釋放度差異的方法。這種比較釋放度差異的方法已被美國FDA 的“藥物評價與研究中心”采納,推薦為比較兩條溶出曲線的首選方法[13-14],認為f2值在50 ~100 時兩條釋放曲線相似,本實驗采用f2值比較三葉片中4 種有效成分溶出曲線的差異。計算的公式如下:
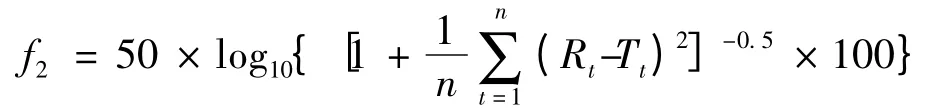
式中Rt為對照成分t 時間的累積溶出率;Tt為試驗成分t 時間的累積溶出率;n 為溶出度實驗的取樣次數。
以荷葉堿的溶出曲線為參比,芍藥苷、蘆丁、金絲桃苷f2值分別為50.84、58.37、55.04。4 條溶出曲線相比f2均大于50 表明運用相似因子法比較中藥口服制劑三葉片中4 種成分的釋放特征,該4 種活性成分溶出具有一定的同步性。
3 討論
本實驗采用分析速度快、高峰容量和高靈敏度的超高效液相色譜技術,大大降低了復雜的中藥復方口服制劑分析時間,整個分析時間在16 min 內完成,經方法學驗證,測定結果準確,具有良好的重復性,可用于三葉片多種成分體外溶出度的分析測定,為體外判斷三葉片體內吸收情況提供科學、可靠的依據。同時,該分析方法靈敏、高效,對制劑中不同極性成分具有一定的覆蓋能力,也可以直接用于三葉片制劑中相關成分的質量控制。
溶出度研究結果表明三葉片中的4 種活性成分的溶出進程較為統一,在5 h 之內累積釋放度均達到了70%以上,基本能夠表現出一致的釋放行為特征,從溶出度角度在一定程度上說明了4 種活性成分可能在體內同時發揮藥效,起到協同增效的作用。三葉片臨床試驗中體內過程研究發現,對比每日服藥3 次與每日服藥兩次受試者的血藥濃度和達峰時間,每日服藥3 次的受試者血藥濃度更穩定,與本研究體外溶出試驗結果較為一致。說明本實驗建立中藥口服藥物多成分體外溶出模型能夠較為真實地反映出三葉片主要藥效成分的體內吸收特征,與體內試驗結果具有一定的相關性。
選取的4 種成分均為每一種組方中藥中具有降脂降糖活性的代表性成分,然而三葉片中還含有另一部分極性較低的成分,同樣具有較好的藥效活性,如槲皮素和丹參酮ⅡA。本實驗也對其溶出情況進行了考察,但因二者極性較小,在水介質中溶出極少,低于本研究UPLC 檢測方法的檢測限,這類成分具體吸收和藥效情況還有待于進行進一步的體內過程研究。
[1] 項秀娣,張 樂,戴瑜來. 桑葉的降血糖活性成分及其作用機制研究進展[J]. 安徽農學通報,2012,18(21):90-93.
[2] 原愛紅,馬 駿,蔣曉峰,等. 桑葉中糖苷酶抑制活性組分的篩選[J]. 中國中藥雜志,2006,31(3):223-227.
[3] 歐陽臻,陳 鈞. 桑葉的化學成分及其藥理作用研究進展[J]. 江蘇大學學報,2003,24(6):39-44.
[4] 李明聰,楊 丹,郭 英,等. 桑葉中黃酮類化學成分及藥理作用研究進展[J]. 遼寧中醫雜志,2012,39(2):377-380.
[5] 王福剛,曹 娟,劉 斌,等. 荷葉的化學成分及其藥理作用研究進展[J]. 時珍國醫國藥,2010,21 (9):2339-2340.
[6] 劉淑萍,樊淑彥,侯海妮,等. 荷葉化學成分及藥理作用研究進展[J]. 河北醫科大學學報,2004,25 (4):254-256.
[7] 耿慧春,滿 瑩,趙智勇. 山楂葉化學成分和藥理作用研究進展[J]. 中國現代醫生,2009,47(26):12-13.
[8] 王 芳. 山楂葉總黃酮的藥理作用[J]. 浙江中醫藥大學學報,2010,34(2):295-296.
[9] 阮金蘭,趙鐘祥,曾慶忠,等. 赤芍化學成分和藥理作用的研究進展[J]. 中國藥理學通報,2003,19 (9):965-970.
[10] 楊媛媛,周 剛,馬曉康,等. 赤芍的研究進展[J]. 醫藥導報,2008,27(1):67-69.
[11] 莫玉蘭. 赤芍總苷藥理作用研究概況[J]. 光明中醫,2009,24(4):782-784.
[12] 國家藥典委員會. 中華人民共和國藥典:2010 年版二部[S]. 北京:中國醫藥科技出版社,2010:附錄XC.
[13] Guidance for industry:Dissolution testing of immediate release solid oral dosage forms[S]. FDA. 1997.
[14] 廖正根,蔣且英,梁新麗,等. 桂枝茯苓膠囊中3 種活性成分體外溶出度的比較研究[J]. 中成藥,2008,30(8):1141-1144.

