ECAP制備超細晶銅在0.5mol/L NaCl溶液中的腐蝕行為
王慶娟,張平平,羅 雷,杜忠澤
(西安建筑科技大學 冶金工程學院,西安710055)
目前,等徑角擠壓(Equal Channel Angular Pressing,ECAP)技術能明顯地細化多晶材料的晶粒,獲得超細晶結構(亞微米級或納米級)材料,近年來已引起材料科學研究者的廣泛關注。這是因為超細晶材料表現出一系列優異的物理性能和力學性能,從而能為提高材料的綜合性能,發展新材料和改善傳統材料性能創造條件[1,2]。近年來,對超細晶材料的研究主要集中在制備技術、微觀結構特征、性能及其應用等方面,而對其耐腐蝕性能的研究卻沒有給予足夠的重視。超細晶金屬的腐蝕性能因制備工藝、晶粒尺寸、腐蝕類型、腐蝕介質等因素不同而有所不同[3-6]。事實上,超細晶材料晶粒小,表面原子數多,表面活性高,并存在大量的晶界,按照傳統的腐蝕理論,晶界是腐蝕的活性區,因此超細晶材料的耐腐蝕性能是值得商榷的。本工作通過Tafel曲線、E-t曲線、失重量和腐蝕形貌等研究ECAP制備的塊體超細晶銅和退火態粗晶銅在0.5mol/L NaCl溶液中的腐蝕性能。
1 實驗材料及方法
實驗材料取自600℃退火態T1紫銅和退火后經過4道次、8道次和12道次“C”方式ECAP擠壓制備的超細晶銅。其微觀組織形貌見圖1,對應的平均晶粒尺寸分別約為50,0.41,0.23μm和0.32μm。

圖1 退火態純銅的光學顯微組織和ECAP不同變形道次的透射電子形貌(a)粗晶銅;(b)4道次;(c)8道次;(d)12道次Fig.1 The OM micro structure of CG copper(a)and TEM images of copper after ECAP for 4passes(b),8passes(c)and 12passes(d)
電化學方法進行腐蝕測試時,將選用的坯料通過線切割加工成φ5mm×8mm的圓柱,圓柱一面焊接銅導線,導線和試件的焊點必須封裝絕緣以防止電偶腐蝕、縫隙腐蝕等的干擾,焊點面積不小于1mm2。露出一個工作面,其面積為0.786cm2,其余面用環氧樹脂封裝。為了消除金屬試件表面狀態的差異,獲得均勻、光潔的表面狀態,工作電極表面在實驗前需要經過嚴格的處理。采用不同規格的金相砂紙(金剛石)粗磨和細磨逐級打磨至1500#,然后用丙酮除油,去離子水清洗,吹干。實驗前通以一個微小的陰極電流以進行活化,去除試樣表面形成的氧化膜。極化曲線測試前浸泡穩定時間為10min,實驗介質為0.5mol/L NaCl溶液。電化學測試系統為三電極體系,輔助電極為鉑電極,參比電極選用飽和甘汞電極。電化學測試由M237A恒電位儀和M5210鎖相放大器完成。極化曲線的掃描范圍為-0.8~-0.1VvsSCE,掃描速率0.5mV/s。浸泡腐蝕試樣經過切割拋光,然后進行浸泡腐蝕,腐蝕前后使用電子天平稱重,精確度為10-4g,實驗采用失重法計算腐蝕速率。腐蝕介質采用0.5mol/L NaCl溶 液,環 境 掃 描 電 子 顯 微 鏡(SEM,FEI Quanta 200)用來觀察腐蝕產物及腐蝕表面的形貌。
2 實驗結果與分析
2.1 電化學腐蝕
圖2(a)給出了退火態和ECAP不同變形道次的純銅在0.5mol/L NaCl溶液中的Tafel曲線,可以看出,隨著變形道次的增加,陰陽極電流密度降低。通過數學分析,將圖2(a)擬合可得Tafel曲線陰陽極的斜率bc,ba和腐蝕電流密度Icorr,擬合結果見表1,可以看出,陰陽極的斜率bc,ba值隨變形道次的增加而降低,在室溫條件下,退火態粗晶Cu的ba值為65.08mV/dec,而經ECAP12道次變形后的超細晶Cu的ba值為50.55mV/dec。根據Stem-Geary公式,腐蝕電流密度Icorr可以被描述為[7]:
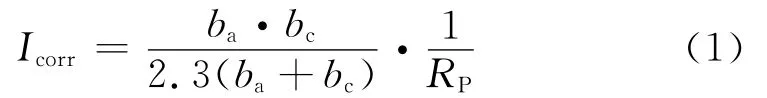
基于公式(1),計算極化電阻RP,計算結果見表1,極化電阻Rp隨變形道次的增加而增大,在Tafel區的初始階段,超細晶Cu的腐蝕速率比粗晶Cu低,粗晶銅比超細晶銅更易受到腐蝕。
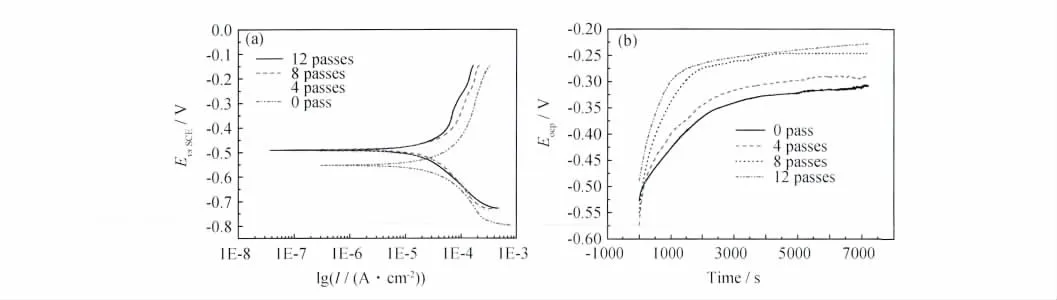
圖2 粗晶Cu和超細晶Cu在0.5mol/L NaCl溶液中的Tafel曲線(a)與E-t曲線(b)Fig.2 The Tafel plots(a)and E-t curves(b)of CG copper and UFG copper in 0.5mol/L NaCl solutions
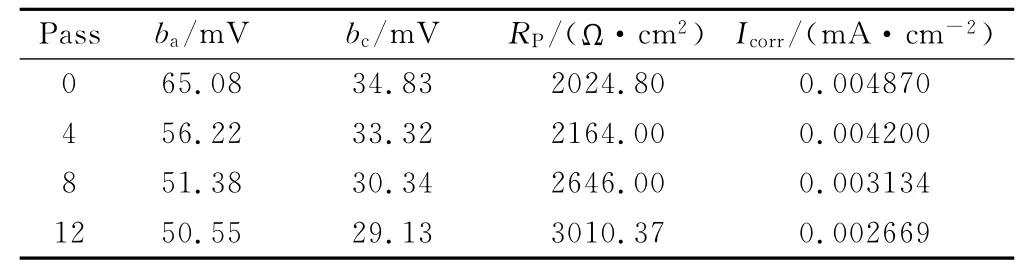
表1 腐蝕參數的擬合結果Table 1 The fitted corrosion parameters
圖2(b)為不同變形道次純銅在0.5mol/L NaCl溶液中開路電位Eocp與時間曲線,可以看出,NaCl溶液中不同狀態的純銅,其電位隨時間的變化趨于正,電極電位在初始階段變化速率較快,隨著時間的延長,腐蝕速率趨于恒定;在整個變化過程中,超細晶銅的電極電位隨時間的變化較為緩和,未發生電極電位突變,經過2h的浸泡,各狀態銅的開路電位都比浸泡初期上升了200mV左右。同時從圖2(b)的曲線對比看出:在任一時間,超細晶銅的開路電位都低于粗晶銅,超細晶銅的電位穩定所需時間比粗晶銅要短,穩定后12道次ECAP變形后的超細晶銅的開路電位Eocp比粗晶銅高100mV左右,表明超細晶銅的耐蝕性比粗晶銅要好,這一結果與Tafel曲線結果是一致的。
2.2 浸泡腐蝕性能
圖3給出了超細晶Cu和粗晶Cu在0.5mol/L NaCl溶液中浸泡4周失重率隨時間變化曲線。由圖3對比不難看出,超細晶和粗晶Cu失重率隨時間變化均表現出相似的行為,隨著浸泡時間的延長,在NaCl溶液中腐蝕速率明顯下降;在實驗時間內,相對于未進行ECAP的粗晶Cu而言,超細晶Cu的失重率明顯低于粗晶Cu。對于兩組超細晶試樣而言,4道次和12道次擠壓材料腐蝕速率接近,12道次的失重率略低于4道次的失重率,這說明隨著變形道次的增加,純Cu在NaCl溶液中的耐蝕性逐漸提高。在浸泡前期不同狀態的腐蝕速率差別較大,隨時間延長差別逐漸縮小,經過3周后,其腐蝕速率幾乎相等,說明粗晶Cu初始階段較易發生腐蝕,當在銅表面產生一層不溶于水的保護膜后,可以較好地阻止腐蝕的進一步進行。
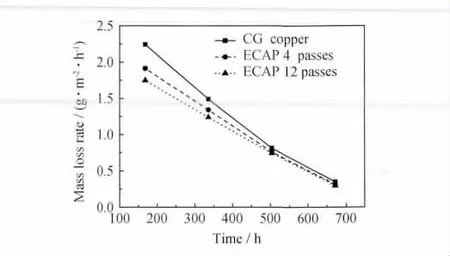
圖3 粗晶Cu和超細晶Cu在0.5mol/L NaCl溶液中的浸泡腐蝕速率Fig.3 Corrosion rate of CG copper and UFG copper in 0.5mol/L NaCl solutions
通過掃描電子顯微鏡觀察,可發現超細晶Cu和粗晶Cu試樣腐蝕膜的微觀形貌有明顯不同,如圖4所示。圖4(a),(b)為退火態粗晶 Cu和12道次ECAP變形后超細晶Cu在0.5mol/L NaCl溶液中自然浸泡680h后的腐蝕形貌。不難看出,粗晶材料和超細晶材料的產物表層形貌特征有很大不同。對于粗晶Cu試樣,腐蝕非常不均勻,晶內和晶界腐蝕都比較嚴重,晶粒之間的堆積并不十分緊密,形成了大量的孔洞,腐蝕產物比較疏松,這樣將明顯降低對腐蝕介質的阻礙效果;而超細晶Cu表面腐蝕比較均勻而且相對光滑,局部的晶界腐蝕較小,晶粒間的空隙較少,堆積緊湊,能夠有效地阻礙腐蝕介質和試樣表面接觸,因此隨時間的延長腐蝕速率明顯降低,這樣也就不難理解為何其腐蝕速率低于粗晶Cu。圖4(c)是超細晶Cu對應的腐蝕產物能譜,從產物分析看,純銅在NaCl溶液中的主要腐蝕產物為CuCl和Cu2O。

圖4 在0.5mol/L NaCl溶液中浸泡680h后的SEM 形貌和EDS分析 (a)粗晶Cu;(b)超細晶Cu;(c)EDSFig.4 SEM images and EDS analysis for copper immersed in 0.5mol/L NaCl solutions after 680h (a)CG Cu;(b)UFG Cu;(c)EDS
為進一步分析超細晶Cu的不均勻腐蝕狀況,圖5給出了超細晶Cu和粗晶Cu浸泡不同時間后電位-時間曲線和動電位掃描曲線,從圖5(a)可以看出,隨著浸泡時間的延長,超細晶Cu和粗晶Cu的自腐蝕電位呈現增大的趨勢;圖5(b)動電位掃描曲線顯示浸泡時間延長,鈍化區間增大,鈍化電流較小;這說明浸泡時間增加,形成腐蝕膜的孔隙率減小,膜的生長更加完整,膜的致密性增大,離子穿越腐蝕膜內的阻力增大,這樣腐蝕膜對基體的保護作用便增大。比較超細晶Cu和粗晶Cu電極電位的變化,可以看出,盡管超細晶Cu的穩定電位略低于粗晶Cu,但其變化非常平緩,在浸泡4h后其電位隨時間緩慢變化趨于正,表示保護膜增強了;當浸泡72h后,其電位幾乎不隨時間變化,表示已經形成穩態的保護膜,表明表面膜的形成過程非常穩定,腐蝕速率已恒定,未出現局部腐蝕現象。粗晶Cu的電極電位隨時間變化波動非常大,通常發生突變,表明金屬表面膜在不斷地生成又不斷地被破壞,出現局部腐蝕,反映了點蝕信息,表明粗晶Cu的孔蝕比超細晶Cu劇烈,在浸泡4h后比浸泡72h后電極電位波動大,說明粗晶Cu的孔蝕隨浸泡時間減弱。圖5(b)動電位掃描曲線粗晶銅(72h)腐蝕電流密度低于超細晶銅曲線,主要由于粗晶銅的局部腐蝕嚴重,導致試樣表面某些區域快速溶解腐蝕并且點蝕向縱深發展,離子擴散路徑長,實際腐蝕面積大于計算面積,腐蝕電流密度測量值偏小,但腐蝕損失卻大于超細晶銅(見圖3)。
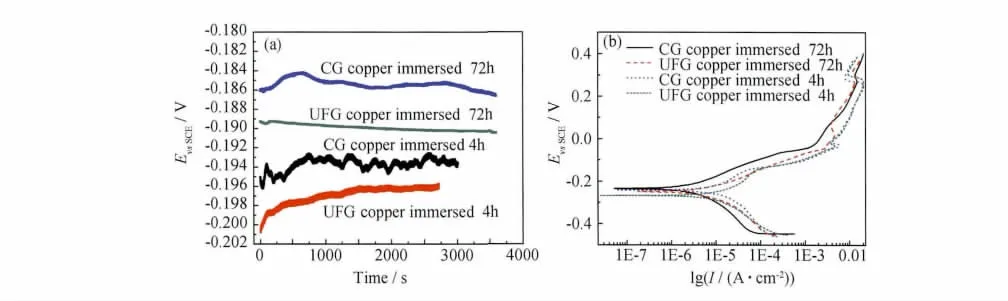
圖5 在0.5mol/L NaCl溶液中浸泡不同時間后超細晶Cu和粗晶Cu的E-t曲線(a)與極化曲線(b)Fig.5 The E-t curves(a)and polarization curves(b)of CG copper and UFG copper in 0.5mol/L NaCl solutions immersed different time
從分析可以得出,超細晶Cu穩態電極電位比粗晶Cu低,腐蝕電流密度大,這是由于超細晶Cu的晶界體積分數大引起的,但其抗點腐蝕性高,主要原因是晶粒細化使雜質均勻分布,降低了點蝕機會,而易發生均勻腐蝕。
3 討論
當有Cl-存在的海水及鹽類溶液中,會加劇銅的腐蝕,使銅在溶液中發生溶解。海水及鹽類溶液中的腐蝕情況大致相同[8,9],鹽的存在使海水的導電性提高,溶解氧含量增高,這些因素為銅的電化學腐蝕提供了條件。研究結果一致表明,銅的陽極溶解只與Cl-濃度有關而與pH值無關。當Cl-濃度小于1mol/L時,銅的腐蝕機理如下[10]:
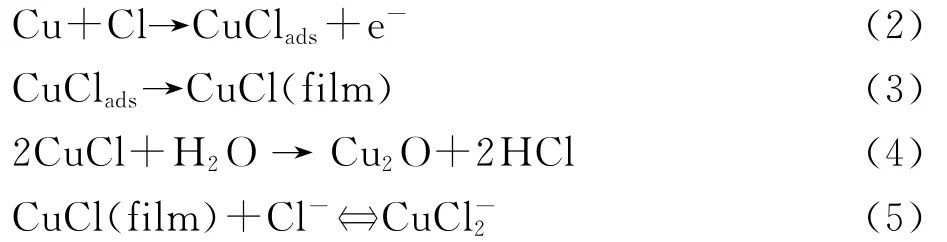
由于Cl-被吸附在銅電極表面上,它對銅的侵蝕性很強,所產生的腐蝕產物為CuCl,CuCl不溶于水,見反應式(2)和(3);產物表層的CuCl可以和H2O作用生成Cu2O,使膜下溶液局部酸化,見反應式(4),Cu2O同樣不溶于水,在CuCl表面形成另一層腐蝕產物膜,銅在電解液中是以亞銅離子的形式保護表面;Cu在NaCl溶液中活性區的溶解機制,是以的形式溶解并受其擴散控制,見反應式(5);當Cu表面出現過飽和溶液時,反應式(5)就發生逆反應生成CuCl,而CuCl是不溶性的,它阻礙了Cl-向電極表面擴散和由表面向本體溶液的擴散,因此,銅在NaCl溶液中隨時間的延長,腐蝕速率下降,腐蝕的主要產物為CuCl和Cu2O。
在不均勻結構材料中,由于晶界和位錯處于高能態,晶界相對于晶內具有較低的半電池電位,因此,在電極表面的電位空間分布不均。不均勻腐蝕與晶內和晶界的半電極電位有關,如果晶內和晶界的電位分布相差減小,晶界的局部腐蝕將減小。當晶內面積比晶界面積大得多,晶界很容易受到攻擊發生局部腐蝕,而隨著晶粒尺寸的減小,晶界比例的升高,晶界的局部腐蝕降低[11]。晶粒尺寸減小可以有效阻止雜質在晶界的偏聚,Rofagha等[12]報道了通過電沉積獲得的納米晶鎳,由于隔離和稀釋了晶界的雜質,有效改善了不均勻腐蝕和晶界腐蝕。隨后Kim等[13,14]的研究也證實了這一點,他們觀察到細晶材料的腐蝕表面非常光滑,在晶界發生較小的滲透腐蝕,因此有效改善了晶間腐蝕。Palumbo等[15,16]估算隨晶粒尺寸變化晶間區域(晶界和三叉界等)的體積分數,研究雜質沿晶界分布規律,根據分析,如晶粒尺寸從10μm變化到0.3μm,晶間體積分數從0.03%升高到1%左右,而晶界雜質的稀釋度卻高達1/30,例如,對于雜質含量為0.04%(原子分數,下同)純銅,對于粗晶Cu雜質幾乎是100%地分布于晶界,而對于超細晶Cu雜質分布于晶界的約為4%,雜質從100%變化到4%,如此大的變化有效降低了晶界腐蝕。晶粒細化后,一方面由于晶界體積分數的增加,使腐蝕性能降低;另一方面主要由于晶粒尺寸變小,雜質沿晶界分布減少,更均勻地分布于晶內和晶界,從而使腐蝕更均勻,有效地改善了材料的腐蝕性能。綜合分析表明,雜質分布均勻性要比晶界增加對腐蝕性能的影響大,因此,超細晶材料具有較好的腐蝕性能。從電化學分析和微觀腐蝕形貌來看,粗晶材料的局部腐蝕現象十分嚴重,超細晶材料的腐蝕較為均勻,超細晶Cu耐蝕性提高。
4 結論
(1)室溫條件下,ECAP制備的超細晶Cu在0.5mol/L NaCl溶液中的自腐蝕電位和腐蝕電流低于退火態粗晶Cu,腐蝕的主要產物為CuCl和Cu2O。
(2)從電化學分析和微觀腐蝕形貌來看,超細晶材料的腐蝕表面非常光滑,在晶界發生較小的滲透腐蝕,有效改善了晶間腐蝕,腐蝕較為均勻;粗晶材料的局部腐蝕現象十分嚴重,超細晶Cu耐蝕性提高。
(3)鈉鹽溶液的浸泡實驗和E-t曲線測定,證實了超細晶Cu發生了均勻腐蝕而粗晶Cu易發生局部腐蝕。
(4)超細晶Cu具有較好的腐蝕性能,主要由于晶粒尺寸變小,雜質沿晶界分布減少,更均勻地分布于晶內和晶界,從而使腐蝕更均勻,有效地改善了材料的腐蝕性能。
[1]SUN P L,KAO P W,CHANG C P.High angle boundary formation by grain subdivision in equal channel angular extrusion[J].Scripta Materialia,2004,51(6):565-570.
[2]羅雷,楊冠軍,王慶娟,等.等徑角擠壓超細晶純銅的耐腐蝕性能[J].機械工程材料,2010,34(8):51-52.LUO Lei,YANG Guan-jun,WANG Qing-juan,etal.Corrosion resistance property of ultra-fine grain copper by equal channel angular pressing[J].Materials for Mechanical Engineering,2010,34(8):51-52.
[3]WANG L C,LI D Y.Mechanical,electrochemical and tribological properties of nanocrystalline surface of brass produced by sandblasting and annealing[J].Surface and Coatings Technology,2003,167(2-3):188-196.
[4]VINOGRADOV A,MIYAMOTO H,MIMAKI T,etal.Corrosion,stress corrosion cracking and fatigue of ultra-fine grain copper fabricated by severe plastic deformation[J].Ann Chim Sci Mat,2002,27(3):65-75.
[5]BALYANOV A,KUTNYAKOVA J,AMIRKHANOVA N A,etal.Corrosion resistance of ultra fine-grained Ti[J].Scripta Materialia,2004,51(8):225-229.
[6]CHUNG M K,CHOI Y K,KIM J G,etal.Effect of the number of ECAP pass time on the electrochemical properties of 1050Al alloys[J].Materials Science and Engineering A,2004,366(2):282-291.
[7]張寶宏,從文博,楊萍.金屬電化學腐蝕與防護[M].北京:化學工業出版社,2005.
[8]盧琳,李曉剛,杜翠薇,等.銅在0.5mol/L NaCl溶液中的縫隙腐蝕現象探討[J].環境裝備工程,2007,4(3):31-34.LU Lin,LI Xiao-gang ,DU Cui-wei,etal.Approach to copper crevice corrosion phenomenon in 0.5mol/L NaCl solution[J].Equipment Environmental Engineering,2007,4(3):31-34.
[9]NUNEZ L,REGUERA E,CORVO F,etal.Corrosion of copper in seawater and its aerosols in a tropical island[J].Corrosion Science,2005,47(2):461-484.
[10]趙春梅.模擬苦咸水中銅腐蝕行為的研究[D].北京:北京化工大學,2000.
[11]MIYAMOTO H,HARADA K,MIMAKI T.Corrosion of ultrafine grained copper fabricated by equal-channel angular pressing[J].Corrosion Science,2008,50(5):1215-1220.
[12]ROFAGHA R,LANGER R,EL-SHERIK A M,etal.The corrosion behavior of nanocrystalline nickel[J].Scripta Metallurgica et Materialia,1991,25(12):2867-2872.
[13]KIM S H,ERB U,AUST K T,etal.The corrosion behavior of nanocrystalline electrodeposits[J].Plat Surf Finish,2004,91(4):68-70.
[14]KIM S H,FRANKEN T,HIBBARD G D,etal.Effect of pH on the corrosion behavior of nanocrystalline cobalt[J].Journal of Metastable and Nanocrystalline Materials,2003,15-16:643-648.
[15]PALUMBO G,THORPE S J,AUST K T.On the contribution of triple junctions to the structure and properties of nanocrystalline materials[J].Scripta Metall Mater,1990,24(7):1347-1350.
[16]WANG N,PALUMBO G,WANG Z,etal.On the persistence of four-fold triple line nodes in nanostructured materials[J].Scripta Metall Mater,1993,28(2):253-256.

