雙黃連注射劑導致類過敏反應的特點
仇士東,劉兆華,劉兆平
(1.山東省醫療器械產品質量檢驗中心 山東省醫療器械生物學評價重點實驗室,山東 濟南 250101;2.山東大學新藥評價中心,山東 濟南 250012)
隨著中藥注射劑在臨床的廣泛應用,其不良反應,尤其是嚴重速發型超敏反應逐年增多,嚴重制約了現有品種的臨床應用。中藥注射劑的速發型超敏反應已成為當前藥物毒理學研究領域的重要課題。速發型超敏反應包括Ⅰ型超敏反應和類過敏反應(anaphylactoid reaction)[1],其中類過敏反應的研究相對較少。同Ⅰ型超敏反應相似,類過敏反應也是通過激活組織內的肥大細胞或循環中的嗜堿性粒細胞脫顆粒釋放過敏介質,作用于平滑肌細胞和血管內皮細胞等效應細胞,引發局部或系統性過敏癥狀。但兩者激活肥大細胞和嗜堿性粒細胞的機制和發病特征具有明顯不同[1],最主要區別在于類過敏反應首次給藥即發生反應,且具有劑量依賴性[2],在臨床上容易被誤診為Ⅰ型超敏反應。據國外統計,77%的臨床過敏反應為類過敏反應[1]。據國內統計,雙黃連注射劑的不良反應居中藥注射劑之首,大多為首次給藥即發生過敏反應。因此推測,雙黃連注射劑可能引起類過敏反應。雙黃連注射劑類過敏反應機制研究對中藥注射劑的發展具有重要意義。本研究采用大鼠、犬和小鼠等動物模型研究雙黃連注射劑類過敏反應的特點,為其他中藥注射劑的類過敏反應研究提供參考。
1 材料與方法
1.1 實驗動物
BN大鼠,體質量170~200 g,雌性,SPF級,北京維通利華實驗動物技術有限公司提供,動物生產許可證號:SCXK(京)2006-0009。比格犬,體質量10~12 kg,雌性,購于上海市新岡實驗動物中心,動物生產許可證號:SCXK(滬)2007-0009。C57BL/6小鼠,體質量18~22 g,雌性,SPF級,北京維通利華實驗動物技術有限公司提供,動物生產許可證號:SCXK(京)2006-0009。
1.2 試劑和儀器
注射用雙黃連,哈藥集團中藥二廠,批號:1012236;Co mpound 48/80,批號:021 M4011 V;伊文思藍,批號:MKBH2094 V,美國Sig ma公司;大鼠和犬組胺及補體SC5b-9,C4d和Bb ELISA試劑盒,美國Rapid Bio公司。Infinite 200多功能酶標儀,瑞士TECAN公司;MP150多導生理記錄儀,美國Biopac公司。
1.3 BN大鼠分組及血壓、血清Ig E、組胺以及補體SC5b-9、C4d和Bb的測定
取BN大鼠25只,平均分為5組,分別為生理鹽水,Compound 48/80 0.34 mg·kg-1以及雙黃連注射劑187.5,375和750 mg·kg-1組,采用微量注射泵恒速120 ml·h-1靜脈推注給予生理鹽水、Co mpound 48/80和雙黃連注射劑。根據《中國藥典》2010版一部關于雙黃連注射劑質量標準,其臨床擬用量為60 mg·kg-1,根據體質量折算,大鼠用量375 mg·kg-1相當于臨床用量。
ip給予3%戊巴比妥鈉1.5 ml·kg-1麻醉大鼠,束縛于固定板。大鼠頸部剃毛,消毒,剪開頸部皮膚,用眼科鑷分離一側頸動脈,結扎遠心端,動脈夾夾住近心端,在動脈夾和遠心端結扎處,小心剪取一小口插入充滿肝素鈉溶液的動脈插管并結扎,打開動脈夾,記錄血壓。分離對側頸靜脈,做靜脈插管,連接注射器,管內充滿肝素鈉溶液。給藥前10 min,給藥后0,2,10,30和60 min記錄大鼠動脈血壓,血壓采用Biopac Acknowledge 4.1軟件采集數據并進行數值統計比較,以藥前平均動脈壓(mean artery pressure,MAP)為基準,降壓幅度≥2.66 k Pa時,認為藥物具有明顯的降壓作用。同時在給藥前10 min,給藥后0,2,10,30和60 min分別取頸動脈血,每次約0.6 ml,同時補充相同體積的肝素鈉溶液以保持血容量不變。血液靜置30 min后,1000×g離心10 min取上清,置-80℃凍存。大鼠血清中Ig E、組胺及補體SC5b-9、C4d和Bb均采用ELISA試劑盒檢測。每只大鼠每個指標均設2個平行樣。
1.4 比格犬的分組及血壓、血清IgE、組胺以及補體SC5b-9、C4d和Bb的測定
取比格犬20只,分為5組,每組4只,分別為生理鹽水,Compound 48/80 0.1 mg·kg-1及雙黃連注射劑56.4、112.8和225.6 mg·kg-1組,分別給予生理鹽水、Compound 48/80和雙黃連注射劑。根據《中國藥典》2010版一部關于雙黃連注射劑質量標準,依據體質量折算,犬用量為112.8 mg·kg-1。
比格犬前肢靜脈注射3%戊巴比妥鈉1 ml·kg-1麻醉,固定于保溫手術臺上。腹股溝處消毒,分離股靜脈,做靜脈插管,以備注射藥物。分離同側股動脈,做動脈插管,連接壓力傳感記錄血壓信號。血壓穩定后,采用微量注射泵恒速120 ml·h-1給藥,全程記錄血壓。采用Biopac Acknowledge 4.1軟件采集數據并進行數值統計比較,以藥前MAP為基準,降壓幅度≥2.66 k Pa時,認為藥物具有明顯的降壓作用。同時股動脈定點采血,每次2 ml,采血后補足相同體積的肝素鈉溶液以保持血容量不變。于藥前20 min,藥后2,10,30,60和120 min采血。血液靜置30 min后,1000×g離心10 min取上清,置-80℃凍存。犬血清中Ig E、組胺及補體SC5b-9、C4d和Bb均采用ELISA試劑盒檢測,每只犬每個指標均設2個平行樣。
1.5 小鼠的分組及皮膚血管滲透性的測定
取C57BL/6小鼠20只,拉丁方分組法分成5組,每組5只,分為生理鹽水,Co mpound 48/80 0.1 mg·kg-1及雙黃連270,540和1080 mg·kg-1組,分別給予生理鹽水,Co mpound 48/80和雙黃連注射劑。根據《中國藥典》2010版一部關于雙黃連注射劑質量標準,小鼠用量為540 mg·kg-1。
小鼠ip給予1.5%戊巴比妥鈉5 ml·kg-1麻醉后,剃去背部毛發。尾靜脈注射50μl 0.5%伊文思藍溶液,15 min后分別在每只小鼠背部左右側sc給予雙黃連注射劑,60 min后處死小鼠,取背部皮膚,剪碎后組織浸出液(丙酮∶生理鹽水=7∶3)(V/V)10 ml浸泡48 h,并測量其610 n m處吸光度值,計算伊文思藍含量(μg·c m-2)。
1.6 統計學分析
2 結果
2.1 雙黃連注射劑致大鼠平均動脈壓降低
大鼠給予雙黃連注射劑后,全程監測血壓的變化。如圖1所示,Compound 48/80組在0~2 min MAP由14.7 k Pa降至8.0 k Pa,在2 min后出現了MAP的劇烈變化,且在60 min以內未見MAP的恢復。與生理鹽水組比較,雙黃連注射劑375和750 mg·kg-1組給藥后2~10 min MAP顯著降低(P<0.05),而187.5 mg·kg-1組 MAP未見明顯變化。
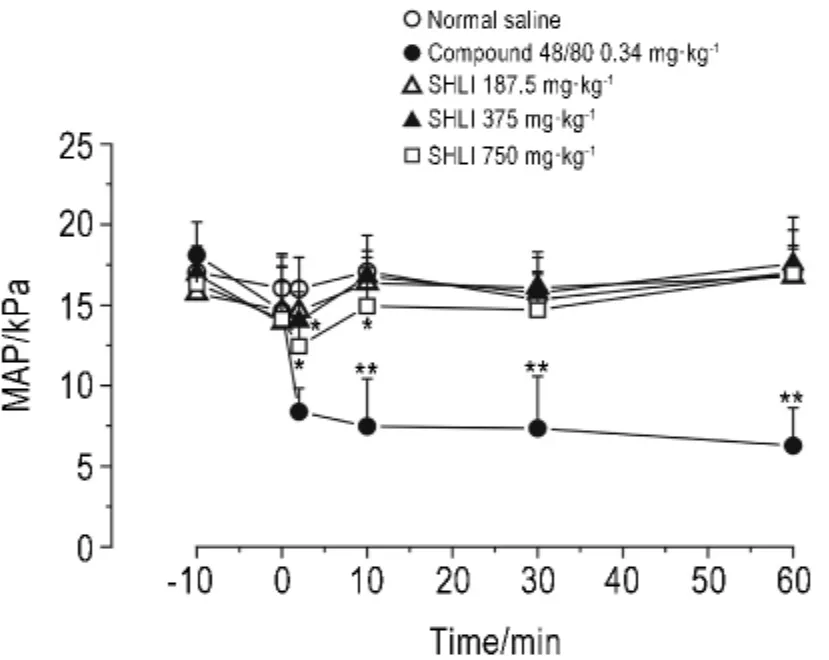
Fig.1 Effect of Shuanghuanglian injection(SHLI)on mean artery pressure(MAP)of r ats.The MAP of rats was detected 10 min bef ore ad ministration(-10 min)and 0,2,10,30 and 60 min after ad ministration.±s,n=5.*P<0.05,**P<0.01,compared with nor mal saline group.
2.2 雙黃連注射劑致大鼠血清組胺和補體SC5b-9含量升高
由表1和表2可見,大鼠給藥后2~10 min,與給藥前(-10 min)比較,雙黃連注射劑375和750 mg·kg-1組組胺升高(P<0.05,P<0.01),Ig E水平未見明顯變化。Co mpound 48/80組與給藥前比較組胺升高(P<0.01),Ig E水平不變,為典型的類過敏反應特點。由表3可見,與生理鹽水組比較,雙黃連注射劑375和750 mg·kg-1組給藥后2~10 min SC5b-9含量升高(P<0.05)。由圖2可見,大鼠給予雙黃連注射劑后,與生理鹽水組比較,補體C4d和Bb濃度未見明顯變化。由此初步判斷,雙黃連注射劑可導致類過敏反應,但不能完全確定是否激活了大鼠的補體途徑而引發類過敏反應。
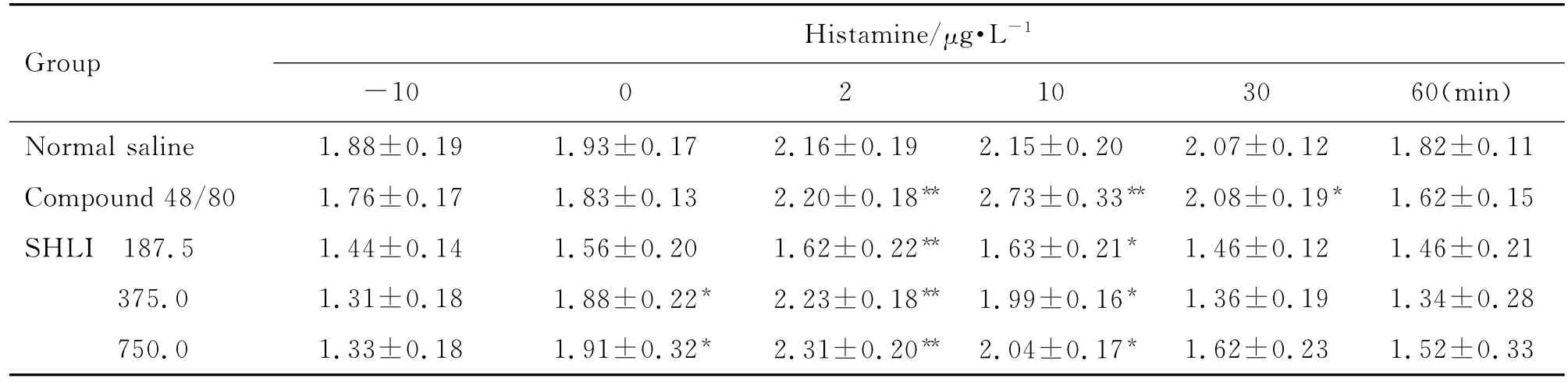
Tab.1 Effect of SHLI on serum histamine level of rats
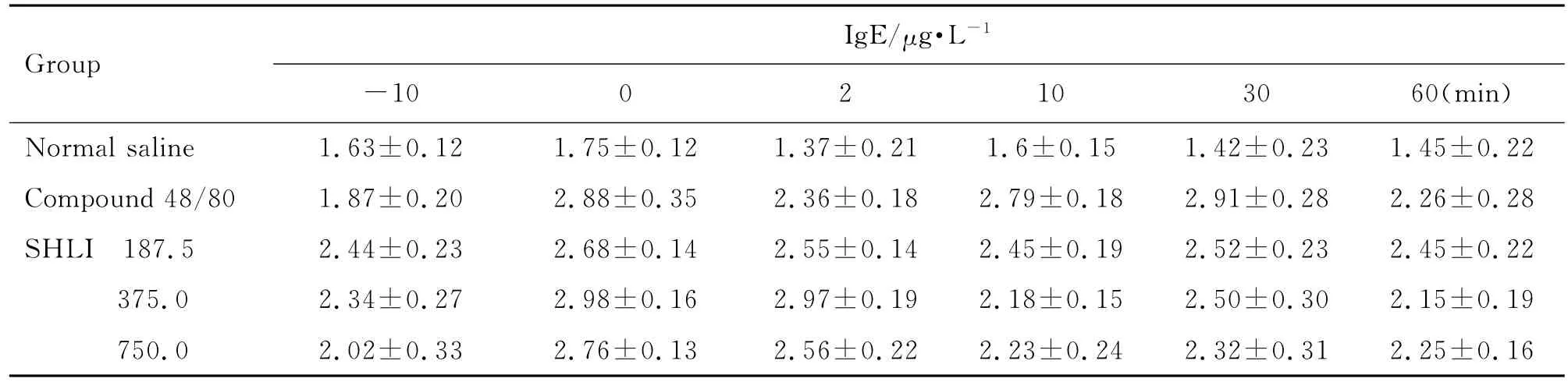
Tab.2 Effect of SHLI on ser um IgE level of rats
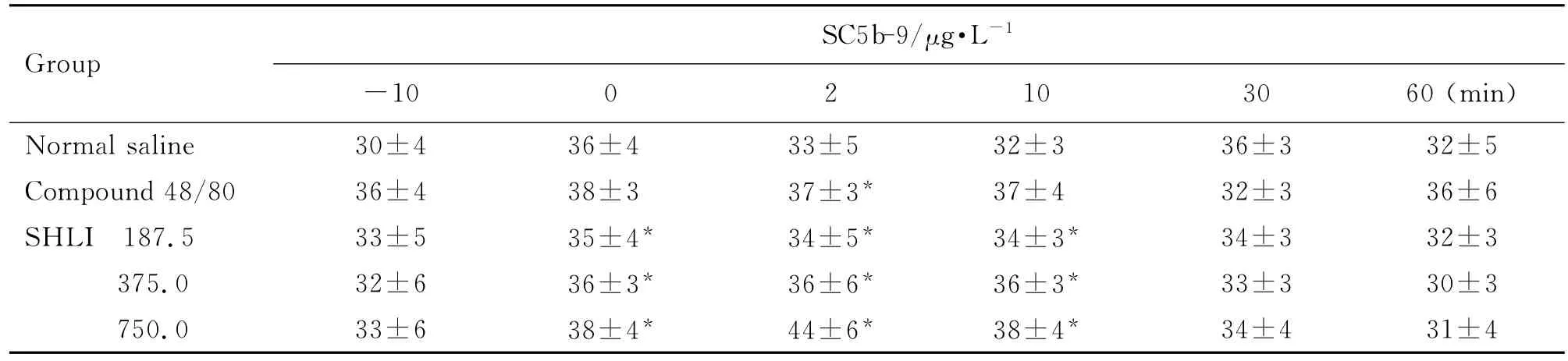
Tab.3 Effect of SHLI on ser um SC5b-9 level of rats
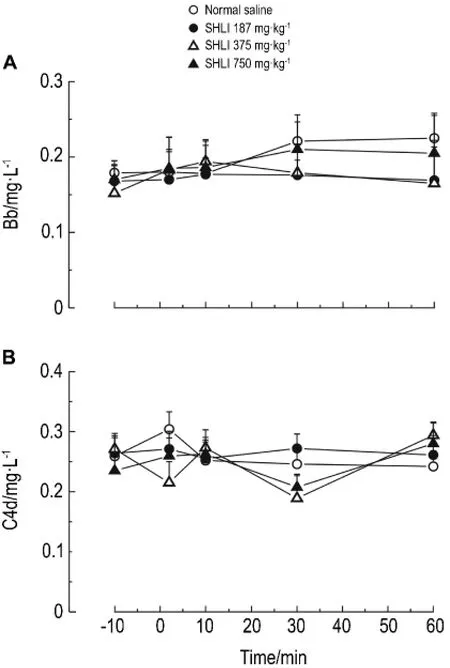
Fig.2 Effect of SHLI on complements Bb and C4d levels in rat seru m.See Fig.1 for t he rat treat ment.±s,n=5.
2.3 雙黃連注射劑致比格犬平均動脈壓降低
雙黃連注射劑按比格犬正常給藥濃度(26.7 g·L-1),以不同的靜脈給藥速度給予比格犬,全程記錄MAP的變化。如圖3所示,雙黃連注射劑在300 ml·h-1時引起 MAP的劇烈變化(圖3 A),同時出現呼吸窘迫癥狀。降低給藥速度至120 ml·h-1,MAP未見明顯降低(圖3B),呼吸亦恢復正常。因此,本研究采用120 ml·h-1速度靜脈給藥。
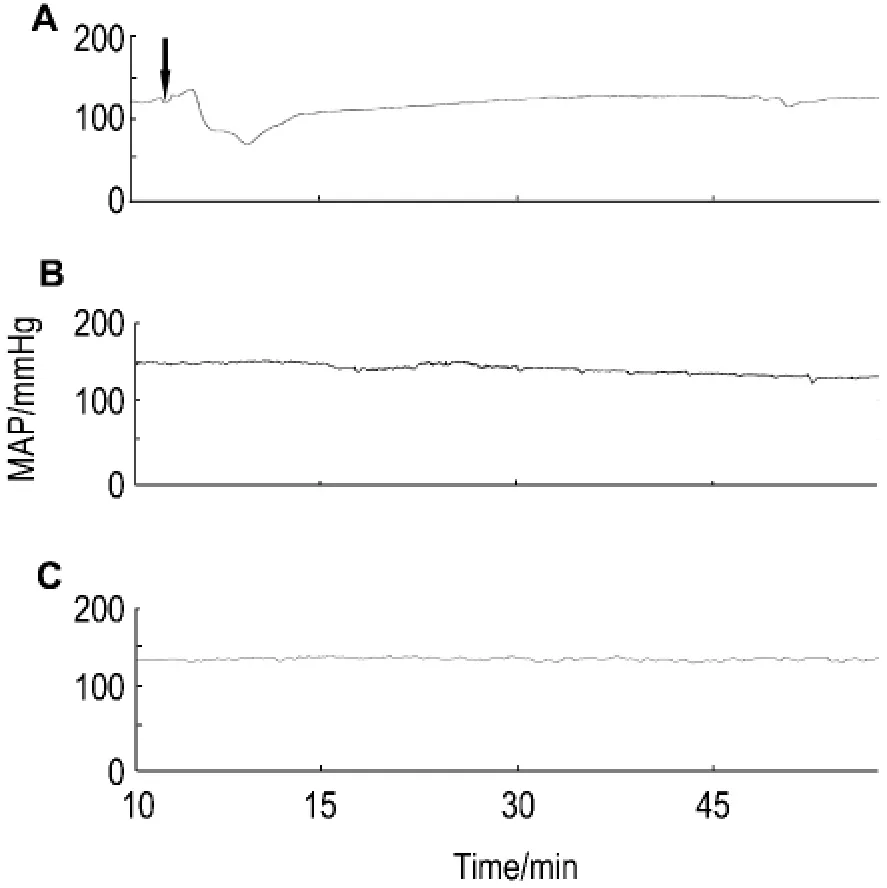
Fig.3 Effect of feed rate of SHLI 26.7 g·L-1 on MAP of Beagle dogs.A:SHLI 300 ml·h-1;B:SHLI 120 ml·h-1;C:normal saline 300 ml·h-1.
2.4 雙黃連注射劑致比格犬血清組胺和SC5b-9含量升高
由表4可見,與生理鹽水組比較,雙黃連注射劑56.4,112.8和225.6 mg·kg-1組在比格犬給藥后2~10 min組胺含量升高(P<0.05,P<0.01)。由表5可見,雙黃連注射劑56.4,112.8和225.6 mg·kg-1組Ig E未見明顯變化。由表6可見,雙黃連注射劑56.4,112.8和225.6 mg·kg-1組給藥后2~30 min犬血清中SC5b-9升高(P<0.05,P<0.01)。Co mpound 48/80組組胺升高,Ig E 不變,且SC5b-9不變,其為典型的非補體介導的類過敏反應。由圖4可看出,雙黃連注射劑56.4,112.8和225.6 mg·kg-1組補體Bb均未發生明顯變化,C4d均升高(P<0.01)。據此可初步判斷,雙黃連注射劑可導致比格犬類過敏反應,且可能屬于補體介導的類過敏反應。
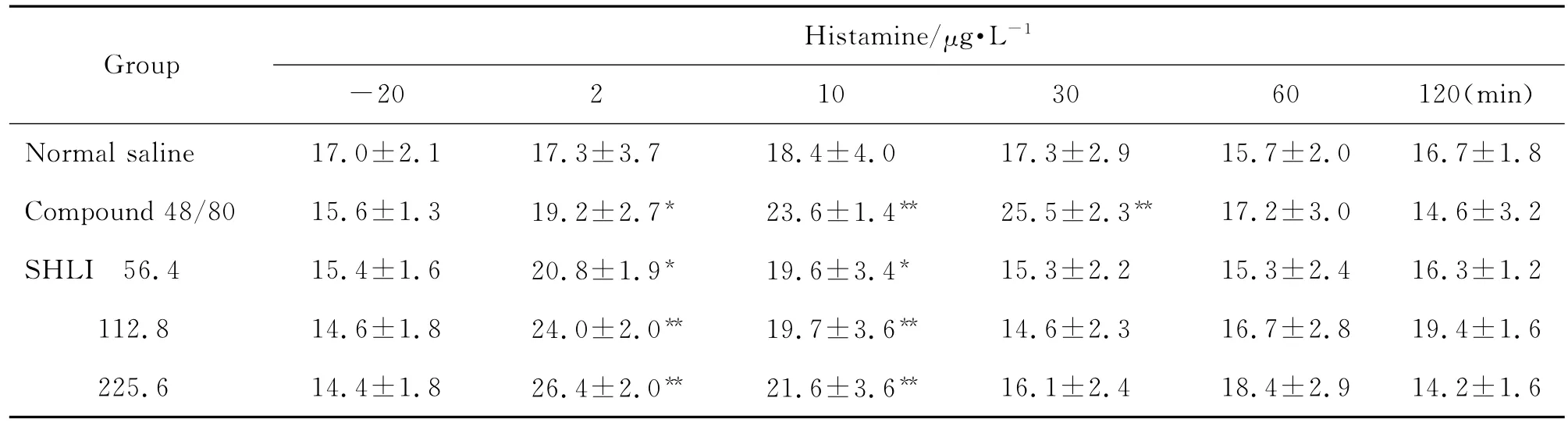
Tab.4 Effect of SHLI on ser um histamine level of Beagle dogs
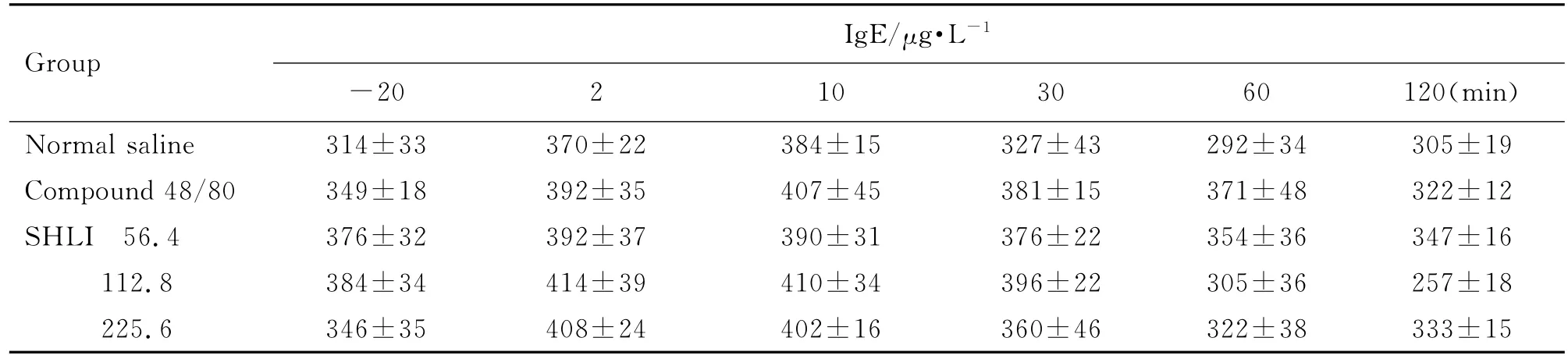
Tab.5 Effect of SHLI on serum IgE level of Beagle dogs
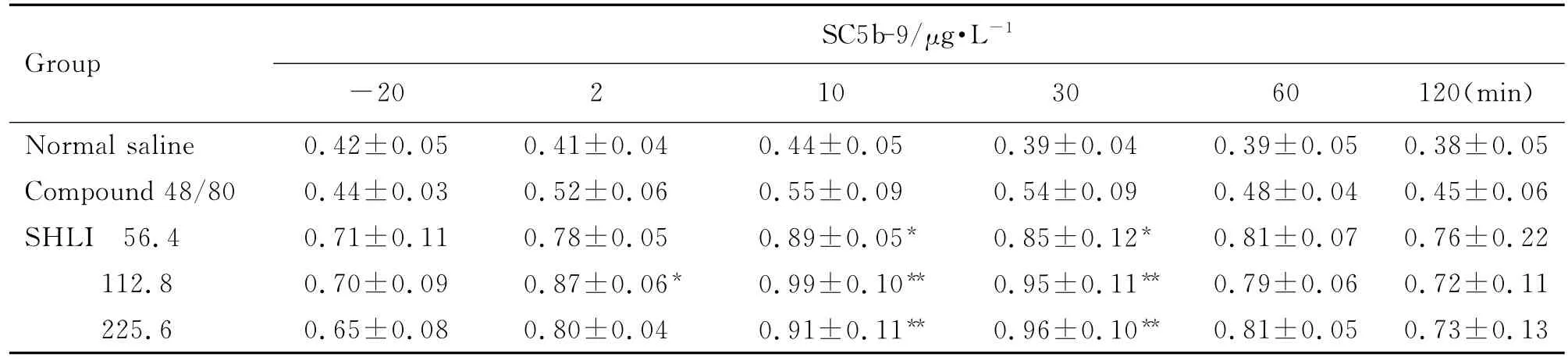
Tab.6 Effect of SHLI on ser um complement SC5b-9 level of Beagle dogs
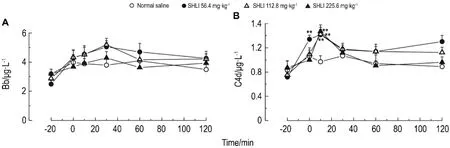
Fig.4 Effect of SHLI on ser um complements Bb(A)and C4d(B)level of Beagle dogs.See Tab.4 f or the Beagle dogtreat ment.±s,n=4.**P<0.01,co mpared wit h bef ore treat ment(-20 min).
2.5 雙黃連注射劑致小鼠皮膚血管滲透性增加
皮膚藍斑實驗結果如圖5和圖6所示。與生理鹽水組比較,Co mpound 48/80組出現明顯的藍斑浸潤(圖5B),皮膚組織中依文思藍含量升高(P<0.01)。雙黃連注射劑270,540和1080 mg·kg-1組亦出現藍斑浸潤(圖5C,D和E),依文思藍含量升高(P<0.01),且隨給藥劑量的增加,藍斑浸潤加重,依文思藍含量升高(P<0.01)。

Fig.5 Effect of SHLI on skin vascular per meability of mice.The mice were iv given 0.5%Evans blue solution 50μl in t he tail.Fifteen minutes later,SHLI was sc given on t he back skin of mice.Sixty minutes later,t he vascular per meability was measured.A:nor mal saline;B:Compound 48/80 0.1 mg·kg-1;C,D and E:SHLI 270,540 and 1080 mg·kg-1,respectively.
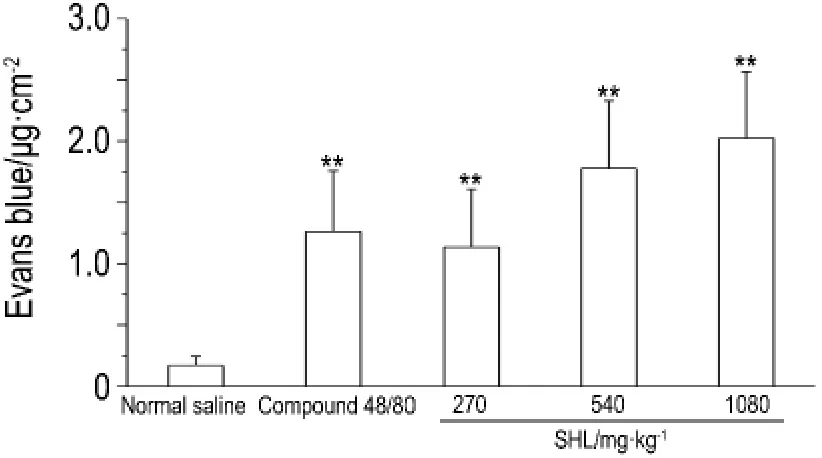
Fig.6 Effect of SHLI on Evans blue content in back skin of mice.See Fig.5 for t he mouse treat ment.±s,n=5.**P<0.01,co mpared wit h nor mal saline gr oup.
3 討論
類過敏反應的研究模型主要分為體外模型和動物模型。體外模型包括細胞模型[3-4]和體外補體激活模型等。動物模型主要有犬[5]、大鼠、小鼠[6]、豚鼠[7]、猴[7]和豬[8]等。每種模型大都以靶細胞(肥大細胞或嗜堿性粒細胞)為研究對象,探求其類過敏介質的釋放機制。類過敏反應動物模型在國內的研究相對成熟。組胺、類胰蛋白酶、特異性Ig E和補體等物質均可以作為生物標志物,用于類過敏反應的診斷[9]。組胺是類過敏反應的重要指標,較為客觀準確,但組胺正常值有較大的個體差異。血清組胺水平與臨床變應癥狀發生的一致性尚有待于進一步確證[9]。單獨依靠組胺升高來判斷致敏性易于產生誤判。為此,本研究增加了血壓、Ig E和補體等指標進行綜合判斷,增加了評價結果的客觀性。
補體系統廣泛參與機體抗微生物防御反應以及免疫調節,是體內具有重要生物學作用的效應系統和效應放大系統[10]。補體介導的類過敏反應是類過敏反應類型中重要組成部分。補體系統激活過程依據其起始順序不同,可分為經典途徑、旁路途徑和凝集素途徑3條途徑。補體C4d和Bb分別是補體經典激活途徑和旁路激活途徑的產物,測定這兩個指標可以判斷不同的激活途徑[11]。本研究的設計思路是先進行組胺和IgE的檢測,若出現組胺升高且Ig E不變的情況,可懷疑為類過敏反應,再進一步測定補體激活情況,即檢測補體SC5b-9含量的變化。若SC5b-9含量升高,則再檢測補體通路的標志物C4d和Bb,從而進一步判斷激活的具體補體通路。
根據比格犬的實驗結果,給予雙黃連注射劑后血壓降低,血清組胺含量升高,Ig E含量不變,SC5b-9升高,說明雙黃連注射劑可以引起類過敏反應。給雙黃連注射劑后血清中C4d含量明顯上升,而Bb含量未見顯著性改變,該結果提示雙黃連注射劑激活補體系統可能是通過激活經典途徑實現的。根據大鼠的實驗結果,給予雙黃連注射劑后血壓降低,血清組胺含量升高,Ig E含量不變,SC5b-9升高,但未見C4d和Bb含量的明顯變化,可見大鼠相對犬來說,對補體的變化不甚明顯。
小鼠血管滲透性實驗中,根據藍斑面積的大小和組織浸提液提取的伊文思藍的含量變化,可判斷給藥后血管滲透性的大小。給予雙黃連注射劑后,小鼠出現劑量依賴性血管通透性增高,血管反應程度隨劑量增高而加重,這可以認為是類過敏反應的證據。小鼠的免疫系統具有非常好的特異性,小鼠皮膚中含有豐富的肥大細胞,非常適合具有直接刺激肥大細胞特點的藥物的篩選。
根據本研究不同動物模型的比較可知,犬和小鼠的類過敏反應模型具有一定的靈敏性。比較而言,大鼠模型對類過敏反應不太敏感。這也正好驗證了犬的類過敏模型的科學性。Szebeni等[12]比較了大鼠、豬和犬對脂質體的類過敏反應敏感性,認為大鼠對血壓變化不甚敏感,犬和豬可用于制備類過敏反應檢測模型。因犬對血壓的變化非常敏感,MAP的檢測具有很好的靈敏性。并且,犬的補體系統較發達,亦非常適合用于補體介導的類過敏反應的評價。閆位娟[13]比較了小鼠、豚鼠和比格犬用于評價類過敏反應的敏感性和準確性,結果也表明比格犬為最佳實驗動物。
綜上所述,雙黃連注射劑可引起類過敏反應,其特點是既可激活皮膚中的肥大細胞又可激活血液中的嗜堿性粒細胞,且具有補體介導的類過敏反應的特征。在其他種屬的動物以及人體上是否具有相似的反應,尚待進一步研究。
[1]Szebeni J.Co mplement activation-related pseudoaller gy:a new class of drug-induced acute i mmune toxicity[J].Toxicology,2005,216(2-3):106-121.
[2]FDA.Guidance for Industr y-Immunotoxicology Evaluation of Investigational New Dr ugs[EB/OL].htt p://www.fda.gov/downloads/Drugs/GuidanceComplianceRegulatoryInfor mation/Guidances/uc m079239.pdf
[3]Guo W,Chen YC,Liu SP,Cheng JD.Detection met hods of mast cells degranulation in vitr o[J].Chin J Pat hophysiol(中國病理生理雜志),2002,18(8):1023-1024.
[4]Li J,Jin J,Guan CW,Li P,Tu JS,Sun H M,et al.Study of degranulation in mast cell RBL-2 H3 induced by Tween 80[J].Drug Eval Res(藥物評價研究),2010,33(5):379-383.
[5]Wang ZG, Wang DQ, Yu YH, Li YK,Sui Y,Cui HF.Experi mental model of hista mine-induced anaphylactoid reaction on Beagle dogs[J].China J Chin Mater Med(中國中藥雜志),2011,36(14):1842-1844.
[6]Li CY,Liang AH,Gao SR,Liu T,Hao R,Cao CY,et al.Develop ment of ani mal model for anaphylactoid test of rodent[J].China J Chin Mater Med(中國中藥雜志),2011,36(4):488-491.
[7]Sun L,Liu XM,Wang X,Qi WH,Shen LZ,Li B.Tentative exploration in reasons of ani mals′pseudoallergic reactions caused by Tween 80[J].J Toxicol(毒理學雜志),2007,21(4):322.
[8]Szebeni J,Fontana JL,Wassef NM,Mongan PD,Morse DS,Dobbins DE,et al.Hemodynamic changes induced by liposomes and liposome-encapsulated hemoglobin in pigs:a model for pseudoallergic cardiopul monary reactions to liposomes.Role of complement and inhibition by soluble CR1 and anti-C5a antibody[J].Circulation,1999,99(17):2302-2309.
[9]Cheng F,Shi YQ,qin HD,Liu ZP.Inquiry into the biomarkers of drug anaphylactoid reactions[J].Chem Life(生命的化學),2008,28(6):795-798.
[10]Chen WF.Medical Immunology(醫學免疫學)[M].4th ed.Beijing:People′s Medical Publishing House,2004:49-59.
[11]Szebeni J,Baranyi L,Savay S,Milosevits J,Bodo M,Bunger R,et al.The interaction of liposomes with the complement system:in vitro and in vivo assays[J].Methods Enzy mol,2003,373:136-154.
[12]Szebeni J,Alving CR,Rosivall L,Bünger R,Baranyi L,Bed?cs P,et al.Animal models of complement-mediated hypersensitivity reactions to liposomes and other lipid-based nanoparticles[J].J Liposome Res,2007,17(2):107-117.
[13]Yan WJ. The allergenicity study of traditional Chinese medicine injections(中藥注射劑致敏性研究)[D].Guangxi Medical University,2009.

