某混合銅礦生物浸出銅的試驗研究
胡杰華,謝洪珍,董博文,朱莞燁,范道焱
(廈門紫金礦冶技術有限公司,福建 廈門 361101)
細菌浸出是借助某些細菌的催化作用,直接或間接地氧化含銅硫化物,使銅浸出[1]。低品位銅礦的細菌堆浸能耗低、工藝簡單、投資少、環境污染小、適應性強,但浸出周期長、浸出速率慢[2-3]。細菌浸出過程既有細菌生長繁殖和生物化學反應,又有浸出劑和礦物的化學反應。由于細菌生長繁殖速度比礦物化學浸出反應慢得多,所以細菌的生長狀況是整個細菌浸出過程的制約環節。金屬礦物的浸出速度與浸出介質中細菌的濃度成正比,要取得礦物浸出的高速度,須保持細菌生長繁殖的高速度,而做到這一點的重要條件就是提供細菌生長所必需的足夠營養物質[4-5]。一般礦石中都含有鎂、鉀、鐵等無機鹽,需要補充的主要有氮、磷元素,因此,研究細菌浸出過程中鐵、氮、磷元素的濃度變化對細菌活性及金屬浸出率的影響很有意義。
1 試驗部分
1.1 試驗礦樣
試驗礦樣取自黑龍江某銅礦,其中主要有用礦物為氧化銅、斑銅礦、黃銅礦,脈石礦物為石英、斜長石、絹云母、綠泥石等。礦石呈土狀及皮殼狀。礦石多元素和銅物相分析結果見表1、2。銅平均品位為0.32%,屬低品位混合銅礦。
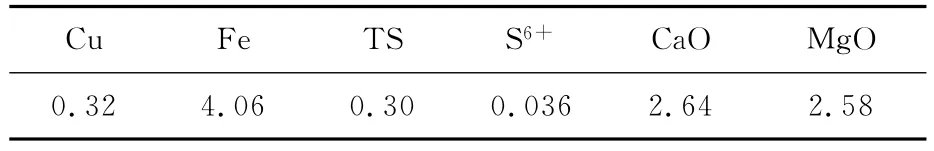
表1 混合銅礦多元素分析結果 %
混合銅礦理論耗酸量為109.4kg/t。-200目占90%的礦石加入自來水,攪拌,用硫酸調礦漿pH至2.0,并穩定6h,實際耗酸量為46.83 kg/t。礦石實際酸耗量低于理論酸耗量。
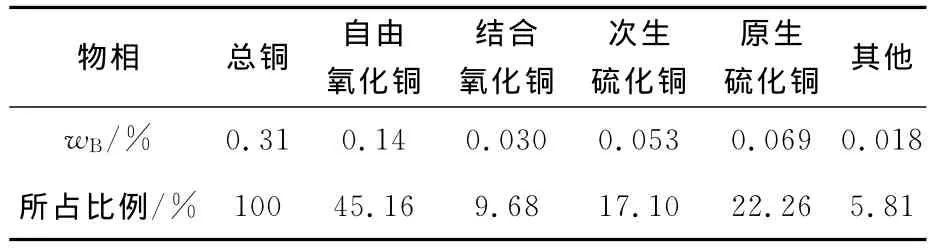
表2 混合銅礦物相分析結果 %
礦石中的銅以氧化銅為主,次生硫化銅占17.10%,原生硫化銅占22.26%,礦石氧化率為54.84%,為典型的混合礦。結合氧化銅因與脈石礦物之間有致密的包裹關系和共生關系,較難與浸出劑發生反應;而原生硫化銅因化學鍵結構牢固,不易被外力破壞,較難被氧化。
1.2 試驗方法及藥劑
1.2.1 試驗方法
搖瓶浸出試驗:搖瓶浸出試驗在恒溫振蕩器中進行。取120mL 9K培養基于150mL錐形瓶中,按20%接種量加入菌液30mL,調初始pH至1.8,搖瓶振蕩至電位升至530mV,加入一定量礦石,控制體系pH維持在1.8左右。室溫下振蕩一段時間后,過濾,渣、液分別送分析。
3L半連續浸出試驗:在室溫和一定pH條件下培養菌液,當電位達到600mV后分批次加入磨細后的礦樣,使最終礦漿濃度為10%。氧化過程中,用碳酸鈉或硫酸調整體系pH為2.0。當電位穩定且大于600mV一段時間后,取樣。每次取樣300mL,過濾,返回濾液270mL,補加礦樣30g,并用自來水補足所差液量,繼續攪拌。
柱浸試驗:將破碎至一定粒度的礦石裝入直徑為200mm的柱中,先用6g/L硫酸溶液噴淋至浸出液pH穩定在2.0以下,再用菌液循環噴淋,每天測Eh、pH,并補水至指定刻度,維持總液量不變。每周取樣并補充相同體積的9K培養基,檢測浸出液pH、Eh及Cu、Fe、N、P、H2SO4濃度,判斷細菌的生長狀況、銅浸出速率、浸出周期和最終浸出率。模擬現場條件,采用6g/L硫酸溶液循環噴淋,當浸出液pH>1.5時,換新的6 g/L硫酸溶液,持續噴淋。
1.2.2 分析方法
水樣中的金屬離子用日本HITACHI公司生產的原子吸收分光光度計測定,氨氮用UV-5200比色測定,總磷用美國PE公司的電感耦合等離子體發射光譜儀測定;渣樣中的銅用原子吸收分光光度計測定,鐵用滴定法測定。
2 試驗結果與討論
2.1 搖瓶浸出試驗
搖瓶浸出試驗分有菌浸出和無菌浸出。細菌浸出試驗條件:室溫,礦石粒度-200目占90%,用9K培養基培養細菌,礦漿總濃度10%,體系pH控制在1.8。硫酸浸出條件為:室溫,礦石粒度-200目占90%,液固體積質量比3∶1,酸液一次性加入,攪拌反應6d。試驗結果見表3、4。
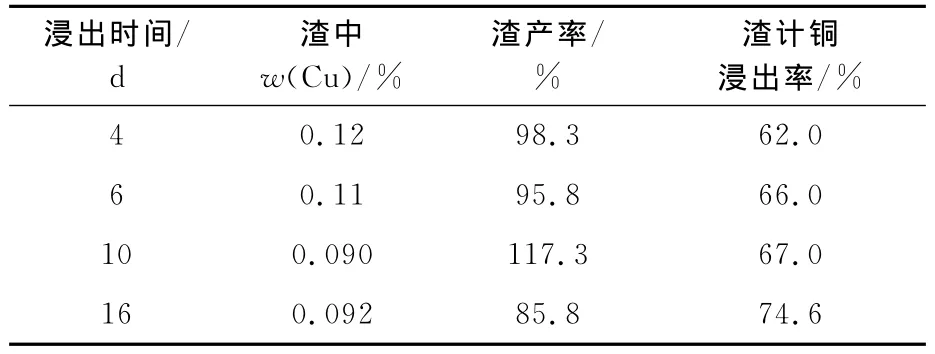
表3 混合礦細菌搖瓶浸出試驗結果
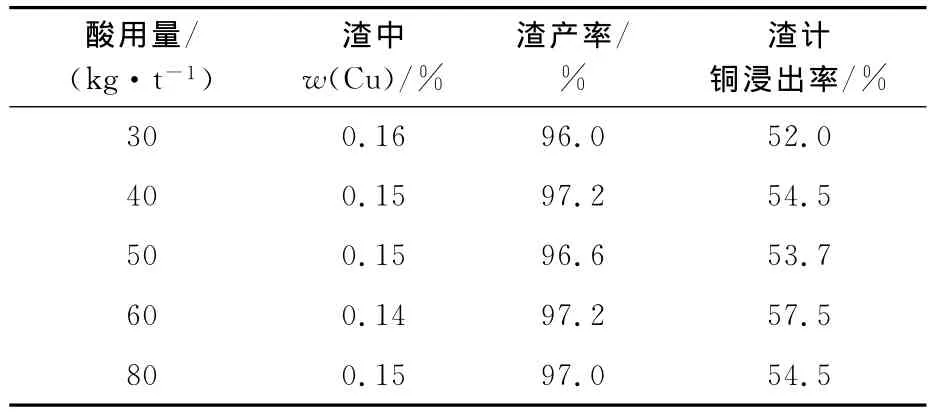
表4 無菌硫酸直接搖瓶浸出試驗結果
可以看出:與硫酸直接浸出相比,引入細菌后,體系pH需控制在1.8,即硫酸用量約為1g/L,銅浸出率即有不同程度提高;當礦漿濃度為10%、細菌浸出6d后,渣計銅浸出率達66.0%,隨浸出時間延長,銅浸出率還有進一步提高。而無菌浸出6d,硫酸用量為30~80kg/t礦,渣計銅浸出率最高僅為57.5%。
2.2 3L模擬半連續浸出試驗
試驗條件:室溫,礦石粒度-200目占90%,用9K培養基培養菌液,礦漿濃度為10%。從第35d開始,只取樣、加礦石和自來水,不添加營養物質,考察Fe、N、P的濃度變化及對生物活性的影響。試驗結果見表5。
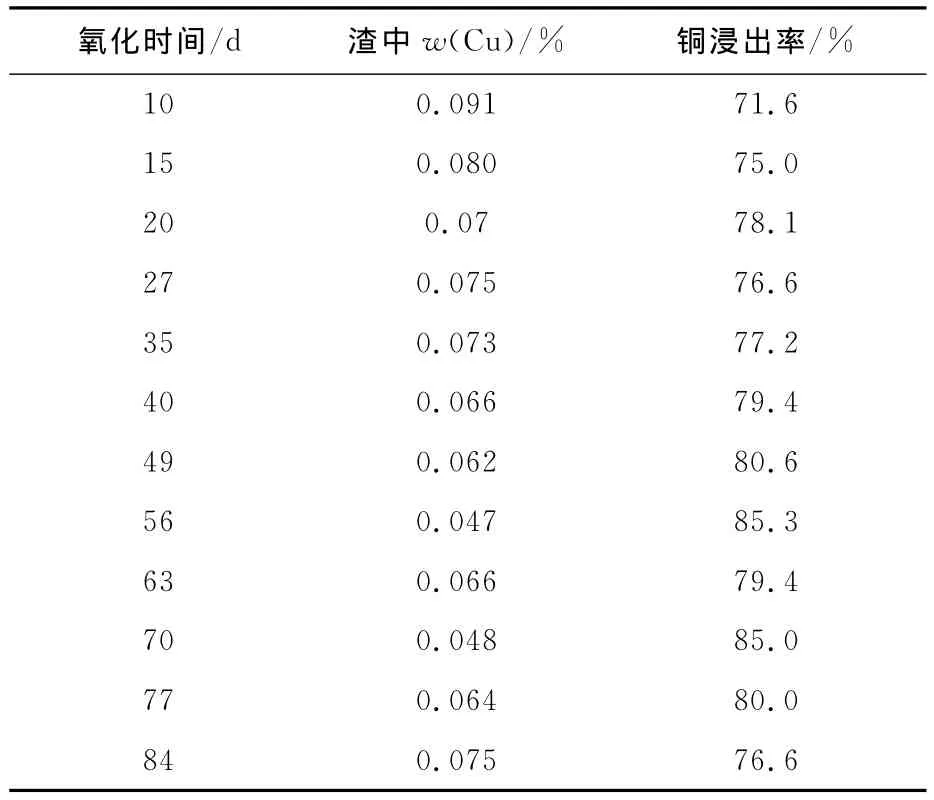
表5 氧化時間對銅浸出的影響
連續取樣12次,尾渣中w(Cu)/%基本穩定在0.075%以下,銅浸出率最高可達85.3%。氧化浸出10d,銅浸出率為71.6%,高于搖瓶浸出10d時的67.0%,說明攪拌浸出有利于提高細菌活性。
浸出35~84d,Fe、N、P質量濃度變化趨勢如圖1所示。

圖1 pH為2.0條件下,Fe、N、P質量濃度與氧化時間的關系
隨礦樣質量增加,菌液中Fe、NH+4、∑P質量濃度逐步降低,且其濃度越高,越快被消耗,但銅浸出率維持在80%左右。說明菌液對Fe、N、P的要求并不高,Fe維持在100mg/L,∑P為5 mg/L,NH4為200mg/L,菌液仍保持較高活性。實際浸出過程可根據需要補充N和P。
2.3 柱浸試驗
礦石破碎至-15mm占90%,均勻裝入有機玻璃柱中,再用6g/L硫酸溶液反復滲洗中和堿性脈石礦物,同時浸出銅。當浸出液pH連續24 h恒定在2.0以下時,接種菌液。液計浸出率及Fe、N、P質量濃度變化分別如圖2、3所示。

圖2 液計銅浸出率變化曲線
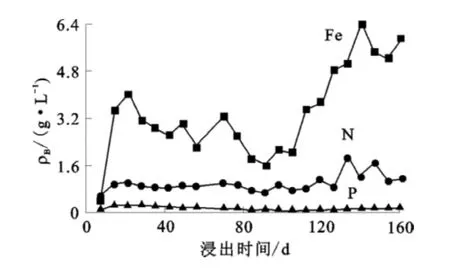
圖3 柱浸過程中,Fe、N、P質量濃度變化曲線
第1周,硫酸直接滴淋,中和脈石礦物并浸出部分氧化銅。待浸出液pH穩定在2.0以下時,加菌液滴淋。第1周硫酸耗量為10.1kg/t礦,銅浸出率為29.97%。
細菌浸出前10周,每周銅浸出率均超過1%,Fe質量濃度維持在2~4g/L,NH+4-N質量濃度保持在0.8~1.0g/L之間,而∑P質量濃度不斷降低。說明礦樣在堆浸時有必要適當補充P元素。
細菌浸出11~16周,浸出液中Fe、P質量濃度持續走低,鐵質量濃度為1.5~2.6g/L,∑P質量濃度繼續降低至17mg/L。銅浸出速率放緩,平均每周浸出率約為0.40%。故從第16周開始,每天每公斤礦石補加9K培養基0.585mL,經過一段時間的適應,第19周銅浸出速率略微提高,但隨培養基添加量的累積,從第21周起,銅浸出速率再次放緩。說明營養物質并非越多越好。
第23周,停止滴淋菌液,用pH=2.0的酸性水繼續滴淋2d后卸柱,柱浸渣表面覆蓋一層粉狀綠色物質,推測是銅的復鹽沉淀或鐵礬沉淀。為了考察沉淀物的可溶解性,對氧化渣繼續進行酸洗試驗。將柱浸渣用pH=2.0的稀硫酸溶液在1mm篩子上洗礦篩分,分為+1mm部分和-1mm部分。分析結果見表6、7。
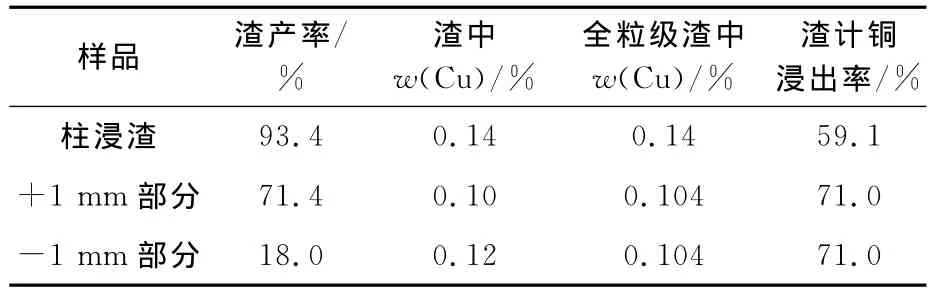
表6 柱浸渣分析結果
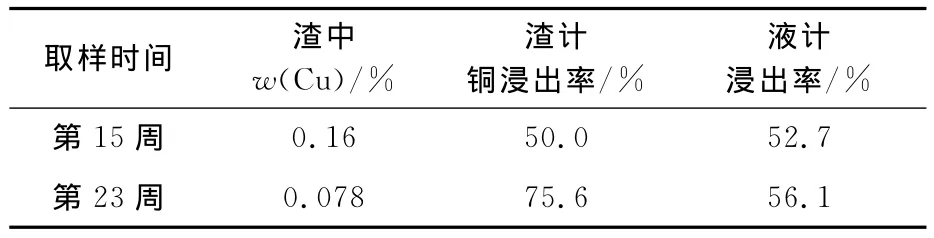
表7 柱浸表面浸出渣分析結果
第23周,表面取樣渣計銅浸出率為75.6%,卸柱后整柱縮分取樣渣計銅浸出率為59.1%。卸柱后重新用pH=2.0的硫酸溶液洗滌,渣計銅浸出率為71.0%,液計累計銅浸出率為56.1%。生物氧化柱表面取樣與卸柱后尾渣縮分取樣銅浸出率的差別可能是由于生物氧化柱pH控制在2.0左右,部分銅浸出后在柱下端析出造成的。細粒級礦石銅品位較高,進一步證明了部分銅以復鹽形式沉淀析出。用pH=2.0的稀硫酸洗滌后,尾渣平均品位降至0.104%,銅總浸出率提高到71.0%,說明部分浸出的銅在柱下端析出且析出物較易溶于稀酸中。
3 結論
某低品位混合銅礦可以用細菌浸出方式有效回收銅。體系中,Fe質量濃度維持在2~4g/L,NH+4-N質量濃度保持在0.8~1.0g/L之間,∑P質量濃度保持在5~200mg/L之間比較適宜,細菌活性良好。
礦石粒度15mm,柱浸23周,細菌浸出渣計銅浸出率達到71.0%。
生物氧化后,柱表面取樣與卸柱后尾渣縮分取樣的銅浸出率有差別,可能是由于生物氧化后,浸出的部分銅在柱下端析出造成的。用pH=2.0稀硫酸洗滌后,銅浸出率提高,說明析出物較易溶于稀酸。
[1]董鐵廣,華一新.黃銅礦濕法冶金研究進展[J].有色礦冶,2009,25(3):28-31.
[2]袁明華,李德,普倉鳳.低品位硫化銅礦的細菌冶金[M].北京:冶金工業出版社,2008:71-75.
[3]張冬艷,張通.硫化銅礦的細菌浸出試驗研究[J].濕法冶金,1996(2):23-26.
[4]賴紹師,覃文慶,楊聰仁,等.低品位硫化銅礦的細菌浸出[J].中國有色金屬學報,2011,21(6):1473-1479
[5]《浸礦技術》編委會.浸礦技術[M].北京:原子能出版社,1994:431-441.

