磷酸亞鐵鋰材料的研究與發展
費定國,林逸全
(1“國立中央大學”化學工程與材料工程系,中國臺灣 中壢 32001;2倍特利能源科技股份有限公司,中國臺灣 中壢 32001)
鋰離子電池系統是21世紀二次電池主流之一,目前已廣泛應用于個人計算機、移動電話、數碼照相機及攝錄像機等小型電子產品,由于傳統 3C產品用的鋰離子電池正極材料 LiCoO2價格昂貴,且無法承受較大的電流,使其應用范圍局限于低功率電子產品。現今環保意識逐漸抬頭,對各種電動車輛的需求更是迫切,因此,具備安全性高、循環壽命長、環境污染小、原料成本低,且能承受大電流充放電等優點的LiFePO4鋰離子電池便成為發展重點,現已應用于混合動力汽車、電動手工具、電動自行車、高爾夫球車、大型儲能裝置等各個領域,其中油電混合車、電動巴士與全電動車是未來數年內新能源汽車的主要發展方向,隨著電動車產量不斷的增加,動力 LiFePO4電池市場規模將會快速成長。
近幾年全球變暖現象日益嚴重,主要元兇來自于人類活動中排放的大量二氧化碳,各國政府提倡節能減排,挽救日益惡化的全球氣候。于2009年12月舉行的哥本哈根氣候會議,為 2012年到 2020年全球各國應對氣候變暖商議對策,并且推廣節能減排,以減少溫室氣體排放量。2009年美國能源部貸款59億美元給福特(Ford)汽車公司,發展節能減排型汽車,同年法國公布“電動車戰役”計劃,投入15億歐元發展電動車。2011年,中國“十二五”計劃提出“新能源汽車”為七大戰略新興產業之一,全力支持電動汽車科技與產業發展。過去電動車電池系統受限于傳統鋰電池的功率低與熱安全性差,無法有效發展,而目前油電混合車動力電池仍以鎳氫電池為主,但未來將會逐步被鋰離子電池所取代。
目前動力鋰離子電池的正極材料主要為LiMn2O4、LiNi1/3Co1/3Mn1/3O2與 LiFePO4等,其中LiFePO4為正交晶系(orthorhombic)橄欖石結構,理論上鋰離子可進行接近100%的嵌入與釋出反應,并且在充放電循環過程中,材料結構不會崩解或遭到破壞,其安全性與長循環穩定性皆相當優異,甚至能承受 30 C-rate以上的大電流充放電。此外,LiFePO4正極材料也具有無毒性、高安全性、低原物料成本、高熱穩定性、良好的高溫性能、平穩充放電平臺等優點,使得LiFePO4正極材料特別受到全球汽車和儲能設備大廠的重視,是未來新能源汽車與儲能系統所需的綠色材料。
1 磷酸亞鐵鋰材料研究與發展
1.1 碳涂布改質
Ravet等[1]于1999年首先提出以蔗糖作為碳源加入前體中,經由700 ℃高溫煅燒,使蔗糖產生熱裂解而獲得碳包覆的LiFePO4/C復合材料,可大幅提升材料電化學性能,于 0.1 C的充放電速率與80 ℃環境溫度下,放電電容量可達 160 mA·h/g。由于磷酸亞鐵鋰材料的導電性與鋰離子擴散度差,使得碳涂布改質對LiFePO4材料的研究發展扮演著重要的角色。材料表面涂布碳層不僅可以增強導電性,還能在制備LiFePO4/C復合材料的過程中抑制粉體團聚,甚至提高比表面積,穩定材料電化學性能。過去各國學者使用的碳源大多為純炭黑系列[2]、糖類[3]、有機酸[4-5]與分散劑[6],直到近年,碳源的種類也包括聚合物[7]、高比表面積碳材[8]與導電性高分子[9]等。此外,碳源在碳化的過程中,碳源涂布的均勻性、碳層厚度[10-11]、類石墨化碳與非石墨化碳的比值[5,12]等都是影響材料特性與電化學性質的重要因素,也是過去許多文獻探討的重點。
2008年,Fey等[5]利用高溫固態法,分別以不同的羧酸(carboxylic acid)化合物作碳源(見表1)于600 ℃煅燒溫度制備出LiFePO4/C復合材料,再以Raman光譜分析表面碳層結構,如圖1所示,于1400 cm?1及1600 cm?1處有明顯的特征峰,皆代表碳層中 sp3與 sp2中混成鍵的強度。利用折積(convolution)積分,分別計算兩特征峰的ID/IG值,見表 2,ID/IG值越小,表示有越多的類石墨化碳結構,其中使用丙二酸為碳源的LiFePO4/C復合材料具有較小的ID/IG值,而且在0.2 C的充放電速率下,具有最高的初始放電電容量149 mA·h/g。
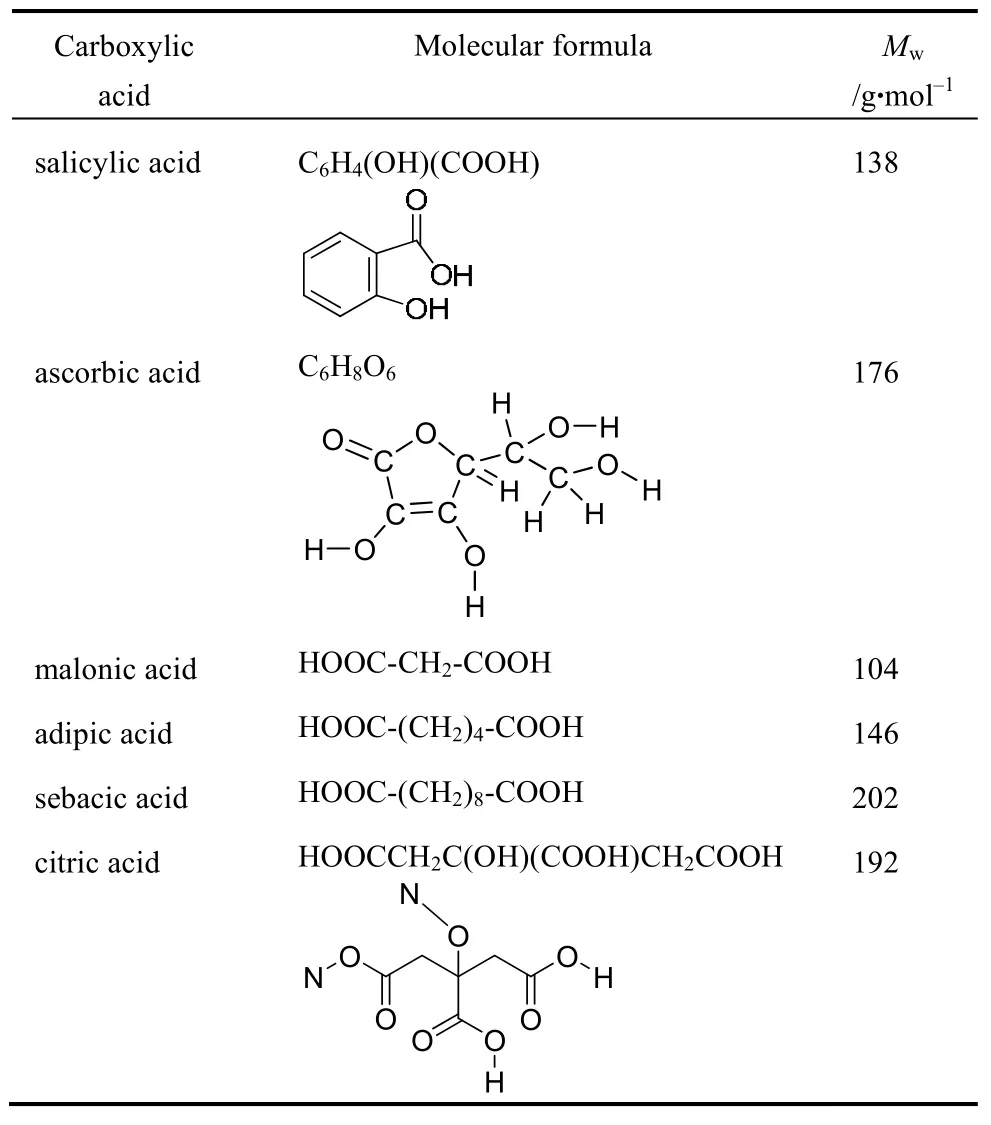
表1 合成LiFePO4/C所添加的各種羧酸[5]Table 1 LiFePO4 samples processed with organic acid additives[5]
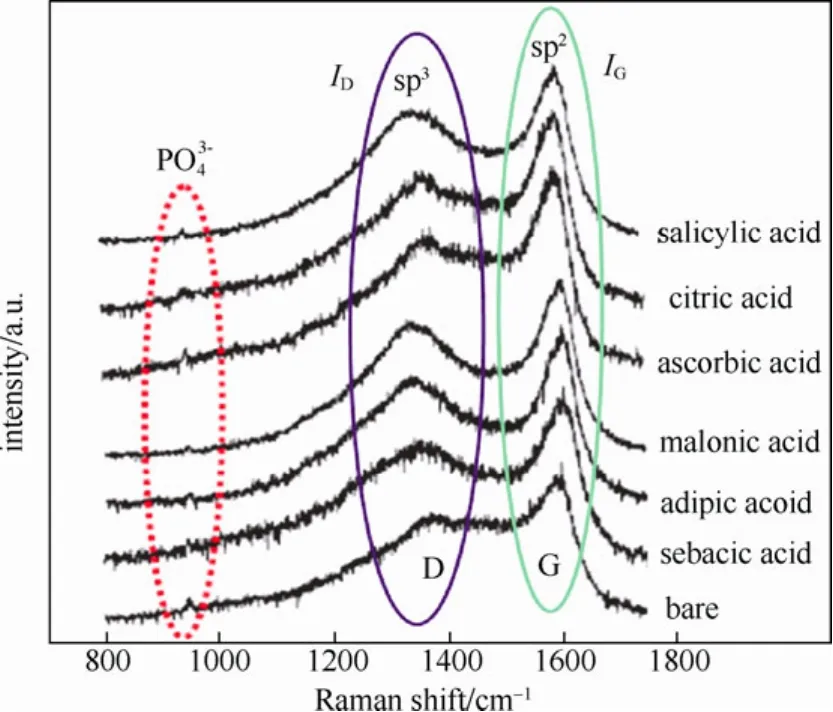
圖1 添加不同羧酸所合成出LiFePO4/C的拉曼光譜圖[5]Fig.1 Raman spectra of LiFePO4 synthesized with various carboxylic acids[5]
同年,Fey等[13]提出同類傾向同類理論(like influences like),結晶型碳層(crystalline carbon)較傾向于分布在結晶型 LiFePO4(crystalline LiFePO4)表面,而非結晶型碳層(amorphous carbon)則遠離結晶型LiFePO4表面,如圖2(a)為LiFePO4/C材料的穿透式電子顯微鏡分析圖(transmission electron microscopy,TEM)所示,深灰色區域為LiFePO4晶粒,淺灰色區域則為碳層;圖 2(b)及(c)為LiFePO4晶粒及其表面局部放大圖,其中圖2(c)顯示LiFePO4晶粒間的灰色碳層為結晶型碳,遠離LiFePO4晶粒表面的碳層為非結晶型碳。
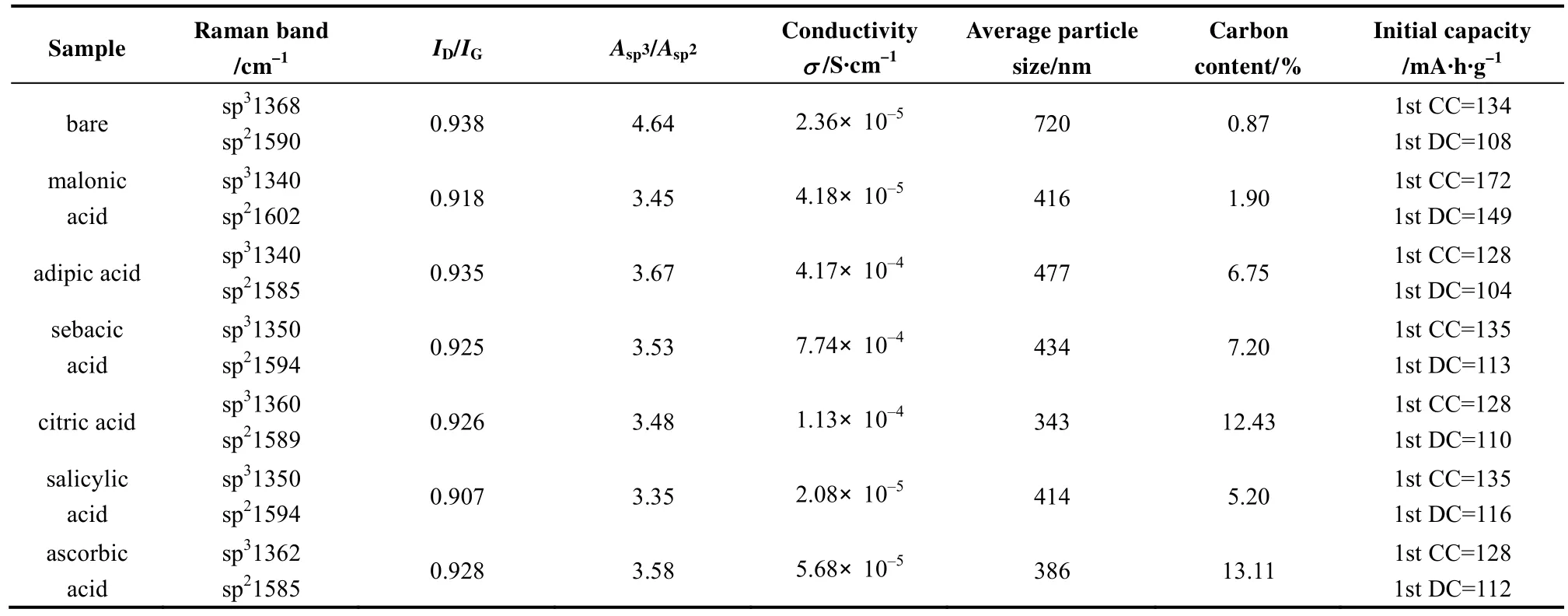
表2 添加羧酸所合成出的LiFePO4/C,其電導率、碳含量、粒徑大小、放電電容量、拉曼光譜分析[5]Table 2 Electronic conductivity, carbon content, average particle size, discharge capacity and Raman spectral analysis of LiFePO4 coated with various carboxylic acids[5]
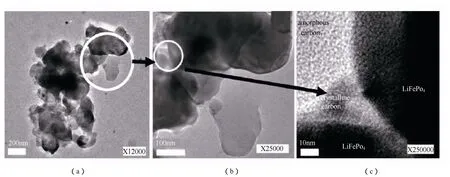
圖2 碳涂布LiFePO4表面的TEM圖[13]Fig.2 TEM micrographs of LiFePO4 coated with 60% malonic acid (a and b); a HRTEM image of LiFePO4 crystals(c)[13]
2009年,Fey等[8]利用高溫固態法,以高表面積碳材(High surface area carbon,HSAC;比表面積為2099 m2/g)為碳源,分別添加質量分數為6% 、8% 、10%與 12%的 HSAC,合成出不同材料特性的LiFePO4/C復合材料,見表3,當高比表面積碳材的添加量越多,材料的碳含量、比表面積與電導率逐漸提升,但添加質量分數為 8% HSAC的LiFePO4/C復合材料則具有最佳初始放電電容量以及長循環穩定性,如圖3所示。
同年,Fey等[11]又開發出一種新型碳蒸鍍LiFePO4的制備方法,其使用兩種不同的碳源,分別與鋰、鐵、磷起始物球磨混合,再預煅燒形成前體后,放置于管狀高溫爐內,利用碳蒸鍍方式,經過600 ℃煅燒制備成LiFePO4/C復合材料,如圖4所示。type I是以 20%(質量分數)聚苯乙烯(polystyrene,PS)為碳源的錠狀前體,type II是以50%(質量分數)丙二酸為碳源的錠狀前體。利用氣體由上游往下游的流動,將放置上游type II錠狀前體的碳蒸氣吹到下游的type I錠狀前體,使碳蒸氣能蒸鍍于type I錠狀前體表面。分別放入不同數量的type II錠狀前體,經過煅燒后的 type I錠狀前體則為主要的LiFePO4/C復合材料,其中product-1為1顆type II錠狀前體,product-2為2顆type II錠狀前體,以此類推,見表4。由表4顯示出所使用的type II前體錠越多,則LiFePO4/C的碳含量越多,電導率也較好,并同時形成不同的碳層厚度,但最佳制程條件則是使用2顆type II錠狀前體(product-2),其LiFePO4/C復合材料具有較均勻的碳層厚度,僅4~8 nm。
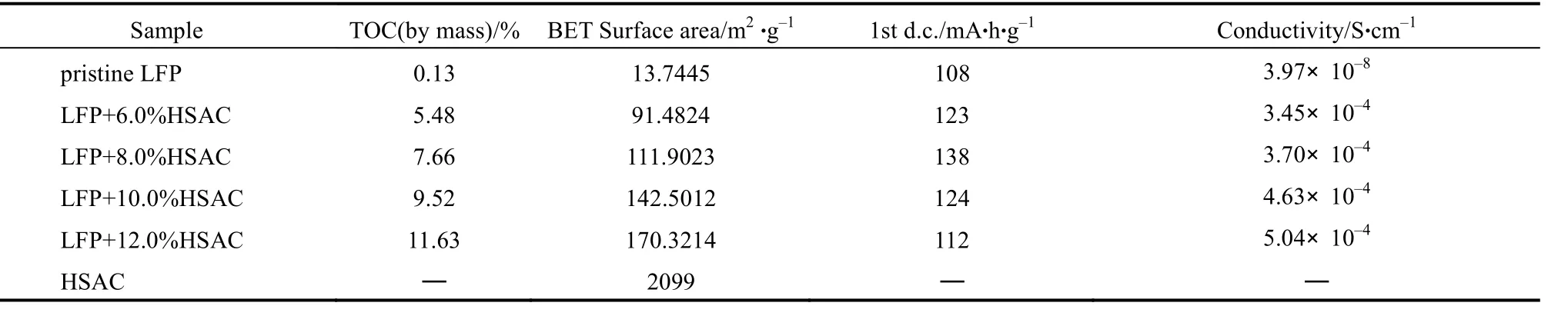
表3 以HSAC為碳源制備出LiFePO4/C復合材料的碳含量、比表面積、電導率與初始放電電容量(0.2 C,2.8~4.0 V)[8]Table 3 Carbon content, specific surface area, electronic conductivity, initial discharge capacity of the pristine LiFePO4 and various content HSAC-coated LiFePO4 cathode materials[8]
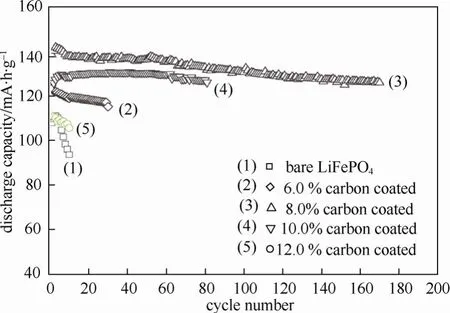
圖3 以HSAC為碳源制備出LiFePO4/C復合材料的長循環性能圖(0.2 C,2.8~4.0 V)[8]Fig.3 Cycling performance of the pristine LiFePO4 and various content HSAC-coated LiFePO4 cathode materials[8](Charge–discharge: a 0.2 C rate between 2.8 and 4.0 V)
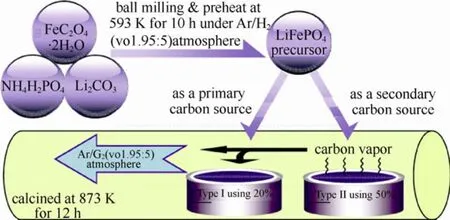
圖4 新型碳蒸鍍LiFePO4的制程方法示意圖[14]Fig.4 A schematic diagram of new carbon vapor deposition[14]

表4 新型碳蒸鍍LiFePO4/C復合材料的碳含量、電導率、碳層厚度與放電電容量(0.2 C,2.8~4.0 V)[11]Table 4 A comparison of electronic conductivity, carbon content, carbon thickness, and discharge capacity of LiFePO4/C composites[11]
2011年,Fey等[14]分別使用粒徑大小為2.75 μm、1.50 μm、0.70 μm 與 0.22 μm 的聚苯乙烯作為碳源,以高溫固態法制備出不同材料特性與電池性能的LiFePO4/C復合材料,見表5。以較小粒徑PS球為碳源,其LiFePO4/C復合材料具有較低的碳含量與比表面積,但初始放電電容量則相對較高,而以較大粒徑 PS球為碳源時,材料特性與初始放電電容量則相反,但其卻有最佳的長循環穩定性,如圖 5所示。于2.8~4.0 V截止電壓下,以0.2 C-rate進行充放電測試,當電荷維持率(capacity retention,C.R.)為80%時,使用碳源為2.75 μm PS球的LiFePO4/C復合材料,其充放電循環次數可達755次;若改變碳源為0.22 μm PS球,則充放電循環次數僅有289次。因此,不同粒徑大小的 PS球碳源,將會制備出不同材料特性的LiFePO4/C復合材料,進而影響其電化學性質。
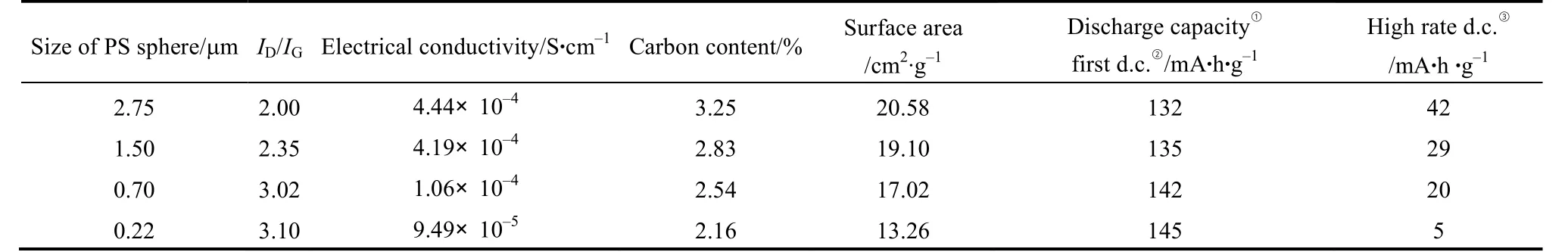
表5 不同粒徑大小的聚苯乙烯為碳源所合成的LiFePO4/C復合材料,其電導率、碳含量、比表面積、放電電容量、拉曼光譜分析[14]Table 5 Electronic conductivity, carbon content, specific surface area, discharge capacity and Raman spectral analysis of LiFePO4/C composites synthesized with different sizes of PS spheres[14]
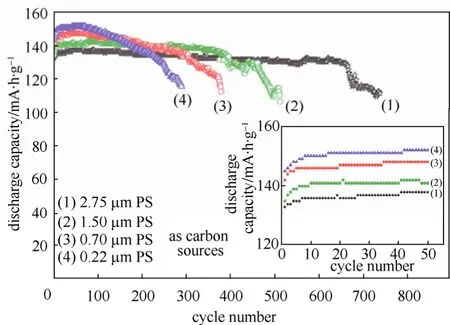
圖5 利用不同粒徑大小的聚苯乙烯為碳源,以高溫固態法所合成的LiFePO4/C復合材料,其長循環性能圖(0.2 C,2.8~4.0 V)[14]Fig.5 Long cyclability of LiFePO4/C composites using different sizes of PS spheres as carbon sources between 4.0 and 2.8 V at a 0.2 C rate[14]
1.2 金屬摻雜改質
藉由高價金屬離子化學摻雜方式提高 LiFePO4內部的電導率從而提高材料電化學性質的研究方面,Chung等[15]于2002年首先在Li1-xMxFePO4中摻入了Mg2+、Al3+、Ti4+與Nb5+等金屬元素取代Li+,將材料電導率從10-9~10-10S/cm提高至10-3S/cm以上。由于 LiFePO4或 FePO4皆屬于近絕緣體,而Li1-xMxFePO4屬于導電性較佳的非整數比化合物,因此該文獻學者認為,若陽離子缺陷固態化合物能持續地保持,電極材料將形成電導率佳的P型半導體。換句話說,若是Li+或是Fe2+能夠被較高氧化價數陽離子所取代,將能有效地增加原先為 N型半導體LiFePO4的電導率。為了提高磷酸亞鐵鋰復合材料的電化學性質,近年來已有許多學者嘗試摻雜Al[16]、Mg[17]、Ti[18]、La[19]等金屬元素進行改質,以提高材料電導率與鋰離子擴散度,改善材料電化學性質。
2008年,Fey等[19]利用高溫固態法,并且摻雜微量La過渡金屬元素,以及添加50 %(質量分數)水楊酸作為碳源,制備出LiFe0.99La0.01PO4/C復合材料。利用掃描式電子顯微鏡(scanning electron microscope,SEM)的元素分布圖(elemental mapping)與能量分散光譜(energy dispersive spectroscopy)進行鑒定,如圖 6所示,La元素均勻分布于LiFePO4材料晶體內部。此外,由表6顯示,純LiFePO4材料的電導率為5.88×10?6S/cm,而藉由La過渡金屬摻雜與碳涂布的LiFe0.99La0.01PO4/C復合材料,其電導率則提升至 3.06×10?4S/cm。由于LiFe0.99La0.01PO4/C復合材料的電導率較高,使其初始放電電容量可達151 mA·h/g。
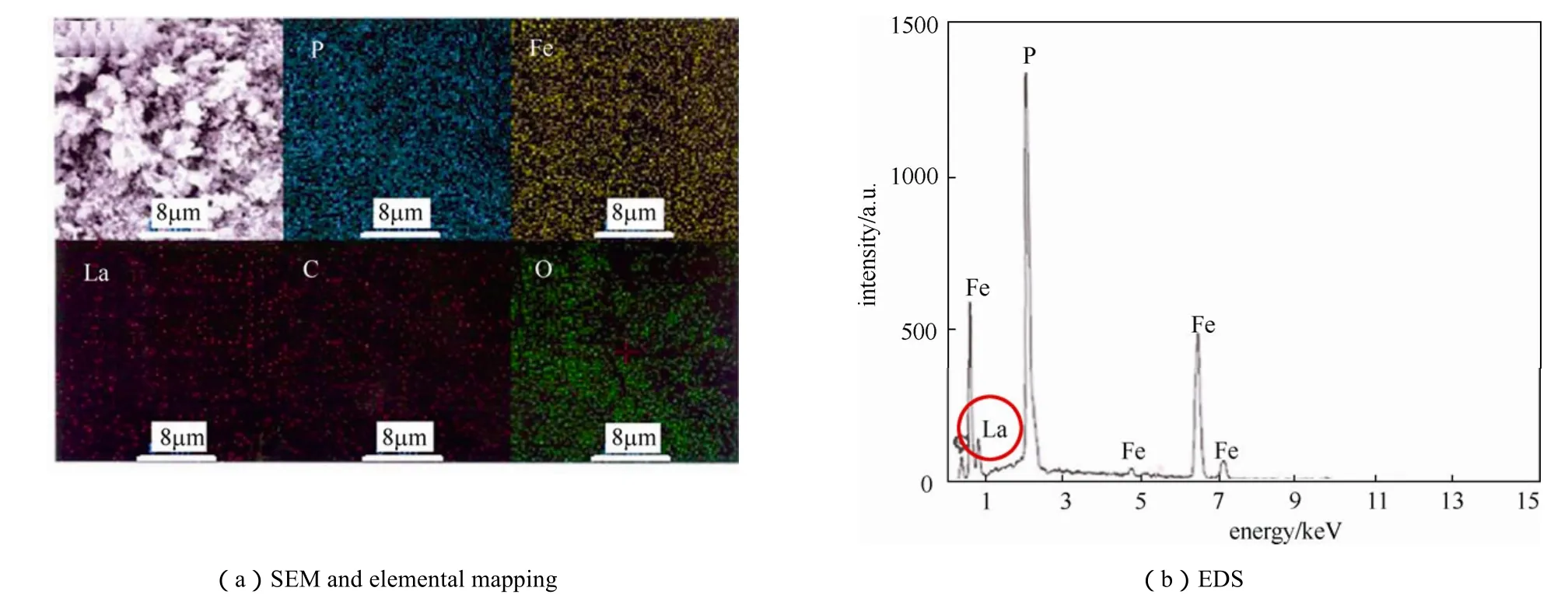
圖6 LiFe0.99La0.01PO4/C復合材料[19]Fig.6 (a) SEM micrographs and elemental mapping; (b) EDS of LiFe0.99La0.01PO4/C powders[19]
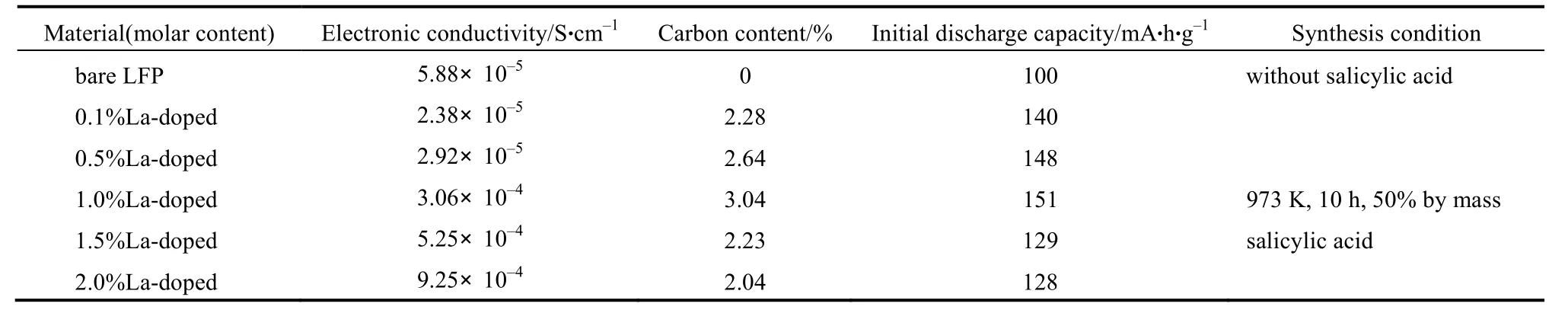
表6 純LiFePO4與不同La摻雜量的LiFePO4/C復合材料,其電導率、碳含量、初始放電電容量[19]Table 6 Electronic conductivity, carbon content and initial discharge capacity of bare LiFePO4 and various molar conten La-doped LiFePO4/C composite materials[19]
1.3 粒徑大小與振實密度的改質研究
Gaberscel等[20]在2007年提出,若欲合成出高鋰離子擴散速度的解質液,使得鋰離子易包覆在粉體表面,增加鋰離子于活性物質表面的含量,藉由提高鋰離子于LiFePO4粉體表面的擴散速度,將是提升材料承受大電流充放電能力的重要因素。因此當粉體粒徑越小時,不論表面碳層是否均勻分布,鋰離子擴散度將不再受限于粉體表面電導率,進而有較佳的電化學性質。近年已有許多學者針對磷酸亞鐵鋰復合材料的粒徑大小做了一系列的研究,皆指出粉體粒徑越小,材料電導率與比表面積越高,導致有較佳的電化學性質[21-22]。
2009年,Fey等[22]利用高速球磨與碳蒸鍍技術,分別合成出不同粒徑的商業用com-LFP/C與實驗室自行合成的 lab-LFP/C復合材料,其材料特性與初始放電電容量見表7。在電流速率0.2 C與充放電截止電壓4.3~2.8 V的電池測試條件下,不論是商業用或是實驗室自行合成的LiFePO4/C復合材料,具有最小粒徑的com-LFP/C(232 nm)與lab-LFP/C (205 nm),皆分別顯現出較高的初始放電電容量,為155 mA·h/g 與 157 mA·h/g。因此,LiFePO4/C 復合材料粒徑越小,比表面積與電導率越大,導致材料的放電電容量與長循環穩定性越佳,如圖7與圖8所示。
利用高溫固態法、溶液法、共沉淀法等制程所合成的 LiFePO4/C復合材料振實密度約為 0.6~1.0 g/cm3,導致其涂布成正極片時,其壓實密度僅有2.1 g/cm3,限制電池芯的體積能量密度,不利于實際的應用。過去研究此領域的學者皆是以特殊的制程方法來合成高振實密度材料,而且所合成出的材料皆具有以下特征: ①表面型態圓滑,類似球型的LiFePO4[23];②材料粉體粒徑越大,振實密度越高[24]。另外,碳涂布雖能使LiFePO4的電導率得以提升,但非結晶型碳是一種低密度的非電活性物質,當碳添加量增加時,將造成LiFePO4/C復合材料的振實密度下降,而且也容易抑制粉體粒徑的成長。因此,制備高振實密度的LiFePO4/C復合材料,除了適當的控制碳含量外,還必須于高煅燒溫度700 ℃以上進行合成,形成大粒徑的粉體團聚。
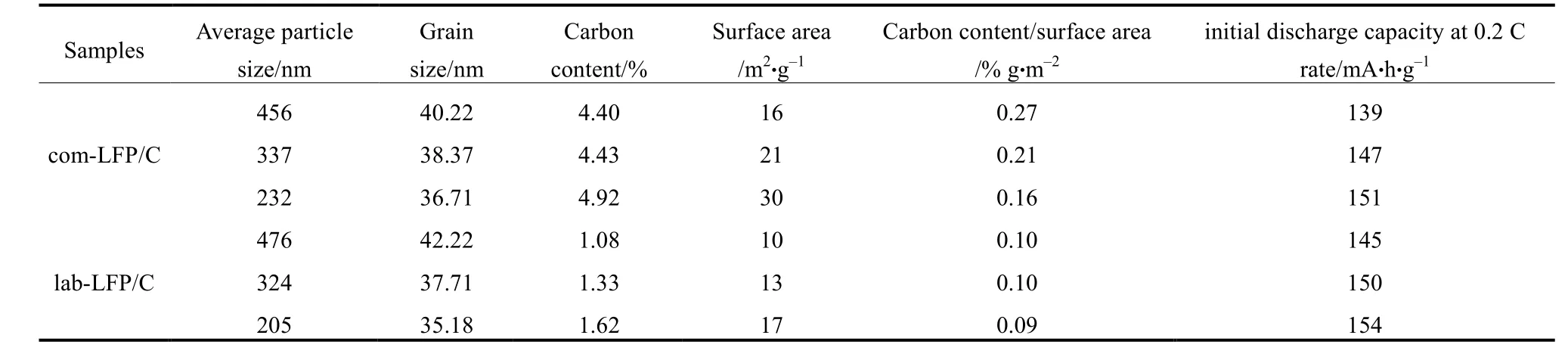
表7 利用球磨與碳蒸鍍技術,分別合成出不同粒徑的com-LFP/C以及lab-LFP/C復合材料,其材料特性與初始放電電容量[22]Table 7 A comparison of materials characterization and initial discharge capacities between commercial and in-house LiFePO4/C composites with different particle sizes synthesized by using ball milling and carbon coating techniques[22]
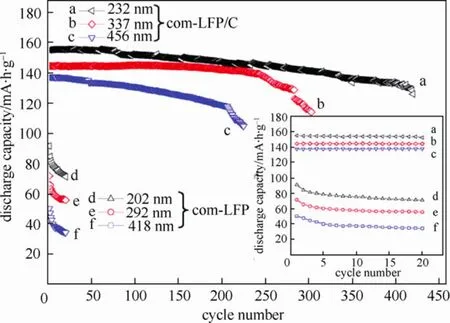
圖7 不同粒徑大小的商業用LiFePO4(com-LFP)及其復合材料(com-LFP/C)在電流速率0.2 C與充放電截止電壓4.3~2.8 V下的長循環測試圖[22]Fig.7 Cycling performance of commercial carbon-coated and bare LiFePO4 samples denoted as com-LFP/C and com-LFP, respectively, with three particle sizes com-LFP/C: (a) 232 nm, (b) 337 nm, (c) 456 nm; com-LFP:(d) 202 nm, (e) 292 nm, (f) 418 nm; at a 0.2 C rate in the voltage range of 4.3~2.8 V[22]
2012年,Fey等[25]以碳熱還原法結合KCl融鹽法(molten salt,MS)進行改質,利用 KCl于 755 ℃高溫煅燒環境下形成融熔態介質,包覆于碳熱還原法(carbon reduction,CR)所合成的LiFePO4/C粉體(CR sample)表面,修飾其表面形態為光滑且橢圓形,并且于煅燒時間1.0~5.0 h內,造成粉體團聚,二次粒徑變大,制備出高振實密度LiFePO4/C復合材料(MS sample),見表8,當融鹽煅燒時間增加時,材料振實密度明顯地增加,可提升最高振實密度至 1.69 g/cm3,但放電電容量卻隨著煅燒時間增加而減少。因此,為了兼具振實密度與放電電容量,將采用融鹽煅燒時間為1.0 h,其LiFePO4/C復合材料具有高振實密度為1.5 g/cm3,而且于0.2 C電流速率與4.0~2.8 V截止電壓下,其也有不錯的放電電容量(140 mA·h/g)。另外,從掃描式電子顯微鏡(scanning electron microscope,SEM)鑒定,如圖9所示,經過融鹽法改質的MS sample,比起未改質的CR sample,其粉體粒徑相對較大,而且MS sample也呈現出光滑且橢圓形的表面形態。
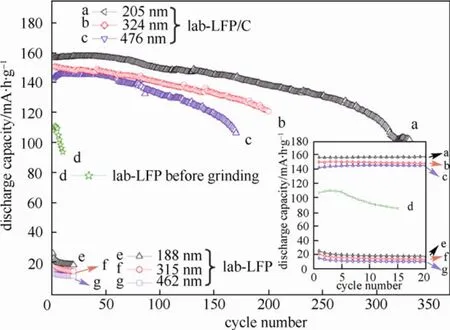
圖8 不同粒徑大小的實驗室自行合成LiFePO4(lab-LFP),及其復合材料(lab-LFP/C),于電流速率0.2 C與充放電截止電壓4.3-2.8 V下的長循環測試圖[22]Fig.8 Cycling performance of in-house ground LiFePO4 samples with three particle sizes after carbon coating: (a)205 nm, (b) 324 nm, (c) 476 nm; and in-house bare LiFePO4 samples before and after grinding: (d) no grinding, (e) 188 nm, (f) 315 nm, (g) 462 nm; at a 0.2 C rate in the voltage range of 4.3~2.8 V[22]
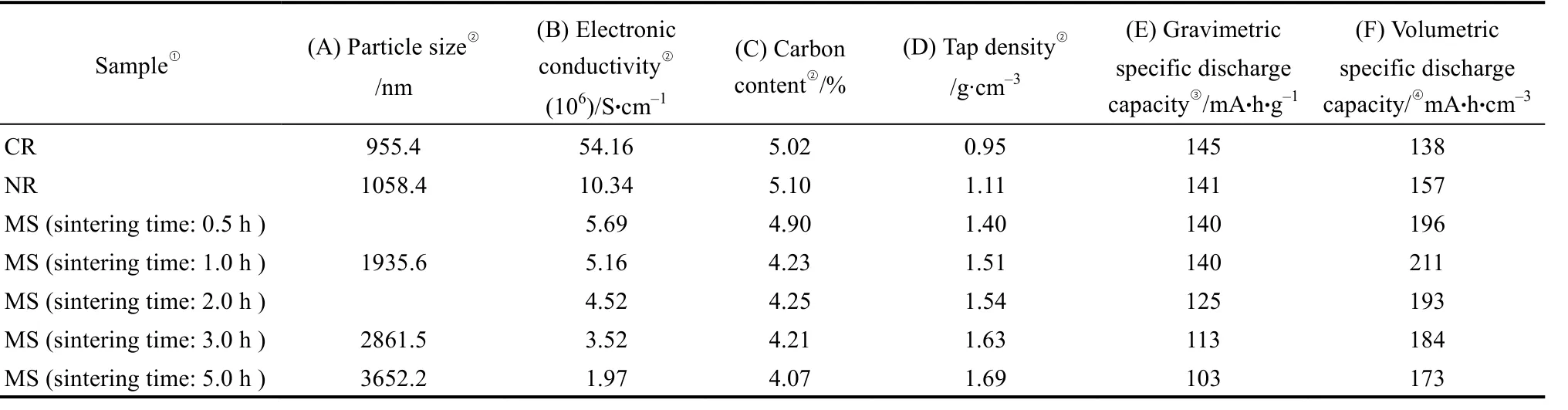
表8 碳熱還原法結合KCl融鹽法合成的LiFePO4/C復合材料,其電導率、碳含量、粉體粒徑、振實密度、與放電電容量[25]Table 8 A comparison of the tap density, carbon content, particle size, electronic conductivity and specific discharge capacity of the CR and MS samples prepared at different sintering times[25]

圖9 碳熱還原法所合成的LiFePO4/C產物,以KCl融鹽作為介質,于1028 K高溫進行二次煅燒,于不同融鹽煅燒時間下合成LiFePO4/C的SEM圖[25]Fig.9 SEM images of LiFePO4/C composites prepared by the molten salt method: (a)、(c)、(e)、(g) MS samples sintered at 1028 K for 0, 1.0, 3.0 and 5.0 h, respectively; (b)、(d)、(f)、(h) are partial enlargements of them respectively[25]
2 結 語
結合不同制程技術優點,致力于高質量磷酸亞鐵鋰量產技術的研究與開發,采用多種碳涂布與金屬摻雜技術,形成均勻碳層分布于粉體表面,以及摻雜金屬離子于晶體內部,分別改善材料電導率與鋰離子擴散速度,提高放電電容量、長循環穩定性與大電流充放電能力。此外,為生產出高質量、高性能產品,有效地控制碳含量、雜質含量、粒徑大小、比表面積、粒徑均一性、碳涂布均勻性等材料參數,這些過程與努力將是提高磷酸亞鐵鋰材料一致性與批次穩定性的關鍵。
[1] Ravet N,Goodenough J B,Besner S.Abstract of the electrochemical society fall meeting[C]//Honolulu:[s.n.],1999.
[2] Kwon S J,Kim C W,Jeong W T,Lee K S.Synthesis and electrochemical properties of olivine LiFePO4as a cathode material prepared by mechanical alloying[J].J.Power Sources,2004,137 :93-99.
[3] Chen Z H,Dahn J R.Reducing carbon in LiFePO4/C composite electrodes to maximize specific energy,volumetric energy,and tap density[J].J.Electrochem.Soc.,2002,149(9):A1184-A1189.
[4] Doeff M M,Hu Y Q,McLarnon F,Kostecki R.Effect of surface carbon structure on the electrochemical performance of LiFePO4[J].Electrochem.Solid State Lett.,2003,6(10):A207-A209.
[5] Fey G T K,Lu T L,Wu F Y,Li W H.Carboxylic acid-assisted solid-state synthesis of LiFePO4/C composites and their electrochemical properties as cathode materials for lithium-ion batteries[J].Solid State Electrochem.,2008,12(7-8):825-833.
[6] Meligrana G,Gerbaldi C,Tuelb A,Bodoardo S,Penazzi N.Hydrothermal synthesis of high surface LiFePO4powders as cathode for Li-ion cells [J].J.Power Sources,2006,160:516.
[7] Chen J M,Hsu C H,Lin Y R,Hsiao M H,Fey G T K.High-power LiFePO4cathode materials with a continuous nano carbon network for lithium-ion batteries[J].J.Power Sources,2008,184(2):498-502.
[8] Lu C Z,Fey G T K,Kao H M.Study of LiFePO4cathode materials coated with high surface area carbon[J].J.Power Sources,2009,189(1):155-162.
[9] Murugan A V,Muraliganth T,Manthiram A.Rapid microwave-solvothermal synthesis of phospho-olivine nanorods and their coating with a mixed conducting polymer for lithium ion batteries[J].Electrochem.Commun.,2008,10:903-906.
[10] Dominko R,Bele M,Gaberscek M,Remskar M,Hanzel D,Pejovnik S,Jamnika J.Impact of the carbon coating thickness on the electrochemical performance of LiFePO4/C composites[J].J.Electrochem.Soc.,2005,152(3):A607-A610.
[11] Cho Y D,Fey G T K,Kao H M.The effect of carbon coating thickness on the capacity of LiFePO4/C composite cathodes[J].J.Power Sources,2009,189(1):256-262.
[12] Salah A A,Mauger A,Zaghib K,Goodenough J B,Ravet N,Gauthier M,Gendron F,Julien C M.Reduction Fe3+of impurities in LiFePO4from pyrolysis of organic precursor used for carbon deposition[J].J.Electrochem.Soc.,2006,153(9):A1692-A1701.
[13] Fey G T K,Lu T L.Morphological characterization of LiFePO4/C composite cathode materials synthesized via a carboxylic acid route[J].J.Power Sources,2008,178(2):807-814.
[14] Fey G T K,Tu H J,Huang K P,Lin Y C,Kao H M,Chan S H.Particle size effects of carbon sources on electrochemical properties of LiFePO4/C composites[J].J.Solid State Electrochem.,2012,16(5):1857-1862.
[15] Chung S Y,Bloking J T,Chiang Y M.Electronically conductive phospho-olivines as lithium storage electrodes[J].Nature Materials,2002,1:123-128.
[16] Hsu K F,Tsay S Y,Hwang B J.Physical and electrochemical properties of LiFePO4/carbon composite synthesized at various pyrolysis periods[J].J.Power Sources,2005,146(1-2):529-533.
[17] Roberts M R,Vitins G,Owen J R.High-throughput studies of Li1-xMgx/2FePO4and LiFe1-yMgyPO4and the effect of carbon coating[J].J.Power Sources,2008,179(2):754-762.
[18] Wu S H,Chen M S,Chien C J,Fu Y P.Preparation and characterization of Ti4+-doped LiFePO4cathode materials for lithium-ion batteries[J].J.Power Sources,2009,189(1):440-444.
[19] Cho Y D,Fey G T K,Kao H M.Physical and electrochemical properties of La-doped LiFePO4/C composites as cathode materials for lithium-ion batteries[J].J.Solid State Electrochem.,2008,12(7-8):815-823.
[20] GaberscekM,Dominko R,Jamnik J.Is small particle size more important than carbon coating? An example study on LiFePO4cathodes[J].Electrochem.Commun.,2007,9(12):2778-2783.
[21] Meligrana G,Gerbaldi C,Tuelb A,Bodoardo S,Penazzi N.Hydrothermal synthesis of high surface LiFePO4powders as cathode for Li-ion cells[J].J.Power Sources,2006,160(1):516-522.
[22] Fey G T K,Chen Y G,Kao H M.Electrochemical properties of LiFePO4prepared via ball-milling[J].J.Power Sources,2009,189(1):169-178.
[23] Ni J F,Zhou H H,Chen J T,Zhang X X.Molten salt synthesis and electrochemical properties of spherical LiFePO4particles[J].Mater.Lett.,2007,61(4-5):1260-1264.
[24] Gao F,Tang Z Y,Xue J J.Effects of different iron sources on the performance of LiFePO4/C composite cathode materials[J].Journal of University of Science and Technology Beijing,2008,15(6):802-807.
[25] Fey G T K,Lin Y C,Kao H M.Characterization and electrochemical properties of high tap-density LiFePO4/C cathode materials by a combination of carbothermal reduction and molten salt methods[J].Electrochim.Acta,2012,80(1):41-49.

