溶劑熱法合成納米LiFePO4及其尺寸控制
劉 洋,周興平
(東華大學 化學化工與生物工程學院,上海 201620)
溶劑熱法合成納米LiFePO4及其尺寸控制
劉 洋,周興平
(東華大學 化學化工與生物工程學院,上海 201620)
以乙二醇為溶劑、氫氧化鋰為Li+源、七水合硫酸亞鐵為Fe2+源、磷酸為源,采用溶劑熱法制備出了形貌均一、粒徑分布較均勻的LiFePO4納米材料,并探討了反應時間和反應物摩爾比等對產物尺寸和形態的影響.同時,首次嘗試利用異種晶的影響,在其他反應條件相同的條件下合成了不同尺寸的LiFePO4納米材料.采用了X射線粉末衍射儀(XRD)、傅里葉紅外光譜儀(FTIR)和透射電子顯微鏡(TEM)等對產物進行了表征.試驗結果表明:當反應時間為12h,反應溫度為180℃,反應物 (Li+∶Fe2+∶)摩爾比為2.7∶1.0∶1.0時,產物為菱形片狀具有正交晶系Pnma空間群的LiFePO4納米材料,而經過異種晶控制得到的LiFePO4納米顆粒尺寸有明顯減小.
溶劑熱法;LiFePO4納米材料;尺寸控制;異種晶
LiFePO4具有工作電壓穩定(3.5V)、熱穩定性和循環穩定性好、對環境友好以及價格低廉等優點[1-3],是極具發展前景的鋰離子電池正極材料.由于LiFePO4自身極低的電子電導率(室溫下為10-10~10-9S/cm)和 鋰 離 子 擴 散 系 數 (10-16~10-14m2/s)[4-5],使其只有在低倍率充放電條件下才有很好的電化學性能,這嚴重阻礙了LiFePO4正極材料的發展.研究[6-9]表明,LiFePO4材料的納米化可以減弱極化、減小電阻、提高自身的電子電導率和鋰離子擴散系數、提高電池的充放電容量與循環穩定性等,從而可以有效提升其電化學性能,促進LiFePO4正極材料的進一步發展.
目前LiFePO4納米材料的合成方法主要有高溫固相法、微波合成法、溶膠-凝膠法、共沉淀法和溶劑熱法等.高溫固相法具有制備工藝簡單、易于產業化和進行大規模生產等優點[10],但是該方法在較高的反應溫度下容易產生雜質,而且得到的納米顆粒尺寸分布范圍廣,顆粒形貌不均勻[11].微波合成法的優點包括加熱時間短、加熱速度快、熱能利用率高等,但是它具有反應過程難控制和工業化生產難以實現等缺點[12].合成納米LiFePO4的溶膠-凝膠法的設備簡單,得到的顆粒粒徑均勻、分布窄,但生產周期過長,不利于工業化生產[13-14].共沉淀法合成溫度低,易于大規模生產,但是由于各組分的沉淀速度不同,會導致材料組成的偏離和不均勻[15],然而它仍然是一種很有發展前景的合成方法.溶劑熱法具有操作簡單,合成溫度較低等優點,而且利用該方法合成出的LiFePO4納米材料結晶良好,無需煅燒即具有優異的電化學性能,因而引起了更多相關研究人員的重視[16-17].但是,溶劑熱法合成納米LiFePO4的機理研究目前還很少,而納米LiFePO4顆粒尺寸控制方面的文獻報道更是非常少見.
本文采用溶劑熱法合成LiFePO4納米材料,所得產物形貌均一,粒徑分布較均勻,同時討論了反應時間和反應物摩爾比等對產物尺寸和形態影響.依據文獻[18]在合成EU-1分子篩中添加異質晶種來促進晶化的方法,本文首次嘗試利用添加異種晶探索了其對產物尺寸的影響,并初步探索了其反應機理.
1 試驗部分
1.1 試劑與儀器
氫氧化鋰、磷酸、七水合硫酸亞鐵(國藥集團化學試劑有限公司),乙二醇(上海凌峰化學試劑有限公司),無水乙醇(常熟市楊園化工有限公司),試劑均為分析純.
D/max-2550PC型X射線粉晶衍射光譜儀(日本Rigaku公司,Cu靶,λ=0.154 056nm),H-800型透射電子顯微鏡(日本 HITACHI公司),Avatar380型傅里葉紅外光譜儀(FTIR,美國熱電集團).
1.2 LiFePO4納米材料的合成及尺寸控制
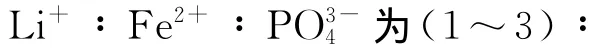
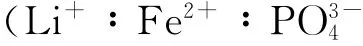
2 結果與討論
2.1 結構分析
2.1.1 X射線衍射分析
反應時間為12h,反應溫度為180℃,反應物(Li+∶Fe2+∶PO3-4)摩爾比為2.7∶1.0∶1.0時,溶劑熱法所合成LiFePO4的XRD譜圖如圖1所示.對照JCPDF 81-1173標準譜圖,圖1中樣品為具有正交晶系Pnma空間群的橄欖石結構LiFePO4,而且峰型尖銳,說明溶劑熱法在180℃的反應溫度下,不經過高溫煅燒即可得到晶型完整的LiFePO4晶體.
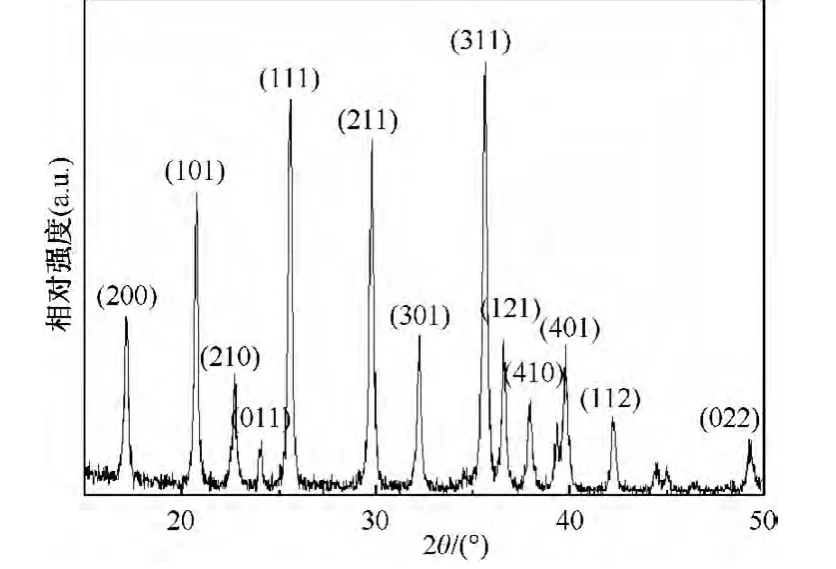
圖1 LiFePO4納米材料的XRD圖Fig.1 X-ray diffraction pattern of LiFePO4nano-matetials
2.1.2 FTIR分析
反應時間為12h,反應溫度為180℃,反應物(Li+∶Fe2+∶PO3-4)摩爾比為2.7∶1.0∶1.0時,溶劑熱法所合成樣品的紅外光譜圖如圖2所示.由圖2可看到PO3-4的紅外吸收峰,各吸收峰的位置與文獻[19-21]報道的基本一致.其中469和503 cm-1處的吸收峰屬于O—P—O的彎曲振動模式或是磷酸鹽的晶格振動;546cm-1處的吸收峰屬于O—P—O的對稱彎曲振動模式;585cm-1處歸屬于O—P—O的反對稱彎曲振動;639cm-1處歸屬于O—P—O的對稱伸縮振動模式;967cm-1處的吸收峰歸屬于P—O的對稱伸縮振動模式;1 078~1 140cm-1區域的3個吸收峰均歸屬于P—O的反對稱伸縮振動模式.此外,1 625和3 450cm-1處出現了O—H彎曲及伸縮振動吸收峰,這是因為樣品在處理過程中沒有干燥完全或者在空氣中暴露時吸收了水分.
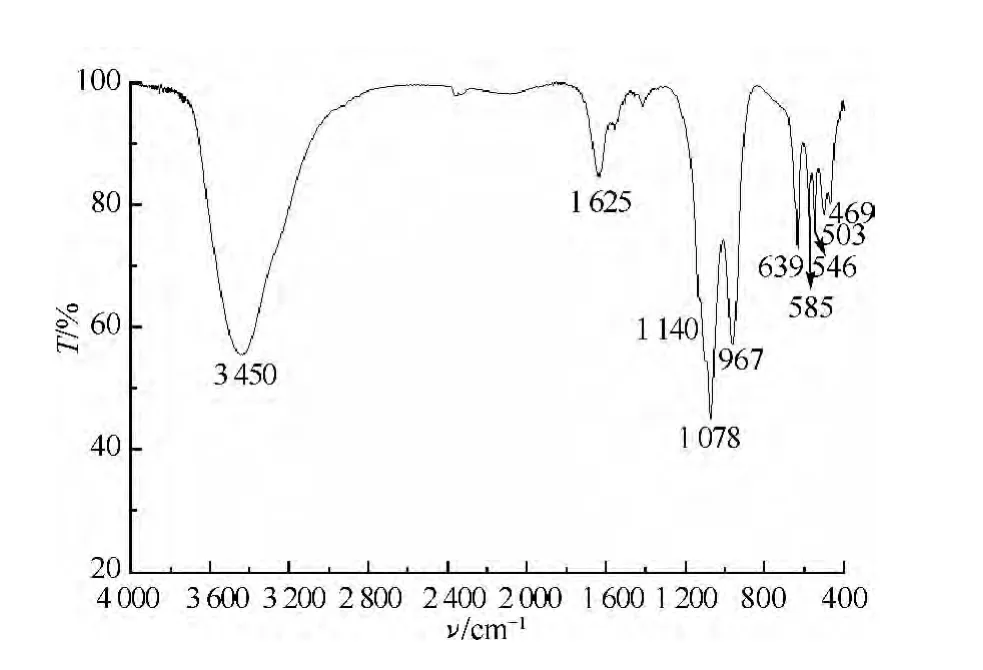
圖2 LiFePO4納米材料的傅里葉紅外光譜圖Fig.2 FTIR spectrum of LiFePO4nano-materials
2.2 不同反應條件對制得的LiFePO4納米顆粒尺寸的影響
2.2.1 反應時間對制得的LiFePO4納米顆粒尺寸的影響
180℃下反應物(Li+∶Fe2+∶PO3-4)摩爾比為2.7∶1.0∶1.0時,不同反應時間制備的產物的XRD譜圖如圖3所示.將圖3中的XRD譜圖與JCPDF 30-0662和JCPDF 81-1173標準譜圖進行對照可以得知:當反應時間為0.5h時,所得到的產物為Fe3(PO4)2·8H2O,而反應進行至1h時所得產物是LiFePO4,其后,隨著反應時間的增長,產物皆為LiFePO4.這說明本文中溶劑熱法合成納米LiFePO4的過程是先生成磷酸亞鐵,然后由磷酸亞鐵轉變為LiFePO4.
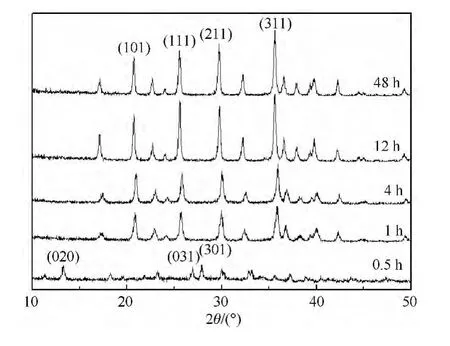
圖3 反應時間不同時所得到產物的XRD圖譜Fig.3 X-ray diffraction pattern of products prepared at different reaction time
180℃下反應物(Li+∶Fe2+∶PO3-4)摩爾比為2.7∶1.0∶1.0時,不同反應時間制備的 LiFePO4納米顆粒的TEM圖如圖4所示.由圖4(a)可知,1h合成的試樣主要為幾十納米的不規則顆粒,顆粒大小分布極不均勻.隨著反應時間進行,至4h時部分顆粒繼續長大,另外試樣中還存在很多非常細小的納米顆粒(見圖4(b)).反應時間為12h時,反應基本上已經進行完全,得到的產物為近似菱形的納米顆粒(見圖4(c)),形貌和大小分布較為均勻,長度分布在170~200nm,寬度為80~100nm.而當反應進行到48h后,所得到的顆粒為矩形片狀顆粒(見圖4(d)),形貌較反應12h的樣品有些改變.從圖4可以看出,在180℃溶劑熱法合成過程中,隨著反應時間的進行,產物(LiFePO4)顆粒逐漸長大,而形狀則由不規則的納米顆粒逐漸生長為規則的菱形片狀顆粒,且粒徑分布較為均勻.其生長機理可能是先形成許多微小的晶核,而后各反應組分在晶核表面沉積使晶核逐漸長大,從而得到最終的產物.

圖4 不同反應時間下合成的LiFePO4納米顆粒TEM圖Fig.4 TEM images of LiFePO4nano-particles prepared at different reaction time
2.2.2 反應物摩爾比不同對制得的LiFePO4納米顆粒尺寸的影響
在180℃下反應時間均為12h,反應物摩爾比不同時進行溶劑熱反應得到的產物的XRD譜圖如圖5所示.將圖5中的XRD譜圖與JCPDF 81-1173標準譜圖進行對照可以發現:當反應物(Li+∶Fe2+∶PO3-4)摩爾比為1∶1∶1時,得到的產物并非LiFePO4納米材料,而其余摩爾比條件下反應得到的產物均為LiFePO4.
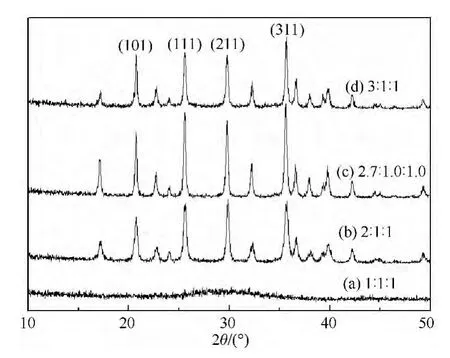
圖5 反應物(Li+∶Fe2+∶)摩爾比不同時所合成的產物XRD譜圖Fig.5 X-ray diffraction pattern of products prepared at different molar ratio of Li+ ∶Fe2+ ∶
在180℃下反應時間均為12h,反應物(Li+∶Fe2+∶)摩爾比不同時得到的產物的TEM圖如圖6所示.由圖6(b)可知,當摩爾比為2∶1∶1時,得到的產物為LiFePO4納米材料,但是所得到的產物主要是不規則顆粒,而且團聚現象較為嚴重.摩爾比為2.7∶1.0∶1.0時得到的產物為近似菱形的納米顆粒,并且形貌和大小分布較為均勻(見圖6(c)).摩爾比為3∶1∶1時,得到的產物中出現了菱形、矩形片狀納米顆粒,同時還有部分細小的納米顆粒(見圖6(d)).由圖6可知,在180℃溶劑熱反應12h的條件下,反應物摩爾比選擇2.7∶1.0∶1.0獲得的LiFePO4納米顆粒形貌和大小分布較為均勻.
2.3 異種晶對LiFePO4納米顆粒尺寸的影響
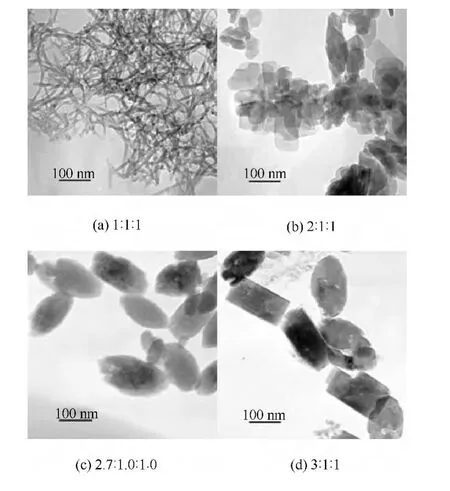
圖6 反應物摩爾比(Li+∶Fe2+∶)不同時所合成的產物TEM圖Fig.6 TEM images of products prepared at different molar ratio of Li+ ∶Fe2+ ∶
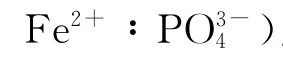

圖7 Fe3(PO4)2異種晶以及加入不同數量的異種晶得到的LiFePO4納米顆粒TEM圖Fig.7 TEM images of heterologous seed crystals-Fe3(PO4)2 and LiFePO4nano-particles prepared with addition of different amount of heterologous seed crystals
文獻[22]在銳鈦礦TiO2納米顆粒形成過程和尺寸控制的研究中對晶體的生長機理和種晶效應做了詳細的論證,其研究內容在晶體生長的研究領域具有重要作用.根據LaMer模型[23],相比于顆粒生長,顆粒成核受到促進,有利于生成較小而均勻的顆粒.如果在成核前加入遠比自成核數多的種子,通過觀察在此情況下最后所產生的顆粒的大小和合成速率的變化,可以研究和判斷該物質顆粒在液相中形成的機理.在本文的反應過程中,當反應時間為0.5h時溶液中只有磷酸亞鐵異種晶生成,而沒有LiFePO4產生;當反應時間延長至1h時溶液中已經全部是LiFePO4;隨著反應時間的不斷延長,反應物不斷在已經成核的LiFePO4表面進行反應,促使LiFePO4晶體的不斷生長,最終形成了形貌均一、粒徑分布較均勻的納米LiFePO4.本文同時發現,Fe3(PO4)2異種晶的加入,不僅可以提高反應速率,而且還使產物顆粒粒徑變小,這些現象都揭示了溶劑熱法合成納米LiFePO4的過程符合表面反應控制機理,而不是聚集生長模型.研究結果表明,異種晶在LiFePO4納米材料溶劑熱法合成中對其尺寸控制是有效的.以TiO2合成中同種晶的影響[22]為基礎,作為異種晶影響的初步嘗試,本文對尺寸可控的均勻的納米材料的液相合成及其形成機理研究具有非常重要的意義.
3 結 語
本文采用溶劑熱法成功地合成出了LiFePO4納米材料,所得產物形貌均一,粒徑分布較為均勻,其長度為170~200nm,寬度為80~100nm.首次嘗試利用添加異種晶,在其他反應條件相同的條件下,減小了所合成LiFePO4納米材料的尺寸.在加入摩爾分數為5%異種晶的情況下,使產物長度為80~120nm,寬度為30~70nm;在加入摩爾分數為10%異種晶的情況下,產物尺寸進一步減小,長度為50~80nm,寬度為20~50nm.試驗結果表明,利用種晶效應合成不同尺寸LiFePO4納米材料是可行的.通過種晶效應對其反應機理的探索表明,晶體的生長過程符合表面反應控制機理,這對尺寸可控的均勻的納米材料的液相合成及其合成機理研究具有非常重要的意義,為下一步合成出不同尺寸的LiFePO4納米材料以及研究尺寸與其性能的關系等研究打下了良好的基礎.
參 考 文 獻
[1]ANDERSSON A S,THOMAS J O.The source of first-cycle capacity loss in LiFePO4[J].J Power Sources,2001,97/98:498-502.
[2]YANG S F,ZAVALIJ P Y, WHITTINGHAM M S.Hydrothermal synthesis of lithium iron phosphate cathodes[J].Electrochem Commun,2001,3(9):505-508.
[3]TAKAHASHI M,OHTSUKA H,AKUTO K,et al.Confirmation of long term cyclability and high thermal stability of LiFePO4in prismatic lithium-ion cells [J].J Electrochem Soc,2005,152(5):A899-A904.
[4]YAMADA A,HOSOYA M,CHUNG S C,et al.Olivine-type cathodes achievements and problems [J].J Power Sources,2003,119/120/121:232-238.
[5]WANG Y,SUN B,PARK J,et al.Morphology control and electrochemical properties of nanosize LiFePO4cathode material synthesized by co-precipitation combined with in situ polymerization [J].J Alloys Compd,2011,509 (3):1040-1044.
[6]李軍,黃慧民,夏信德,等.鋰離子電池納米正極材料的研究進展[J].化工新型材料,2007,35(3):21-27.
[7]唐開枚,陳立寶,林曉園,等.鋰離子電池正極材料納米LiFePO4[J].納米材料與結構,2009,46(2):84-90.
[8]KANG B,CEDER G.Battery materials for ultrafast charging and discharging[J].Nature,2009,458:190-193.
[9]NAN C Y,LU J,CHEN C,et al.Solvothermal synthesis of lithium iron phosphate nanoplates[J].J Mater Chem,2011,21:9994-9996.
[10]石璐,胡社軍,李偉善,等.鋰離子電池正極材料LiFePO4的研究進展[J].材料導報,2007,21(S3):295-298.
[11]ZHANG W J.Structure and performance of LiFePO4cathode materials:A review [J].J Power Sources,2011,196(6):2962-2970.
[12]李發喜,仇衛華,胡環宇,等.微波合成鋰電池正極材料LiFePO4電化學性能[J].電源技術,2005,29(6):346-348.
[13]李昕洋,張培新,黃小倩,等.濕化學法制備鋰電池材料LiFePO4研究進展[J].稀有金屬材料與工程,2008,37(S2):591-594.
[14]CHOI D,KUMTA P N.Surfactant based sol-gel approach to nano-structured LiFePO4for high rate Li-ion batteries[J].J Power Sources,2007,163(2):1064-1069.
[15]賴春艷.鋰離子電池正極材料LiFePO4的制備與改性研究[D].上海:中國科學院上海微系統與信息技術研究所,2006:14-17.
[16]JUGOVIC D,MITRIC M,KUZMANOVIC M,et al.Rapid crystallization of LiFePO4particles by facile emulsion-mediated solvothermal synthesis[J].Powder Technol,2012,219:128-134.
[17]張淑萍,倪江鋒,周恒輝,等.溶劑熱法控制合成規則的LiFePO4顆粒[J].物理化學學報,2007,23(6):830-834.
[18]李曉峰,王麗麗,徐景炎,等.在EU-1分子篩合成中的同、異質晶種效應[J].石油學報,2006(S):93-95.
[19]白瑩,吳鋒,吳川.新型鋰離子電池正極材料LiMPO4(M=Fe,Mn)的譜學和電化學研究[J].光散射學報,2004,15(4):231-236.
[20]LU J B,TANG Z L,ZHANG Z T,et al.Preparation of LiFePO4with inverse opal structure and its satisfactory electrochemical properties[J].Mater Res Bull,2005,40(12):2039-2046.
[21]SUN Y H,LIU X Q.Preparation and characterization of novel Ti-doped M-site deficient olivine LiFePO4[J].Chinese Chem Lett,2006,17(8):1093-1096.
[22]SUGIMOTO T,ZHOU X P,MURAMATSU A.Synthesis of uniform anatase TiO2nanoparticles by gel-sol method 3:Formation process and size control[J].J Colloid Interface Sci,2003,259(1):43-52.
[23]扈玫瓏,白晨光,徐盛明,等.粒徑可控球形TiO2的制備[J].物理化學學報,2008,24(12):2287-2292.
Synthesis and Size Control of LiFePO4Nano-materials by a Solvothermal Method
LIUYang,ZHOUXing-ping
(College of Chemistry,Chemical Engineering and Biotechnology,Donghua University,Shanghai 201620,China)
Uniform lithium iron phosphate nano-particles were obtained by a solvothermal method,using ethylene glycol as the solvent,while lithium hydroxide,ferrous sulfate and phosphoric acid were used as Li+,Fe2+andsources,respectively.And effects of the reaction time and molar ratio among the reactants were also investigated.Meanwhile,LiFePO4nano-particles with different sizes were synthesized with addition of heterologous seed crystals when the otherwise reaction conditions were same.The products were characterized by X-ray diffraction(XRD),Fourier transform infrared spectroscopy(FTIR)and transmission electron microscopy(TEM).Experiment results indicated that with the starting materials in a molar ratio(Li+∶Fe2+∶)of 2.7∶1.0∶1.0,aging at 180 ℃for 12 h,the obtained flake like diamond nano-particles were orthorhombic phase LiFePO4(space group Pnma),while significant changes happened on the size of LiFePO4nano-particles obtained by adding heterologous seed crystals.
solvothermal method;LiFePO4nano-materials;size control;heterologous seed crystals
TB 34;TQ 131.11
A
1671-0444(2013)06-0774-06
2012-10-25
上海市自然科學基金資助項目(10ZR1400600);上海市納米科技專項基金資助項目(1052nm06400)
劉 洋(1986—),男,山東菏澤人,碩士,研究方向為磷酸鐵鋰納米材料的合成與表征.E-mail:2100459@mail.dhu.edu.cn
周興平(聯系人),男,研究員,E-mail:xpzhou@dhu.edu.cn

