金魚藻對重金屬Cr6+的吸附特征研究
盛周君,陳 玉
(1.安徽綠華環境科技發展有限公司,安徽 合肥 230061;2.安徽省環境科學研究院,安徽 合肥 230061)
1 引言
鉻(Cr)遍布于自然界,在水體和大氣中均含有微量的鉻。鉻有多種價態,其中僅Cr3+與Cr6+具有生物意義[1]。鉻是人體必需的微量元素,但存在大量的鉻污染環境,則會危害人體健康。隨著鉻的價態不同,人體吸收鉻的效率也不一樣,大量攝入鉻可以在體內造成明顯的蓄積。Cr3+和Cr6+對水生生物都有致死作用[2]。其中,Cr6+和毒性比Cr3+高100倍左右。
鉻及其化合物是冶金工業、金屬加工電鍍、制革、油漆、顏料、印染、制藥、照相制版等行業必不可少的原料,因此廣泛應用于工業生產的各個領域。目前,處理鉻污染的方法主要有還原沉淀法、電解法沉淀過濾、膜分離法、吸附法、光催化法等。其中,生物吸附法是一種新興的重金屬廢水處理技術[3,4],它利用廉價的生物材料對重金屬進行吸附,尤其適宜低濃度重金屬廢水的處理,并且具有吸附量高,吸附速度快等優點。
近年來,植物材料作為一種有競爭力的、潛在的生物吸附劑開始受到廣泛關注[5]。但以往的這些研究多以葉幅較寬的輪葉黑藻等為對象,較少涉及具針狀葉的金魚藻;另外,所研究的重金屬多為 Cu2+和 Cd2+[6~8],涉及Cr6+的研究不多;此類研究多針對非活性的植物材料[9~12],而對活體沉水植物則研究較少。
金魚藻為安徽安慶地區常見的沉水植物,2006年安慶沿江湖泊通江以來,通江渠已成為工農業廢水入江的主要通道。相關調查表明[13],金魚藻在通江渠內繁殖較快,具有明顯的競爭優勢。金魚藻對Cr6+的吸附,能直接影響電鍍廢水入江的污染物濃度。研究金魚藻對Cr6+的吸附特征,對電鍍廢水中重金屬的去除以及重金屬污染水體水質功能恢復具有十分重大的意義。
2 材料和方法
2.1 儀器
JH722可見分光光度計(上海菁華科技儀器有限公司);比色皿(1cm);50mL具塞比色管;移液管;容量瓶;錐形瓶(250mL);FA2104N電子天平(上海精密科學儀器有限公司);SHA-C水浴恒溫振蕩器(JinTan Heng-Feng Instrument Factory)。
2.2 試劑
丙酮;(1+1)硫酸;(1+1)磷酸;鉻標準貯備液:稱取于120℃干燥2h的重鉻酸鉀(分析純)0.2829g,用水溶解,移入1000mL容量瓶中,用水稀釋至標線,搖勻。每毫升貯備液含0.100mgCr6+;5)二苯碳酰二肼溶液:稱取二苯碳酰二肼0.2g溶于50mL丙酮中,加水稀釋至100mL,搖勻,貯于棕色瓶內,置于冰箱中保存。
2.3 材料準備
沉水植物金魚藻取自長江,實驗前室內馴化2周后,截取新鮮健康形態較一致的頂枝,用3%的鹽酸溶液浸洗后再用蒸餾水沖洗,用濾紙吸干植物表面水分后備用。將分析純鉻標準貯備液配制成濃度為1mg/L的Cr6+使用液于1000mL容量瓶(25℃)中備用。
2.4 實驗辦法
2.4.1 金魚藻處理
取100mL初始Cr6+濃度分別為0、0.1、0.2、0.4、0.6、0.8、1.0mg/L的溶液于一系列的250mL錐形瓶中,用0.1mol/L的 H2SO4溶液調pH值至5~6,最后加入1g金魚藻(鮮重),在實驗過程中不再調節pH值。將反應器(250mL錐形瓶)放在搖床中振蕩(200r/min,25℃±1℃)。由于沉水植物對重金屬離子的吸附速度較快,一般在20min內即可達到吸附平衡[14],因此本實驗為使吸附完全選定吸附時間為90min。停止振蕩后,過濾錐形瓶中的溶液,使植物與溶液分離。用分光光度法測定濾液中Cr6+濃度。實驗設置2個平行組,同時進行一系列未加植物材料的實驗對照組,以避免玻璃容器的器壁對Cr6+的吸附和水解沉淀。對照實驗表明,實驗容器(錐形瓶)的器壁沒有吸附Cr6+也沒有產生水解沉淀現象。
2.4.2 實驗標定
(1)標準曲線的繪制。取9支50mL比色管,依次加入 0、0.20、0.50、1.00、2.00、4.00、6.00、8.00、和10.00mL鉻標準使用液,用水稀釋至標線,分別加入(1+1)硫酸0.5mL和(1+1)磷酸0.5mL,搖勻。加入2mL顯色劑溶液(二苯碳酰二肼溶液),搖勻。5~10min后,于540nm波長處,用1cm比色皿,以去離子水做參比,測定吸光度。以吸光度為縱坐標,相應Cr6+含量為橫坐標繪出標準曲線。
(2)樣品的測定。取10mL濾液于50mL比色皿中,用水稀釋至標線,以下步驟同標準溶液測定。進行空白校正后根據標準曲線查得Cr6+含量。
2.4.3 計算
Cr6+(mg/L)=m/V。式中,m 為從標準曲線上查得得Cr6+量,ug;V 為水樣的體積,mL。
2.4.4 數據處理
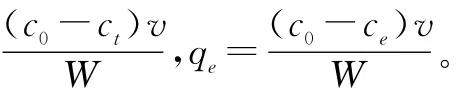
3 結果與討論
3.1 吸附模型
將整個吸附過程用吸附等溫線來描述[15]常用來評價吸附劑的吸附能力。為了研究沉水金魚藻對Cr6+的最大吸附量和吸附模型,采用2種最常用的吸附等溫式Langmuir和Freundlich模型來擬合吸附過程。
3.1.1 Langmuir模型
Langmuir模型是根據氣固二相間的單分子層吸附的假設而推導得出的,適用于短時間的單組分重金屬的生物吸附,其方程表達式如(1)式:

(1)式可寫成以下線性表達式如式(2):

式中,qm最大吸附量;ka是吸附平衡常數。以ce/qe對ce做圖,運用最小乘法進行線性擬合。根據斜率和截距可求出吸附參數qm和ka。
3.1.2 Freundlich模型
Freundlich方程是一個半經驗方程,可用于各種非理想條件下的表面吸附以及多分子層吸附。Freundlich方程表達式如(3)式:

等式兩邊分別求對數可得其線性表達式如(4)式:

式中,kF和n是常數。同樣可以根據斜率和截距求出吸附參數n和kF。
3.2 擬合結果分析
分別采用式(2)、(4)對金魚藻吸附Cr6+的等溫曲線進行線性擬合。結果見表1。

表1 沉水植物金魚藻吸附Cr6+的Langmuir和Freundlich模型的線性擬合參數
根據表1分析結果,金魚藻對Cr6+的吸附既符合Langmuir模型(R2=0.9947),也符合Freundlich模型(R2=0.9568)。為了比較不同模型擬合的效果,本實驗利用實驗測得的數據與2種擬合模型重新計算獲得的數據進行了比較,結果見圖1。
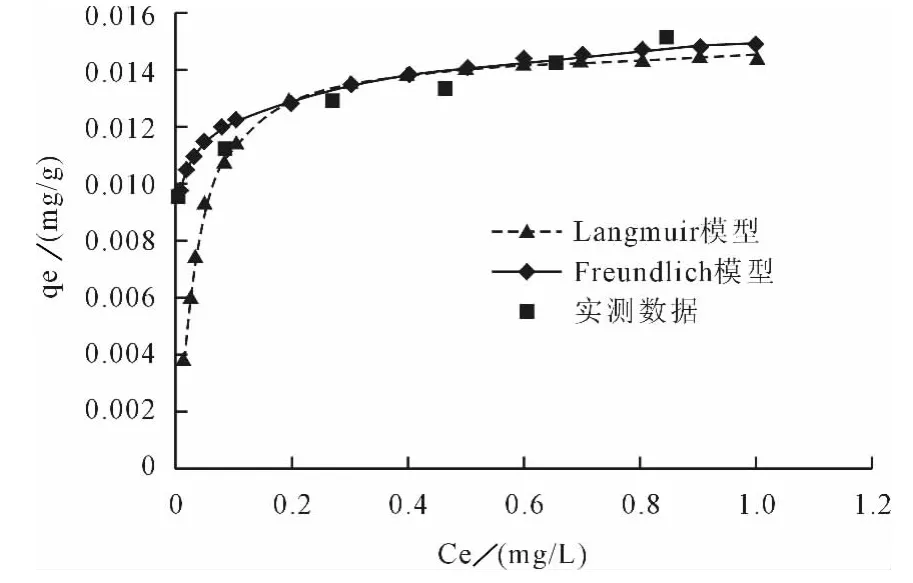
圖1 線性擬合的Langmuir、Freundlich吸附等溫線與實測數據的比較
由圖1可見:在平衡質量濃度較低(ce<0.2mg/L)時,Freundlich模型擬合的效果更符合客觀實際;在平衡質量濃度較高(ce>0.2mg/L)時,兩種模型的擬合效果基本重合,均和實測數據較為吻合。根據R2比較,Langmuir模型擬合效果較好,但圖1所示,Freundlich模型擬合效果相對更好。造成這一差異的原因是:R2僅僅是擬合效果的一個參數,它能反映擬合效果,但不能僅僅根據R2的大小來判斷何種模型擬合效果更適合。因此為了獲得更為真實的擬合結果,在實踐中可以利用實驗測得的數據與擬合模型重新計算獲得的數據進行了比較,并根據吸附反應本身的特點進行綜合判斷,然后選擇合適的吸附模型。
3.3 金魚藻對Cr6+的等溫吸附特征
沉水植物金魚藻對Cr6+的吸附等溫曲線見圖2。
如圖2所示,吸附等溫曲線在開始階段有較大的斜率,表明沉水植物金魚藻對Cr6+有較強的吸附親合力,在后一階段吸附曲線較為平緩。Wang等[16]的研究結果表明,死亡后的水生植物吸附能力依然存在,這表明水生植物的這種吸附作用與細胞的生理活動無關,本實驗在較短的時間內達到吸附平衡,說明本實驗中沉水植物對重金屬離子的去除主要是通過吸附過程來實現的,與生理代謝活動無關。本實驗可初步反映沉水植物金魚藻對Cr6+的吸附容量大小,然而,有關沉水植物生物吸附機理的解釋仍需更進一步的詳細研究。
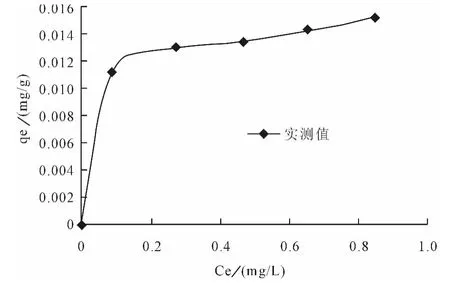
圖2 沉水植物金魚藻對Cr6+的吸附等溫曲線
4 結語
(1)采用不同等溫吸附模型評價植物對重金屬的吸附時,根據擬合參數R2進行適用性判斷并不準確,在實踐中應利用實測數據與擬合模型重新計算獲得的數據進行比較,并根據吸附反應本身的特點進行綜合判斷選擇合適的吸附模型。
(2)在本實驗中,沉水植物金魚藻吸附Cr6+的行為在平衡質量濃度較低(ce<0.2mg/L)時,Freundlich模型擬合的效果更符合客觀實際;在平衡質量濃度較高(ce>0.2mg/L)時,兩種模型的擬合效果基本重合,均和實測數據較為吻合;且在Cr6+的濃度小于0.2mg/L時,金魚藻對Cr6+有較強的吸附親合力。
(3)根據Langmuir模型線性擬合參數,沉水植物金魚藻對Cr6+的最大吸附量為1.5142×10-2mg/g。
[1]欒廣忠,李宏軍,張宗巖.鉻─人體重要的保健微量元素[J].中國乳品工業,1999(6).
[2]陸祖宏.基因芯片的研究和應用[J].中國病理生理雜志,2000(10).
[3]王文華,馮詠梅,常秀蓮,等.玉米芯對廢水中鉛的吸附研究[J].水處理技術,2004,30(2):95~98.
[2]劉 剛,李清彪.重金屬生物吸附的基礎和過程研究[J].水處理技術,2002,28(1):17~22.
[3]Wang X S,Qin Y.Equilibrium sorption isotherms for Cu2+ on rice bran[J].Process Biochem,2005,40(2):677~680.
[4]Schneider I A H,Rubio J,Smith R W.Effect of some mining chemicals on biosorption of Cu(Ⅱ)by the non-living biomass of the freshwater macrophyte Potamogeton lucens[J].Mineral Engineering,1999,12:255~260.
[5]Ho Y S,Huang C T,Huang H W.Equilibrium sorption isotherm for metal ions on tree fern[J].Process Biochem,2002,37:1421~1430.
[6]曾阿妍.沉水植物對重金屬Cu2+的吸附特征及其逆境生理研究[D].長春:吉林大學,2006.
[7]曾阿妍,昌 宙,相 燦,等.金魚藻對Cu2+的生物吸附特征[J].中國環境科學,2005,25(6).
[8]李國新,李慶召,薛培英,等.黑藻吸附Cd2+和Cu2+的拓展Langmuir模型研究,農業環境科學學報,2010,29(1).
[9]王圣瑞,趙海超,金相燦,等.沉水植物黑藻對不同磷化合物的轉化與吸收[J].中國環境科學,2005(6).
[10]鄭逢中,洪麗玉,鄭文教.紅樹桿物落葉碎屑對水中重金屬吸附的初步研究[J].廈門大學學報:自然科學版,1998(1).
[11]張亞楠.綠色巴夫藻的重金屬脅迫效應及吸附能力的研究[D].暨南大學,2003
[12]王圣瑞,趙海超,金相燦,等.沉水植物黑藻對不同磷化合物的轉化與吸收[J].中國環境科學,2005(6).
[13]陳書琴,路 楊,儲昭升,等.破罡湖通江前后湖濱帶夏季水生植物對比研究[J].生物學雜志,2009(3).
[14]施 紅.生物吸附法處理廢水中重金屬離子的研究[D].南京:河海大學,2006.
[15]顏昌宙,曾阿妍,金相燦,等.沉水植物輪葉黑藻和穗花狐尾藻對Cu2+的等溫吸附特征[J].環境科學,2006,27(6).
[16]Wang T C,Weissman J C,Ramesh G,et al.Parameters for removal of toxic heavy metals by water milfoil(My riophyllumspicat um)[J].Bull Environ Contam Toxicol,1996(57):779~786.
- 綠色科技的其它文章
- 遂昌縣林地資源現狀及開發利用的保障措施研究

