不同污染條件下微生物礦化固結Zn2+的作用及機理
陸兆文 錢春香 許燕波 王明明
(東南大學材料科學與工程學院,南京 211189)
(東南大學江蘇省土木工程材料重點實驗室,南京 211189)
重金屬對環境的污染是一個全球性的問題,而土壤的重金屬污染尤其嚴重.重金屬污染土壤的主要途徑有以下2種:① 工業廢氣中的重金屬擴散沉降累積于周圍的土壤之中;② 工廠污染造成河流海洋等重金屬水污染,將這些廢水灌溉農田會造成土壤重金屬污染[1-3].
微生物修復重金屬污染處理具有時間短、投資少、無二次污染、操作簡單等優點,引起了人們的廣泛關注和重視.微生物修復重金屬污染的機理非常復雜,主要有以下2種:① 細胞代謝.某些途徑可使金屬生物沉淀或通過生物轉化使其低毒或易于回收.②生物吸附.將活細胞、無生命的生物體、金屬結合蛋白和多肽或生物多聚體作為生物吸附劑,空泡吞飲重金屬離子或使其發生沉淀和氧化還原反應.
目前,國內外主要利用微生物對重金屬的吸附作用原理來處理重金屬污染[4-5],也有微生物礦化重金屬離子產生沉淀的研究報道.van Roy等[6]發現硫酸鹽還原菌可通過2種途徑將硫酸鹽還原為硫化物:①在呼吸過程中,硫酸鹽作為電子受體被還原;② 在同化過程中,利用硫酸鹽合成氨基酸(如胱氨酸和蛋氨酸),再通過脫硫作用使S2-分泌于體外,S2-可以和重金屬 Cd2+形成沉淀.Fujita等[7]利用細菌對尿素的分解作用,使得分解產物和Sr共沉淀固結在方解石礦物中,修復被Sr污染的地下水.然而,這些研究仍然停留在實驗室階段,無法應用于大面積修復,而且其機理過于復雜,目前尚未完全探明,只能大致推測.
在前期實驗[8-10]中發現,碳酸鹽礦化菌能夠在生長過程中產生特定酶,并通過適當酶化作用產生,固結污染體系中的重金屬離子.在眾多重金屬離子污染中,Zn2+的污染最常見,對微生物的毒性最小,實驗環境下不會對人體造成較大危害,故本文選用Zn2+作為研究對象,對不同環境體系中微生物礦化重金屬Zn2+離子的機理和作用進行研究.
1 實驗
1.1 菌液培養
實驗材料包括菌種A、培養基、ZnCl2溶液、CuCl2溶液以及PbCl2溶液.培養基中包含5.0 g/L的蛋白胨和3.0 g/L的牛肉膏.
將菌種A接種至培養基中,于搖床中30℃下振蕩培養(轉速為170 r/min),初始pH值為7.0,培養24 h后取出.
1.2 礦化產物
緩慢摻入濃度為2 mol/L的ZnCl2溶液,迅速產生沉淀,將其過濾、烘干,待定性分析.所得沉淀為白色細狀粉末,取樣分別進行X射線衍射分析和掃描電子顯微鏡觀測.
1.3 多種污染條件下的礦化效果
當pH<5或pH>9時,菌種A的酶活性會受到較大的影響,因此,在實際應用中,需將pH值調節到5~9.當環境溫度低于20℃時,菌種的酶活性也會降低,故建議將溫度設置在20℃以上.復合污染條件下,酶活性可能會受到影響.
考慮到以上因素,本實驗中通過改變溶液的pH值、溫度、Zn2+濃度,并考慮其他重金屬離子(Pb2+,Cu2+)復合污染情況,研究微生物礦化固結Zn2+的作用效果與機理.
2 結果與討論
2.1 礦化機理分析
為了定性分析所得沉淀物質,對樣品進行X射線衍射分析及掃描電子顯微鏡觀測,結果見圖1.
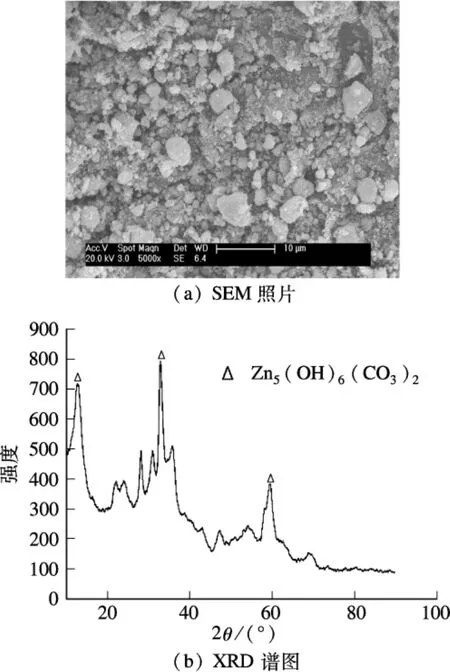
圖1 微生物礦化鋅離子產物分析
由圖1(b)可知,礦化產物XRD圖譜的特征衍射峰與純堿式碳酸鋅Zn5(OH)6(CO3)2一致,證明產物主要為堿式碳酸鋅.由圖1(a)可知,產物的形狀不規則,顆粒尺寸分布不均勻且團聚嚴重,說明生物礦化過程中晶體生長過程受到外界高分子有機物的調控作用.
進一步對礦化機理進行分析,將菌種A接種至培養基中,并以培養基中的底物B為營養源,產生酶化作用,底物B不斷分解,致使溶液中pH值適宜升高,更利于菌體的生長繁殖,酶化作用也得以不斷增強.在這一循環過程中,底物B的不斷分解使溶液中的CO2-3濃度不斷增加.此時在溶液中引入Zn2+,菌體細胞膜界面處帶負電荷的可溶有機質(SM)立即螯合Zn2+,導致局部的晶體陰離子濃度進一步增大,從而吸引更多的Zn2+.晶體前驅物濃度不斷增大達到過飽和,沉積出Zn5(OH)6(CO3)2顆粒.反應過程可表示為
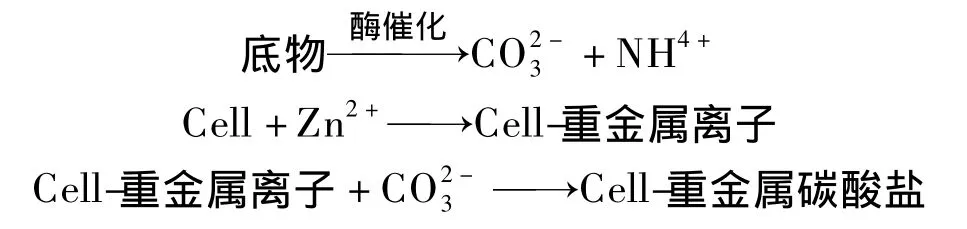
然而,在堿式碳酸鋅的沉積過程中,外界條件(如環境pH值、溫度、反應物濃度、復合污染條件等因素)都可能會影響礦化效果,甚至礦化產物形貌.
2.2 pH值對礦化效果的影響
實驗中,將體系的pH值分別調整至9,7,5,對樣品進行X射線衍射分析和掃描電子顯微鏡觀測.
從圖2中可以看出,在不同的pH值下,沉淀物質都為堿式碳酸鋅.當pH=5時,特征衍射峰的強度比pH=7,9時弱,說明在pH=5時,堿式碳酸鋅結晶較差.而在pH=7,9時,衍射峰強度相似,說明當pH≥7時,堿式碳酸鋅結晶較好,基本不受pH的影響.
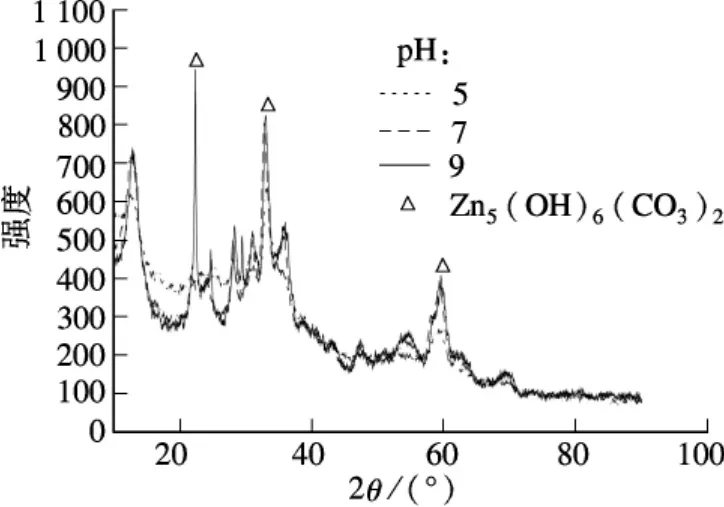
圖2 不同pH值下鋅離子產物的XRD譜圖
從圖3中可以看出,礦化產物的形貌發生了變化,尤其是晶粒的尺寸差別較大.隨著pH值的降低,礦化產物的粒徑逐漸變小.為了進一步確定不同pH值下鋅礦化產物粒徑的分布,對礦化產物進行粒徑分析,結果見圖4.
由圖4可以看出,當pH=9時,礦化產物的平均粒徑約為95 μm;當 pH=7時,平均粒徑約為80 μm;當 pH=5 時,平均粒徑僅為 30 μm 左右.這一結果與SEM的結果一致.由此可見,當pH值較低時,礦化產物不穩定,極易被分解,不利于晶體成核以及晶粒的生長,故整體粒徑較小.

圖3 不同pH值下鋅離子產物的SEM照片
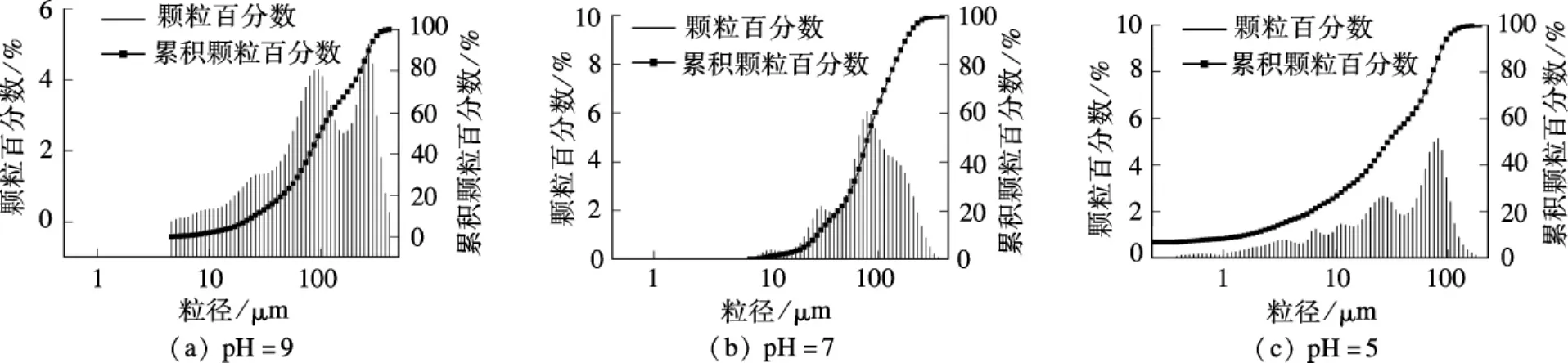
圖4 不同pH值下的礦化粒徑分布圖
2.3 溫度對礦化效果的影響
在15~40℃范圍內,隨著溫度的升高,微生物菌種A的酶活性也逐漸升高.在一定的時間內,同樣菌液用量下會分解產生更多的底物和碳酸根離子,從而對礦化率產生影響.
將培養好的菌液,分別置于20和30℃的恒溫水槽中,完成Zn2+的礦化沉積實驗.基于底物分解量和礦化率,研究溫度對微生物礦化固結Zn2+的影響(理論生成量以Zn2+礦化產物為Zn5(OH)6(CO3)2計算),結果見表1.
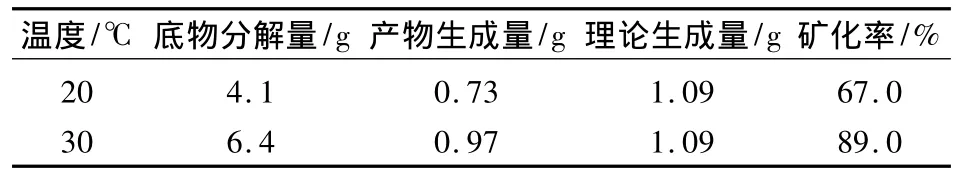
表1 不同溫度下的礦化率
由表1可知,20℃時的礦化率相比30℃時降低22%,這是因為溫度會影響碳酸鹽礦化菌粉的脲酶活性:一方面不利于脲酶的穩定性;另一方面也影響著脲酶分解底物反應的進行.因此,溫度越低,越不利于脲酶的活性,微生物礦化固結Zn2+的效果越差.
2.4 Zn2+濃度對礦化效果的影響
取1 L培養好的菌液,加入8 g底物(固體),根據重金屬的污染情況再加入不同濃度的ZnCl2溶液,充分反應后,將產物過濾、烘干,對所得樣品進行X射線衍射分析和掃描電子顯微鏡觀測.3組樣品的礦化產物成分均為Zn5(OH)6(CO3)2.不同Zn2+濃度下的SEM 照片見圖5.當 ρ(Zn2+)=65 mg/L時,礦化產物呈小球狀,粒徑較小;當ρ(Zn2+)=650,6500 mg/L 時,礦化產物形貌類似;當Zn2+濃度更低時,沒有足夠的Zn2+供晶體繼續生長,限制了晶粒的長大.

圖5 不同Zn2+濃度下的SEM照片
在不同Zn2+濃度下,菌液的酶活性以及礦化率見表2.由表可知,從底物分解量來看,Zn2+濃度對脲酶的分解能力影響不大,說明污染體系中Zn2+濃度的高低對微生物礦化固結Zn2+幾乎沒有影響.
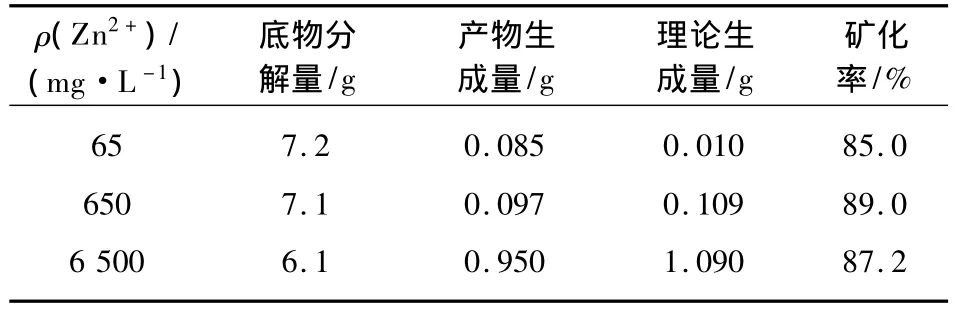
表2 不同Zn2+濃度下Zn5(OH)6(CO3)2的礦化率
2.5 Pb2+,Cu2+對礦化效果的影響
取300 mL培養好的菌液,加入24 g底物,然后向底物中分別加入100 mL濃度為0.1 mol/L的CuCl2,ZnCl2,PbCl2溶液,過濾烘干礦化產物.對礦化產物進行X線衍射分析和掃描電子顯微鏡觀測,結果見圖6.

圖6 Pb2+,Cu2+,Zn2+混合條件下礦化產物的SEM照片
從圖6中可以看出,反應生成了圓球塊狀和長棒狀2種礦化產物.圖7為其XRD譜圖.由圖可知,僅存在Pb2+礦化產物PbCO3的衍射峰,并沒有Zn2+,Cu2+混合礦化產物的衍射峰.究其原因主要是:① 在Pb2+,Zn2+,Cu2+混合污染條件下,Zn2+,Cu2+的混合礦化產物結晶不好,故沒有出現明顯的衍射峰;② PbCO3的衍射峰很強,在它的干擾下,Zn2+,Cu2+混合礦化產物的衍射峰無法顯示出來.
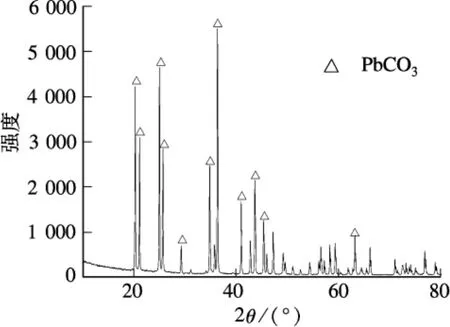
圖7 Pb2+,Cu2+,Zn2+混合條件下礦化產物的XRD譜圖
為了進一步確定礦化產物的成分,對其進行能譜分析.Pb2+礦化產物的形態及能譜分析結果見圖8;Cu2+,Zn2+混合礦化產物的形態及能譜分析見圖9.由圖8和圖9可知,Pb的礦化產物呈長棒狀,而Zn2+,Cu2+的混合礦化產物呈圓球塊狀.由此表明,在Pb2+,Cu2+,Zn2+混合離子條件下,Pb2+單獨礦化結晶,Zn2+和Cu2+的礦化產物則結合在一起.

圖8 混合條件下Pb2+礦化產物的形態及能譜分析

圖9 混合條件下Cu2+與Zn2+混合礦化產物的形態及能譜分析
3 結論
1)在環境pH值為5,7,9的條件下,形成的礦化產物形貌不同,礦化產物粒徑也有較大差別.當pH=9時,平均礦化粒徑約為95 μm;當pH=7時,平均礦化粒徑約為80 μm;當 pH=5時,平均礦化粒徑僅為30 μm左右.因此,pH值較低的反應環境不利于晶體成核以及晶粒的生長.
2)不同礦化固結溫度下得到的礦化產物不同.當溫度為20℃時,沉積出的Zn5(OH)6(CO3)2結晶不好,顆粒細小,為團聚無定形狀;當溫度為30℃時,顆粒呈塊狀,粒徑較大,且分布較均勻.由此可見,溫度的升高有利于脲酶分解底物反應的進行以及礦化產物的沉積和成型.
3)不同的污染濃度會導致礦化效果不同.當ρ(Zn2+)=65 mg/L時,礦化產物呈小球狀,粒徑僅為幾微米;當ρ(Zn2+)=650,6500 mg/L時,兩者的礦化產物形貌相似.由此可見,當Zn2+濃度較低時,沒有足夠的Zn2+供晶體繼續生長,限制了晶粒的長大.此外,Zn2+濃度對脲酶的分解能力影響不大.
4)在 Pb2+,Zn2+,Cu2+混合污染條件下,Pb2+單獨礦化結晶,Zn2+和Cu2+的礦化產物則結合在一起.
References)
[1]楊蘇才,南忠仁,曾靜靜.土壤重金屬污染現狀與治理途徑研究進展[J].安徽農業科學,2006,34(3):549-552.Yang Sucai,Nan Zhongren,Zeng Jingjing.Current situation of soil contaminated by heavy metals and research advances on the remediation techniques[J].Journal of Anhui Agricultural Sciences,2006,34(3):549-552.(in Chinese)
[2]韋朝陽,陳同斌.重金屬超富集植物及植物修復技術研究進展[J].生態學報,2001,21(7):1197-1203.Wei Chaoyang, Chen Tongbin.Hyperaccumulators and phytoremediation of heavy metal contaminated soil:a review of studies in China and abroad[J].Acta Ecologica Sinica,2001,21(7):1197-1203.(in Chinese)
[3]Tessier A,Campbell P G C,Bisson M.Sequential extraction procedure for the speciation of particulate trace metals[J].Analytical Chemistry,1979,51(7):844-851.
[4]滕應,黃昌勇.重金屬污染土壤的微生物生態效應及其修復研究進展[J].土壤與環境,2002,11(1):85-89.Teng Ying,Huang Changyong.Ecological effect of heavy metals on soil microbes and research advances on the mechanisms of bioremediation[J].Soil and Enviromental Scinences,2002,11(1):85-89.(in Chinese)
[5]Gadd G M,Fry J C.Microbial control of pollution[M].Cambridge,UK:Cambridge University Press,1992:59-84.
[6]van Roy S,Vanbroekhoven K,Dejonghe W,et al.Immobilization of heavy metals in the saturated zone by sorption and in situ bioprecipitation process[J].Hydrometallurgy,2006,83(1/2/3/4):195-203.
[7]Fujita Yoshiko,Redden George D,Ingram Jani C,et al.Strontium incorporation into calcite generated by bacterial ureolysis[J].Geochimica et Cosmochimica Acta,2004,68(15):3261-3270.
[8]成亮,錢春香,王瑞興,等.碳酸鹽礦化菌株A固結土壤Cd2+的生物礦化過程[J].硅酸鹽學報,2008,36(S1):215-221.Cheng Liang,Qian Chunxiang,Wang Ruixing,et al.Bioremediation process of Cd2+removal soil by bacteria A biomineralization[J].Journal of the Chinese Ceramic Society,2008,36(S1):215-221.(in Chinese)
[9]王瑞興,錢春香,吳淼,等.微生物礦化固結土壤中重金屬研究[J].功能材料,2007,38(9):1523-1527.Wang Ruixing,Qian Chunxiang,Wu Miao,et al.Study on heavy metals in soil mineralized by bacteria[J].Journal of Functional Materials,2007,38(9):1523-1527.(in Chinese)
[10]王瑞興,錢春香,王劍云.微生物沉積碳酸鈣研究[J].東南大學學報:自然科學版,2005,35(S1):192-195.Wang Ruixing, QianChunxiang, WangJianyun.Study on microbiological precipitation of CaCO3[J].Journal of Southeast University:Natural Science Edition,2005,35(S1):192-195.(in Chinese)

