TfR、sTfR表達與2型糖尿病大鼠大血管病變的關系
劉江月 張代娟 劉同美 郭軍堂 李香玲
(濰坊醫學院病理生理學教研室,山東 濰坊 261042)
糖尿病(DM)引起的大血管病變如冠狀動脈性心臟病、腦血管病及周圍血管病已成為DM患者致死、致殘的主要原因。動脈粥樣硬化(AS)是2型糖尿病(T2DM)常見的伴發病之一。越來越多的證據揭示,鐵代謝和糖代謝之間存在相互影響,二者的關系可能是雙向的,即鐵代謝異常可以影響糖代謝;而長期高血糖又可損傷鐵代謝通路〔1〕。鐵儲存的增加預示著T2DM的發生,鐵誘導的損傷還會影響到DM并發癥的發展。本研究旨在探討T2DM血管并發癥與鐵代謝之間的關系。
1 材料與方法
1.1 實驗動物 健康雄性 Wistar大鼠,清潔級,日齡30~50 d,體重160~180 g,由山東魯抗醫藥股份有限公司實驗動物中心提供,許可證號SCXK魯20090017。
1.2 主要試劑 鏈脲佐菌素(STZ)(美國Sigma公司);胰島素放免試劑盒(北京原子高科技股份有限公司);血糖(BS)試劑盒(中生北控生物科技股份有限公司產品);糖化血紅蛋白(HbA1c)測試盒(美國Bio公司);轉鐵蛋白受體(TfR)多克隆抗體(美國Sigma公司);sTfR酶聯免疫吸附法試劑盒(美國BPB生物醫學公司生產)。
1.3 動物分組及模型建立 Wistar大鼠分為對照組、模型組各10只。①對照組:喂以標準飼料不作任何處理(蛋白質占23%,碳水化合物占53%,脂肪占5%);②模型組:動物以自制高糖高脂飼料喂養1個月(含碳水化合物占48%,脂肪占22%,蛋白質占20%)誘導胰島素抵抗后,按25 mg/kg腹腔注射STZ誘發DM,2 w后測量尾靜脈血糖濃度達到16.7 mmoL/L為建模成功標準。
1.4 檢測項目及方法 各組分別于最后1 d禁食12 h。然后腹腔注射3%戊巴比妥鈉1 ml/kg,麻醉固定后,快速由頸總動脈取血4~5 ml,室溫靜置20 min后,離心10 min,分離血清,檢測BS、采用微柱親和層析法測定HbA1c、放射免疫法檢測胰島素(INS)及sTfR水平。同時取主動脈壁,分別固定、-80℃超低溫冰箱保存,以備電鏡觀察和TfR mRNA表達檢測。
2 結果
2.1 實驗大鼠一般情況 對照組大鼠毛色光澤,活動自如,活潑,飲食正常。模型組大鼠體重增長較快,皮下脂肪厚,但隨實驗進程,毛色色澤暗淡,活動減少,精神狀態較差,進食量減少。
2.2 各組BS、HbA1c、INS、ISI值的比較 模型組BS、HbA1c、INS均明顯高于對照組,而ISI明顯低于對照組(P<0.05)。見表1。
2.3 各組總膽固醇(TC)、甘油三酯(TG)、低密度脂蛋白(LDL)、高密度脂蛋白(HDL)水平比較 模型組 TC、TG、LDL水平均明顯高于對照組,而HDL明顯低于對照組(P<0.05)。見表2。
2.4 血清sTfR水平的比較 模型組大鼠血清sTfR較對照組顯著升高〔(4.25±0.18)vs(2.92±3.75)mg/L,P<0.05〕。
2.5 主動脈壁平滑肌細胞TfR mRNA表達 模型組大鼠主動脈壁平滑肌細胞TfR mRNA表達較對照組明顯升高(0.826±0.003 vs 0.213±0.001,P <0.05)。
2.6 T2DM大鼠主動脈弓動脈壁內皮細胞超微結構的影響對照組大鼠主動脈壁平滑肌細胞核內異染色質成團塊狀分布于核周,胞質內有正常形態和大小的粗面內質網、高爾基復合體和線粒體,所觀察的粗面內質網上都有豐富的核糖體。模型組可見主動脈壁平滑肌細胞成異常改變,核內電子密度升高,異染色質增多,胞質內大量線粒體出現明顯嵴斷裂、空泡樣變、髓鞘樣變,高爾基復合體內出現大空泡。見圖1。
2.7 血清 sTfR 水平與 BS、HbA1c、INS、ISI、TC、TG、LDL、HDL的關系 模型組 sTfR水平與 BS、HbA1c、INS呈明顯正相關(r=0.23、0.26、0.21,P <0.05),與HDL呈負相關(P <0.05)。
表1 各組大鼠BS、HbA1c、INS、ISI的比較=10)

表1 各組大鼠BS、HbA1c、INS、ISI的比較=10)
與對照組比較:1)P<0.05,下表同
?
表2 各組大鼠TC、TG、LDL、HDL的比較,n=10)
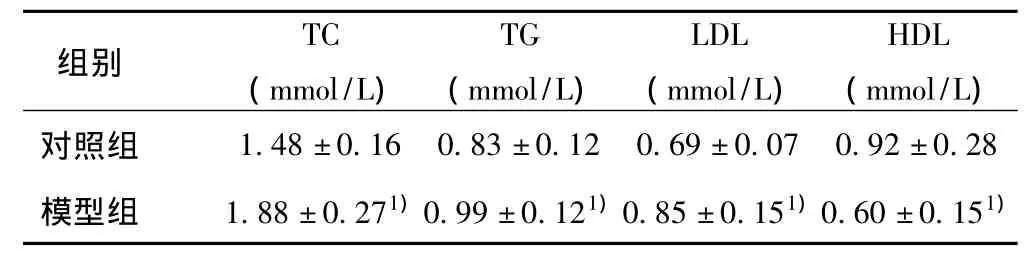
表2 各組大鼠TC、TG、LDL、HDL的比較,n=10)
?

3 討論
近年來Brownlee〔2〕提出,高血糖致內皮細胞線粒體活性氧簇(ROS)生成增加是DM血管病變發病機制中的關鍵因素。而鐵是體內最重要的脂質過氧化反應促進劑,可啟動或催化Haber-Weiss反應,產生ROS,并能使低活性自由基轉變為高活性自由基,特別是通過Fenton反應產生羥基。高活性自由基及其他氧化產物是損傷血管舒張及引起內皮細胞內生性抗氧化劑缺失的主要因子。同時鐵和ROS可作為生長因子促進血管平滑肌增生,在動脈硬化粥樣斑塊形成過程中,鐵蛋白基因表達是提高的〔3〕。另有研究發現,AS的動脈內膜細胞質含鐵量明顯高于AS組織,且鐵沉積量與AS程度直接相關〔4〕。本研究提示T2DM大鼠大血管病變可能與TfR mRNA高表達有關,而TfR mRNA高表達與高糖導致的血管內皮細胞ROS生成增加及氧化應激反應增強有關。
胰島素是一種合成激素,它刺激細胞攝取許多營養素。腸道吸收非血紅素鐵是與人體的需求緊密相關的,人體內總鐵儲存正常時這種鐵的攝取量很小。然而,血紅素鐵的吸收卻不依賴于總鐵含量。穩態下,循環鐵是通過高親和力的特異的轉鐵蛋白受體從血液中吸收的,并與轉鐵蛋白結合在一起。TfR復合物被吞入細胞后,釋放進入一個無酸性的細胞間隔中,消化成為細胞基本的組成成分。胰島素可以顯著加速脂肪細胞攝取鐵,將TfR重新由細胞內膜間隔分布到細胞表面,從而介導細胞對鐵的攝取,致使細胞內鐵超負荷。在鼠神經膠質瘤細胞上發現,INS也影響鐵蛋白合成的增加〔5〕。更重要的是,TfR使得胰島素敏感的葡萄糖載體和胰島素樣生長因子受體在微粒體膜上聚集,意味著胰島素調節鐵的攝取與其調節葡萄糖的轉運存在著關聯。相反地,鐵也影響胰島素的功能。鐵干擾胰島素限制肝糖輸出的作用。鐵負荷增加可以抑制肝臟攝取和清除胰島素,干擾胰島素對肝糖原異生的抑制作用,造成循環中高胰島素血癥〔6〕。這樣,胰島素與鐵潛在的相互作用形成惡性循環,加重胰島素抵抗和誘導DM的發生。本研究提示高胰島素血癥可能導致鐵代謝紊亂,T2DM大鼠大血管病變可能與高胰島素血癥導致鐵代謝紊亂有關。
1 Fernandezr JM,Lope BA,Ricart W.Cross-talk between iron metabolism and diabetes〔J〕.Diabete,2002;51(8):2348-54.
2 Brownlee M.Biochemistry and molecular cell biology of diabetic complications〔J〕.Nature,2001;414(3):813.
3 Wu EX,Kim D,Tosti CL,et al.Magnetic resonance assessment of iron overload by separate measurement of tissue ferritin and hemosiderin iron〔J〕.Ann N Y Acad Sci,2010;1202(2010):115-22.
4 Vlasakova Z,Pelikanova T,Kazadova L,et al.Serum ferritin,oxidation and risk factors for atherogenes in healthy of spring of hypertensive patients〔J〕.Vnitr Lek,2002;48(2):105-11.
5 Cameron NE,Cotter MA.Effects of an extracellular metal chelator on neurovascular function in diabetic rats〔J〕.Diabetologia,2001;44(5):621-8.
6 賈 悅,董凌燕.鐵元素在糖尿病中的作用〔J〕.國外醫學·內科學分冊,2004;31(5):201.

