5-甲基尿苷的合成
吳嘉圣
(上虞盛暉化工有限公司,浙江 上虞 312369)
核苷類藥物是當今人類治療病毒、腫瘤、艾滋病的重要手段,5-甲基尿苷(5)是核苷和脫氧核苷藥物的重要中間體,是合成抗艾滋病藥物齊多夫定(AZT)和司他夫定(D4T),氟鐵龍(5-脫氧氟尿苷)等一系列基因治療法藥物的重要中間體[1]。目前報道的5-甲基尿苷制備主要有化學合成法、發酵法[2-4]等,生物方法生產條件要求高,成本昂貴,現有一般以化學合成法為主。
1 合成路線
1.1 雙三甲硅基胸腺嘧啶(2)的合成
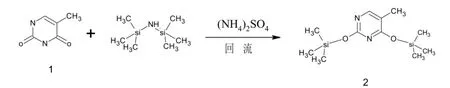
1.2 5-甲基尿苷(5)的合成
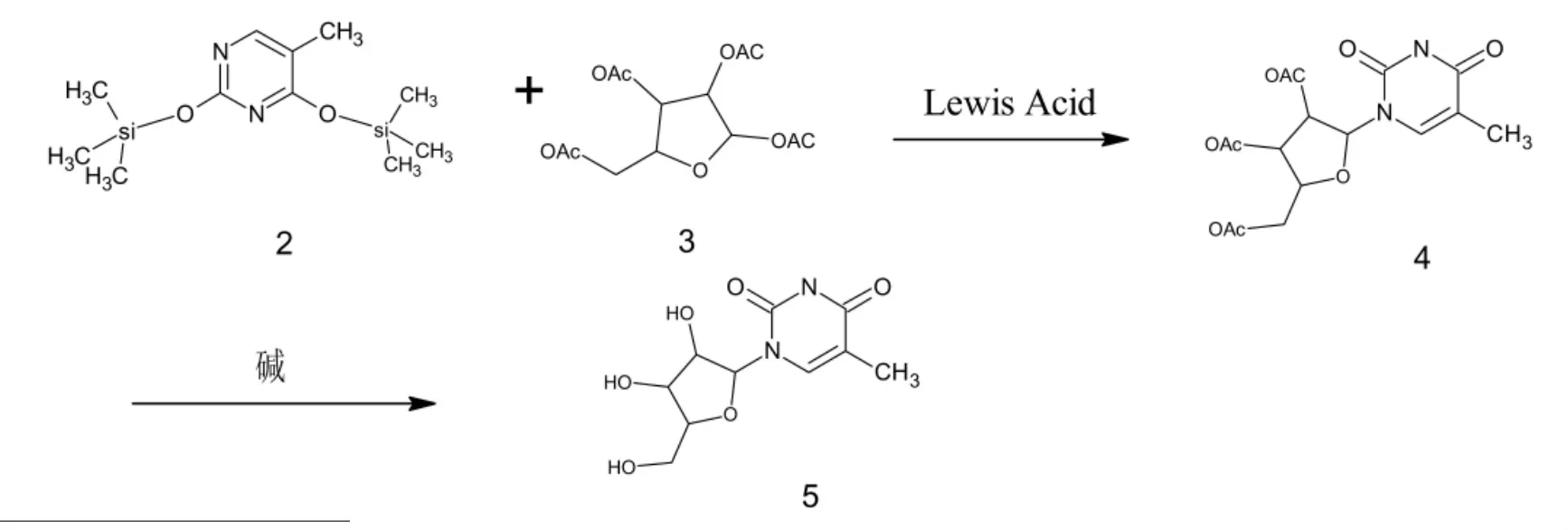
2 實驗部分
2.1 實驗試劑和儀器
胸腺嘧啶:紹興縣晨曉化工有限公司;六甲基二硅胺烷:浙江碩而博化工有限公司;四乙酰核糖:新鄉市創新生物科技有限公司;其他原料為市售產品(分析純)。
采用浙江福立GC-9790氣相色譜儀;安捷侖Agilent1100高效液相色譜;上海精密科學儀器有限公司WRS-2A/2型微機熔點儀;德國Bruker公司 Esquire 3000plus型質譜儀;Bruker Avance公司DMX 500型核磁共振儀
2.2 實驗
2.2.1 雙三甲硅基胸腺嘧啶(2)的合成
在帶有回流冷凝器、攪拌和溫度計的250 mL四口燒瓶中,加入胸腺嘧啶(1)63.0 g (0.5 mol),六甲基二硅胺烷128 mL(0.6 mol),硫酸銨3.0 g混合攪拌,加熱回流至溶液變澄清,約4 h,常壓蒸去大部分未反應的六甲基二硅胺烷,減壓蒸餾,收集餾分126℃~129℃/18 mmHg,得到無色透明的液體(2)126.2 g,自然冷卻后凝固,收率 93.5%。
2.2.2 5-甲基尿苷(5)的合成(含縮合和醇解兩步)
縮合反應:在帶有恒壓滴加漏斗、攪拌和溫度計的500 ml四口燒瓶中,加入四乙酰核糖(3)18.0 g(0.057 mol),1,2-二氯乙烷 200 mL,雙三甲硅基胸腺嘧啶(2)16 g(0.059 mol),冰鹽浴冷卻至0℃后,加入或滴加入所需的路易斯酸催化劑,控制反應溫度,保溫12 h后取樣分析。若反應不完全,則繼續保溫至完全。然后攪拌下加入飽和碳酸氫鈉溶液200 mL,分去水層,再用100 mL水洗后分層,蒸掉溶劑,得到金黃色稠狀物三乙酰5-甲基尿苷(4)。
醇解反應:用甲醇150 mL溶解上述產物(4)通氨或加入甲醇鈉催化劑,50℃~60℃攪拌下反應,HPLC檢測跟蹤,反應完全后,蒸去溶劑,重結晶精制后得到5-甲基尿苷(5)。
5-甲基尿苷熔點:183.0 ℃~184.5 ℃與文獻一致[5]。
1HNMR(DM SO—d6) δ:1.75(d,J=1.0 Hz.3H,CH3),3.52~3.65 (m,2H,CH2-5’),3.77 ~3.88(m,1H.H-4’),3.94~ 4.05 (m,2H,H-2’ and H-3’),5.02~5.12(加 D2O 峰消失,OH),5.30(加 D2O 峰消失,OH),5.77(d,J=4.9 Hz,1H,H-1’),7.73(s,1H,H-6),11.27(S,1H,加 D2O 峰消失,NH),MS(ESI):m/z=281.8(M++Na)。
3 結果與討論
3.1 縮合用不同路易斯酸催化劑對總收率的影響
雙三甲硅基胸腺嘧啶(2)與 四乙酰核糖(3)在路易斯酸催化下,經縮合反應得到三乙酰5-甲基尿苷(4),再經醇解反應制得5-甲基尿苷(5)。縮合反應的路易斯酸催化劑,分別選用了三氯化鋁、四氯化錫和氯化鋅,采用1,2-二氯乙烷作為反應介質,比較其反應收率,見表1。
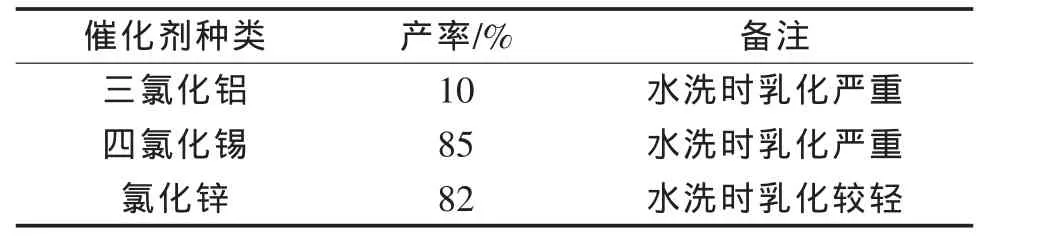
表1 Lewis催化劑種類對產率的影響Table1 Lewis catalyst type on the influence of the yield
結果表明:催化效果:四氯化錫>氯化鋅>三氯化鋁,雖然氯化鋅催化的產率低于四氯化錫,但價格成本上較四氯化錫具有巨大的優勢,且水洗時乳化較輕易于分層處理。
3.2 醇解用不同堿催化劑對總收率的影響
在路易斯酸氯化鋅催化下經縮合反應得到三乙酰5-甲基尿苷 (4),再經醇解后去乙酰基得到5-甲基尿苷(5),醇解時用了不同催化劑,見表2。

表2 堿催化劑種類對反應的影響Table2 base catalyst type on the influence of the reaction
結果表明:去乙酰基時,用氨和甲醇鈉催化的最終產率接近,催化速度:甲醇鈉>氨,與甲醇鈉的堿性強有關,但甲醇鈉須配合使用陽離子交換樹脂除鈉離子,否則會影響產品質量。氨回收后無殘留,便于回收套用。
4 結論
1) 雙三甲硅基胸腺嘧啶(2)的合成收率為93.5%。
2) 縮合催化效果:四氯化錫>氯化鋅>三氯化鋁,雖然氯化鋅的產率低于四氯化錫,但價格成本上較四氯化錫具有巨大的優勢,且水洗時乳化較輕易于分層處理。
3) 醇解去乙酰基時,催化用氨和甲醇鈉最終產率接近,催化速度:甲醇鈉>氨,與甲醇鈉的堿性強有關,但甲醇鈉須配合使用陽離子交換樹脂除鈉離子,否則會影響產品質量。
[1]李鳳軍,熊云茂,寧向陽,等.一種5-甲基尿苷的合成方法:CN,201010578777.8[P],2010-12-08.
[2]Hori N,Watanabe M,Yamazaki Y,et al.Synthesis of 5-methyluridine by a thermophile,bacillus stearothermophilus JTS 859[J].Agricultural and Biological Chemistry,1989,53(1):197-202.
[3]Hori N,Uehara K,Mikami Y.Enzymatic synthesis of 5-methyluridinefrom adenosineand thyminewith high efficiency[J].Bioscience,biotechnology and biochemistry,1992,56(4):580-582.
[4]上官俊龍,蘇境坦,鄭桂蘭,等.乙酰微小桿菌生物合成5-甲基尿苷的研究[J].廣東海洋大學學報,2011,31(4):7-30.
[5]Tanaka H.Hayakawa H,Obi K,et a1.Synthetic route to 5-substituted uridines via a new type of desulfurizative stannylation[J].Tetrahedron,1986,42:4187-4189.

